急性期所見

急性後部多発性斑状色素上皮症(APMPPE)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 急性後部多発性斑状色素上皮症とは
Section titled “1. 急性後部多発性斑状色素上皮症とは”急性後部多発性斑状色素上皮症(acute posterior multifocal placoid pigment epitheliopathy; APMPPE)は、1968年にGassが初めて報告した両眼性の急性炎症性疾患である10)。両眼の眼底後極部に網膜深層〜網膜色素上皮(RPE)レベルの円板状白斑が多発することを特徴とする。
ぶどう膜炎診療ガイドライン(日眼会誌 2019;123(6):635-696)の分類では、非感染性・眼底病変主体の後部ぶどう膜炎に位置づけられ、両眼性・急激発症・一過性経過という臨床特性が記載されている1)。
発症機序としては、脈絡膜毛細血管板の輸入細動脈に発生した遅延型過敏反応(IV型アレルギー)による閉塞性血管炎が想定されている。ウイルス感染(インフルエンザ・ムンプス等)などが誘因として疑われているが、詳細は不明である。
好発年齢は20〜30歳代(平均25歳)で、性差はない1)。両眼性発症が多い。半数以上の症例で先行する感冒様症状が報告されている1)。まれに全身血管炎・腎症・髄膜脳症・甲状腺炎との関連が報告されている1)。
好発年齢は40歳以下の若年成人であり、高齢者や小児での発症はまれである。40歳代以降に同様の病変を認めた場合は蛇行性脈絡膜炎(地図状脈絡膜炎)との鑑別が重要となる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”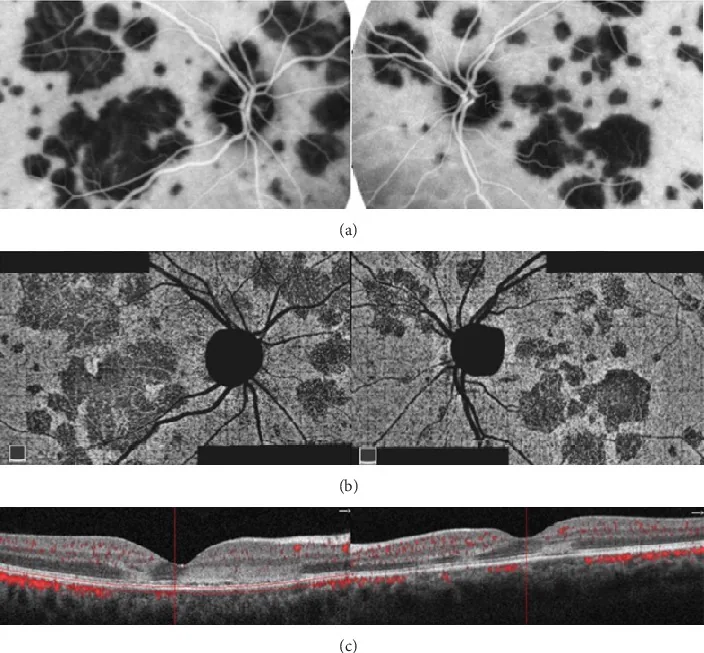
両眼の後極部に網膜深層〜RPEレベルの厌白色(クリーム色〜白色)円板状白斑が多発する。病巣は境界鮮明・大きさ1/4〜1/2乳頭径でほぼ均一で、数個〜多数出現し、融合・拡大傾向は少ない。軽度の視神経乳頭軽度発赤浮腫・軽度硝子体細胞を認めることがある1)。多発消失性白点症候群(MEWDS)の白斑よりも大きい点が鑑別ポイントである。
寛解期所見
白斑の消退:白斑は7〜12日で中心部から退縮し、軽度の脱色素変化を残して消失する。
OCT回復:数か月の経過でellipsoid zone が回復する場合があるが、視細胞層の菲薄化が残存することもある1)。
網脈絡膜萎縮:一部の症例では軽度の網脈絡膜萎縮斑が残存する1)。
多くの場合、白斑は発症後7〜12日で退縮し、脱色素を残して消失する。視力予後は通常良好で再発もまれである。ただし地図状脈絡膜症(蛇行性脈絡膜炎)への移行例では進行が見られるため、定期的な経過観察が必要である。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”脈絡膜毛細血管板の輸入細動脈への遅延型過敏反応(IV型アレルギー)による閉塞性血管炎が本態と推測される。OCT-A(OCTアンギオグラフィ)では急性期病変部に choriocapillaris レベルの flow void(血流信号欠損)が認められ、脈絡膜毛細血管板虚血が病態の中核にあることを支持する3)。Klufasらは、placoid chorioretinitis の3疾患(APMPPE・PPM・RPC)において OCT-A が FA・ICGA と高い一致率で choriocapillaris flow void を検出したことを報告している4)。
誘因・全身合併症
Section titled “誘因・全身合併症”- 先行感冒様症状(インフルエンザ・ムンプス等)、上気道感染、ワクチン接種後に発症する例がある
- 全身血管炎(脳血管炎)・腎症・結節性多発動脈炎・甲状腺炎との関連が報告されている1)
まれではあるが、APMPPEに中枢神経血管炎が合併した症例が報告されている。神経症状(激しい頭痛・意識変化・麻痺)が出現した場合は緊急で脳MRI・MRAを施行し、神経内科とも連携した対応が必要となる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”APMPPEの診断は特徴的な眼底所見と蛍光造影(FA・ICGA)所見に基づいて行われる。マルチモーダルイメージングにより病態の多面的評価が可能である2)。
マルチモーダルイメージング
Section titled “マルチモーダルイメージング”| 検査法 | 特徴的所見 |
|---|---|
| FA(フルオレセイン蛍光眼底造影) | 急性期: 早期低蛍光→後期過蛍光(「蛍光の逆転現象」)1) |
| ICGA(インドシアニングリーン蛍光眼底造影) | 早期から後期まで終始低蛍光。慢性期は縮小・境界不鮮明化5) |
| SD-OCT | 急性期: ellipsoid zone の高反射性乱れ。寛解期: 視細胞層菲薄化1) |
| OCT-A | choriocapillaris レベルの flow void。FA/ICGAと高い一致率4) |
| FAF(眼底自発蛍光) | 急性期: 病変部低自発蛍光または過蛍光。OCT所見と相関9) |
| 多局所ERG | 急性期に黄斑部付近の振幅の著明な平坦化 |
蛍光の逆転現象について
Section titled “蛍光の逆転現象について”FAで認める早期低蛍光→後期過蛍光という「蛍光の逆転現象」は、APMPPEの最も特徴的な所見である。早期に脈絡膜毛細血管板への色素流入が阻害され(閉塞性血管炎のため)、後期に周囲から滲出することで過蛍光が生じると解釈される1)。ICGAでは早期から後期まで終始低蛍光を示し、脈絡膜毛細血管板虚血をより直接的に反映する5)。
OCT-AによるChoriocapillaris評価
Section titled “OCT-AによるChoriocapillaris評価”OCT-AはAPMPPEにおける脈絡膜毛細血管板の血流障害を非侵襲的に評価できる画像モダリティである。Furinoらは、急性APMPPE病変においてOCT-Aが FA・ICGAと高い一致率でchoriocapillaris flow voidを描出できると報告した8)。回復期においてflow void の縮小とともに視機能の改善が見られることが確認されており、活動性モニタリングのバイオマーカーとして有用である。
- 地図状(蛇行性)脈絡膜炎:40歳代・片眼性・進行拡大・地図状・予後不良1)
- フォークト‐小柳‐原田病:滲出性網膜剝離・多発性網膜下漏出点1)
- 多発消失性白点症候群(MEWDS):若年女性・赤道部までの広範囲・FA初期過蛍光1)
- 持続性プラコイド黄斑症(PPM)・relentless placoid chorioretinitis(RPC):APMPPEと類似した病型として「placoid chorioretinitis spectrum」内で再分類の議論がある4)7)
5. 標準的な治療法
Section titled “5. 標準的な治療法”自然軽快傾向が強く、特別な治療なく自然回復することが多い1)。軽症例では経過観察を基本とする。Jones(1995)の長期経過報告でも、多くの症例が最終的に良好な視力を回復したことが示されている10)。
抗炎症療法の適応
Section titled “抗炎症療法の適応”視力低下が著しい場合・乳頭炎を合併する場合・黄斑近傍の病変がある場合に以下を考慮する。
- プレドニゾロン錠(5 mg):30 mg/日より開始し、2週間〜1か月かけて漸減
- カルナクリン錠(カリジノゲナーゼ 25〜50単位):3錠 分3(脈絡膜微小循環改善薬として併用)
地図状脈絡膜症への移行例や中枢神経血管炎合併例では、ステロイドパルス療法(メチルプレドニゾロン大量静注)や免疫抑制薬の使用を検討する1)。脈絡膜新生血管(CNV)を生じた場合は抗VEGF薬硝子体内注射を検討するが、まれな合併症である。持続性プラコイド黄斑症(PPM)への移行例では、Kolomeyer・Bruckerが系統的レビューで指摘するように長期管理を要することがある7)。
軽症例では経過観察のみで自然回復する。視力低下が著しい・乳頭近傍の炎症が強い・中枢神経症状を伴う場合にステロイド療法が考慮される。ぶどう膜炎診療ガイドラインでも「特別な治療なく自然回復」が基本方針とされている1)。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”APMPPEの病態は、脈絡膜毛細血管板閉塞を中心とした虚血性変化として理解されている。
脈絡膜毛細血管板の輸入細動脈に発生した遅延型過敏反応(IV型アレルギー)による閉塞性血管炎が本態と推測される。閉塞 → RPE・網膜外層の虚血性変化(浮腫・混濁)→ 円板状白斑が形成される。Mrejenらは脈絡膜病変がより深層にまで及ぶことを示し、脈絡膜毛細血管板のみならず中・大血管レベルにも関与する可能性を示唆した3)。
OCT-Aではinner choroid レベルのflow voidが観察され、APMPPEと同様の「placoid disorder spectrum」(persistent placoid maculopathy・relentless placoid chorioretinitis を含む)の疾患群の病態基盤として脈絡膜毛細血管板虚血が一貫して認められることが示されている4)。Klufasらは、3疾患間でOCT-Aによるchoriocapillaris flow voidが共通のパターンを示すことを報告し、placoid chorioretinitis spectrum の概念を支持した。
蛍光の逆転現象の機序:造影早期は脈絡膜毛細血管板への色素流入が阻害されるため低蛍光を呈し、後期には周囲正常組織から色素が滲出して過蛍光に転じる。ICGAが終始低蛍光を示す点も、脈絡膜毛細血管板の閉塞性変化を反映する5)。FAFはRPE障害の分布を非侵襲的に評価でき、OCT所見と高い対応関係を示す9)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”- COVID-19感染・ワクチン後のAPMPPE:感染後に急性APMPPE様病変が出現した症例が報告されており、ウイルス誘発性免疫応答との関係が注目されている
- 中枢神経血管炎(cerebral vasculitis)合併:神経症状を伴う症例における脳MRI・MRAの推奨が強まっている。APMPPEに脳卒中や脳血管炎が合併した症例が複数報告されており、眼症状のみならず全身的なモニタリングが重要である6)
- マルチモーダル画像の進歩:OCT-Aによるchoriocapillaris flow void のモニタリングが活動性評価のバイオマーカーとなる可能性がある8)。非侵襲的かつ繰り返し施行可能な点で、FAやICGAを補完する重要モダリティとなりつつある
- 病型の再分類:persistent placoid maculopathy・relentless placoid chorioretinitis を含む「placoid chorioretinitis spectrum」としての統合的理解が進んでいる4)。Mirza・Jampol(2012)はrelentless placoid chorioretinitis の独立疾患概念としての特徴を整理し、APMPPE との連続性を論じた6)
8. 参考文献
Section titled “8. 参考文献”- 日本眼炎症学会・日本眼科学会. ぶどう膜炎診療ガイドライン(「13. 急性後部多発性斑状色素上皮症」節). 日本眼科学会雑誌. 2019;123(6):635-696.
- Testi I, Modugno RL, Pavesio C. Multimodal imaging supporting the pathophysiology of white dot syndromes. J Ophthalmic Inflamm Infect. 2021;11:32.
- Mrejen S, Sarraf D, Chexal S, et al. Choroidal involvement in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2016;47:20-26.
- Klufas MA, Phasukkijwatana N, Iafe NA, et al. Optical coherence tomography angiography reveals choriocapillaris flow reduction in placoid chorioretinitis. Ophthalmol Retina. 2017;1(1):77-91.
- Park D, Schatz H, McDonald HR, Johnson RN. Indocyanine green angiography of acute multifocal posterior placoid pigment epitheliopathy. Ophthalmology. 1995;102:1877-1883.
- Mirza RG, Jampol LM. Relentless placoid chorioretinitis. Int Ophthalmol Clin. 2012;52(4):237-242.
- Kolomeyer AM, Brucker AJ. Persistent placoid maculopathy: a systematic review. Retina. 2018;38(10):1881-1895.
- Furino C, Shalchi Z, Grassi MO, et al. Optical coherence tomography angiography in acute posterior multifocal placoid pigment epitheliopathy. Ophthalmic Surg Lasers Imaging Retina. 2019;50(7):428-436.
- Souka AA, Hillenkamp J, Gora F, Gabel VP, Framme C. Correlation between optical coherence tomography and autofluorescence in acute posterior multifocal placoid pigment epitheliopathy. Graefes Arch Clin Exp Ophthalmol. 2006;244(10):1219-1223.
- Jones NP. Acute posterior multifocal placoid pigment epitheliopathy. Br J Ophthalmol. 1995;79:384-389.
