
視界が歪む・欠けるときの考えられる原因まとめ
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 視界が歪む・欠けるとは
Section titled “1. 視界が歪む・欠けるとは”「ものが歪む」「直線が曲がって見える」「視野の一部が欠ける・暗い」という症状は、黄斑疾患・網膜疾患・緑内障・視神経疾患・脳疾患など多様な原因で生じる。これらの症状は大きく2つの病態に分類される。
**変視症(へんししょう)**は、物の形・大きさ・直線が変形して見える症状である。原因は主に黄斑(網膜の中心部)の構造的変化であり、格子や直線が波打って見えるのが典型的である。
視野欠損は、視野の一部分が見えなくなる(暗く感じる・欠ける)症状である。緑内障・網膜剥離・網膜血管閉塞症・視神経疾患・脳疾患など幅広い疾患が原因となる。
加齢黄斑変性(AMD)の有病率は久山町研究で進行期1.6%(滲出型1.5%、萎縮型0.1%)と報告されており、前駆病変は長浜スタディで22.8%に認められる。AMDは50歳以上・男性に多く(男性:女性=3:1)、両眼罹患は40%にのぼる。一方、緑内障の有病率は40歳以上の約5%とされ1)、日本における主要な視覚障害原因疾患の一つである。
症状の種類と発症様式を正確に把握し、適切な時期に眼科を受診することが視力保護の鍵となる。片眼ずつ確認する習慣が早期発見につながる。
2. 変視症(歪み)の原因疾患
Section titled “2. 変視症(歪み)の原因疾患”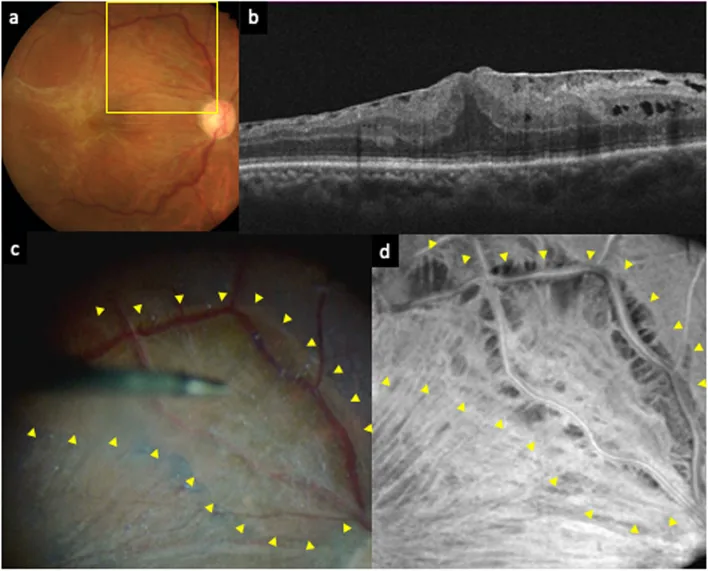
変視症は黄斑(眼の中心部)の構造的変化によって生じることが多い。格子や直線が波打って見える、中央部が暗くなる(中心暗点)などの症状が代表的である。
| 疾患 | 好発年齢・性別 | 主な特徴 | 緊急度 |
|---|---|---|---|
| 黄斑上膜(黄斑前膜) | 中高年 | 変視症・大視症。Gass分類 Grade 0〜2。OCTで確定診断 | 低〜中(経過観察→手術) |
| 加齢黄斑変性(AMD) | 50歳以上・男性優位 | 変視・中心暗点が初発。進行で視力0.1以下 | 中〜高(早期治療が重要) |
| 黄斑円孔 | 中高年女性 | 中心窩全層欠損→中心暗点・変視症 | 中(手術適応あり) |
| 中心性漿液性脈絡網膜症(CSC) | 若〜中年男性 | ストレス・ステロイド使用が誘因。小視症も2) | 低〜中(多くは自然軽快) |
| 糖尿病黄斑浮腫(DME) | 糖尿病患者 | 黄斑部の浮腫による変視・視力低下3) | 中〜高(治療介入で悪化防止) |
黄斑上膜(黄斑前膜)の詳細
Section titled “黄斑上膜(黄斑前膜)の詳細”黄斑上膜は、特発性では網膜グリア細胞が内境界膜上で増殖し線維性組織を形成することで生じる。炎症・網膜剥離・外傷・網膜血管腫への続発例も存在する。症状は視力低下・変視症で、時に大視症を伴う。Gass分類でGrade 0(セロハン黄斑症:透明で網膜変形なし)からGrade 2(灰色不透明膜・著明な皺)まで分類される。OCT検査による黄斑上膜の確認と網膜厚の増加が確定診断の根拠となる。視力障害・著明な網膜肥厚・強い歪視がある場合は硝子体手術+黄斑上膜剥離の適応となる。術後視力は術前視力とよく相関し、回復には長期間(1年以上)を要することがある。
加齢黄斑変性(AMD)の分類
Section titled “加齢黄斑変性(AMD)の分類”AMDは前駆病変(軟性ドルーゼン・網膜色素上皮異常)から進行し、萎縮型(地図状萎縮)と滲出型(脈絡膜新生血管:CNV)に分かれる。滲出型のうち、ポリープ状脈絡膜血管症(PCV)は日本人に多い特殊病型である。滲出型AMDは変視・中心暗点に始まり、放置すると約9割が視力0.1以下に低下する。大量出血例では突然の高度視力低下をきたすことがある。
3. 視野欠損(欠け)の原因疾患
Section titled “3. 視野欠損(欠け)の原因疾患”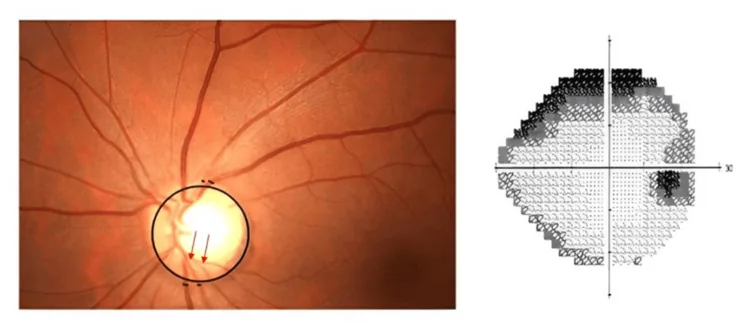
視野欠損は、視野の一部が暗く感じる・欠けて見える・カーテンがかかったように見えるなどの症状として現れる。緑内障のように緩徐に進行するものから、網膜剥離・網膜動脈閉塞症のように突然発症する緊急疾患まで多様な原因がある。
| 疾患 | 視野欠損のパターン | 緊急度 |
|---|---|---|
| 緑内障 | 弓状暗点・傍中心暗点。中心視力は末期まで保たれる1) | 低〜中(慢性進行。定期管理が必要) |
| 網膜剥離(裂孔原性) | カーテン状・幕状の視野欠損。片側から広がる | 緊急(当日手術が必要な場合あり) |
| 網膜静脈閉塞症(分枝型) | 扇形の視野欠損(閉塞した静脈領域に一致)4) | 中〜高(早期治療が予後に影響) |
| 網膜動脈閉塞症 | 突然の無痛性視力喪失・広範な視野欠損5) | 緊急(発症後数時間が勝負) |
| 両側性視野欠損 | 垂直線を境にした半盲(同名半盲)→ 脳疾患疑い6) | 緊急(神経内科・脳外科との連携) |
緑内障の視野欠損の特徴
Section titled “緑内障の視野欠損の特徴”緑内障では視神経線維の変性・脱落により、対応する視野に弓状暗点・傍中心暗点が出現する。初期〜中期では中心視力が正常に保たれるため自覚が遅れやすく、自覚したときにはすでに相当な視野が失われていることが多い1)。多治見スタディによると原発開放隅角緑内障の有病率は40歳以上の日本人の約3.9%であり1)、定期的な眼圧測定と眼底検査が早期発見に不可欠である。
網膜剥離の視野欠損
Section titled “網膜剥離の視野欠損”裂孔原性網膜剥離では、網膜裂孔から網膜下液が広がる過程でカーテン状・幕状の視野欠損が片側から拡大する9)。発症前には光視症・飛蚊症の急増が先行することが多い。視野欠損が黄斑部(中心部)に達すると視力が著しく低下するため、それ以前の緊急手術が視力予後を大きく左右する。
脳疾患による視野欠損
Section titled “脳疾患による視野欠損”両側の視野が対称的に欠ける「同名半盲」は、視放線・後頭葉などの脳病変を示す。脳梗塞・脳腫瘍・頭蓋内出血が原因となり6)、神経内科・脳外科との迅速な連携が必要である。
4. 突然の視野変化(閃輝暗点・一過性黒内障)
Section titled “4. 突然の視野変化(閃輝暗点・一過性黒内障)”突然の一時的な視野変化は、自然に消える偏頭痛関連の閃輝暗点から、緊急精査を要する一過性黒内障まで病態が異なる。鑑別のポイントは片眼性か両眼性か、持続時間、随伴症状である。
| 症状 | 持続時間 | 眼別 | 特徴 | 緊急度 |
|---|---|---|---|---|
| 閃輝暗点(偏頭痛前兆) | 20〜30分で自然消失 | 両眼性(視野の同側) | ギザギザした光のリング・カラフルな光が拡大 | 低(偏頭痛クリニック相談) |
| 一過性黒内障(TIA眼症状) | 数秒〜数分 | 片眼性 | 片眼が完全に見えなくなる・上から幕が下りる感覚7) | 緊急(同日に神経内科・眼科) |
| 網膜剥離前駆(光視症) | 反復性 | 片眼性 | 暗い場所で閃光・稲妻状の光。飛蚊症増加を伴う | 高(数日以内に眼科) |
| 硝子体出血 | 突然・持続 | 片眼性 | 急激な飛蚊症増加・霞み・視力低下 | 高(早急な眼科受診) |
両側性半盲の緊急性
Section titled “両側性半盲の緊急性”片眼ではなく両眼の同側半分が同時に欠けて見える場合(例:右視野が両眼ともに欠ける)は、脳梗塞・脳腫瘍・後頭葉の病変を示す緊急サインである6)。速やかに救急受診が必要である。
5. セルフチェック法(アムスラーチャート)と受診の目安
Section titled “5. セルフチェック法(アムスラーチャート)と受診の目安”アムスラーチャートの使い方
Section titled “アムスラーチャートの使い方”アムスラーチャートを用いた自己検査はAMDや黄斑疾患のモニタリングに有用であり、AMD検出感度は中心5度以内で約70%と報告されている8)。ただし感度に限界があるため、チャートで異常がなくても定期的な眼科受診は継続する必要がある。
受診の緊急度
Section titled “受診の緊急度”| 緊急度 | 症状 | 推奨行動 |
|---|---|---|
| 即日受診(救急含む) | 突然のカーテン状視野欠損 / 片眼の突然の無痛性視力喪失 / 片眼の一過性視力消失 / 両眼の同側視野欠損 | 当日中に眼科・救急へ。網膜剥離・RAO・TIAの可能性 |
| 早期受診(数日以内) | アムスラーチャートで歪み・暗点を検出 / 片眼で見え方が変化した / 飛蚊症の急増+光視症 | 1〜3日以内に眼科でOCT検査 |
| 定期受診 | AMD家族歴・片眼既往・緑内障リスク因子(高眼圧・家族歴・強度近視)あり1) | 年1〜2回の眼科定期検診 |
初期〜中期の緑内障は中心視力が正常に保たれるため、視野欠損を自覚することが非常に難しい。欠けた視野を反対の眼や脳が無意識に補完してしまうためである。片目を閉じて見え方を確認する習慣や、定期的な眼科での視野検査が早期発見に重要である。多治見スタディによると緑内障患者の約90%が未診断とされており1)、無症状でも40歳以上の定期検診が推奨される。
6. 歪み・欠けの病態生理
Section titled “6. 歪み・欠けの病態生理”黄斑疾患による変視症の機序
Section titled “黄斑疾患による変視症の機序”黄斑上膜では、網膜グリア細胞が内境界膜上で増殖して線維性組織を形成し、網膜表面に皺を生じる。この皺が光受容細胞の配列を乱すことで変視症・大視症が生じる。
**加齢黄斑変性(AMD)**では、まず黄斑部の網膜色素上皮(RPE)が障害を受け、ドルーゼン形成・網膜色素上皮異常が生じる。萎縮型AMDでは地図状萎縮(GA)に進行して視細胞が失われ、滲出型AMDでは脈絡膜新生血管(CNV)が形成されて出血・滲出液が黄斑部を障害する。この過程で光受容細胞の機能が失われ、変視症・中心暗点が生じる。
黄斑円孔では中心窩の全層が欠損し、中心暗点・変視症が生じる。
**中心性漿液性脈絡網膜症(CSC)**では、脈絡膜の透過性亢進によりRPE下・神経網膜下に液体が貯留し、黄斑部が局所的に隆起する。この隆起により焦点距離が変化し、変視症・小視症が生じる2)。
緑内障による視野欠損の機序
Section titled “緑内障による視野欠損の機序”緑内障では視神経乳頭での軸索障害・眼圧による機械的圧迫・虚血などの機序で視神経線維が変性・脱落する1)。脱落した線維に対応する網膜領域の視野が欠損し、典型的には弓状暗点・傍中心暗点として現れる。末期になるまで中心視力が保たれることが、自覚遅延の主因である。
網膜剥離の病態
Section titled “網膜剥離の病態”裂孔原性網膜剥離では、後部硝子体剥離に伴う網膜牽引により網膜裂孔が形成される。裂孔から液化硝子体が網膜下腔に侵入し、感覚網膜がRPEから剥離する9)。剥離した網膜の光受容体は虚血状態となり、対応する視野が欠損する。中心部(黄斑)が剥離すると視力が著しく低下し、長期経過により視力回復が困難となる。
7. 最新の治療と研究
Section titled “7. 最新の治療と研究”新世代抗VEGF薬(faricimab)
Section titled “新世代抗VEGF薬(faricimab)”Heierら(2022年)のTENAYA/LUCERNEランダム化比較試験では、VEGF-AとAngiopoietin-2(Ang-2)を二重阻害するfaricimabが滲出型AMDに対して最長16週間隔の投与で非劣性を示した10)。投与間隔の延長により患者負担の軽減が期待される。
萎縮型AMD(地図状萎縮)への補体阻害薬
Section titled “萎縮型AMD(地図状萎縮)への補体阻害薬”補体C3阻害薬pegcetacoplanは、萎縮型AMDの地図状萎縮(GA)の進行抑制を目的とした第2相試験で、プラセボ比較でGA面積の拡大抑制効果を示した11)。萎縮型AMDはこれまで有効な治療がなく、新たな治療選択肢として注目されている。
黄斑上膜手術における内境界膜剥離の有効性
Section titled “黄斑上膜手術における内境界膜剥離の有効性”Azumaら(2017年)のシステマティックレビューおよびメタ解析では、黄斑上膜手術に内境界膜(ILM)剥離を追加することで術後視力・解剖学的改善が向上することが示された12)。再発リスクの低下も報告されている。
在宅モニタリングデバイスによるAMD早期検出
Section titled “在宅モニタリングデバイスによるAMD早期検出”Chewら(2014年)のHOME研究(ランダム化比較試験)では、在宅モニタリングデバイス(ForeseeHome)が通常ケアと比較して滲出型AMDへの移行をより早期に検出し、視力予後改善に貢献することが示された13)。デジタル技術を用いた患者自身による日常的モニタリングが今後さらに普及する見通しである。
8. 参考文献
Section titled “8. 参考文献”- Iwase A, Suzuki Y, Araie M, et al. The prevalence of primary open-angle glaucoma in Japanese: the Tajimi Study. Ophthalmology. 2004;111(9):1641-1648.
- Daruich A, Matet A, Dirani A, et al. Central serous chorioretinopathy: recent findings and new physiopathology hypothesis. Prog Retin Eye Res. 2015;48:82-118.
- 日本糖尿病眼学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2020;124(12):955-981.
- Ehlers JP, Fekrat S. Retinal vein occlusion: beyond the acute event. Surv Ophthalmol. 2011;56(4):281-299.
- Hayreh SS. Acute retinal arterial occlusive disorders. Prog Retin Eye Res. 2011;30(5):359-394.
- Zhang X, Kedar S, Lynn MJ, et al. Homonymous hemianopia in stroke. J Neuroophthalmol. 2006;26(3):180-183.
- Biousse V, Trobe JD. Transient monocular visual loss. Am J Ophthalmol. 2005;140(4):717-721.
- Faes L, Bodmer NS, Bachmann LM, et al. Diagnostic accuracy of the Amsler grid and the preferential hyperacuity perimetry in the screening of patients with age-related macular degeneration: systematic review and meta-analysis. Eye (Lond). 2014;28(7):788-796.
- Feltgen N, Walter P. Rhegmatogenous retinal detachment—an ophthalmologic emergency. Dtsch Arztebl Int. 2014;111(1-2):12-22.
- Heier JS, Khanani AM, Quezada Ruiz C, et al. Efficacy, durability, and safety of intravitreal faricimab up to every 16 weeks for neovascular age-related macular degeneration (TENAYA and LUCERNE): two randomised, double-masked, phase 3, non-inferiority trials. Lancet. 2022;399(10326):729-740.
- Liao DS, Grossi FV, El Mehdi D, et al. Complement C3 inhibitor pegcetacoplan for geographic atrophy secondary to age-related macular degeneration: a randomized phase 2 trial. Ophthalmology. 2020;127(2):186-195.
- Azuma K, Ueta T, Eguchi S, et al. Effects of internal limiting membrane peeling combined with removal of idiopathic epiretinal membrane: a systematic review of literature and meta-analysis. Retina. 2017;37(10):1813-1819.
- Chew EY, Clemons TE, Bressler SB, et al. Randomized trial of the ForeseeHome monitoring device for early detection of neovascular age-related macular degeneration. The HOME Study. Ophthalmology. 2014;121(2):535-544.
