
Causes possibles lorsque la vision est déformée ou manquante
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que la déformation ou la perte de vision ?
Section intitulée « 1. Qu’est-ce que la déformation ou la perte de vision ? »Les symptômes tels que « les objets se déforment », « les lignes droites semblent courbes » ou « une partie du champ visuel manque ou est sombre » peuvent être causés par diverses affections : maladies maculaires, maladies rétiniennes, glaucome, maladies du nerf optique, maladies cérébrales, etc. Ces symptômes sont classés en deux grandes catégories pathologiques.
La métamorphopsie est un symptôme où la forme, la taille ou les lignes droites des objets apparaissent déformées. La cause principale est un changement structurel de la macula (partie centrale de la rétine), et il est typique de voir des grilles ou des lignes droites ondulées.
Le déficit du champ visuel est un symptôme où une partie du champ visuel devient invisible (sensation d’obscurité ou de perte). Il peut être causé par un large éventail de maladies : glaucome, décollement de rétine, occlusion vasculaire rétinienne, maladies du nerf optique, maladies cérébrales, etc.
La prévalence de la dégénérescence maculaire liée à l’âge (DMLA) est rapportée à 1,6 % pour le stade avancé (1,5 % pour la forme exsudative, 0,1 % pour la forme atrophique) dans l’étude de Hisayama, et les lésions précurseurs sont observées chez 22,8 % des participants dans l’étude de Nagahama. La DMLA est plus fréquente chez les hommes de 50 ans et plus (hommes : femmes = 3:1), et l’atteinte bilatérale atteint 40 %. En revanche, la prévalence du glaucome est d’environ 5 % chez les personnes de 40 ans et plus 1), ce qui en fait l’une des principales causes de déficience visuelle au Japon.
Il est essentiel de déterminer avec précision le type et le mode d’apparition des symptômes et de consulter un ophtalmologiste au moment opportun pour protéger la vision. L’habitude de vérifier chaque œil séparément contribue à une détection précoce.
2. Maladies responsables de la métamorphopsie (déformation)
Section intitulée « 2. Maladies responsables de la métamorphopsie (déformation) »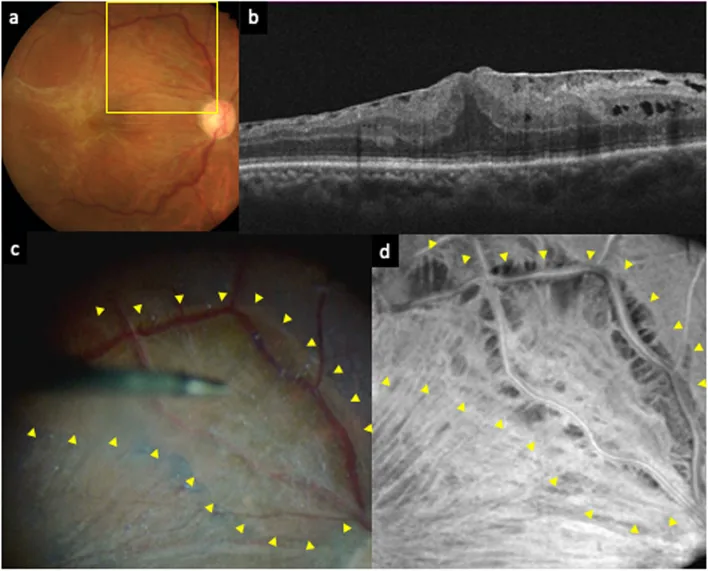
La métamorphopsie est souvent due à des modifications structurelles de la macula (partie centrale de l’œil). Les symptômes typiques incluent l’impression que les grilles ou les lignes droites sont ondulées, ou l’apparition d’une zone sombre au centre (scotome central).
| Maladie | Âge et sexe prédominants | Caractéristiques principales | Urgence |
|---|---|---|---|
| Membrane épirétinienne (membrane prémaculaire) | Personnes d’âge moyen ou avancé | Métamorphopsie, macropsie. Classification de Gass grade 0 à 2. Diagnostic confirmé par OCT. | Faible à modérée (surveillance puis chirurgie) |
| Dégénérescence maculaire liée à l’âge (DMLA) | 50 ans et plus, prédominance masculine | Métamorphopsie et scotome central comme premiers symptômes. En l’absence de traitement, l’acuité visuelle peut descendre en dessous de 0,1. | Modérée à élevée (traitement précoce important) |
| Trou maculaire | Femmes d’âge moyen à avancé | Perte de pleine épaisseur de la fovéa → scotome central et métamorphopsie | Moyen (indication chirurgicale) |
| Choriorétinopathie séreuse centrale (CSC) | Hommes jeunes à d’âge moyen | Le stress et l’utilisation de stéroïdes sont des facteurs déclenchants. Micropsie également 2) | Faible à moyen (souvent résolution spontanée) |
| Œdème maculaire diabétique (OMD) | Patients diabétiques | Métamorphopsie et baisse de l’acuité visuelle dues à l’œdème maculaire 3) | Moyen à élevé (le traitement prévient l’aggravation) |
Détails de la membrane épirétinienne (membrane prémaculaire)
Section intitulée « Détails de la membrane épirétinienne (membrane prémaculaire) »La membrane épirétinienne idiopathique résulte de la prolifération de cellules gliales rétiniennes sur la membrane limitante interne, formant un tissu fibreux. Des cas secondaires à une inflammation, un décollement de rétine, un traumatisme ou une tumeur vasculaire rétinienne existent également. Les symptômes sont une baisse de l’acuité visuelle et une métamorphopsie, parfois accompagnées de macropsie. La classification de Gass va du grade 0 (maculopathie cellophane : transparente, sans déformation rétinienne) au grade 2 (membrane grise opaque avec plis marqués). Le diagnostic est confirmé par l’OCT montrant la membrane épirétinienne et une augmentation de l’épaisseur rétinienne. En cas de trouble visuel, d’épaississement rétinien important ou de métamorphopsie sévère, une vitrectomie avec pelage de la membrane épirétinienne est indiquée. L’acuité visuelle postopératoire est bien corrélée à l’acuité préopératoire, et la récupération peut prendre plus d’un an.
Classification de la dégénérescence maculaire liée à l’âge (DMLA)
Section intitulée « Classification de la dégénérescence maculaire liée à l’âge (DMLA) »La DMLA progresse à partir de lésions précurseurs (drusen mous, anomalies de l’épithélium pigmentaire rétinien) et se divise en forme atrophique (atrophie géographique) et forme exsudative (néovascularisation choroïdienne : NVC). Parmi les formes exsudatives, la polypose choroïdienne (PCV) est un sous-type particulier fréquent chez les Japonais. La DMLA exsudative débute par une métamorphopsie et un scotome central, et si elle n’est pas traitée, environ 90 % des cas voient leur acuité visuelle chuter à 0,1 ou moins. En cas d’hémorragie massive, une baisse soudaine et sévère de la vision peut survenir.
Si les lignes de la grille d’Amsler apparaissent déformées, manquantes par endroits ou si vous percevez un scotome, cela peut être un signe de maladie maculaire. Il est recommandé de consulter un ophtalmologiste dans les jours suivants et de passer un examen OCT (tomographie par cohérence optique). La priorité est élevée si l’anomalie est détectée en testant chaque œil séparément. La sensibilité de la grille d’Amsler pour détecter la DMLA dans les 5 degrés centraux est rapportée à environ 70 % 8), et des examens réguliers sont importants même en l’absence de symptômes.
3. Maladies responsables des déficits du champ visuel (scotomes)
Section intitulée « 3. Maladies responsables des déficits du champ visuel (scotomes) »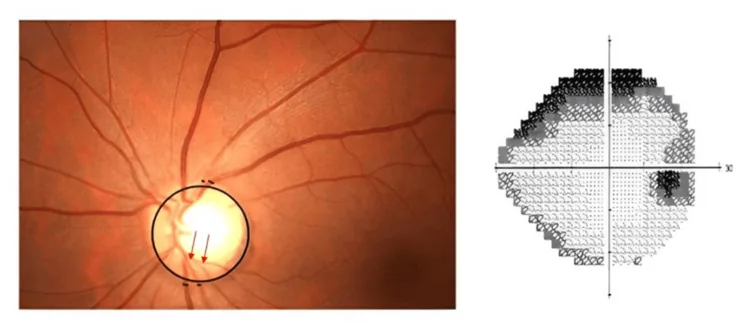
Les déficits du champ visuel se manifestent par des symptômes tels qu’une zone sombre, une perte de vision partielle ou une sensation de rideau. Les causes sont variées, allant de maladies à progression lente comme le glaucome à des urgences soudaines comme le décollement de rétine ou l’occlusion de l’artère rétinienne.
| Maladie | Motif du déficit du champ visuel | Urgence |
|---|---|---|
| Glaucome | Scotome arqué, scotome paracentral. La vision centrale est préservée jusqu’aux stades avancés 1) | Faible à modérée (chronique progressive, nécessite une gestion régulière) |
| Décollement de rétine (rhgmatogène) | Déficit du champ visuel en forme de rideau, s’étendant d’un côté | Urgent (une chirurgie le jour même peut être nécessaire) |
| Occlusion veineuse rétinienne (type branche) | Déficit du champ visuel en éventail (correspondant à la zone veineuse occluse) 4) | Moyen à élevé (le traitement précoce influence le pronostic) |
| Occlusion artérielle rétinienne | Perte soudaine et indolore de la vision, déficit visuel étendu 5) | Urgence (les premières heures après l’apparition sont cruciales) |
| Déficit visuel bilatéral | Hémianopsie le long de la ligne verticale (hémianopsie homonyme) → suspicion de maladie cérébrale 6) | Urgence (coordination avec neurologie et neurochirurgie) |
Caractéristiques du déficit visuel dans le glaucome
Section intitulée « Caractéristiques du déficit visuel dans le glaucome »Dans le glaucome, la dégénérescence et la perte des fibres nerveuses optiques entraînent l’apparition de scotomes arqués et de scotomes paracentraux dans le champ visuel correspondant. Aux stades précoces à intermédiaires, l’acuité visuelle centrale reste normale, ce qui retarde la prise de conscience, et lorsque le patient s’en rend compte, une partie considérable du champ visuel est déjà perdue 1). Selon l’étude de Tajimi, la prévalence du glaucome primitif à angle ouvert est d’environ 3,9 % chez les Japonais de plus de 40 ans 1), et des mesures régulières de la pression intraoculaire et des examens du fond d’œil sont essentiels pour un diagnostic précoce.
Déficit visuel dans le décollement de la rétine
Section intitulée « Déficit visuel dans le décollement de la rétine »Dans le décollement de la rétine rhegmatogène, à mesure que le liquide sous-rétinien se propage à partir de la déchirure rétinienne, un déficit visuel en forme de rideau ou de voile s’étend d’un côté 9). L’apparition est souvent précédée d’une augmentation soudaine des photopsies et des corps flottants. Lorsque le déficit visuel atteint la macula (zone centrale), la vision diminue considérablement, donc une chirurgie d’urgence avant ce stade influence grandement le pronostic visuel.
Déficit visuel dû à une maladie cérébrale
Section intitulée « Déficit visuel dû à une maladie cérébrale »L’hémianopsie homonyme, où les deux champs visuels sont symétriquement déficitaires, indique une lésion cérébrale au niveau des radiations optiques ou du lobe occipital. Les causes incluent l’infarctus cérébral, les tumeurs cérébrales et les hémorragies intracrâniennes 6), nécessitant une coordination rapide avec la neurologie et la neurochirurgie.
4. Changements soudains du champ visuel (scotome scintillant, amaurose fugace)
Section intitulée « 4. Changements soudains du champ visuel (scotome scintillant, amaurose fugace) »Les changements soudains et temporaires du champ visuel peuvent aller du scotome scintillant lié à la migraine, qui disparaît spontanément, à l’amaurose fugace nécessitant une évaluation urgente. Les points clés pour le diagnostic différentiel sont l’atteinte monoculaire ou binoculaire, la durée et les symptômes associés.
| Symptôme | Durée | Œil concerné | Caractéristiques | Urgence |
|---|---|---|---|---|
| Scotome scintillant (aura migraineuse) | Disparaît spontanément en 20 à 30 minutes | Binoculaire (même côté du champ visuel) | Anneau lumineux dentelé, lumières colorées qui s’étendent | Faible (consulter une clinique de la migraine) |
| Amaurose fugace (symptôme oculaire d’AIT) | Quelques secondes à quelques minutes | Monoculaire | Perte totale de la vision d’un œil, sensation de rideau tombant d’en haut7) | Urgente (consulter le jour même un neurologue et un ophtalmologiste) |
| Précurseur de décollement de rétine (photopsie) | Récurrent | Unilatéral | Éclairs lumineux en forme d’éclair dans l’obscurité. Souvent accompagné d’une augmentation des corps flottants. | Élevée (consulter un ophtalmologiste dans les jours suivants) |
| Hémorragie du vitré | Soudain et persistant | Unilatéral | Augmentation soudaine des corps flottants, vision trouble, baisse de l’acuité visuelle | Élevée (consulter un ophtalmologiste en urgence) |
Urgence de l’hémianopsie bilatérale
Section intitulée « Urgence de l’hémianopsie bilatérale »Si la moitié du même côté des deux yeux manque simultanément (par exemple, le champ visuel droit est absent dans les deux yeux), il s’agit d’un signe d’urgence indiquant un infarctus cérébral, une tumeur cérébrale ou une lésion du lobe occipital 6). Une consultation urgente aux urgences est nécessaire.
5. Méthode d’auto-examen (grille d’Amsler) et critères de consultation
Section intitulée « 5. Méthode d’auto-examen (grille d’Amsler) et critères de consultation »Utilisation de la grille d’Amsler
Section intitulée « Utilisation de la grille d’Amsler »L’auto-examen avec la grille d’Amsler est utile pour surveiller la DMLA et les maladies maculaires. La sensibilité de détection de la DMLA dans les 5 degrés centraux est d’environ 70 % 8). Cependant, comme la sensibilité est limitée, même si la grille ne montre aucune anomalie, des consultations ophtalmologiques régulières doivent être maintenues.
Urgence de la consultation
Section intitulée « Urgence de la consultation »| Urgence | Symptômes | Action recommandée |
|---|---|---|
| Consultation le jour même (y compris aux urgences) | Déficit du champ visuel soudain en rideau / Perte de vision soudaine et indolore d’un œil / Perte de vision transitoire d’un œil / Déficit du champ visuel homonyme bilatéral | Se rendre chez l’ophtalmologiste ou aux urgences le jour même. Possibilité de décollement de rétine, RAO, AIT |
| Consultation précoce (dans les quelques jours) | Détection de distorsions ou de scotomes à la grille d’Amsler / Changement de vision d’un œil / Augmentation soudaine des corps flottants + photopsies | Consultation chez l’ophtalmologiste dans les 1 à 3 jours pour un OCT |
| Consultation régulière | Antécédents familiaux de DMLA, antécédent unilatéral, facteurs de risque de glaucome (pression intraoculaire élevée, antécédents familiaux, forte myopie)1) | Examen ophtalmologique régulier 1 à 2 fois par an |
Aux stades précoces à modérés du glaucome, l’acuité visuelle centrale reste normale, ce qui rend très difficile la perception d’un déficit du champ visuel. En effet, l’autre œil ou le cerveau compense inconsciemment le champ manquant. Il est donc important de prendre l’habitude de vérifier sa vision en fermant un œil et de réaliser régulièrement des examens du champ visuel chez l’ophtalmologiste pour une détection précoce. Selon l’étude de Tajimi, environ 90 % des patients atteints de glaucome ne sont pas diagnostiqués1), et un dépistage régulier est recommandé à partir de 40 ans, même en l’absence de symptômes.
6. Physiopathologie des distorsions et des déficits
Section intitulée « 6. Physiopathologie des distorsions et des déficits »Mécanisme de la métamorphopsie dans les maladies maculaires
Section intitulée « Mécanisme de la métamorphopsie dans les maladies maculaires »Dans la membrane épirétinienne, les cellules gliales rétiniennes prolifèrent sur la limitante interne pour former un tissu fibreux, créant des plis à la surface de la rétine. Ces plis perturbent l’alignement des photorécepteurs, entraînant une métamorphopsie et une macropsie.
Dans la dégénérescence maculaire liée à l’âge (DMLA), l’épithélium pigmentaire rétinien (EPR) de la macula est d’abord endommagé, entraînant la formation de drusen et des anomalies de l’EPR. Dans la DMLA atrophique, l’évolution vers une atrophie géographique (AG) entraîne une perte des photorécepteurs, tandis que dans la DMLA exsudative, la formation de néovascularisation choroïdienne (NVC) provoque des hémorragies et des exsudats qui endommagent la macula. Ce processus entraîne une perte de fonction des photorécepteurs, une métamorphopsie et un scotome central.
Trou maculaire : une perte de pleine épaisseur de la fovéa entraîne un scotome central et une métamorphopsie.
Choriorétinopathie séreuse centrale (CSC) : une hyperperméabilité choroïdienne provoque une accumulation de liquide sous l’EPR et sous la rétine neurosensorielle, soulevant localement la macula. Ce soulèvement modifie la distance focale, entraînant une métamorphopsie et une micropsie2).
Mécanisme des déficits du champ visuel dans le glaucome
Section intitulée « Mécanisme des déficits du champ visuel dans le glaucome »Dans le glaucome, les fibres du nerf optique dégénèrent et disparaissent en raison de lésions axonales au niveau de la tête du nerf optique, de la compression mécanique due à la pression intraoculaire et de l’ischémie1). La perte de champ visuel correspond aux zones rétiniennes des fibres disparues, se manifestant typiquement par des scotomes arqués et paracentraux. La préservation de l’acuité visuelle centrale jusqu’aux stades avancés est la principale cause du retard de prise de conscience.
Physiopathologie du décollement de rétine
Section intitulée « Physiopathologie du décollement de rétine »Dans le décollement de rétine rhegmatogène, une traction rétinienne due au décollement postérieur du vitré forme une déchirure rétinienne. Le vitré liquéfié pénètre dans l’espace sous-rétinien par la déchirure, décollant la rétine neurosensorielle de l’EPR9). Les photorécepteurs de la rétine décollée deviennent ischémiques, entraînant une perte du champ visuel correspondant. Le décollement de la macula réduit considérablement l’acuité visuelle, et une évolution prolongée rend la récupération visuelle difficile.
7. Traitements et recherches récents
Section intitulée « 7. Traitements et recherches récents »Nouvelle génération d’anti-VEGF (faricimab)
Section intitulée « Nouvelle génération d’anti-VEGF (faricimab) »Dans les essais randomisés TENAYA/LUCERNE de Heier et al. (2022), le faricimab, qui inhibe doublement le VEGF-A et l’angiopoïétine-2 (Ang-2), a montré une non-infériorité pour la DMLA exsudative avec des injections espacées jusqu’à 16 semaines10). L’allongement de l’intervalle entre les injections devrait réduire la charge pour les patients.
Inhibiteurs du complément pour la DMLA atrophique (atrophie géographique)
Section intitulée « Inhibiteurs du complément pour la DMLA atrophique (atrophie géographique) »Le pegcetacoplan, un inhibiteur du C3 du complément, a montré dans un essai de phase 2 pour la DMLA atrophique (atrophie géographique) un effet de ralentissement de l’expansion de la surface de l’AG par rapport au placebo11). La DMLA atrophique n’avait jusqu’à présent aucun traitement efficace, et cette molécule suscite l’intérêt comme nouvelle option thérapeutique.
Efficacité du pelage de la membrane limitante interne dans la chirurgie de la membrane épirétinienne
Section intitulée « Efficacité du pelage de la membrane limitante interne dans la chirurgie de la membrane épirétinienne »Dans une revue systématique et méta-analyse d’Azuma et al. (2017), l’ajout du pelage de la membrane limitante interne (ILM) à la chirurgie de la membrane épirétinienne a amélioré l’acuité visuelle postopératoire et les résultats anatomiques12). Une réduction du risque de récidive a également été rapportée.
Détection précoce de la DMLA par dispositif de télésurveillance à domicile
Section intitulée « Détection précoce de la DMLA par dispositif de télésurveillance à domicile »L’étude HOME de Chew et al. (2014) (essai contrôlé randomisé) a montré que le dispositif de télésurveillance à domicile (ForeseeHome) permettait de détecter plus précocement la transition vers la DMLA exsudative par rapport aux soins habituels, contribuant ainsi à améliorer le pronostic visuel 13). La surveillance quotidienne par le patient lui-même à l’aide de technologies numériques devrait se généraliser à l’avenir.
8. Références
Section intitulée « 8. Références »- Iwase A, Suzuki Y, Araie M, et al. The prevalence of primary open-angle glaucoma in Japanese: the Tajimi Study. Ophthalmology. 2004;111(9):1641-1648.
- Daruich A, Matet A, Dirani A, et al. Central serous chorioretinopathy: recent findings and new physiopathology hypothesis. Prog Retin Eye Res. 2015;48:82-118.
- 日本糖尿病眼学会. 糖尿病網膜症診療ガイドライン(第1版). 日眼会誌. 2020;124(12):955-981.
- Ehlers JP, Fekrat S. Retinal vein occlusion: beyond the acute event. Surv Ophthalmol. 2011;56(4):281-299.
- Hayreh SS. Acute retinal arterial occlusive disorders. Prog Retin Eye Res. 2011;30(5):359-394.
- Zhang X, Kedar S, Lynn MJ, et al. Homonymous hemianopia in stroke. J Neuroophthalmol. 2006;26(3):180-183.
- Biousse V, Trobe JD. Transient monocular visual loss. Am J Ophthalmol. 2005;140(4):717-721.
- Faes L, Bodmer NS, Bachmann LM, et al. Diagnostic accuracy of the Amsler grid and the preferential hyperacuity perimetry in the screening of patients with age-related macular degeneration: systematic review and meta-analysis. Eye (Lond). 2014;28(7):788-796.
- Feltgen N, Walter P. Rhegmatogenous retinal detachment—an ophthalmologic emergency. Dtsch Arztebl Int. 2014;111(1-2):12-22.
- Heier JS, Khanani AM, Quezada Ruiz C, et al. Efficacy, durability, and safety of intravitreal faricimab up to every 16 weeks for neovascular age-related macular degeneration (TENAYA and LUCERNE): two randomised, double-masked, phase 3, non-inferiority trials. Lancet. 2022;399(10326):729-740.
- Liao DS, Grossi FV, El Mehdi D, et al. Complement C3 inhibitor pegcetacoplan for geographic atrophy secondary to age-related macular degeneration: a randomized phase 2 trial. Ophthalmology. 2020;127(2):186-195.
- Azuma K, Ueta T, Eguchi S, et al. Effects of internal limiting membrane peeling combined with removal of idiopathic epiretinal membrane: a systematic review of literature and meta-analysis. Retina. 2017;37(10):1813-1819.
- Chew EY, Clemons TE, Bressler SB, et al. Randomized trial of the ForeseeHome monitoring device for early detection of neovascular age-related macular degeneration. The HOME Study. Ophthalmology. 2014;121(2):535-544.
