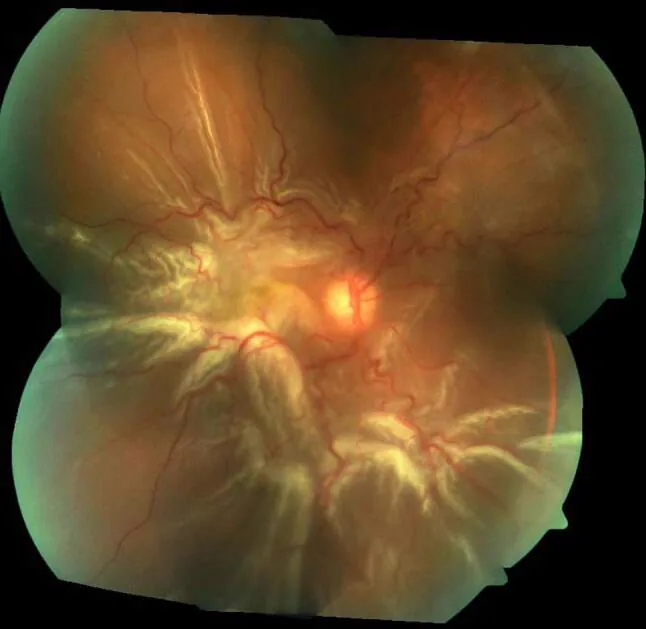
裂孔原性網膜剥離は網膜裂孔 を介して液化硝子体 が網膜 下腔に流入し、神経網膜 が色素上皮から分離する眼科的緊急疾患である。
発症率は人口1万人当たり年間1〜1.5人。近視 (原因の40〜80%)・格子状変性 ・後部硝子体剥離 が主要リスクである。
飛蚊症 ・光視症 の急激な増悪や視野欠損 (カーテン感)は緊急受診を要するサインである。診断は散瞳 下倒像鏡検査 と強膜 圧迫が基本。Shafer’s sign(前部硝子体 のtobacco dust様色素)は裂孔発症を強く示唆する。
手術(強膜バックリング術 ・硝子体 切除術・気体網膜復位術 )が唯一の根治法。初回手術で90%以上が復位し、複数回手術で98%に達する。
黄斑 が剥離すると不可逆的な視細胞 変性が始まる。黄斑 前剥離での緊急手術が視力 予後を左右する。増殖性硝子体網膜症 (PVR )は最大の合併症であり、適切な術式選択と過剰凝固の回避が予防の鍵となる。 裂孔原性網膜剥離(Rhegmatogenous Retinal Detachment; RRD)は、網膜 に裂孔が形成されて液化硝子体 が網膜 下腔に侵入し、神経網膜 (感覚網膜 )が網膜色素上皮 (RPE )層から剥離する病態である。rhegmatogenousはギリシャ語の「裂け目」に由来する。
網膜剥離 には3つの型がある。裂孔原性(RRD)は最も頻度が高く、牽引性(TRD:増殖膜 による機械的牽引)および滲出性(ERD:脈絡膜 ・網膜 血管からの滲出液貯留)と区別される。本記事では裂孔原性を中心に解説する。
滲出性網膜剥離 は裂孔を伴わず、体位変換で剥離部位が移動するshifting fluidが特徴的である。治療は原因疾患の治療が主体であり、裂孔原性とは根本的に異なる。
滲出性網膜剥離
血液網膜関門の破綻による非裂孔原性網膜剥離の病態と治療
裂孔閉鎖による修復の概念は1920年代にJules Goninによって確立された。それ以前の治癒率は5%未満であったが、Goninのイグニパンクチャー(熱凝固)により30〜60%へと向上した。その後の発展は以下のとおりである。
1949年 :Ernst Custodisがポリビオール製バックルを報告1950年代 :Charles Schepensがシリコーンゴム素材・倒像検眼鏡・冷凍凝固 術を普及させ、強膜バックリング術 の基礎を確立Harvey Lincoff :裂孔位置推定のLincoffの法則を確立1960年代後半 :Robert Machemerが閉鎖系硝子体 切除術(PPV )を開発2002年〜 :25G微小切開硝子体手術 (MIVS)が登場し、近年は27Gへの超小切開化も進む
現在では初回手術復位率90%超、複数回手術で98%に達している。
発症率 :人口1万人当たり年間1〜1.5人(0.01〜0.015%)2) 両眼性 :約10%家族内発症 :約20%年齢分布 :2峰性。20歳代ピーク(格子状変性 内の萎縮円孔による扁平な剥離)と50歳代ピーク(急性後部硝子体剥離 に伴う弁状裂孔 による丈の高い剥離)がある近視 との関連近視 が占める発症率の増加傾向 :ドイツのレジストリデータでは年間発症率が15.6から24.8/10万人へと増加傾向にあり、2) 高齢化・近視 人口増加・白内障 手術件数増大が背景として挙げられる白内障 手術後のリスク白内障 手術歴がある。術後RRDリスクは約0.21%(約1/500)であり、術式改善に伴い低下傾向にある2) 外傷性 :RRD全体の約10%を占め、若年男性に多い2) 黄斑円孔 網膜剥離 強度近視 の女性に多く、全網膜剥離 症例の約5%を占める(欧米の0.5〜2.0%と比べて高い)
Q
裂孔原性網膜剥離はどのくらい珍しいのか?
A
人口1万人あたり年間1〜1.5人の発症率であり、比較的まれな疾患である。ただし近視 人口が多い地域・集団では発症数が増加傾向にある。約10%は両眼に発症するため、片眼に手術を受けた患者では対側眼の定期的な観察が重要である。
裂孔原性網膜剥離の眼底写真。広範な剥離網膜とPVRによるstar foldsを認める。 Xiong J, et al. A review of rhegmatogenous retinal detachment: past, present and future. Wien Med Wochenschr. 2025. Figure 3. PM
CI D: PMC12031774. License: CC BY.
飛蚊症 後部硝子体剥離 による硝子体混濁 。飛蚊症 の約6%に網膜裂孔 が認められる。急激な増加・新たな形状の出現は要注意。光視症 網膜 が硝子体 で牽引されることで生じる。暗所で増強し、閉瞼時でもみられ、眼球運動で誘発される。光視症 は裂孔の反対側に生じるため、発生部位の問診が原因裂孔の位置推定に役立つ。視野欠損 緑内障 の進行や眼瞼下垂 と誤りやすい。視力 低下・変視症 網膜剥離 が黄斑部 に及ぶと出現する。
眼圧 脈絡膜 剥離を伴うとより顕著に低下する。Schwartz症候群 :眼圧 上昇を伴う網膜剥離 。剥離網膜 から脱落した視細胞 外節が線維柱帯 に詰まって生じる。Shafer’s sign :前部硝子体 に浮遊するtobacco dust様色素(網膜色素上皮 細胞由来)。裂孔発症を強く示唆する重要所見。前房 所見
弁状裂孔(馬蹄形裂孔)
硝子体 牽引により網膜 が引き裂かれた孔。網膜 フラップが馬蹄形を呈する。
中高年の後部硝子体剥離 に伴い**耳側上方60%**に好発する。丈の高い剥離を起こしやすい。
operculum伴う円孔
硝子体 牽引により裂孔フラップが完全に外れて形成。外れたフラップ(operculum)が硝子体 内に浮遊する。
牽引が解除されるため進行は遅め。ただし開大した孔から液化硝子体 が流入しやすい。
萎縮円孔
格子状変性 内の網膜 の萎縮性変化で生じる。蓋(operculum)を伴わない。
若年者・女性・高度近視 に多い。硝子体 牽引を伴わないため進行が緩徐なことが多い。
裂孔の好発部位は網膜 周辺部であり全体の2/3を占める。象限別では耳側上方60%、耳側下方15%、鼻側上方15%、鼻側下方10%である。
Q
光視症が出たらすぐ受診すべきか?
A
光視症 は後部硝子体剥離 に伴う網膜 牽引の徴候であり、裂孔形成の前駆症状となりうる。特に飛蚊症 と同時に出現した場合や、視野欠損 が加わった場合は当日受診が望ましい。急性PVD 症状で受診した患者の5.4〜8%に網膜裂孔 が認められ、硝子体出血 を伴う場合は2/3に裂孔が発見される。2)
裂孔原性網膜剥離の発症には(1)網膜 に孔的存在があること、(2)硝子体 の液化の2つが絶対条件である。網膜 に孔が生じるには、網膜 に菲薄化した変性巣があるか、硝子体 牽引や強い外力が眼球に及ぶ必要がある。
近視 近視 (-1〜-3D)で約4倍、-3D超で約10倍のリスク上昇が報告されている。2) 眼軸 延長に伴う周辺網膜 の菲薄化が主な機序である。格子状変性 (lattice degeneration)網膜剥離 患者の眼の約30%に認められる。2) RRD全体の20〜30%に関与する。有症状馬蹄形裂孔 は未治療で少なくとも半数がRRDに進行するが、レーザー光凝固 で5%未満に抑制できる。無症状馬蹄形裂孔 の自然経過でのRRD移行率は約5%である。2) 後部硝子体剥離 (PVD )PVD に伴う硝子体 牽引が弁状裂孔 形成の主要機序。高齢者では生理的変化として生じる。硝子体出血 を伴う患者の約88%では上方象限に裂孔が認められる。2) 白内障 手術歴白内障 手術歴がある。2) 術後RRDリスクは約0.21%であり、後嚢Nd:YAGレーザー切開後は約4倍に上昇する。2) 外傷 :RRD全体の約10%を占める。2) 若年男性に多く、鋸状縁 断裂・巨大裂孔の主要原因となる。対側眼の既往 :約10%に両眼性発症がある。遺伝性結合組織疾患 :Stickler症候群・Marfan症候群・Ehlers-Danlos症候群では早期発症・重篤化に注意する。Stickler症候群では360°予防的レーザー光凝固 が推奨される。2)
以下のリスクが高い網膜裂孔 は予防的レーザー網膜光凝固術 の積極的対象となる。
飛蚊症 や光視症 などの自覚症状がある網膜裂孔 網膜剥離 の僚眼に発症した網膜裂孔 無水晶体 眼や眼内レンズ 挿入眼・白内障 手術前の網膜裂孔
網膜剥離 の家族歴がある網膜裂孔
格子状変性 に対する予防的治療の危険因子:①僚眼の網膜剥離 の既往、②無水晶体 眼または眼内レンズ 挿入眼、③高度の格子状変性 を伴った強度近視 眼、④網膜剥離 の家族歴、⑤Marfan症候群・Stickler症候群・Ehlers-Danlos症候群の合併。
レーザー光凝固 の条件:0.2秒、150 mW、200 μmから少しずつパワーを上げ、厚白色程度の凝固斑とする。格子状変性 に対しては三面鏡または広角倒像コンタクトレンズを用いて病巣部を隙間のない2〜3列の凝固斑で囲む(凝固サイズ400〜500 μm)。
Q
近視の人は全員網膜剥離になるのか?
A
近視 はRRDの最大リスク因子だが、発症率は人口の0.01〜0.015%であり、近視 があっても大半は発症しない。ただし強度近視 (-6D以上)では格子状変性 の合併率が高く、格子状変性 内の萎縮円孔からRRDに至るのは0.3〜0.5%と報告されている。定期的な眼底検査 が特に重要となる。
診断は倒像鏡および前置レンズや三面鏡を用いた細隙灯顕微鏡による眼底検査 を行い、剥離した網膜 と原因裂孔を確認する。細隙灯顕微鏡では硝子体 の観察も同時に行い、後部硝子体剥離 の有無・裂孔への硝子体 牽引を評価する。黄斑部 に剥離が及んでいるかどうかは術後の視力 予後に影響するため、必ず確認する。
外来診察では双眼倒像鏡による強膜 圧迫併用検査が最も有用であり、裂孔と偽裂孔の鑑別・裂孔周囲の網膜下液 の有無・剥離範囲の評価が方針決定において極めて重要である。
問診では以下の情報が診断と治療方針決定に重要である:2)
光視症 ・飛蚊症 の有無と発症時期視野欠損 の有無と範囲(カーテン感の方向)近視 の有無と程度眼手術歴(白内障 手術・Nd:YAGレーザー後嚢切開)
外傷歴
家族歴(RRD・Stickler症候群)
OCT (光干渉断層計 )黄斑部 の微細な剥離を検出する。網膜分離症 との鑑別・黄斑 下液の有無の確認に有用。2) 術後視力 予後の予測にも活用される。Bスキャン超音波 :硝子体出血 などの混濁媒体が存在する場合に必須。剥離範囲・形態・増殖膜 の評価が可能。2)
剥離の形態から原因裂孔の位置を推定する実用的な法則である。
剥離の形態 予測される裂孔位置 的中率 耳側または鼻側の上方剥離 高い方の境界から1.5時計時間以内 98% 12時を越えて両側に下降する上方剥離 12時頂点の三角形内 93% 下方剥離 高い境界側に裂孔 95% 下方水疱性剥離 上方裂孔に由来する —
網膜分離症 (Retinoschisis)網膜 層間の分離。OCT で内層・外層の2葉構造を確認。外層に穿孔がなければ剥離は生じない。滲出性網膜剥離 Vogt-小柳-原田病 ・脈絡膜 腫瘍等)の同定が重要。牽引性網膜剥離 増殖糖尿病網膜症 等で生じる。脈絡膜 剥離眼圧 低下時に生じる。超音波で厚みのある脈絡膜 剥離を確認。
Q
眼底検査だけで診断できるか?
A
倒像鏡による散瞳 眼底検査 が診断の基本であるが、硝子体出血 などで眼底透見が不良な場合はBスキャン超音波が必須となる。また黄斑部 の微細な剥離はOCT による補助が有用である。裂孔の完全な同定のために強膜 圧迫法を組み合わせた全周検査が推奨される。
網膜剥離 は緊急的な手術治療が原則である。治療の必須条件は裂孔の完全閉塞であり、裂孔が残存すると再剥離を生じる。初回手術で90%以上が、複数回の手術で98%が復位する。
術後視力 は術前の黄斑部 剥離の有無・剥離期間に大きく左右される。黄斑部 が既に剥離している症例では可及的速やかに手術を予定する。適切な時期に手術を行えば95%以上が治癒するが、網膜 復位後の視力 は約半数が0.5以下であり、視野欠損 や歪視症が残ることも多い。
Cochrane系統的レビューおよびメタ解析では、硝子体手術 (PPV )と強膜バックリング術 (SB)の解剖学的・視力 転帰に有意差はなく(低〜極めて低いエビデンス)、術式選択は個々の症例の特性に基づいて判断する。2)
黄斑 が剥離すると視細胞 の不可逆的変性が始まる。黄斑 非剥離型では術後2ヶ月で73%が矯正視力 0.5以上を達成する。黄斑 剥離型では約半数の視力 が0.5以下にとどまる。
術前の体位保持が黄斑 への液流入を抑制しうる:
上方の胞状剥離がある場合 → 仰臥位(トレンデレンブルグ体位)
下方剥離の場合 → 座位
年齢・後部硝子体剥離 の有無・裂孔の位置と大きさなどで術式選択を行う。
若年者の萎縮性円孔 :強膜バックリング術 (強膜 アプローチ)が第一選択中高年の弁状裂孔 :硝子体手術 (硝子体 アプローチ)が主体難治性PVR 合併 :シリコーンオイル タンポナーデが必要限局した上方裂孔 :外来での気体網膜復位術 も選択肢となる
眼球外側の強膜 にシリコン素材のバックルを縫合固定し、眼球壁を内側へ圧迫陥凹させて裂孔を閉鎖する眼外手術である。
適応 :
若年者・有水晶体 眼・単純なRRD
裂孔が周辺部に限局
水晶体 温存が可能な症例
手技の流れ :
結膜 切開・外眼筋 の露出冷凍凝固 (cryotherapy):裂孔辺縁と変性部位に最小限の凝固を加える。過剰凝固はPVR 促進の要因となるため回避するバックルの選択と設置:局所バックル(単一裂孔)または輪状締結(多発裂孔・PVR 合併例)
バックル材料 形状 主な用途 シリコンスポンジ 局所隆起型 単一・局所裂孔 シリコンバンド 帯状・輪状 輪状締結・360°バックル シリコンタイヤ 幅広の帯状 広範囲裂孔・格子状変性
網膜下液 の排液(必要時):高い網膜下液 貯留がある場合に強膜 部分切開で排液する。非排液法(non-drainage technique)も選択可能で合併症リスクが低いガス注入(必要時):SF₆・C₃F₈による内方タンポナーデを追加
成績 :初回解剖学的復位率90%以上。有水晶体 眼では硝子体手術 と比べて視力 転帰が優れる可能性があり、5, 6) 黄斑 非剥離型に限ればSBが有意に良好な転帰を示すとの報告がある。6)
主な合併症 :再剥離、PVR 、SINS(バックル誘発性の感染・壊死・皮膚露出)、4) 屈折 変化(近視 化)、眼球運動障害 ・複視 。
適応 :
複数裂孔・下方裂孔
増殖硝子体網膜症 (PVR )合併混濁媒体・後極部病変
中高年の弁状裂孔
方法 :硝子体 切除後に裂孔を封鎖し、ガス(20% SF₆・14% C₃F₈)またはシリコーンオイル による内タンポナーデを行う。
成績 :初回解剖学的復位率は強膜バックリング術 と同等。2) 白内障 促進が短所であり、有水晶体 眼の若年者では慎重な適応が必要である。
黄斑 非剥離型の術中黄斑 保護黄斑 が剥離していない症例では術中の黄斑 保護が特に重要である。
バルブ付きカニューレによる術中眼圧 変動の防止
大きな開放裂孔を通じた灌流液の網膜 下流入の回避
胞状剥離がある場合には先に排液用網膜 切開でSRFを減少させる
後極部にパーフルオロカーボン液(PFCL)を配置し中心窩 下への液移動を防止
完全な液ガス置換前にSRFを十分排液(不十分な場合に黄斑 剥離を惹起することがある)
スチームローラー法 :黄斑 近傍の胞状剥離で、ガスを黄斑 を越えて転がすことで医原性黄斑 剥離を防止する手技。黄斑 非剥離型RRDにおける独自の術中管理法として知られる。
膨張性ガスを硝子体 内に注入し、ガスの浮力で裂孔を閉鎖した後、冷凍凝固 または光凝固で裂孔周囲を瘢痕化させる外来処置である。
適応 :
上方(10時〜2時方向)120〜180°の範囲内に裂孔が収まるRRD
弁状裂孔 (1つまたは近接した集簇裂孔)PVR B以下術後の体位保持が可能な患者
ガスの種類と特性 :
ガス 注入量 膨張倍率 眼内滞留期間 SF₆(六フッ化硫黄) 0.5〜0.6 mL 約2倍 約2週間 C₃F₈(八フッ化プロパン) 0.3 mL 約4倍 約8週間
手技の流れ :
散瞳 ・点眼麻酔(または球後麻酔 )凝固処置(冷凍凝固 先行または光凝固をガス注入後に施行)
前房穿刺 :27〜30G針で房水 0.2〜0.4 mLを排出ガス注入:耳側毛様体 扁平部(有水晶体 眼では輪部 後方4mm)より注入
眼圧 ・血流確認:中心網膜 動脈の血流を確認。拍動消失が数分続く場合は再減圧体位指導:5〜8日間の裂孔部位へのガス位置保持
PIVOT試験(PRとPPV の無作為化比較試験)の結果 :
評価項目 気体網膜復位術 (PR)群硝子体 切除術(PPV )群初回復位率 80.8% 93.2% 最終復位率 98.7% 98.6% 術後視力 (6ヶ月) 78.4±12.3文字 68.5±17.8文字 白内障 手術(12ヶ月・有水晶体 眼)16% 65%
最終復位率はほぼ同等であり、術後視力 ・変視症 の少なさはPR群が優位であった。
主な合併症 :網膜 下ガス迷入(フィッシュエッグ現象)、10) 新裂孔形成、中心網膜 動脈閉塞、白内障 進行。
排液を行わない分節的強膜バックリング術 であり、裂孔原性網膜剥離の約90%に適用可能とされる。初回復位率91%、再手術後97.4%、PVR 発生率0.9%と良好な成績が報告されている。
適応外となるのは以下の場合である:
異なる緯度に存在する複数裂孔
後方裂孔
70°超の広範囲剥離
巨大裂孔
C2超のPVR
術式 主な適応 初回復位率 特徴 強膜 バックリング 若年・萎縮円孔・単純RRD 90%以上 水晶体 温存・眼外手術硝子体手術 複雑・多裂孔・PVR 90%前後 広範囲対応・白内障 促進 気体網膜復位術 上方限局裂孔 80.8% 外来・体位制限・視力 良好 Lincoff-Kreissig法 RRDの約90% 91% 非排液・最小侵襲
増殖性硝子体網膜症 (PVR )の重症度に応じて術式を選択する。
Grade A・B・軽度C :強膜バックリング術 で治療可能なことが多い網膜 固定皺襞が裂孔近傍・後極に位置する症例、深部裂孔硝子体手術 を選択タンポナーデ材料 :20% SF₆、14% C₃F₈、またはシリコーンオイル
眼内ガス残存中の航空機搭乗・急速な高所移動は禁忌。気圧変化でガスが膨張し眼圧 が急上昇して中心網膜 動脈閉塞を起こす危険がある。SF₆では注入後約2週間、C₃F₈では約8週間が禁忌期間の目安。
黄斑部 剥離がある場合は待機せず早急に手術を予定する。全身麻酔を受ける場合は眼内ガスの存在を必ず麻酔科医に伝えること。亜酸化窒素(笑気)はガスを膨張させるため禁忌となる。
Q
手術後の視力はどの程度回復するか?
A
初回手術で90%以上が解剖学的に復位するが、術後視力 は約半数が0.5以下であり、視野欠損 や歪視症が残ることも多い。視力 予後を決定する最大因子は黄斑部 剥離の有無と持続期間である。黄斑 剥離前の早期手術では視力 予後が良好だが、黄斑 剥離後でも早期手術ほど良好な転帰が期待できる。
Q
硝子体手術とバックリング術はどちらが良いか?
A
有水晶体 眼の単純なRRD(特に若年者)では強膜バックリング術 の視力 転帰が優れる可能性がある。2, 5, 6) PVR が高度な場合・後極に裂孔がある複雑なRRDでは硝子体手術 が選択される。術式の選択は裂孔の性状・位置・PVR 重症度・患者背景・術者の習熟度を総合して判断する。
裂孔原性網膜剥離の発症条件は(1)網膜 の「孔」的存在と(2)硝子体 液化の2つである。
弁状裂孔 の形成後部硝子体剥離 による硝子体 牽引が格子状変性 や硝子体 強付着部に集中する。格子状変性 や硝子体 強付着部位が存在すると裂孔形成に至る。耳側上方60%に好発する。
萎縮円孔の形成 :硝子体 牽引を伴わず、格子状変性 内の網膜 菲薄化・壊死から形成される。若年者・女性・高度近視 に多い。後部硝子体剥離 前に生じるため硝子体 が残存しており、進行が緩徐なことが多い。
網膜剥離 が生じると視細胞 と網膜色素上皮 細胞は分断され、脈絡膜 からの酸素と栄養供給が阻害される。発症早期から視細胞 外節の変性と脱落が生じ、次第に不可逆性変性に至る。
網膜下液 が黄斑部 へ進展する主な要因を以下に示す。
重力 :上方裂孔からの液は重力によって黄斑部 に向かいやすい。下方剥離では重力が黄斑 到達を遅らせる眼球運動の慣性力 :サッカード(急速眼球運動)が裂孔縁に牽引力を加え、液の流入を促進する。術前の安静が有効とされる理論的根拠である硝子体 液化の程度硝子体 が流入しやすく胞状剥離として急速に進行する。若年者では硝子体 がゲル状のため、流入が緩徐で扁平な剥離になることが多い
排液を行わず強膜 バックリング のみで網膜 を復位させる機序は以下のとおりである。
眼壁と網膜 の中央移動による硝子体 網膜 牽引の減少
バックル位置からの網膜下液 の移動(眼底周辺部への再分布)
術後のバックル高さの増加による更なる効果
裂孔と隣接する硝子体 ゲルの接近
裂孔を通過する流体流に対する抵抗増加
PVR はRRD術後の最大の合併症であり、網膜 前・網膜 下の増殖膜 形成による牽引性再剥離として定義される。
機序:網膜剥離 →血液網膜関門 の破綻→RPE 細胞・グリア細胞・マクロファージが硝子体 腔に流出→TGF-βなどのサイトカイン刺激→細胞の上皮間葉転換と増殖→収縮性膜形成→再剥離。
RPE は線維芽細胞様に形質転換してコラーゲンを産生し、膜状・索状の増殖組織を形成する。旧分類(Retina Society 1983)によるPVR 重症度分類は以下のとおりである。
Grade A :硝子体混濁 、硝子体 中の色素塊、網膜 上の色素塊Grade B :網膜 表層皺襞の形成、網膜 血管の蛇行、裂孔縁の立ち上がり、硝子体 の可動性低下Grade C :網膜 全層皺襞(C-1: 1象限、C-2: 2象限、C-3: 3象限)Grade D :4象限にわたる網膜 全層皺襞(D-1: 広い漏斗、D-2: 狭い漏斗、D-3: 閉鎖漏斗)
1991年のMachemer新分類は前部PVR および網膜 下病変を考慮し、病変範囲を時計の時間で表記する。
Arndtら(2023)は非糖尿病RRD73名とERD64名を対象とした研究で、RD眼の硝子体 内グルコース濃度(2.28 mmol/L)がERM 眼(1.60 mmol/L)より有意に高値(p<0.0001)であることを報告した。1) 硝子体 内グルコースはマクロファージ密度と有意に相関し(p=0.002)、RD範囲とも相関した(r=0.38)。術後中心窩 厚(MFT)とは逆相関(r=-0.51)を示し、上皮細胞密度とPVR -Cグレードの間に有意な相関(p=0.002)が認められた。1) 終末糖化産物(AGE)によるコラーゲン架橋が硝子体 の硬直化に関与するという仮説も提唱されている。1)
Arndtら(2023)のデータはインスリンが錐体の保護的役割を果たす可能性を示唆する。1) RD眼の高グルコース環境が光受容体障害を増悪させるという仮説に基づき、代謝介入による視力 予後改善が研究課題となっている。
ドイツのレジストリデータでは年間発症率が15.6から24.8/10万人へと増加しており、高齢化・近視 人口の増加・白内障 手術件数の増大が背景要因として挙げられている。2) 白内障 術後RRDリスクは術式改善に伴い0.21%まで低下している。2)
未治療ROP 既往眼の長期観察では、18歳以下の18.4%、19〜30歳の35.1%に裂孔が認められた。3) 後部硝子体剥離 前の強い硝子体 網膜 付着が主な機序であり、網膜剥離 例では再手術率が36%と高い。小児・若年成人の背景疾患に応じた手術戦略の最適化が課題となっている。3)
広角観察システムとシャンデリア照明を組み合わせ、従来術式の視認性の制限を補う手技である。7) メタ解析では従来法と視力 ・解剖学的成功率は同等で、手術時間の短縮が示されている。9)
術後の光受容体再整列は機能的転帰に関わる可能性があり、強膜バックリング術 と硝子体手術 の術後視機能差を説明する要素として研究されている。6)
RRD修復後に発生する嚢胞様黄斑浮腫 (CME )に対して、デキサメタゾン徐放性インプラントなどの新規治療が検討されている。8)
Ahmed Iら(2025)は、RRD修復後にドルーゼン が消失した83歳女性の1例を報告した。11) 機序として網膜下液 の溶解および局所炎症応答の関与が示唆されている。
ガス注入による硝子体 黄斑 牽引(VMT )や黄斑円孔 の非手術的解除を目指す研究段階の手技である。
RCOphth iFTMH Guideline(2025年版)では、pneumatic vitreolysisによる黄斑円孔 閉鎖率は47.8%、黄斑円孔 の新規発生率は5.3%と報告されている。12)
AAO ERM /VMT PPP(2019)が引用するDRCR無作為化比較試験では、C₃F₈による硝子体 黄斑 牽引解除率が78% vs 9%(偽手術群)であったが、安全性上の懸念により試験は早期中止となっている。13) 現時点では適応が限定的であり、標準治療には至っていない。
Al-Salehら(2025)は、外傷性の黄斑 非剥離RRDに対してSF₆ガスを用いた気体網膜復位術 を施行し、24時間以内に復位達成・最終視力 20/40を報告した。14) 適切な症例選択のもとで外傷性RRDにも本術式が有効な可能性を示す。
Deanら(2023)は、硝子体手術 +強膜バックリング術 後2〜3週で悪化する炎症・角膜 後面沈着物・硝子体混濁 を呈した症例を報告した。15) ステロイド 増量とNSAIDs全身投与で改善し、術後遷延炎症の鑑別にHLA-B27検査が有用であることを示した。
Au Eongら(2024)は、写真記録で30年持続した特発性黄斑円孔 と急性macula-on RRDの併存例に対してPPV +ILM 剥離+C₃F₈タンポナーデで復位と円孔閉鎖を同時に達成した。16) 長期の視細胞 障害により視力 改善は限定的(6/45のまま)であったが、同時手術の可能性を示した報告として注目される。
3D手術用顕微鏡 :術者の姿勢負担軽減・視野共有・画像記録の容易さが利点27Gシステム(外径0.36mm) :術後乱視 誘発・創口閉鎖問題の減少眼内内視鏡 :角膜 混濁・瞳孔 散大不良例への適応拡大
Arndt C, Hubault B, Hayate F, et al. Increased intravitreal glucose in rhegmatogenous retinal detachment. Eye (Lond). 2023;37(4):638-643. doi:10.1038/s41433-022-01968-w.
American Academy of Ophthalmology. Posterior Vitreous Detachment, Retinal Breaks, and Lattice Degeneration Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2024.
Hamad AE, Moinuddin O, Blair MP, et al. Late-Onset Retinal Findings and Complications in Untreated Retinopathy of Prematurity. Ophthalmol Retina. 2020;4(6):602-612. doi:10.1016/j.oret.2019.12.015.
Jayallan B, Goswami P, Bhakat A. Rhegmatogenous retinal detachment in anterior scleritis associated with ulcerative colitis: a case report. Cureus. 2024;16(6):e61819.
Ferro Desideri L, Bonfiglio V, Russo A, et al. Scleral buckling: a review of clinical aspects and current concepts. J Clin Med. 2022;11(2):314.
Cruz-Pimentel M, Huang CY, Wu L. Scleral buckling: a look at the past, present and future in view of recent findings on the importance of photoreceptor re-alignment following retinal re-attachment. Clin Ophthalmol. 2022;16:1971-1984.
Genovese L, Crisafulli C, Mancuso S, et al. Chandelier-assisted scleral buckling: a literature review. Vision (Basel). 2023;7(3):47.
Bernardi E, Shah N, Ferro Desideri L, et al. Cystoid macular edema following rhegmatogenous retinal detachment repair surgery: incidence, pathogenesis, risk factors and treatment. Clin Ophthalmol. 2025;19:629-639.
Ziafati M, Mirshahi R, Sanadgol N, et al. Functional outcome of chandelier-assisted scleral buckling in rhegmatogenous retinal detachment: a systematic review and meta-analysis. J Curr Ophthalmol. 2025;37:172-182.
Wang JC, Tang WM, Eliott D. Management of large subretinal gas bubble after pneumatic retinopexy with head-positioning maneuver. J VitreoRetin Dis. 2022;6(2):167-170.
Ahmed I, Wu DM. Drusen Disappearance After Retinal Detachment Repair. J VitreoRetin Dis. 2025;9(1):109-112. doi:10.1177/24741264241276603.
Royal College of Ophthalmologists. Idiopathic Full Thickness Macular Holes. Clinical Guideline. London: RCOphth; 2025. Available from: https://www.rcophth.ac.uk/resources-listing/idiopathic-full-thickness-macular-holes/
American Academy of Ophthalmology. Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2019.
Al-Saleh A, Al-Otabi A, Al-Shammari Y, et al. Successful management of macula-sparing retinal detachment following blunt ocular trauma using pneumatic retinopexy. Cureus. 2025;17(6):e85709.
Dean J, McTavish S, Feng Y, et al. Persistent inflammation associated with HLA-B27 after pars plana vitrectomy with scleral buckle placement. J VitreoRetinal Dis. 2023;7(6):557-561.
Au Eong JTW, Lim JHM, George SM, et al. Successful anatomical closure of a photographically documented 30-year-old idiopathic full-thickness macular hole following surgery for concurrent repair of an acute macula-on rhegmatogenous retinal detachment. J Surg Case Rep. 2024;4:rjae231.