基本手順(仰臥位)
仰臥位が基本。以下の順で行う。
- 患者をストレッチャー等に仰臥位にする
- BIOヘッドセットを装着し,照明輝度を適切に調整する(過度に明るいと瞳孔が収縮)
- 患者の胸部にスケッチ用ボードを置く
- 20Dレンズを患者眼前約6〜8 cmの位置に保持する
- 反射光を利用して眼底像をレンズ内に捕捉する
- 上方→下方→耳側→鼻側→黄斑→視神経乳頭の順に系統的に観察する
- 観察しながらスケッチに所見を記録する

双眼倒像鏡検査(Binocular Indirect Ophthalmoscopy: BIO)は,頭部装着型の照明付きヘッドセットを用いて散瞳下に眼底を両眼立体視する眼底検査の基本手技である。集光レンズ(通常20Dまたは25D)を患者眼前に保持し,眼底の倒立実像を眼前に形成して観察する。倍率は使用レンズにより2〜4倍,視野は30〜60°と広く,周辺網膜の全周観察が可能である。
直像鏡に比べて倍率は低いが,広い視野と立体視,強膜圧迫との組み合わせにより,周辺部の網膜裂孔・網膜剥離・格子状変性を高い感度で検出できる。網膜硝子体疾患の診療において欠くことのできない検査であり,網膜剥離術前の全周詳細眼底評価はBIOなくして行えない。米国眼科学会(AAO)のPreferred Practice Pattern 2025 でも,急性後部硝子体剥離・網膜裂孔・格子状変性の評価において散瞳下のBIOと強膜圧迫が推奨されている[2]。
双眼倒像鏡の最大の特長は,集光レンズと強膜圧迫子をそれぞれ両手に持てる点にある。強膜を圧迫しながら網膜を立体的に観察し,圧迫による動的観察(網膜の動き・剥離の程度)や接線方向からの観察(裂孔辺縁の立ち上がり)が可能となる。これらの所見は単眼倒像鏡や前置レンズ法では得ることができない。
BIOの習熟には相応のトレーニングが必要であり,「双眼倒像鏡による眼底検査は面倒なうえに習熟するのに時間がかかるため敬遠されることが多いが,ほかの検査法では得ることのできない多くの所見を観察できる。診断の精度を上げ,正しい治療法の選択のためには必ず必要な検査である」とされている。実際,倒立逆像による空間定位の困難さがレジデントの習熟を妨げる主因とされ,近年は拡張現実シミュレータを用いた教育法の有効性も報告されている[8]。
また,Charles L. Schepens は1945年に双眼倒像鏡を開発し,網膜剥離診療に革命をもたらしたことから「網膜剥離の父」と称される[1]。
倒像鏡では眼底の倒立実像(上下反転・左右反転)が検者の眼前に形成される。すなわち上方網膜が視野の下方に,右側網膜が左側に見える。これは光学的に正確な現象であり,検者は訓練を重ねることにより倒立像を自動的に読み替えながら観察する。慣れるまでは空間的な方向把握に戸惑うが,眼底スケッチを並行して行いながら習熟するのが一般的な手順である。
倒像鏡は直像鏡・前置レンズ法(細隙灯顕微鏡+凸レンズ)と目的に応じて使い分けられる。
| 項目 | 直像鏡 | 双眼倒像鏡(BIO) | 前置レンズ法(78D/90D) |
|---|---|---|---|
| 倍率 | 約15倍 | 約2〜4倍 | 約6〜8倍 |
| 視野 | 約10° | 約30〜60° | 約20〜30° |
| 像の方向 | 正立像 | 倒立・左右反転像 | 倒立像(非接触) |
| 立体視 | なし | あり | あり |
| 散瞳の要否 | 不要(小瞳孔可) | 必要 | 必要(推奨) |
| 周辺網膜観察 | 困難 | 優れている | 赤道部まで良好 |
| 強膜圧迫 | 不可 | 可能 | 不可 |
| 主な用途 | スクリーニング・乳頭観察 | 周辺網膜・剥離・裂孔 | 乳頭・黄斑・ガラス体 |
使い分けの原則として,網膜周辺部の裂孔・剥離・変性の検索には倒像鏡が最適であり,視神経乳頭や黄斑部の詳細評価には前置レンズ法が適する。スクリーニング目的の簡易観察には直像鏡が用いられることもある。
BIOは以下の光路によって倒立実像を形成する。
集光レンズの屈折力(D値)が大きいほど焦点距離が短くなり,倍率は低下するが視野は広くなる。倍率の概算は「眼球の屈折力(約60D)÷ 集光レンズのD値」で求められる。
| レンズ | 焦点距離 | 倍率(概算) | 視野 | 主な用途 |
|---|---|---|---|---|
| 14D | 約71 mm | 約4.3倍 | 約37° | 乳頭・黄斑の詳細観察 |
| 20D | 約50 mm | 約3倍 | 約45° | 成人の標準的な眼底検査 |
| 25D | 約40 mm | 約2.4倍 | 約50° | 未熟児・小児 |
| 28D | 約36 mm | 約2.3倍 | 約53° | 周辺網膜の広角観察 |
| 30D | 約33 mm | 約2倍 | 約60° | 最周辺部・小瞳孔 |
レンズと患者眼の距離は焦点距離に相当する約5〜8 cmが目安となる。散瞳が十分なほど(瞳孔径が大きいほど)立体視の質が向上する。
倒像鏡は照明光と観察光の両方が瞳孔を通過する構造上,散瞳径が大きいほど明るく広い眼底像が得られる。小瞳孔(4 mm未満)では観察可能な視野が制限され,特に周辺部の強膜圧迫が行いにくくなる。
散瞳薬を点眼し,完全散瞳後に検査を開始する。
標準的な散瞳薬: トロピカミド0.5%(ミドリンM®)+フェニレフリン塩酸塩0.5%の配合点眼液(ミドリンP®)
基本手順(仰臥位)
仰臥位が基本。以下の順で行う。
強膜圧迫手順(周辺網膜検索)
赤道部より周辺は強膜圧迫を追加する。
強膜圧迫を併用したBIOは周辺網膜裂孔の検出におけるゴールドスタンダードであり[3],非接触細隙灯検査では急性の馬蹄形裂孔が見逃されうるとの報告がある[5]。一方,超広角眼底撮影(UWF)と比較した近年の検討では,馬蹄形裂孔の約半数がUWFのみでは検出できなかったとされ,UWF単独では強膜圧迫付きBIOを完全には代替できないと考えられている[4]。なお,強膜圧迫中の眼内圧は外来検査でも平均65 mmHg程度・最大88 mmHgまで上昇しうるとの報告があり,眼灌流に影響を及ぼす可能性があるため,高眼圧症例や緑内障症例では圧迫の強さと時間に配慮する[6]。
眼底所見は以下の形式で記録する。
座位での検査も可能だが,耳側・鼻側の立体視が困難になるほか,圧迫検査できる範囲が制限される。全周の精密検索を行う場合は仰臥位が推奨される。
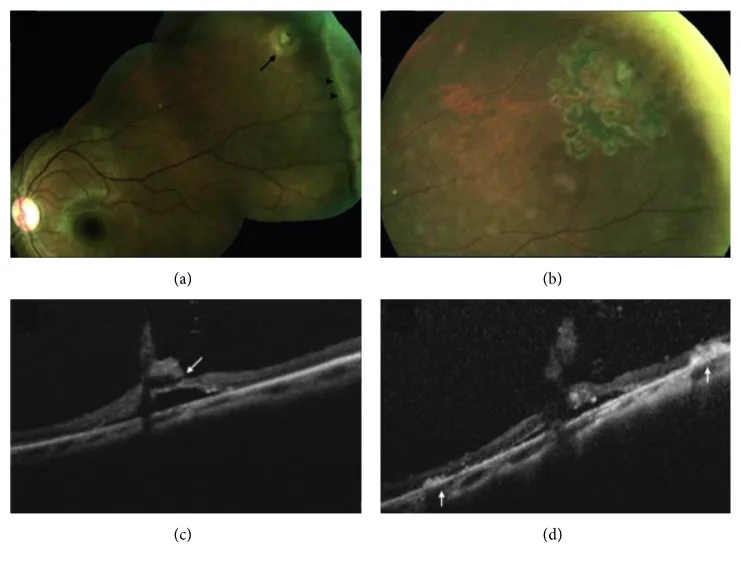
| 所見 | 疑う疾患・状態 | 緊急度 | 対応 |
|---|---|---|---|
| 灰白色の波打つ隆起(網膜がなびく) | 裂孔原性網膜剥離 | 緊急 | 即日手術(バックリング/硝子体手術) |
| 馬蹄形・円孔・蓋付き裂孔 | 網膜裂孔(剥離前) | 準緊急 | 予防的レーザー光凝固術を1〜2日以内に施行 |
| 格子状・蝸牛状の周辺変性 | 格子状変性(裂孔好発部位) | 経過観察 | 自覚症状悪化時に再診指導 |
| 眼底透見不良(赤み) | 硝子体出血 | 準緊急〜経過観察 | 原因精査(糖尿病・静脈閉塞・裂孔等) |
| 新生血管・出血・白斑・浮腫 | 増殖糖尿病網膜症 | 準緊急〜経過観察 | 福田分類等で病期評価。レーザー/硝子体手術 |
| 乳頭の発赤・隆起 | うっ血乳頭・乳頭浮腫 | 準緊急 | 頭蓋内圧亢進を疑い神経内科に紹介 |
| 乳頭蒼白・境界鮮明 | 視神経萎縮 | 経過観察〜精査 | 原因精査(緑内障・虚血・視神経炎) |
| 周辺の白色リング状病変 | 未熟児網膜症(ROP)Stage分類 | 緊急〜準緊急 | 25D/30Dレンズ使用。ICROP3分類で評価 |
強膜圧迫は裂孔と偽裂孔(white with pressure: WWP)の鑑別にも有用である。
この鑑別は,予防的レーザー凝固が必要か経過観察で良いかの判断において極めて重要である。
BIOで観察される倒立実像の形成は幾何光学に基づく。集光レンズの屈折力(D)と眼球の等価屈折力(約60D)の比から倍率(M)が概算される。
実際の倍率はレンズの設計(非球面・平面鏡補正)により上記より若干高くなる。
集光レンズは現代では非球面設計が標準となっており,周辺部の球面収差・色収差が補正されている。これにより20D/28Dレンズで実用的な視野端まで鮮明な像が得られる。
倒像鏡の立体視は検者の両眼が瞳孔を通じて眼底を異なる角度から同時に観察することで生じる。
瞳孔径が大きいほど立体感が向上するため,十分な散瞳(6 mm以上が理想)が検査精度を左右する要因となる。
患者を仰臥位にすると以下の利点がある。
座位では耳側・鼻側の立体視が困難になるほか,圧迫検査できる範囲が制限される。
Optos®(200°超広角走査型レーザー検眼鏡)やCLARUS®(45〜133°超広角眼底カメラ)は非散瞳・非接触で広角眼底像を取得できる。スクリーニング・記録・患者説明・遠隔読影において有用性が高い。
ただし,超広角眼底撮影は平面画像であり,BIOが提供する立体視・動的観察(強膜圧迫による所見変化)・鋸状縁近傍の最周辺部評価を代替することはできない。二次元画像上で「裂孔様に見える病変」の最終確認にはBIOが不可欠であり,両者は補完関係にある。
デジタルセンサーを内蔵した記録機能付きヘッドセット(Digital BIO)が実用化されている。リアルタイムの映像を外部モニターに表示し,動画・静止画として記録できるため,術前説明・教育・遠隔コンサルテーションへの応用が進んでいる。
途上国・離島・NICU施設では眼科専門医の常駐が困難な場合があり,BIO検査の映像をリアルタイムで遠隔地の専門医に転送し読影するシステムの開発が進んでいる。未熟児網膜症(ROP)スクリーニングは特に有望な応用領域であり,デジタルBIOと遠隔読影の組み合わせは医療アクセスの格差解消に貢献する可能性がある。なお,ROPスクリーニングを広視野デジタル眼底撮影とBIOで前向きに比較した試験では,デジタル撮影は単独でBIOを置き換えるのではなく補助的位置づけにとどまるべきであるとされている[7]。
AIを用いた広角眼底カメラによる糖尿病網膜症・ROP・緑内障スクリーニングが商業化されつつある。これらのシステムはファーストスクリーニングとして有用だが,精密診療(手術適応判断・治療モニタリング)の場面では依然としてBIOが主要な検査手技として機能し続けると考えられている。