解剖学的素因

急性緑内障発作(急性原発閉塞隅角症)
1. 急性緑内障発作とは
Section titled “1. 急性緑内障発作とは”急性緑内障発作は、隅角の急速な閉塞により眼圧が突然かつ高度に上昇する眼科救急疾患である。眼圧はしばしば40〜80 mmHgに達し、数時間以内に適切な処置を行わなければ不可逆的な視神経障害を来す。眼科医療のなかで最も緊急性の高い疾患の一つに位置付けられる。
アジア太平洋緑内障学会(APGS)と Academy of Asia-Pacific Professors of Ophthalmology(AAPPO)は、2025年の国際コンセンサスにおいて用語を acute primary angle closure attack(APACA) に統一することを提唱した1)。この用語は疾患の急性性と緊急性を強調し、「glaucoma」という語を意図的に除外している。迅速な処置により緑内障性視神経障害を未然に防げる可能性があるためである1)。APGS 2025のパネル投票では94.11%の合意で採択された。
疫学的には中国人・アジア人に最も多く、年間発症率は10万人あたり6〜16例と報告されている1)。一方で欧米白人における発症率は10万人あたり2〜4.1例にとどまり、アジア人のほうが約3〜4倍高い1, 14)。Dayらの系統的レビューでは欧州由来集団における原発閉塞隅角緑内障の有病率が報告されており、人種差が大きいことが明らかとなっている14)。さらにアジア人症例は欧米症例に比べて視機能予後が不良であることが知られ、Aungらのシンガポールにおける長期追跡研究では、フォローアップ4〜10年の時点で罹患眼の17.8%が失明、47.8%に緑内障性視神経症、57%で6/9スネルン未満の矯正視力が認められた1, 7)。日本の多治見スタディでは40歳以上の原発閉塞隅角緑内障(PACG)有病率は0.6%、久米島スタディでは2.2%と地域差があり、とりわけ沖縄県では閉塞隅角緑内障の頻度が高い2)。Quigleyらの世界推計では、2020年時点で全世界の原発閉塞隅角緑内障患者数は約2,100万人に達するとされ、アジア地域が大部分を占める10)。
発作は解剖学的に素因を持つ眼に、何らかの誘因が重なって生じる。典型的には短眼軸・浅前房・遠視眼を有する高齢女性が、抗コリン薬や散瞳薬の投与後、あるいは長時間の下向き作業や夜間の自然散瞳を契機に発症する。動物実験では眼圧が50 mmHg以上で12時間以上持続した場合、網膜神経線維・神経節細胞・視神経に不可逆的な障害が生じることが示されており1)、発症から治療開始までの時間が視力予後を大きく左右する。
急性発作の概念は歴史的にも長く認識されており、従来「急性閉塞隅角緑内障(acute angle-closure glaucoma: AACG)」「急性緑内障発作(acute glaucoma attack)」「acute angle-closure crisis(AACC)」「acute primary angle closure(APAC)」など多様な呼称が用いられてきた1)。APGS 2025は、これらの用語の混在を整理する目的でAPACAを推奨用語と位置付け、急性性・緊急性・原発性を明確化した1)。さらに「glaucoma」を敢えて含めないことで、迅速な治療により緑内障性視神経障害を免れる可能性があることを示唆している1)。ただし眼圧正常化後も虚血再灌流障害により網膜神経節細胞の消失が進行しうる点には注意を要する1)。
本疾患は遅発性の場合ほど予後が悪く、高齢患者で併存疾患が多く、受診が遅れて高眼圧で来院する例では、従来の薬物治療だけでは十分な眼圧下降が得られないことが多い1)。学歴・症状から治療までの時間・来院時眼圧が失明リスクの独立因子として同定されており1)、啓発活動と迅速な治療アクセスが公衆衛生上の課題となっている。
APGS 2025コンセンサス1.3では「急性緑内障発作は眼科救急であり、即座の眼圧下降が必須である」との文言が100%の合意で採択された1)。また、コンセンサス1.9では「正確な診断は重要だが、臨床的に本疾患が疑われる場合には迅速な眼圧下降を優先すべきである」ことが100%の合意で確認されている1)。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”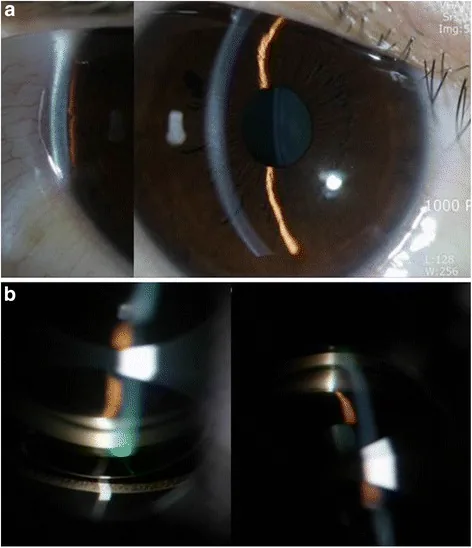
急性緑内障発作は、自覚症状と他覚所見の双方が激烈である点が特徴である。しかし全ての所見がそろわない非典型例もあり、経験の乏しい臨床医では見逃されることがある1)。
自覚症状(三徴)
Section titled “自覚症状(三徴)”急激な眼圧上昇に伴い、以下の強い自覚症状が出現する。
- 激烈な眼痛: 片側の眼球・眼窩深部にかけての激痛
- 同側の頭痛: 前頭部・側頭部に放散する
- 悪心・嘔吐: 消化器症状が前景に立ち、急性胃腸炎やクモ膜下出血と誤診される例もある1)
- 霧視・視力低下: 角膜浮腫による
- 虹視症(ハロー): 光源の周囲に虹の輪が見える
- 結膜充血
全身症状として激しい頭痛・悪心・嘔吐が先行する場合、神経疾患や消化器疾患と誤診されるリスクがある1)。APGS 2025では、これらの全身症状が重要な診断手掛かりであると強調されている1)。
| 所見 | 特徴 |
|---|---|
| 眼圧 | 著明な上昇(40〜80 mmHg)1) |
| 角膜 | 上皮浮腫による霧状混濁 |
| 前房 | 高度に浅小(前眼部OCTでACD約1.3〜1.5 mm) |
| 瞳孔 | 中等度散大・対光反射の減弱または消失 |
| 結膜 | 毛様充血・結膜血管うっ血 |
| 隅角 | 広範な隅角閉塞(両眼で確認) |
| 水晶体 | グラウコムフレッケン(水晶体上皮の虚血性壊死)1) |
| 視神経乳頭 | 急性期に乳頭浮腫、静脈怒張、乳頭出血を見ることがある |
中等度散瞳は、瞳孔括約筋と散大筋の両方が共活性化される位置であり、相対的瞳孔ブロックと瞳孔縁での虹彩-水晶体接触が最大となる状態である。また、高度な眼圧上昇により瞳孔括約筋が虚血に陥り、対光反射が消失する。Goldmann圧平眼圧計での眼圧測定と記録がAPGS 2025コンセンサス1.6で推奨される1)。
慢性閉塞隅角緑内障(CACG)では眼圧上昇は20〜30 mmHg程度と中等度にとどまり、充血は軽度または欠如し、自覚症状に乏しい点で急性発作と区別される。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”急性緑内障発作の発症には、解剖学的素因と発症誘因の二つの要素が関与する。
発症の誘因
散瞳薬:トロピカミド、フェニレフリンなど眼科検査時の点眼薬1)
抗コリン薬:胃内視鏡検査前投薬、睡眠薬、抗精神病薬など1)
三環系抗うつ薬・SSRI:中枢性副交感神経遮断作用と散瞳作用による1)
鼻腔充血除去薬:抗ヒスタミン含有薬、フェニレフリン含有薬1)
交感神経刺激薬・制吐薬:いずれも散瞳作用を介して瞳孔ブロックと隅角混雑を増強する1)
生活場面の誘因:長時間の読書・裁縫など下向き姿勢、暗室・夜間の自然散瞳
APGS 2025コンセンサス1.8では、散瞳・調節麻痺作用を持つ薬剤が解剖学的素因のある眼でAPACAを誘発しうることが88.24%の合意で確認された1)。薬歴の詳細な聴取は診断の重要な手掛かりとなる。
解剖学的要因をさらに分けると、加齢に伴い水晶体が生涯を通じて厚みを増すことが決定的である。遠視眼では眼軸が短く、前房が浅いため、水晶体肥厚の影響を受けやすい。厚みを増した水晶体によって虹彩全体が前方に押し上げられ、これを水晶体因子と呼ぶ。また、瞳孔縁での虹彩-水晶体接触が強まることで房水の流出抵抗が増大し、相対的瞳孔ブロックが進行する。組織学的研究および画像研究では、加齢により毛様体突起の位置が前方偏位することが示されており、久米島スタディではこれが閉塞隅角眼の特徴として確認されている2)。Wangらによる定量的虹彩パラメータ研究では、虹彩厚・虹彩曲率・虹彩面積が狭隅角と有意に関連することが示され、虹彩が前方膨隆する症例ほど発作リスクが高いことが前眼部OCT画像解析から裏付けられている12)。
近視眼は一般に発作リスクが低いとされるが、例外ではない。Yongらの横断研究では、隅角閉塞患者427例のうち94例が近視を有し、このうち11例(11.7%)は−5.0 Dを超える近視であった1)。APGS 2025コンセンサス4.1では、近視眼も隅角閉塞発作から完全に除外されないことが94.11%の合意で採択されている1)。リスクは屈折や眼軸長ではなく、浅前房などの解剖学的素因に主に依存する1)。
4. 診断と検査方法
Section titled “4. 診断と検査方法”急性緑内障発作の診断は、急激な眼圧上昇と自覚症状・他覚所見の組み合わせによる臨床診断が基本である。APGS 2025コンセンサス1.6では「APACAは症状と徴候に基づく臨床診断である」ことが94.11%の合意で採択された1)。ただし、高度な眼圧上昇を来す他疾患との鑑別のためには複数の検査が必要である。
- 視力
- 眼圧測定(Goldmann圧平眼圧計):APGS 2025は本計による測定と記録を推奨する1)
- 角膜内皮細胞検査(スペキュラーマイクロスコープ):レーザー虹彩切開術施行前の必須評価であり、内皮細胞数が低下している例ではレーザーによる水疱性角膜症発症リスクが高い2)
- 前眼部OCT:前房深度を定量する。発作時のACDは1.3〜1.5 mmまで浅小化することがあり、角膜と虹彩がほぼ接触する所見を確認できる
- 眼軸長測定:短眼軸(典型的には22 mm未満)を裏付ける
- 両眼の隅角鏡検査:APGS 2025コンセンサス1.10では両眼での隅角鏡検査が100%の合意で必須とされる1)。罹患眼が角膜浮腫で観察困難でも、僚眼の所見は診断に有用である1)
- 屈折検査(両眼):遠視性屈折が典型的。近視性屈折異常では続発緑内障の可能性を考慮する
- 眼底検査(両眼):糖尿病網膜症、Vogt-小柳-原田病など続発緑内障の原因を除外する
角膜浮腫でゴニオスコピーが困難な場合には 前眼部OCT や 超音波生体顕微鏡(UBM) が有用である1)。特にUBMは毛様体突起や虹彩裏面の形態を評価でき、プラトー虹彩や水晶体亜脱臼の診断に優れる2)。さらに Bモード超音波 は脈絡膜出血、脈絡膜剥離、硝子体出血など後眼部病変の除外に有用であり、薬物・レーザー治療に抵抗する非典型例で必須となる1)。APGS 2025はこれらの画像検査を推奨する一方で、検査のために眼圧下降を遅らせてはならないとも明記している1)。
急性緑内障発作と紛らわしい病態には以下がある1)。
- 悪性緑内障:毛様体前方回旋や硝子体腔内への房水異常流入による硝子体前方偏位が原因。手術歴の有無とUBM所見で鑑別する
- 続発閉塞隅角緑内障
- 新生血管緑内障:ルベオーシス(虹彩新生血管)所見があれば疑う1)
- Posner-Schlossman症候群などのぶどう膜炎性緑内障:眼圧上昇にもかかわらず角膜が比較的透明である点がヒント1)
- 前部水晶体亜脱臼:罹患眼は浅前房で高眼圧だが、僚眼は開放隅角で深前房を呈する場合に疑う1)
APGS 2025コンセンサス1.7では、僚眼が開放隅角で深前房である場合、罹患眼の角膜が比較的透明である場合、虹彩新生血管が見られる場合は二次性原因を積極的に疑うべきと94.11%の合意で採択された1)。これらの所見が認められた場合には、水晶体亜脱臼や新生血管緑内障など侵襲的な処置の適応が変わる病態を除外する必要がある。
5. 標準的な治療法
Section titled “5. 標準的な治療法”急性緑内障発作の治療は、迅速な眼圧下降と相対的瞳孔ブロックの解除が急性期の中心である。発作解除後には、適切な眼圧コントロールと再発予防のための長期管理が重要となる。緑内障診療ガイドライン第5版は、APACに対する第一選択として水晶体再建術を推奨している2)。
発作時には、以下の薬剤を並行して速やかに投与する。
| 薬剤 | 用量・用法 | 作用・注意点 |
|---|---|---|
| 20%マンニトール(高浸透圧薬) | 1.0〜2.0 g/kgを30〜60分で点滴静注2) | 眼圧最低値到達は60〜90分後、持続4〜6時間。腎機能障害で急性腎不全リスク、心不全・肺うっ血で肺水腫リスク2) |
| グリセオール(10%グリセロール) | 300〜500 mLを45〜90分で点滴静注2) | 眼圧最低値到達30〜135分後、持続約5時間。代謝でブドウ糖生成、糖尿病患者で注意2) |
| 1〜2%ピロカルピン塩酸塩 | 1時間に2〜3回点眼2) | 縮瞳により瞳孔ブロック解除を図る。括約筋麻痺例では縮瞳が得られず、かえって毛様体前方移動で瞳孔ブロック増強の危険2) |
| アセタゾラミド | 10 mg/kgを経口または経静脈投与2) | 房水産生抑制による眼圧下降。代謝性アシドーシス・低カリウム血症に注意 |
| β遮断薬点眼 | 1日2回点眼 | 房水産生抑制 |
| α2刺激薬点眼 | 1日2〜3回点眼 | 房水産生抑制と一部流出促進 |
| 0.1%ベタメタゾン点眼 | 1日4回点眼2) | 発作時炎症の沈静化 |
| アプラクロニジン塩酸塩点眼 | 虹彩切開術1時間前と術直後 | 術後一過性眼圧上昇の予防 |
ピロカルピンの使用には慎重な判断が必要である。高眼圧により瞳孔括約筋が虚血状態となっている場合、頻回投与しても縮瞳は得られず、毛様体筋の前方移動により瞳孔ブロックが逆に増強される2)。初期投与時には必ず縮瞳効果の有無を確認すべきである。全身吸収により腹痛などの副交感神経刺激症状が出現することもある2)。
高浸透圧薬の全身投与は高齢者や併存疾患を持つ患者で特にリスクが高い。急激な細胞外液量増加により循環器系に負担がかかり、心不全・肺うっ血患者では肺水腫を起こす可能性がある2)。マンニトールは腎排泄のため腎機能障害例では血漿浸透圧上昇・循環血漿量増加により急性腎不全を来すことがある2)。また、発作時にはすでに嘔吐による脱水に陥っていることが多く、マンニトールの利尿作用で脱水がさらに悪化しうる2)。グリセオールは代謝過程でブドウ糖を生じ、1 Lあたり637 kcalのエネルギーを有するため、糖尿病患者への投与は慎重を要する2)。APGS 2025でも、アセタゾラミドやマンニトール静注は感覚異常・錯乱から致死性肺水腫・急性腎不全に至る重篤な副作用を起こしうるため、高齢者や併存疾患を持つ患者で代替治療が望まれる1)。
レーザー虹彩切開術(LPI)
Section titled “レーザー虹彩切開術(LPI)”薬物治療により眼圧を十分下降させ、角膜が透明化した時点で レーザー虹彩切開術(laser peripheral iridotomy: LPI) を施行する。LPIは相対的瞳孔ブロックを解除する根本治療であり、緑内障診療ガイドライン第5版で推奨度1Aとされる2)。
LPIの要点は以下のとおりである。
- 角膜が十分に透明になってから施行する。不透明な角膜を通したレーザー照射は水疱性角膜症発症のリスクが高い2)
- レーザー選択:アルゴンレーザー単独は照射総エネルギー量が大きく角膜内皮障害のリスクが大きいため、Nd:YAGレーザー単独またはアルゴン+YAG併用が推奨される
- 術前・術直後のアプラクロニジン点眼:術後一過性眼圧上昇を予防する
- 照射部位:虹彩切開用コンタクトレンズ(Abraham・Pollakなど)を装着し、虹彩最周辺部に照射する。上眼瞼で隠れる位置が望ましく、12時方向は気泡が集合するため避ける
標準的なレーザー設定は、アルゴン第1段階Stretch(200〜400 μm、200 mW、0.2秒、2〜10発)で虹彩を伸展し、第2段階Thinner(50 μm、800〜1000 mW、0.02秒、穿孔直前まで、内皮ダメージ考慮で100発未満が望ましい)を行い、Nd:YAG第3段階(2.0〜4.0 mJ、1〜2発)で穿孔仕上げとする。LPIの合併症には前房出血、限局性白内障、再閉塞、水疱性角膜症がある。
水晶体再建術
Section titled “水晶体再建術”緑内障診療ガイドライン第5版はAPACに対する第一選択として 水晶体再建術(超音波乳化吸引術+眼内レンズ挿入) を推奨し(推奨度1A)、瞳孔ブロックの根本解消と隅角開大の両方に有効であるとしている2)。ただし急性期の水晶体摘出術は合併症が生じやすいため、熟練した術者が行うことが推奨される(推奨度1B)2)。
APGS 2025は、従来の「LPI後のwatchful waiting」アプローチには重大な限界があることを指摘している1)。Aungらのアジア人長期追跡では、LPI成功例110眼のうち64眼(58.1%)が慢性眼圧上昇を来し、そのうち26例(40.6%)が薬物療法で制御できたが36例(56.3%)がトラベクレクトミーを要し、2例(1.8%)が失明に至った1, 7)。さらにAungらの別報告では、急性原発閉塞隅角発症例のアジア人長期眼圧転帰が解析され、LPIのみで長期眼圧制御を達成できる割合は限られていることが示されている13)。これらのエビデンスから、LPI単独では長期的管理として不十分であり、早期に水晶体再建術を行うべきとの結論に至っている1)。
英国の5年追跡研究では、白人集団でも早期水晶体再建術はLPI単独と比較して失明86%減、眼圧上昇93%減、薬物必要度69%減という劇的な改善を示した1)。APGS 2025コンセンサス3.2〜3.3では、早期水晶体再建術がLPI単独より良好な長期成績を示すこと、およびAPACA眼に対して低い閾値で水晶体再建術を行うことが適切であるとの合意が得られた1)。コンセンサス3.4では、発作解除後1〜3か月での水晶体再建術が最適なタイミングとされ、これ以上待つとPAS形成と慢性閉塞隅角緑内障(CACG)移行リスクが上昇する1)。
EAGLE試験は原発閉塞隅角疾患に対するclear-lens extractionの長期成績を示した無作為化比較試験であり、原発閉塞隅角緑内障または眼圧>30 mmHgの原発閉塞隅角症例を対象に36か月追跡した結果、早期水晶体摘出群のほうが眼圧コントロール・QOLスコア・費用対効果のいずれにおいても従来治療群より優れることが示された6)。Husainらの無作為化比較試験は、APAC眼に対する一次水晶体乳化術をLPIと比較し、2年追跡で水晶体乳化術群のほうが眼圧コントロール・PAS縮小・薬物必要度のいずれにおいても優位であることを示した8)。さらにLaiらの前向き症例集積では、PACG合併白内障眼に対する水晶体乳化術で術後眼圧・薬物数・隅角開大度のいずれも有意に改善することが報告されている11)。Thamらの別の無作為化比較試験では、薬物治療未制御の慢性原発閉塞隅角緑内障(白内障非合併例)における水晶体乳化術とトラベクレクトミーを比較し、水晶体乳化術群で術後合併症が少なく、長期眼圧制御率が同等以上であったことが示された9)。
日本の緑内障診療ガイドライン第5版でも、これらの国際的エビデンスを踏まえて原発閉塞隅角緑内障・原発閉塞隅角症に対する水晶体摘出術(推奨度1A)が明記されている2)。米国眼科学会のPrimary Angle-Closure Disease Preferred Practice Pattern(2026年版)も、原発閉塞隅角疾患に対するレーザー治療や水晶体摘出術を主要な治療選択肢として扱う3)。欧州緑内障学会(EGS)の第6版ガイドライン(2025年版)も、閉塞隅角疾患を含む緑内障診療の標準的枠組みを更新している4)。
APGS 2025が推奨する代替治療
Section titled “APGS 2025が推奨する代替治療”APGS 2025は、従来の「薬物→LPI→必要時にトラベクレクトミーまたは水晶体乳化術」という段階的アプローチが遅発例や高眼圧例で不十分であるとし、以下の代替治療を早期選択肢として提示している1)。
アルゴンレーザー周辺虹彩形成術(ALPI)
レーザー瞳孔形成術(LPP)
機序:532 nm周波数倍加レーザーで瞳孔縁の虹彩を焼灼し外側に収縮させ、瞳孔ブロックを解除する
利点:角膜透明性が少なくても施行可能、3時・9時方向で実施し疼痛や悪心を伴う患者でも操作しやすい
エビデンス:LPPの単独あるいはALPI併用で発作から2時間以内に有意な眼圧下降が得られる
APGS 2025コンセンサス2.6では88.23%の合意で採択された1)
前房穿刺(ACP)
機序:30G針またはstab knifeを3時または9時方向から刺入し、房水を吸引せずに排出させる。30G針の内腔摩擦により眼圧は自然に12〜15 mmHgで安定する1)
利点:即時的な眼圧正常化。アルゴンレーザー設備や習熟術者がない施設でも実施可能
エビデンス:初発眼圧60 mmHg未満のAPACA眼でマンニトール点滴より視力改善に優れ、重大合併症は観察されなかった1)
APGS 2025コンセンサス2.7では94.12%の合意で採択された1)
角膜陥没(corneal indentation)
機序:小径4鏡隅角鏡レンズ(Posner、Sussmanなど)または平滑な指先で眼瞼越しに角膜を圧迫し、一時的に隅角を開大させ房水流出を促進する
適応:眼科設備へのアクセスが限られる地域での初期対応
APGS 2025コンセンサス4.4では88.23%の合意で採択された1)
一方で、薬物治療でコントロールできないAPACA眼への 緊急線維柱帯切除術 と 緊急水晶体乳化術 は、APGS 2025では避けるべきとされている1)。薬物治療未制御のAPACA眼に対するトラベクレクトミー単独の成功率は限られ、qualified successが56.2%、complete successが9.4%にとどまるとの報告がある1)。さらに「hot and angry」な状態の眼で水晶体乳化術を行うと、角膜浮腫による視界不良、浅前房、小径で変形した瞳孔、アトニック虹彩による脱出リスク、術中炎症など重大な合併症リスクがある1)。
対側眼(僚眼)管理
Section titled “対側眼(僚眼)管理”原発閉塞隅角は両眼性素因のため、片眼に急性発作を起こした症例では対側眼も発作リスクが非常に高い。緑内障診療ガイドライン第5版は、対側眼の狭隅角に対する 予防的レーザー虹彩切開術 と 水晶体摘出術 の両方を推奨度1Aで推奨している2)。APGS 2025コンセンサス2.3では、発作眼を治療中にLPIができるまでの期間、対側眼にピロカルピン点眼を開始することが100%の合意で採択された1)。
実践的な治療フロー
Section titled “実践的な治療フロー”典型的な処置の流れは以下のとおりである2)。
- 視力、眼圧、角膜内皮細胞、前眼部OCT、眼軸長、両眼隅角鏡、屈折、眼底を評価
- 20%マンニトール 1.0〜2.0 g/kgを30〜60分で点滴静注(腎機能障害に注意)
- 1〜2%ピロカルピン頻回点眼開始(縮瞳効果を必ず確認)
- アセタゾラミド投与、β遮断薬点眼、ベタメタゾン点眼を併用
- 対側眼にはピロカルピン点眼を開始
- 角膜透明化後にLPI施行(術前・術直後にアプラクロニジン塩酸塩点眼)
- 術後処方例:0.1%ベタメタゾン点眼1日4回+眼圧に応じた緑内障点眼薬・炭酸脱水酵素阻害薬
- 翌日に前眼部OCTで隅角開大度を評価、PAS残存・高眼圧持続例は速やかに水晶体再建術可能施設へ紹介
- 発作解除後1〜3か月を目安に水晶体再建術を計画
- 対側眼の予防的LPIまたは水晶体再建術
当日緊急手術が施行できない施設では、まず薬物治療とLPIで発作を解除し、発作後1〜3か月を目安に水晶体再建術を行う流れが現実的である1, 2)。
緑内障診療ガイドライン第5版は、APACに対する第一選択として水晶体再建術を推奨度1Aで推奨している2)。APGS 2025の国際コンセンサスでも、LPI後に最大58%がCACGへ移行するというアジア人長期データ1, 7)をふまえ、早期の水晶体再建術が強く推奨されている1)。英国の5年追跡では、LPIのみと比較して失明86%減、眼圧上昇93%減、薬物必要度69%減と劇的な改善が報告されている1)。タイミングは発作解除後1〜3か月が最適とされ、これ以上待つと周辺虹彩前癒着の形成が進み慢性閉塞隅角緑内障への移行リスクが高まる1)。対側眼も両眼性素因があるため、予防的レーザー虹彩切開術または水晶体摘出術が必要である2)。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”急性緑内障発作の主な発症機序は 相対的瞳孔ブロック であり、これに プラトー虹彩機序 や 脈絡膜拡張 が関与する場合がある。
相対的瞳孔ブロックと水晶体因子
Section titled “相対的瞳孔ブロックと水晶体因子”虹彩裏面と水晶体前面は瞳孔縁で生理的に接触しており、後房から前房への房水流は瞳孔を経由する。加齢とともに水晶体は厚みを増し前方へ移動するため、瞳孔縁での虹彩-水晶体接触が強まり、房水流出抵抗が上昇する。これを 相対的瞳孔ブロック と呼ぶ。後房圧が前房圧を上回ると、虹彩は前方凸に膨隆し、周辺部の線維柱帯をほぼ完全に覆うことで急激な眼圧上昇が生じる1)。
遠視眼では眼軸が短く前房が浅いため、水晶体肥厚の影響がいっそう顕著となる。いったん瞳孔ブロックが生じると後房圧上昇により虹彩が前方へさらに膨隆し、同時に眼圧上昇に伴う虹彩実質の浮腫が瞳孔ブロックをさらに増強する悪循環が形成される。こうして数時間のうちに40〜80 mmHgに達する。
中等度散瞳位の危険
Section titled “中等度散瞳位の危険”瞳孔ブロックが最大となるのは 中等度散瞳位 である。この位置では瞳孔括約筋と散大筋の両方が共活性化され、虹彩が最も緩んだ状態で水晶体前面と広く接触する1)。そのため抗コリン薬や交感神経刺激薬による薬理学的散瞳、暗所環境、強いストレスなどによる自然散瞳は発作の誘因となる。一方で完全散瞳や完全縮瞳では瞳孔ブロックの程度は相対的に小さい。
プラトー虹彩機序
Section titled “プラトー虹彩機序”少数ながらプラトー虹彩機序による発作も存在する。虹彩根部が前方に屈曲しており、散瞳時に毛様体が後方から虹彩根部を機械的に押し上げ、隅角を直接閉塞する機序である。プラトー虹彩では前房中央深度は比較的保たれるにもかかわらず周辺部隅角が鋭角的に狭い。UBMでは虹彩中央部が平坦、根部が厚く前方に屈曲し、毛様体突起の前方偏位および毛様溝の消失が特徴的である。レーザー虹彩切開術後も高眼圧が持続する場合にはプラトー虹彩機序の関与を疑い、レーザー隅角形成術(LGP)の追加や水晶体摘出術を検討する2)。
脈絡膜拡張の関与
Section titled “脈絡膜拡張の関与”画像研究では、脈絡膜拡張が後房圧を上昇させ、虹彩-水晶体隔膜を前方に押し出すことで前房角を狭小化させる可能性が示唆されている1)。しかしAPGS 2025コンセンサス1.5「脈絡膜拡張はAPACAの開始要因である」は41.17%の合意にとどまり、成立していない1)。因果関係と寄与度の定量化は今後の大規模画像研究を要する。
虚血障害とグラウコムフレッケン
Section titled “虚血障害とグラウコムフレッケン”眼圧が急激に上昇することで、瞳孔括約筋が虚血に陥り対光反射が消失する。水晶体上皮も虚血性壊死を起こし、瞳孔領に白色の混濁を残す。これを グラウコムフレッケン と呼び、過去の発作既往を示唆する重要所見である1)。
視神経障害は、発作中の高眼圧による機械的および虚血性障害に加え、眼圧正常化後の 虚血再灌流障害 によっても進行しうる1)。APGS 2025は、眼圧が制御された後も網膜神経節細胞の消失が持続する可能性があることを明記している1)。したがって「眼圧が下がったから安心」ではなく、長期的な視神経・視野経過観察が必要である。
炎症・前房反応
Section titled “炎症・前房反応”APACA眼では著明な前房炎症が生じる。高眼圧に伴う虹彩毛細血管からのタンパク漏出、瞳孔括約筋・散大筋の虚血壊死、内皮細胞障害による房水蛋白増加などが前房内に前房炎症細胞・フィブリンとして観察される。APGS 2025コンセンサス2.2では、APACA眼が重度に炎症を呈するため、局所および必要時全身の抗炎症療法を併用すべきであることが100%の合意で採択された1)。炎症の沈静化はLPI後の水疱性角膜症予防、瞳孔癒着予防、早期の水晶体再建術への準備のいずれにも重要である。
長期的な合併症
Section titled “長期的な合併症”急性発作後には様々な合併症が残存しうる。対光反射消失を伴う麻痺性散瞳、グラウコムフレッケン、虹彩実質の色素放出、限局性白内障、周辺虹彩前癒着(PAS)の形成、角膜内皮細胞数の減少が代表的である。LPI後の水疱性角膜症は、滴状角膜、糖尿病、急性発作既往、すでに角膜内皮細胞が減少している例で多いことが知られている2)。したがって術前の角膜内皮細胞検査は必須であり、内皮細胞数が低下している例では手術的周辺虹彩切除術の選択を検討する2)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”急性緑内障発作の治療パラダイムは、2020年代後半にかけて大きく変化している。従来の「薬物治療→LPI」に加え、APGSガイドライン 2025 は以下の新しい治療戦略を提示している1)。
- 早期の代替治療:ALPI、LPP、ACPを初期段階で積極的に選択することで、全身薬の副作用を回避しつつ30分以内に眼圧を安全域まで下降させる1, 5)
- 早期水晶体再建術:LPI単独後の最大58%という高いCACG移行率を鑑み、発作解除後1〜3か月での水晶体再建術をより積極的に選択する1)
- 隅角癒着解離術(GSL)併用:広範なPASを伴うCACG成分がある場合、水晶体再建術にGSLまたはgoniotomyを併用する選択肢も検討されている1)
- 結膜下デキサメタゾン:従来の治療に加えて結膜下デキサメタゾン追加投与で眼圧下降効果と治療成功率が向上したとの無作為化比較試験が報告されている1)。投与経路・用量の最適化は今後の課題
- 資源限定地域での対応:アルゴンレーザーが利用できない地域での角膜陥没法が有力な選択肢として提案されている1)
一方で未解決の論点も多い。水晶体再建術の最適タイミング、MIGS(低侵襲緑内障手術)の閉塞隅角緑内障での役割、新しい薬物併用療法、画像ベースの発症予測モデルなどは、大規模前向き研究による検証が必要である1)。
8. 参考文献
Section titled “8. 参考文献”- Chan PP, Zhang X, Aung T, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Asia Pac J Ophthalmol (Phila). 2025;14(6):100223. PMID: 40615047. doi:10.1016/j.apjo.2025.100223.
- 日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Gedde SJ, Chopra V, Vinod K, Bowden EC, Kolomeyer NN, Challa P, et al.; American Academy of Ophthalmology Preferred Practice Pattern Glaucoma Committee. Primary Angle-Closure Disease Preferred Practice Pattern. Ophthalmology. 2026;133(4):P153-P201. PMID: 41665581. doi:10.1016/j.ophtha.2025.12.030.
- Pazos M, Traverso CE, Viswanathan A; European Glaucoma Society. European Glaucoma Society - Terminology and guidelines for glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):1-212. PMID: 41026937. doi:10.1136/bjophthalmol-2025-egsguidelines.
- Lam DS, Lai JS, Tham CC, Chua JK, Poon AS. Argon laser peripheral iridoplasty versus conventional systemic medical therapy in treatment of acute primary angle-closure glaucoma: a prospective, randomized, controlled trial. Ophthalmology. 2002;109(9):1591-6.
- Azuara-Blanco A, Burr J, Ramsay C, et al. Effectiveness of early lens extraction for the treatment of primary angle-closure glaucoma (EAGLE): a randomised controlled trial. Lancet. 2016;388(10052):1389-1397.
- Aung T, Friedman DS, Chew PT, et al. Long-term outcomes in Asians after acute primary angle closure. Ophthalmology. 2004;111(8):1464-9.
- Husain R, Gazzard G, Aung T, et al. Initial management of acute primary angle closure: a randomized trial comparing phacoemulsification with laser peripheral iridotomy. Ophthalmology. 2012;119(11):2274-81.
- Tham CC, Kwong YY, Baig N, Leung DY, Li FC, Lam DS. Phacoemulsification versus trabeculectomy in medically uncontrolled chronic angle-closure glaucoma without cataract. Ophthalmology. 2013;120(1):62-7.
- Quigley HA, Broman AT. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophthalmol. 2006;90(3):262-7.
- Lai JS, Tham CC, Chan JC. The clinical outcomes of cataract extraction by phacoemulsification in eyes with primary angle-closure glaucoma (PACG) and co-existing cataract: a prospective case series. J Glaucoma. 2006;15(1):47-52.
- Wang B, Sakata LM, Friedman DS, et al. Quantitative iris parameters and association with narrow angles. Ophthalmology. 2010;117(1):11-17.
- Aung T, Ang LP, Chan SP, Chew PT. Acute primary angle-closure: long-term intraocular pressure outcome in Asian eyes. Am J Ophthalmol. 2001;131(1):7-12.
- Day AC, Baio G, Gazzard G, et al. The prevalence of primary angle closure glaucoma in European derived populations: a systematic review. Br J Ophthalmol. 2012;96(9):1162-7.
