角膜所見
角膜実質浮腫:スリガラス状の角膜混濁を呈する。角膜厚が著しく増大し、800μmを超える症例もある
Descemet膜皺襞:内皮機能不全に伴い角膜後面に皺襞が形成される。内皮障害の重要な指標である
上皮下水疱(bullae):進行例ではgiant bullaeが形成され、破裂により上皮欠損と疼痛が生じる
実質瘢痕・血管侵入:慢性化すると周辺部から血管侵入と瘢痕性混濁が生じ、視力低下の一因となる

水疱性角膜症(bullous keratopathy)は、角膜内皮細胞の障害により角膜実質と上皮に不可逆的な浮腫が生じ、進行とともに上皮下に水疱(bulla)を形成する病態である。視力低下の主因は実質の浮腫であるが、疼痛は上皮水疱の破裂によって生じる。
角膜内皮はポンプ機能と選択的透過性をもつバリア機能により、角膜実質の含水率と角膜厚を一定に保っている。内皮細胞密度が400〜500 cells/mm²を下回るとポンプ機能が代償不全に陥り、実質浮腫を生じ、さらに進行すると上皮浮腫と水疱を形成する。角膜内皮細胞は前房内で分裂しないため、障害は不可逆的である。
| 分類 | 代表的な原因 |
|---|---|
| 医原性 | 白内障手術後(偽水晶体眼性・無水晶体眼性)、レーザー虹彩切開術後、角膜移植後拒絶反応 |
| 変性・ジストロフィ | Fuchs角膜内皮ジストロフィ、後部多形性角膜ジストロフィ(PPCD)、ICE症候群 |
| 炎症性 | ヘルペス性角膜内皮炎、サイトメガロウイルス角膜内皮炎、特発性角膜内皮炎 |
| 外傷性 | 鉗子分娩によるDescemet膜破裂、角膜裂傷、鈍的外傷 |
| 薬剤性 | アマンタジン、クロルプロマジン、一部のROCK阻害点眼(ネタルスジル等) |
| 代謝・全身 | 糖尿病、ムコ多糖症、家族性高脂血症(LCAT欠損症、Tangier病)、Schnyder角膜ジストロフィ |
偽水晶体眼性水疱性角膜症(pseudophakic bullous keratopathy: PBK)は、白内障手術を受けた患者の1〜2%に発症し、術後8か月から7年の間に顕在化するとされる1)。白内障手術技術の進歩に伴い発症率は減少傾向にあるが、Fuchs角膜内皮ジストロフィと並んで角膜移植の主要適応疾患である4,8)。
角膜内皮細胞密度は加齢により生理的に減少する。新生児では3,500〜4,000 cells/mm²、20歳代で約2,700 cells/mm²、70歳以上では平均約2,200 cells/mm²まで減少する。通常の生理的減少率は0.5%/年であるが、白内障術後では約2%/年、緑内障術後では約10%/年と加速する。
Fuchs角膜内皮ジストロフィは常染色体優性遺伝を背景にもち、男女比は約1対4で女性に多い4)。白色人種・黒色人種に比し日本人では少ないとされてきたが、前段階にあたる滴状角膜(cornea guttata)は白内障術前患者の1.2%に観察され、長寿化に伴い日本でも増加傾向が指摘されている。
水疱性角膜症は角膜疾患による視力障害の主要な原因の一つであり、世界的にも角膜移植の主要な適応疾患である。白内障手術が世界的に最も行われている眼科手術であることから、偽水晶体眼性水疱性角膜症は公衆衛生学的にも重要である。術式の低侵襲化、粘弾性物質の改良、超音波エネルギー削減技術の進歩により、発症率は年々減少してきたが、完全にはゼロにならない。近年は、超高齢者の白内障手術が増加していることと、Fuchs角膜内皮ジストロフィの保有者が術前から存在することがリスク要因として再認識されている。
角膜移植の主要適応としては、Fuchs角膜内皮ジストロフィと偽水晶体眼性水疱性角膜症が世界的に上位を占める8)。日本では角膜ドナーが慢性的に不足しており、海外ドナーへの依存度が高いことも特徴である。近年の国内統計では、角膜移植全体の約40〜50%が水疱性角膜症(偽水晶体眼性・無水晶体眼性を含む)を占めており、白内障手術の低侵襲化とともに絶対数は減少しているものの、依然として角膜移植の主要適応である。レーザー虹彩切開術(LI)後の水疱性角膜症はかつて日本で多くみられたが、予防的白内障手術への移行に伴い減少している。
いいえ、水疱性角膜症は角膜内皮細胞の不可逆的な障害によって生じる病態であり、自然に治ることはありません。角膜内皮細胞はヒトでは分裂・再生がきわめて困難なため、一度失われた細胞は元に戻りません。根治的な治療は角膜内皮移植術であり、近年は培養角膜内皮細胞を用いた再生医療の実用化も進んでいます。
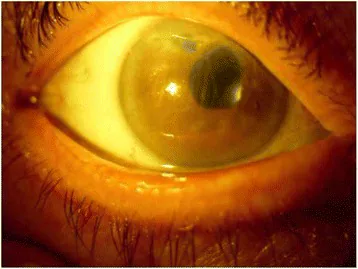
水疱性角膜症の自覚症状は浮腫の程度と罹患層によって変化する。
角膜所見
角膜実質浮腫:スリガラス状の角膜混濁を呈する。角膜厚が著しく増大し、800μmを超える症例もある
Descemet膜皺襞:内皮機能不全に伴い角膜後面に皺襞が形成される。内皮障害の重要な指標である
上皮下水疱(bullae):進行例ではgiant bullaeが形成され、破裂により上皮欠損と疼痛が生じる
実質瘢痕・血管侵入:慢性化すると周辺部から血管侵入と瘢痕性混濁が生じ、視力低下の一因となる
原因別の特徴的所見
細隙灯検査では、炎症所見を伴わない実質浮腫が認められた場合、まず内皮機能不全を考慮する。内眼手術後の実質浮腫は通常、創口部付近に強く、感染性角膜炎の浸潤巣周囲にも実質浮腫がみられる。フルオレセイン染色では、上皮水疱部分がダークスポットとして観察される。
角膜内皮異常を示唆するサインとして、角膜中央部付近の内皮面に観察される灰白色または褐色の滴状物が挙げられる。滴状物が拡大・癒合するとbeaten-metal appearanceと呼ばれる特徴的な所見を示し、鏡面反射法や内皮顕微鏡でdark spotとして捉えられる。
水疱性角膜症の進行はおおむね以下の段階で捉えることができる。
各段階で治療戦略が異なる。実質浮腫期までは保存的治療や薬物療法で経過観察可能だが、水疱形成期以降は疼痛管理と内皮移植の検討が必要となる。
角膜内皮の機能が低下していると、閉瞼中(睡眠中)は涙液蒸散が減少し角膜浮腫が蓄積しやすくなります。日中は涙液の蒸散により角膜から水分が引き出されるため浮腫が軽減し、視力が改善します。このパターンは水疱性角膜症やFuchs角膜内皮ジストロフィ初期の典型症状として知られています。
角膜内皮細胞は生体内で分裂・増殖しない。局所的な障害は隣接細胞の拡大・遊走により修復されるが、一定密度以下に減少すると不可逆的な代償不全に陥る。水疱性角膜症の原因は医原性・変性性・外傷性・炎症性・薬剤性と多岐にわたり、最も頻度が高いのは偽水晶体眼性(PBK)とFuchs角膜内皮ジストロフィである。
白内障手術前後の因子によってリスクが決まる。
前房型IOL(ACIOL)は約14%でPBKを合併するとの報告があり、後房型IOLより高リスクとされる3)。術後の内皮細胞減少率は正常な0.6%/年に対し約2.5%/年と約4倍に加速し、術後5年で術前比約11%、10年以上で約18.7%の減少が報告されている。
常染色体優性遺伝を背景にもつ両眼性の進行性内皮疾患であり、角膜中央部に滴状角膜を生じ、徐々に周辺部へ広がる4)。通常50歳以下では自覚症状を呈さず、ゆるやかに進行する。進行すると内皮のバリア機能とポンプ機能がともに低下し水疱性角膜症に至る。
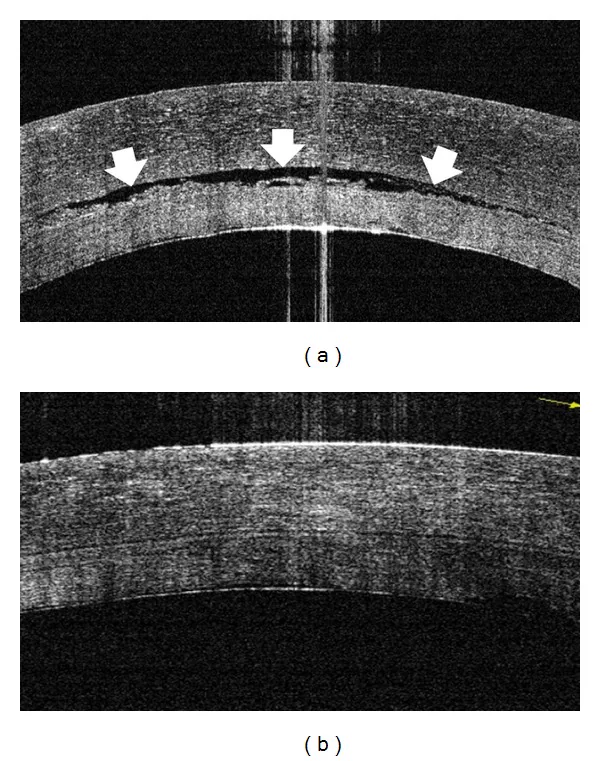
水疱性角膜症の診断は臨床所見に基づき、補助検査で内皮機能と浮腫の程度を評価する。
最も基本的な検査である。徹照法で角膜混濁の範囲と深さを評価し、スクレラルスキャター法で上皮浮腫の広がりを確認する。鏡面反射法を用いると、Fuchs由来では内皮面のbeaten-metal appearanceが観察できる。
浮腫パターンは原因推定に有用である。びまん性浮腫はTASSや薬剤毒性、局所性浮腫はDescemet膜剥離や器具接触、円板状浮腫はヘルペス性角膜内皮炎を示唆する。角膜移植眼では区画性の浮腫と角膜後面沈着物(Khodadoust line)が拒絶反応を示唆する。
角膜内皮細胞密度・形態評価の中心的検査である。
| 指標 | 正常値 | 異常値 |
|---|---|---|
| 細胞密度 | 年齢により2,200〜4,000 cells/mm² | 500 cells/mm²以下で透明性維持困難 |
| CV値(変動係数) | 0.2〜0.3 | 0.35以上 |
| 六角形細胞出現率 | 60〜70% | 50%以下 |
軽症例では術前評価に有用であるが、重度の浮腫がある症例では撮影困難となる。その場合は接触型スペキュラーマイクロスコープや共焦点顕微鏡が有用である。
浮腫の定量的評価に不可欠である。超音波パキメトリが迅速かつ標準的な検査であり、前眼部OCTやScheimpflug撮影は非接触で複数部位の測定が可能である9)。
角膜各層を高解像度で可視化でき、上皮下水疱の範囲、実質肥厚、Descemet膜異常を詳細に評価できる。細隙灯では確認困難な構造異常の同定に有用である9)。特に術後の評価、Descemet膜剥離の検出、上皮浮腫の範囲把握、グラフト接着状態の確認など、幅広い応用が可能である。前眼部OCTは非接触で患者負担が少なく、経時的な観察にも適している。
重症の角膜浮腫でスペキュラーマイクロスコープによる評価が困難な症例では、共焦点顕微鏡が有用である。角膜内皮層の細胞形態を直接観察し、細胞密度や多形性を評価できる。研究用途では、神経叢・ケラトサイト・免疫細胞の観察にも用いられる。
白内障手術を受ける高齢者では、加齢による自然減少に加え、併存する全身疾患や過去の眼科手術・外傷歴が内皮細胞の状態に影響している。術前に得られたスペキュラーマイクロスコピー所見を参考に、手術予後と水疱性角膜症発症リスクを推定する。特に内皮細胞密度が1,000 cells/mm²以下、CV値0.4以上、六角形細胞出現率40%未満の症例では、術後の代償不全リスクが高く、粘弾性物質の豊富な使用・超音波エネルギー最小化・硬い核への対応など術式の工夫が求められる。
水疱性角膜症を疑う際は以下の鑑別が重要である。
水疱性角膜症の治療は、内皮障害の可逆性と視機能要求に応じて内科的治療と外科的治療を組み合わせる。
治療は「原因除去」「内皮機能の温存・回復」「浮腫と疼痛の軽減」「視機能の回復」の4つを柱とする。内皮障害が可逆的な段階(炎症性・薬剤性・術後一過性)では原因解消により浮腫の軽快が期待できる。不可逆的段階では、保存的治療による対症管理と外科的治療による根治が中心となる。
内皮移植までの橋渡し、あるいは手術困難例の対症療法として行われる。
Rho関連コイルドコイル形成キナーゼ(ROCK)阻害薬は、角膜内皮細胞の増殖・遊走・接着を促進しアポトーシスを抑制する。Erdinestらは、通常の保存的治療に反応しなかったPBK 3症例にリパスジル0.4%点眼を1日3回、3〜11か月間投与し、全例で中心角膜厚の減少と矯正視力の改善を認め、角膜移植を回避できたと報告している10)。症例3では11か月の投与で実質混濁が完全に消失し、中心角膜厚が582μmから540μmに、視力が0.3 logMARから0.04 logMARまで改善した。
また、リパスジルの周術期投与により、高リスク眼の白内障術後12か月の内皮細胞減少率がリパスジル群4.5%に対しコントロール群12.8%であったと報告されており、予防的使用の可能性が示唆されている1)。
角膜内皮の不可逆的機能障害に対する根治療法は角膜移植である。
角膜内皮移植術(DSAEK・DMEK)
全層角膜移植術(PK)
適応:実質瘢痕や血管侵入が高度で内皮移植のみでは視力改善が見込めない症例で選択される
特徴:術後拒絶反応リスクが内皮移植より高く、ステロイド点眼の長期管理が必要である
注意点:術後角膜強度が低下し、鈍的外傷で創離開を起こしやすい
Selaらのメタ解析(3件のRCT、2件のfellow-eye研究、3件のコホート研究を含む8研究376眼: DMEK 187眼, UT-DSAEK 189眼)では、12か月時点のlogMAR BCVAはDMEK群が有意に良好であった(平均差 −0.06、95%信頼区間 −0.10〜−0.02)8)。一方、空気再注入(rebubbling)を要する頻度はDMEK 19.79%、UT-DSAEK 8.99%であり、DMEK側で有意に高かった(OR 2.76、95%信頼区間 1.46〜5.22)8)。興味深いことに、グラフト厚が70μm未満のDSAEKではBCVAに有意差は認められず、薄層化により両術式の差が縮小する可能性が示唆されている8)。
| 指標 | PK | DSAEK/UT-DSAEK | DMEK |
|---|---|---|---|
| 12か月BCVA | 回復遅い | UT-DSAEK良好 | 最良8) |
| リバブリング(空気再注入) | 不要 | 約9% | 約20%8) |
| 5年拒絶反応率 | 約22% | 約22% | 約2.8%9) |
| グラフト脱落率 | 低い | 中等度 | 比較的高い3,9) |
| 術後外傷抵抗性 | 低い | 良好 | 良好 |
術後6か月経過しても浮腫が改善しない症例は内皮代償不全と判断し、角膜内皮移植の適応となる9)。小角膜やACIOL残存などの複雑眼でもDSAEKは実施可能で、IOL交換なしで良好な視力回復が得られた報告がある3)。
DMEKとDSAEKの選択は、患者の複雑眼の有無、術者の経験、期待される視力予後、術後管理体制に基づいて判断される。複雑眼(広範な虹彩欠損、前房型IOL、硝子体手術既往、緑内障チューブ挿入眼、無水晶体眼)ではグラフトの展開と位置決めが困難となるため、DSAEK(または超薄型DSAEK)が安全である3,8)。一方、未合併症例ではDMEKが早期の視力回復と低い拒絶反応率という利点を提供する9)。
術後管理では、空気または気体(SF6・C3F8など)による前房タンポナーデを行い、グラフトと後部実質を密着させる。患者は術後数日間仰臥位保持を求められ、グラフト剥離が生じた場合は空気再注入(rebubbling)を行う。術後ステロイド点眼は拒絶予防のため数か月から1年以上継続され、その後は低用量維持療法となる。
Kinoshitaらは、培養ヒト角膜内皮細胞をROCK阻害薬Y-27632とともに前房内に注入する治療法を開発した。水疱性角膜症11眼のうち10眼で5年後も角膜透明性が維持され、平均内皮細胞密度は1,257 cells/mm²であったと報告されている14)。本治療は日本で第II/III相臨床試験を経て2022年に製造販売承認を取得しており、ドナー角膜不足を補う再生医療として国際的に注目されている1,14)。
本療法の手順は、ドナー角膜から内皮細胞を分離・培養し、ROCK阻害薬Y-27632を加えた細胞懸濁液を前房内へ注入するというものである。注入後は数時間の腹臥位(顔を下に向けた姿勢)を保持し、細胞が重力によって角膜内皮面に沈着・接着するよう誘導する。従来の角膜内皮移植術と比べ、切開が小さく、ドナー角膜1眼分から複数例の治療が可能であることから、ドナー角膜の有効利用という点でも大きな意義がある。
治療方針は、浮腫の進行度、内皮細胞密度、視機能要求、併存疾患、全身状態、患者希望を総合的に判断して決定する。軽症・初期症例では保存的治療やROCK阻害点眼で経過観察し、中等症〜進行例では内皮移植を検討する。実質混濁や血管侵入を伴う進行例では全層角膜移植が選択される。手術適応となった症例でも、疼痛が主訴であり視力予後が乏しい場合は、羊膜移植や治療的PTKによる対症療法が有用である。
視力改善の見込みがなく水疱による激しい疼痛がある症例では、前部実質穿刺(ASP)、治療的エキシマレーザー角膜切除術(PTK)、羊膜移植などが疼痛緩和目的で選択される。
軽症から中等症の水疱性角膜症では、ROCK阻害薬(リパスジル)の点眼により角膜浮腫が改善し、角膜移植を遅延または回避できた症例が報告されています。ただし内皮細胞が高度に減少した進行例では効果は限定的です。現時点でROCK阻害点眼は標準治療としてはまだ確立されておらず、根治治療の柱は角膜内皮移植です。主治医と相談のうえ個々の病状に適した治療を選択してください。
はい、2022年に日本で培養角膜内皮細胞注入療法が製造販売承認を取得しました。ただし実施可能な施設は限定されており、対象となる病態や適応基準があります。すべての水疱性角膜症患者に適応されるわけではなく、担当医と相談のうえ治療の可否を判断する必要があります。角膜ドナー不足が深刻な状況のなか、日本発の再生医療として発展が期待されています。
角膜は約78%の含水率を維持することで透明性を保つ(deturgescence)。この相対的な脱水状態は以下の5因子の平衡により保たれる。
角膜内皮の水分調節はMauriceの提唱したpump-leak mechanismで説明される。内皮細胞は一次性・二次性能動輸送機構を介して角膜実質から前房側へのネットイオンフラックスを駆動し、浸透圧勾配を形成する。このポンプ機能は主にHCO₃⁻とCl⁻に依存し、Na⁺/K⁺-ATPaseが中核を担う11)。
健常眼の吸水圧 IP は IP = IOP − SP で表され、通常は約 −35〜−45 mmHg の陰圧となる。内皮機能不全では実質水分が増加しSPが低下、さらに進行するとSPがIOPを下回りIPが陽圧に転じる。陽圧状態では水分が実質から上皮側へ汲み出され、上皮浮腫と水疱を形成する。一方、高眼圧(約50 mmHg超)では内皮が健常でも前房水が上皮層へ押し込まれ上皮浮腫が生じうるが、この場合SPは変化せず実質浮腫は伴わない。
Toneらの報告によれば、Fuchs角膜内皮ジストロフィの初期段階ではNa⁺/K⁺-ATPase密度の代償性増加が認められるが、病態の進行に伴い漸進的に低下する11)。リアルタイムPCRでは進行例でNa⁺/K⁺-ATPase密度の有意なダウンレギュレーションが検出され、MCT1およびMCT4のダウンレギュレーションとともに内皮ポンプ機能の破綻を裏付ける。角膜内皮の透過性亢進(バリア機能障害)はポンプ機能障害に先行することも示されている11)。
白内障手術後の内皮細胞減少は複数の機序で生じる。術中の器具やIOLの接触、超音波エネルギーによる機械的・物理的障害が主因であり、虹彩損傷は前房内炎症性サイトカイン濃度を上昇させ長期的な内皮減少を加速させる1,2)。
IOLの存在下に角膜浮腫が生じた場合、たとえ角膜内皮のguttaeが存在してもPBKと定義される。Fuchs角膜内皮ジストロフィとは異なり、PBKでは角膜浮腫が周辺部から始まり中心に進行する傾向がある。
角膜内皮細胞密度が約2,000 cells/mm²を下回ると透過性は徐々に増加するが、代償的なポンプ機構により500〜400 cells/mm²前後までdeturgescenceが維持される。この閾値を下回ると水疱性角膜症へ進展する可能性が高い。ただし閾値には個人差があり、同じ細胞密度でも浮腫を生じるかは個々の内皮機能に依存する。
角膜内皮細胞は前房内環境では細胞分裂が事実上行われず、欠損が生じた際は周囲細胞の拡大と遊走によって被覆される。この修復過程で細胞面積が増加し、形状の不同性(pleomorphism)と大小不同(polymegethism)が顕著となる。スペキュラーマイクロスコピーでは、CV値(変動係数)の上昇と六角形細胞出現率の低下としてこれらの変化が定量評価される。細胞密度が高いうちはポンプ機能が維持されるが、代償の限界に達すると急速に浮腫へ移行する。内皮細胞の機能低下は密度低下に先行することもあり、密度の絶対値のみでは水疱性角膜症の発症を完全には予測できない。
白内障手術や他の内眼手術後の慢性的な内皮細胞減少には、前房内の炎症性サイトカイン(TNF-α、IL-1、IL-6)が関与する。これらのサイトカインは内皮細胞のアポトーシスを誘導し、バリア機能とポンプ機能の両方を低下させる。術後の遷延性炎症はPBKの重要なリスク因子である1)。
EndoArt(EyeYon Medical社)は、角膜後面の曲率に適合する直径6.0 mm・厚さ50μmのドーム型人工内皮層である。親水性アクリル素材からなり、DMEKと同様の手技で前房内に挿入される。非生体材料であるため免疫抑制療法は不要で、長期保存が可能である。Auffarthらは、慢性角膜浮腫2例にEndoArtを移植し、角膜厚が症例1で730から526μm、症例2で761から457μmに減少し、17か月時点で安定していたと報告した12)。米国FDAのBreakthrough Therapy Designationを取得しており、複雑眼(無虹彩・硝子体手術後・チューブ挿入眼)での応用が期待されている。
DSOは中心部のDescemet膜のみを除去し、周辺の健常な内皮細胞が中心部へ遊走・再生することで角膜浮腫の消退を図る術式である。Fuchs角膜内皮ジストロフィの早期例が主な適応であったが、近年はMIGSチューブ接触などの限局性角膜浮腫への応用も報告されている。KhanとLinはMIGSデバイス挿入中止後のDescemet膜剥離に伴う角膜浮腫にDSOを施行した症例を報告し、偏心descemetorrhexisで6週間後に浮腫が消退、中心部の角膜内皮細胞密度が検出不能から975 cells/mm²へ回復したと述べている13)。ROCK阻害点眼(リパスジル・ネタルスジル)の補助療法としての併用も検討されている。
Fuchs角膜内皮ジストロフィに対しては、TCF4遺伝子のCTGリピート伸長を標的とするアンチセンスオリゴヌクレオチドや、酸化ストレス経路を標的とする分子治療が基礎研究段階にある。酸化ストレス経路の異常(Nrf2/NQO1シグナル低下、ミトコンドリア機能不全)が細胞死に関与することが示されており、ミトコンドリア保護薬や抗酸化物質の応用が検討されている。
日本発の培養角膜内皮細胞注入療法に加え、諸外国でもiPS細胞や幹細胞由来の角膜内皮細胞を用いた研究が進められている。ドナー角膜1眼分から多数の眼を治療できる可能性があり、世界的な角膜ドナー不足への解決策として期待されている1,14)。加えて、ROCK阻害薬の長期効果・安全性、内皮細胞移動の定量評価、至適濃度・投与期間に関する臨床試験が進行中である。
水疱性角膜症の進行予測や治療反応の評価には、中心角膜厚の経時変化、内皮細胞密度、前眼部OCTによる上皮浮腫・ミクロ嚢胞の検出、涙液中のサイトカイン濃度などが研究されている。術前評価の精度向上により、個々の患者に最適な治療戦略(保存的治療の継続、ROCK阻害点眼、内皮移植、PK)を早期に判断することが期待される。
水疱性角膜症は両眼性に進行することが多く、日常生活における視機能への影響は甚大である。朝方の視力低下は家事や通勤に支障をきたし、進行すると読書・運転・細かい作業が困難となる。近年は、視機能に関する患者報告アウトカム(patient-reported outcome measures, PROMs)を術前後に評価する試みが進んでおり、視覚関連QOLの改善度を客観的に把握することが治療選択の指標として活用されつつある8)。内皮移植前後のVisual Function Questionnaire-14やNEI VFQ-25によるQOL評価では、DMEK群での改善度がより大きい傾向が示されている8)。
水疱性角膜症の治療は、ドナー角膜を用いた全層または内皮移植から、選択的な細胞治療・薬物治療・人工内皮デバイスへと多様化しつつある。日本発の培養角膜内皮細胞前房内注入療法はその先駆けであり、世界的な角膜ドナー不足に対する解決策として注目されている。ROCK阻害点眼の応用範囲拡大、EndoArtの臨床普及、DSOの適応拡大、遺伝子治療の実用化により、今後10年で治療の選択肢はさらに広がることが期待される。早期診断と段階的治療戦略の確立により、角膜移植の必要性を減少させ、患者の視機能と生活の質を大きく改善することが目標である。
Jukić A, Pavan J, Čapić Ivančić B, et al. RhoKinase (ROCK) Inhibition as a Therapeutic Strategy for Pseudophakic Bullous Keratopathy: A Comprehensive Review. J Clin Med. 2025;14(17):6093.
European Society of Cataract and Refractive Surgeons. ESCRS Clinical Guidelines for Cataract Surgery. 2024.
Singhal A, Kaushik J, Singh A, et al. Descemet Stripping Endothelial Keratoplasty in Microcornea for Pseudophakic Bullous Keratopathy With Anterior Chamber Intraocular Lens. Cureus. 2021;13(11):e19262.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Vandevenne MMS, Berendschot TTJM, Visser N, Dickman MM, Nuijts RMMA. Late-onset corneal edema after customized crosslinking for progressive keratoconus. Am J Ophthalmol Case Rep. 2024;35:102090.
Chu MJ, Song M, Palmares T, Song A, Song J. Rhopressa-induced corneal edema: a case report. J Med Case Rep. 2021;15:182.
Arici C, Mergen B, Kılıçarslan O, Ağaçhan A, Tülü Aygün B, Özdamar A. Diffuse corneal edema after uneventful pterygium surgery: toxic anterior segment syndrome or toxic keratopathy? Turk J Ophthalmol. 2022;52:69-71.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. BMJ Open Ophthalmol. 2023;8:e001397.
American Academy of Ophthalmology Cornea/External Disease PPP Panel. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2019.
Erdinest N, Shemesh N, Weill Y, et al. Managing pseudophakic bullous keratopathy with a topical rho kinase inhibitor: a case series. J Med Case Rep. 2025;19:214.
Tone SO, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: the vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Auffarth GU, Son HS, Koch M, et al. Implantation of an artificial endothelial layer for treatment of chronic corneal edema. Cornea. 2021;40:1633-1638.
Khan NC, Lin CC. Descemet stripping only for Descemet’s membrane detachment and sectoral corneal edema. Am J Ophthalmol Case Rep. 2023;29:101784.
Kinoshita S, Koizumi N, Okumura N, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.