Grade 0-1(無〜軽症)
所見: 中央部に12個以下(Grade 0)または12個超の非融合性 guttae(Grade 1)
症状: 通常無症状。スペキュラマイクロスコープで dark spot として検出される。

フックス角膜内皮ジストロフィ(Fuchs Endothelial Corneal Dystrophy; FECD)は、角膜内皮細胞が両眼性に異常をきたす進行性疾患である。1910年 Ernst Fuchs が13例の症例を「dystrophia epithelialis corneae」として初報告し、後に内皮疾患であることが判明して現在の名称となった1)。
角膜中央部の内皮面に滴状角膜(guttae/guttata)が出現し、徐々に周辺へ広がる。内皮細胞のバリア機能・ポンプ機能(Na⁺/K⁺-ATPase)が低下すると角膜実質の浮腫、さらに上皮浮腫・水疱形成へと進行する。Descemet膜が肥厚し不整となることで角膜の透明性が失われる。
IC3D(国際角膜ジストロフィ分類)第2版(Weiss 2015)では、FECDは「角膜内皮ジストロフィ」カテゴリに分類される15)。発症時期によって以下の2型に大別される。
| 指標 | 数値 | 出典 |
|---|---|---|
| 白内障術前患者の滴状角膜頻度 | 1.2% | 国内多施設調査 |
| 日本・Kumejima Study 40歳以上有病率 | 4.1% | Higa 20117) |
| 日本・女性有病率(40歳以上) | 5.8% | Higa 20117) |
| 日本・男性有病率(40歳以上) | 2.4% | Higa 20117) |
| アイスランド・Reykjavik Eye Study 55歳以上 | 女性11%, 男性7% | Zoega 200610) |
| 男女比(国際) | 2.5:1〜3.5:1(女性優位) | Matthaei 20191) |
| 日本人におけるTCF4リピート拡張の頻度 | 47例中12例(26%) | Nakano 20158) |
黄色人種である日本人は、白色人種・黒色人種に比べてFECDの発症頻度が低い傾向がある。しかし、わが国でも高齢化社会の進行に伴い、今後さらに増加すると予測される。日本人は白人に比べ角膜内皮細胞密度が高いため、相対的に発症が遅いと考えられている。
狭隅角眼が多い日本人ではレーザー虹彩切開術(LI)後に内皮細胞が減少する症例が少なくなく、FECDの早期発見に注意が必要である。
沖縄・久米島で行われた住民研究(Kumejima Study)では、40歳以上の4.1%に角膜 guttae が検出されました。女性では5.8%、男性では2.4%でした7)。白内障術前検査を受けた患者の1.2%に滴状角膜がみられるという国内データもあります。日本人は欧米人より頻度が低いとされていますが、長寿化社会とともに増加傾向にあります。
通常、50歳以下では無症状で推移する。症状は浮腫の程度と相関しながら緩徐に進行する。
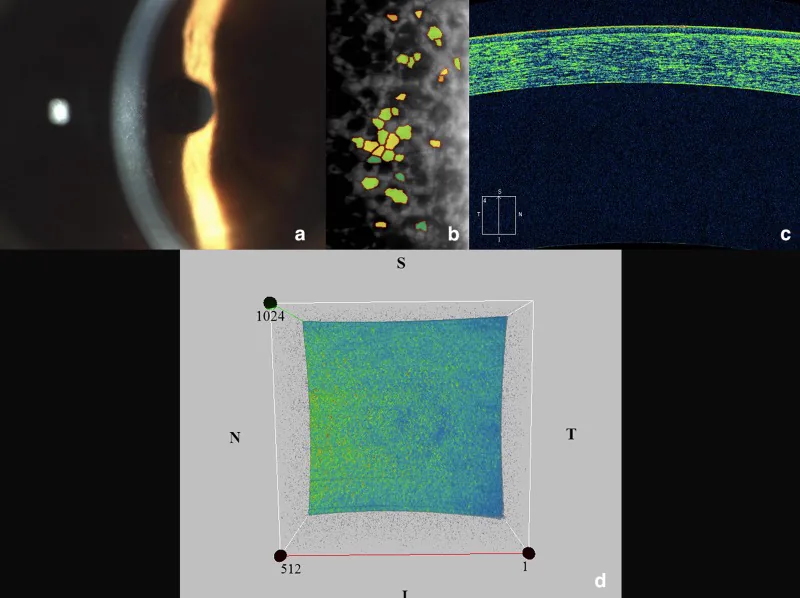
細隙灯顕微鏡検査が基本である。直接照明・後方散乱照明・鏡面反射法を組み合わせて観察する。
Grade 0-1(無〜軽症)
所見: 中央部に12個以下(Grade 0)または12個超の非融合性 guttae(Grade 1)
症状: 通常無症状。スペキュラマイクロスコープで dark spot として検出される。
Grade 2-3(中等症)
所見: 中央1〜5 mmに融合性 guttae。軽度の beaten-metal appearance。
症状: 朝方の霧視。スペキュラで内皮像が不鮮明になる。
Grade 4(重症)
所見: 中央5 mm超の広範融合性 guttae。色素沈着を伴う beaten-metal appearance。
症状: 朝方から日中にかけての持続的霧視・羞明。
Grade 4+浮腫(最重症)
所見: 実質浮腫・上皮浮腫・水疱形成。角膜混濁が著明。
症状: 終日の重篤な視力低下・眼痛・流涙。生活の質が著しく低下。
この臨床的病期分類は Krachmer ら(1978年)による修正分類に基づく5)。
スリットランプ所見の詳細:
健康な角膜は内皮細胞が常に水分を前房側へポンプアウトして透明性を保っています。FECDでは内皮のポンプ機能が低下しているため、眠っている間(まぶたを閉じている間)は蒸発による水分排出も止まり、朝方に角膜が最も浮腫んで霧視が強くなります。目を開けていると角膜表面から水分が蒸発し、昼間は浮腫がある程度改善するため視力が回復します。病気が進行するとこの日内変動がなくなり、終日霧視が続くようになります。
FECDは常染色体優性遺伝が主体だが、浸透率(penetrance)や表現度(expressivity)にばらつきがあり、家族歴が明らかでない例も存在する。
主要原因遺伝子:
日本人では TCF4 リピート拡張の頻度が欧米より低いため、他の遺伝的背景の解明が求められている8)。
FECDは主に常染色体優性遺伝のパターンで遺伝します。理論上、子どもへの遺伝確率は50%です。ただし発症の時期や重症度には大きなばらつきがあり(浸透率が不完全)、遺伝子を受け継いでも症状がごく軽微なまま一生を過ごす方も多くいます。特に日本人では欧米で最多原因であるTCF4遺伝子異常の割合が低く8)、遺伝背景が異なる可能性があります。ご心配な場合は遺伝専門医へのご相談をお勧めします。
日本の統一された診断基準は存在しないが、以下の検査を組み合わせた臨床診断が行われる。
FECD の診断・経過観察に最も重要な検査である。
| パラメータ | 正常値 | 異常の閾値 |
|---|---|---|
| 内皮細胞密度(新生児期) | 3,500〜4,000 cells/mm² | — |
| 内皮細胞密度(20代) | 2,700 cells/mm² | — |
| 内皮細胞密度(70歳以上) | 平均 2,200 cells/mm² | — |
| 透明性維持限界 | — | 400〜500 cells/mm² 以下 |
| CV値(変動係数) | 0.2〜0.3 | ≥ 0.35 |
| 六角形細胞出現率(hexagonality) | 60〜70% | ≤ 50% |
| 疾患 | 鑑別のポイント |
|---|---|
| 後部多形性角膜ジストロフィ(PPCD) | AD遺伝、両眼性、Descemet膜の帯状・水疱様混濁。遺伝子は PPCD1(20p11.2-q11.2)、PPCD2(COL8A2)、PPCD3(ZEB1) |
| 先天性遺伝性角膜内皮ジストロフィ(CHED) | AR遺伝(SLC4A11変異)、出生時〜乳児期発症、出生時から角膜浮腫・混濁 |
| 偽水晶体性水疱性角膜症(PBK) | 白内障手術後の内皮障害。guttae なし、手術歴あり |
| 偽落屑症候群角膜症 | PEX物質沈着、眼圧上昇、水晶体前面のPEX物質が鑑別の鍵 |
| ICE(虹彩角膜内皮)症候群 | 片眼性、虹彩萎縮・前方癒着・緑内障を伴う。guttae なし |
| 狭隅角眼の内皮変化 | 滴状角膜様所見が出ることがある。眼圧・隅角形態で鑑別 |
スペキュラーマイクロスコープ(鏡面反射型内皮細胞撮影装置)は、角膜の最内層にある内皮細胞を特殊な光の反射を利用して非侵襲的に撮影・計測する装置です。検査では内皮細胞の数(細胞密度)・大きさのばらつき(CV値)・形の均一性(六角形細胞率)などを測定します。FECDでは guttae の部分が黒い点(dark spot)として映り、病期の評価に役立ちます。撮影は数分で終わり、痛みはありません。
治療の目標は角膜透明性の回復と視力の維持である。病期に応じて対症療法から手術療法を選択する。
手術適応前の症状緩和を目的とする。内皮細胞数の回復や病勢進行の抑制効果はない。
DMEK(デスメ膜角膜内皮移植術)
グラフト: Descemet膜+内皮のみ(厚さ約15 μm)
特徴: 2006年 Melles が初報告11)。視力回復が速く、拒絶率が低い。熟練した術者が必要。
日本保険適用: 2016年〜
DSAEK(デスメ膜剥離自動装置補助角膜内皮移植術)
PKP(全層角膜移植)
グラフト: 全層角膜(直径7.0〜8.5 mm)
特徴: 古典的な選択肢。縫合・乱視管理・長期の拒絶リスクが課題。FECD分野では内皮移植術に徐々に置換されている。
DSO(Descemetorhexis Without Endothelial Keratoplasty)
手技: Descemet膜中央4 mmを選択的に剥離のみ。グラフト不要。
適応: 残存末梢内皮細胞が中央へ遊走・増殖できる症例。約75%で角膜透明化14)。
ROCK阻害点眼: リパスジルを術後に併用することで不応例でも透明化が促進される14)。
| 指標 | DMEK | UT-DSAEK | 出典 |
|---|---|---|---|
| 12か月BCVA(logMAR差) | −0.06(DMEK優位) | — | Sela 2023 メタ解析3) |
| 20/25以上達成率 | 66% | 33%(p=0.02) | Dunker 2020 RCT4) |
| リバブリングのOR | — | 2.76(DSAEK优位) | Sela 20233) |
| 12か月ECD | 差なし | 差なし | Dunker 20204) |
| グラフト厚 <70 μm | — | DMEKと視力差なし | Sela 20233) |
Sela ら(2023年)のメタ解析(8研究376眼)では、12か月時点のBCVAはDMEKが有意に良好だった(−0.06 logMAR)3)。Dunker ら(2020年)の多施設RCTでもDMEKは UT-DSAEK より20/25以上達成率が高かった(66% vs 33%, p=0.02)4)。ただしグラフト厚70 μm未満のUT-DSAEKではDMEKとの差が縮小した3)。
京都大学グループ(Kinoshita 2018)は、培養した健常ドナー角膜内皮細胞をROCK阻害薬(Y-27632)と同時に前房内注入する治療法を開発した13)。
ROCK阻害薬は内皮細胞の接着促進・アポトーシス抑制・細胞周期進行を促すことで効果を発揮する13)。
FECDでは白内障との合併が多く、手術時期と方法の選択に注意が必要である。
正常角膜内皮細胞は前房内では細胞分裂が起こらない。内皮が欠損すると隣接する細胞が拡大・遊走して欠損部を補うため、細胞密度は加齢とともに不可逆的に低下する。400〜500 cells/mm² を下回ると角膜の透明性維持が困難になる。
FECDでは変性した内皮細胞が異常なコラーゲン様物質をDescemet膜後面に産生・堆積させ、guttae を形成する。Descemet膜は肥厚・不整となり、内皮機能をさらに障害する悪循環が成立する。
加齢・UV曝露・喫煙はいずれも酸化ストレスを増大させ、悪循環の入り口となる2)。
角膜内皮のポンプ機能は Na⁺/K⁺-ATPase に依存する。内皮細胞が障害されると以下の経路で浮腫が生じる。
角膜実質の膨潤圧を超えるような眼圧上昇(高眼圧)がある場合は、内皮が比較的健常でも上皮浮腫が生じることがあり注意を要する。
日本人ではTCF4リピート拡張の寄与が相対的に小さいため8)、日本人に特有の遺伝的・環境的背景の解明が今後の重要課題である。
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.