ग्रेड 0-1 (अनुपस्थित से हल्का)
निष्कर्ष: केंद्रीय क्षेत्र में 12 या उससे कम गैर-संगम गुट्टे (ग्रेड 0) या 12 से अधिक गैर-संगम गुट्टे (ग्रेड 1)।
लक्षण: आमतौर पर लक्षणहीन। स्पेक्युलर माइक्रोस्कोप में डार्क स्पॉट के रूप में पता लगाया जाता है।

फुक्स कॉर्नियल एंडोथेलियल डिस्ट्रोफी (FECD) एक प्रगतिशील बीमारी है जिसमें कॉर्नियल एंडोथेलियल कोशिकाएं द्विपक्षीय रूप से असामान्य हो जाती हैं। 1910 में अर्न्स्ट फुक्स ने 13 मामलों को ‘डिस्ट्रोफिया एपिथेलियलिस कॉर्निया’ के रूप में पहली बार रिपोर्ट किया, और बाद में यह पाया गया कि यह एक एंडोथेलियल रोग है, जिससे वर्तमान नाम आया 1)।
कॉर्निया के केंद्रीय एंडोथेलियल सतह पर गुट्टे (guttae/guttata) दिखाई देते हैं और धीरे-धीरे परिधि की ओर फैलते हैं। जब एंडोथेलियल कोशिकाओं का अवरोध और पंप कार्य (Na⁺/K⁺-ATPase) कम हो जाता है, तो कॉर्नियल स्ट्रोमा में एडिमा होती है, फिर उपकला एडिमा और बुला गठन होता है। डेसीमेट झिल्ली मोटी और अनियमित हो जाती है, जिससे कॉर्निया की पारदर्शिता खत्म हो जाती है।
IC3D (अंतर्राष्ट्रीय कॉर्नियल डिस्ट्रोफी वर्गीकरण) दूसरे संस्करण (Weiss 2015) में, FECD को ‘कॉर्नियल एंडोथेलियल डिस्ट्रोफी’ श्रेणी में वर्गीकृत किया गया है 15)। शुरुआत की उम्र के अनुसार इसे दो मुख्य प्रकारों में विभाजित किया गया है।
| संकेतक | मान | स्रोत |
|---|---|---|
| मोतियाबिंद सर्जरी से पहले रोगियों में गुट्टाटा कॉर्निया की आवृत्ति | 1.2% | राष्ट्रीय बहुकेंद्रीय सर्वेक्षण |
| जापान (कुमेजिमा अध्ययन) में 40 वर्ष और उससे अधिक आयु में व्यापकता | 4.1% | Higa 20117) |
| जापानी महिलाओं में व्यापकता (40 वर्ष और अधिक) | 5.8% | Higa 20117) |
| जापान में पुरुष प्रसार (40 वर्ष और अधिक) | 2.4% | Higa 20117) |
| आइसलैंड - रेक्जाविक आई स्टडी, 55 वर्ष और अधिक | महिलाएं 11%, पुरुष 7% | Zoega 200610) |
| लिंग अनुपात (अंतर्राष्ट्रीय) | 2.5:1 से 3.5:1 (महिला प्रधान) | Matthaei 20191) |
| जापानियों में TCF4 पुनरावृत्ति विस्तार की आवृत्ति | 47 में से 12 मामले (26%) | Nakano 20158) |
पीली जाति के जापानी, श्वेत और अश्वेत जातियों की तुलना में FECD की कम घटना दर रखते हैं। हालांकि, जापान में बढ़ती वृद्ध आबादी के साथ, भविष्य में इसमें और वृद्धि होने का अनुमान है। माना जाता है कि जापानियों में श्वेतों की तुलना में कॉर्नियल एंडोथेलियल कोशिका घनत्व अधिक होता है, जिससे रोग की शुरुआत अपेक्षाकृत देर से होती है।
संकीर्ण कोण वाले कई जापानियों में, लेजर इरिडोटॉमी (LI) के बाद एंडोथेलियल कोशिकाओं में कमी असामान्य नहीं है, और FECD के शीघ्र पता लगाने के लिए सावधानी आवश्यक है।
ओकिनावा के कुमेजिमा में किए गए एक जनसंख्या अध्ययन (कुमेजिमा स्टडी) में, 40 वर्ष और उससे अधिक आयु के 4.1% लोगों में कॉर्नियल गुट्टे पाए गए। महिलाओं में यह 5.8% और पुरुषों में 2.4% था 7)। मोतियाबिंद सर्जरी से पहले जांचे गए रोगियों में से 1.2% में गुट्टेट कॉर्निया पाए जाने का राष्ट्रीय डेटा भी है। जापानियों में यूरोपीय या अमेरिकियों की तुलना में आवृत्ति कम मानी जाती है, लेकिन बढ़ती उम्र की आबादी के साथ इसमें वृद्धि हो रही है।
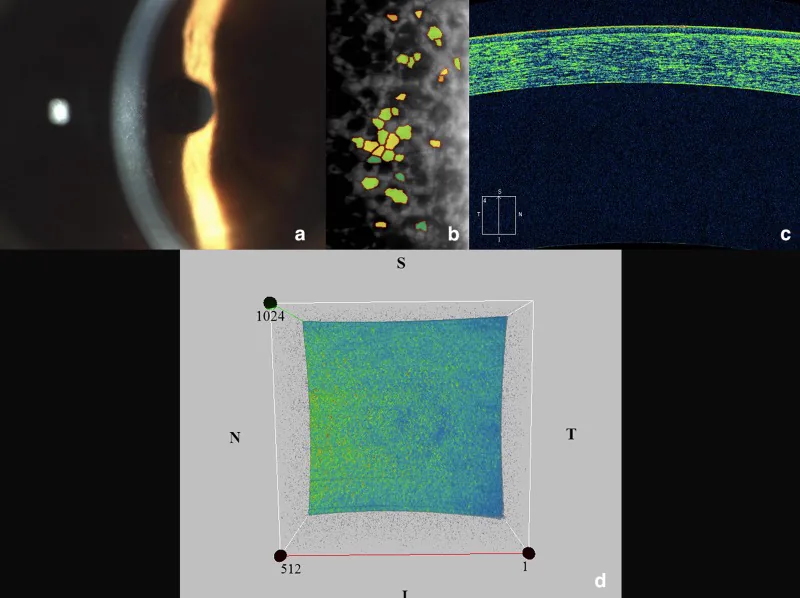
आमतौर पर, 50 वर्ष की आयु से पहले रोग लक्षणहीन होता है। लक्षण एडिमा की डिग्री के साथ सहसंबंधित होते हुए धीरे-धीरे बढ़ते हैं।
स्लिट लैंप माइक्रोस्कोपी मौलिक है। प्रत्यक्ष प्रकाश, पश्च प्रकीर्णन और दर्पण प्रतिबिंब विधियों को संयोजित किया जाता है।
ग्रेड 0-1 (अनुपस्थित से हल्का)
निष्कर्ष: केंद्रीय क्षेत्र में 12 या उससे कम गैर-संगम गुट्टे (ग्रेड 0) या 12 से अधिक गैर-संगम गुट्टे (ग्रेड 1)।
लक्षण: आमतौर पर लक्षणहीन। स्पेक्युलर माइक्रोस्कोप में डार्क स्पॉट के रूप में पता लगाया जाता है।
ग्रेड 2-3 (मध्यम)
निष्कर्ष: केंद्रीय 1-5 मिमी में संगम गुट्टे। हल्का बीटन-मेटल दिखावट।
लक्षण: सुबह धुंधली दृष्टि। स्पेकुलर माइक्रोस्कोपी में एंडोथेलियम अस्पष्ट दिखता है।
ग्रेड 4 (गंभीर)
निष्कर्ष: केंद्रीय 5 मिमी से अधिक व्यापक संगम गुट्टे। वर्णक जमाव के साथ बीटन-मेटल दिखावट।
लक्षण: सुबह से दिन भर लगातार धुंधली दृष्टि, प्रकाश के प्रति संवेदनशीलता।
ग्रेड 4+ शोथ (अत्यंत गंभीर)
निष्कर्ष: स्ट्रोमल शोथ, उपकला शोथ, बुला निर्माण। कॉर्निया में स्पष्ट धुंधलापन।
लक्षण: पूरे दिन गंभीर दृष्टि हानि, आंख में दर्द, आंसू आना। जीवन की गुणवत्ता में काफी कमी।
यह नैदानिक चरणीकरण क्रैचमर एट अल. (1978) द्वारा संशोधित वर्गीकरण पर आधारित है5)।
स्लिट लैंप निष्कर्षों का विवरण:
स्वस्थ कॉर्निया में, एंडोथेलियल कोशिकाएं पारदर्शिता बनाए रखने के लिए लगातार पानी को पूर्वकाल कक्ष में पंप करती हैं। FECD में, एंडोथेलियल पंप फ़ंक्शन कम हो जाता है, इसलिए सोते समय (पलकें बंद होने पर) वाष्पीकरण द्वारा पानी का निष्कासन भी रुक जाता है, और सुबह कॉर्निया सबसे अधिक सूजा हुआ होता है और धुंधली दृष्टि बढ़ जाती है। आँखें खोलने पर, कॉर्निया की सतह से पानी वाष्पित हो जाता है, और दिन के दौरान सूजन कुछ हद तक कम हो जाती है, जिससे दृष्टि में सुधार होता है। जैसे-जैसे बीमारी बढ़ती है, यह दैनिक भिन्नता गायब हो जाती है और पूरे दिन धुंधली दृष्टि बनी रहती है।
FECD मुख्य रूप से ऑटोसोमल प्रमुख वंशानुक्रम है, लेकिन पैठ और अभिव्यक्ति में भिन्नता होती है, और कुछ मामलों में स्पष्ट पारिवारिक इतिहास नहीं होता है।
प्रमुख कारण जीन :
जापानियों में, TCF4 रिपीट विस्तार की आवृत्ति पश्चिम की तुलना में कम है, इसलिए अन्य आनुवंशिक पृष्ठभूमि की व्याख्या की आवश्यकता है8)।
FECD मुख्य रूप से ऑटोसोमल डॉमिनेंट पैटर्न में वंशानुगत होता है। सैद्धांतिक रूप से, बच्चे में संचरण की संभावना 50% है। हालांकि, शुरुआत की उम्र और गंभीरता में काफी भिन्नता होती है (अपूर्ण पैठ); जीन प्राप्त करने वाले कई लोग जीवन भर बहुत हल्के लक्षणों के साथ रहते हैं। विशेष रूप से जापानियों में, पश्चिमी देशों में सबसे आम कारण TCF4 जीन असामान्यता का अनुपात कम है8), और आनुवंशिक पृष्ठभूमि भिन्न हो सकती है। यदि चिंता है, तो आनुवंशिक विशेषज्ञ से परामर्श की सलाह दी जाती है।
जापान में कोई एकीकृत निदान मानदंड नहीं है, लेकिन निम्नलिखित जांचों के संयोजन से नैदानिक निदान किया जाता है।
FECD के निदान और अनुवर्ती के लिए यह सबसे महत्वपूर्ण जांच है।
| पैरामीटर | सामान्य मान | असामान्यता की सीमा |
|---|---|---|
| एंडोथेलियल कोशिका घनत्व (नवजात अवधि) | 3,500 से 4,000 कोशिकाएं/मिमी² | — |
| एंडोथेलियल कोशिका घनत्व (20 वर्ष की आयु) | 2,700 कोशिकाएं/मिमी² | — |
| एंडोथेलियल कोशिका घनत्व (70 वर्ष और अधिक) | औसत 2,200 कोशिकाएं/मिमी² | — |
| पारदर्शिता बनाए रखने की सीमा | — | 400 से 500 कोशिकाएं/मिमी² या उससे कम |
| CV मान (भिन्नता गुणांक) | 0.2 से 0.3 | ≥ 0.35 |
| षट्कोणीय कोशिका दर (hexagonality) | 60-70% | ≤ 50% |
| रोग | विभेदक निदान के बिंदु |
|---|---|
| पोस्टीरियर पॉलीमॉर्फस कॉर्नियल डिस्ट्रॉफी (PPCD) | AD वंशानुक्रम, द्विपक्षीय, डेसीमेट झिल्ली का बैंड-जैसा और बुलस धुंधलापन। जीन: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| जन्मजात वंशानुगत कॉर्नियल एंडोथेलियल डिस्ट्रॉफी (CHED) | AR वंशानुक्रम (SLC4A11 उत्परिवर्तन), जन्म से या शैशवावस्था में शुरुआत, जन्म से कॉर्नियल एडिमा और धुंधलापन |
| स्यूडोफेकिक बुलस केराटोपैथी (PBK) | मोतियाबिंद सर्जरी के बाद एंडोथेलियल क्षति। गुट्टे नहीं, सर्जरी का इतिहास |
| स्यूडोएक्सफोलिएशन सिंड्रोम केराटोपैथी | PEX पदार्थ का जमाव, अंतर्गर्भाशयी दबाव में वृद्धि, लेंस की पूर्वकाल सतह पर PEX पदार्थ विभेदन की कुंजी है |
| ICE (इरिडोकॉर्नियल एंडोथेलियल) सिंड्रोम | एकपक्षीय, परितारिका शोष, पूर्वकाल सिनेशिया और ग्लूकोमा के साथ। गुट्टे नहीं |
| संकीर्ण कोण वाली आंखों में एंडोथेलियल परिवर्तन | कभी-कभी गुटेट कॉर्निया जैसा दिखाई दे सकता है। अंतर्गर्भाशयी दबाव और कोण आकृति विज्ञान द्वारा विभेदन |
स्पेक्युलर माइक्रोस्कोप (स्पेक्युलर रिफ्लेक्शन एंडोथेलियल सेल फोटोग्राफी उपकरण) एक उपकरण है जो कॉर्निया की सबसे भीतरी परत में एंडोथेलियल कोशिकाओं को विशेष प्रकाश प्रतिबिंब का उपयोग करके गैर-आक्रामक रूप से फोटोग्राफ और मापता है। परीक्षण एंडोथेलियल कोशिकाओं की संख्या (कोशिका घनत्व), आकार में भिन्नता (CV मान) और आकार की एकरूपता (षट्कोणीय कोशिका प्रतिशत) को मापता है। FECD में, गुट्टे काले धब्बों (डार्क स्पॉट) के रूप में दिखाई देते हैं, जो रोग की अवस्था का आकलन करने में मदद करते हैं। फोटोग्राफी में कुछ मिनट लगते हैं और दर्द रहित होती है।
उपचार का लक्ष्य कॉर्निया की पारदर्शिता बहाल करना और दृष्टि बनाए रखना है। रोग की अवस्था के अनुसार लक्षणात्मक उपचार से लेकर शल्य चिकित्सा तक का चयन किया जाता है।
इसका उद्देश्य शल्य चिकित्सा से पहले लक्षणों को कम करना है। इसका एंडोथेलियल कोशिका संख्या की बहाली या रोग की प्रगति को रोकने पर कोई प्रभाव नहीं है।
DMEK (डेसिमेट झिल्ली एंडोथेलियल केराटोप्लास्टी)
ग्राफ्ट: केवल डेसिमेट झिल्ली + एंडोथेलियम (लगभग 15 μm मोटा)
विशेषताएं: 2006 में मेल्स द्वारा पहली रिपोर्ट 11)। दृष्टि वापसी तेज, अस्वीकृति दर कम। अनुभवी सर्जन की आवश्यकता।
जापान में बीमा कवरेज: 2016 से
DSAEK (डेसिमेट स्ट्रिपिंग ऑटोमेटेड एंडोथेलियल केराटोप्लास्टी)
PKP (पूर्ण मोटाई कॉर्निया प्रत्यारोपण)
ग्राफ्ट: पूर्ण मोटाई कॉर्निया (व्यास 7.0–8.5 मिमी)
विशेषताएँ: क्लासिक विकल्प। टांके, दृष्टिवैषम्य प्रबंधन, दीर्घकालिक अस्वीकृति जोखिम चुनौतियाँ हैं। FECD क्षेत्र में धीरे-धीरे एंडोथेलियल प्रत्यारोपण द्वारा प्रतिस्थापित किया जा रहा है।
DSO (डेसीमेटोरेक्सिस विदाउट एंडोथेलियल केराटोप्लास्टी)
प्रक्रिया: केवल केंद्रीय डेसीमेट झिल्ली के 4 मिमी का चयनात्मक पृथक्करण। ग्राफ्ट की आवश्यकता नहीं।
संकेत: ऐसे मामले जहां शेष परिधीय एंडोथेलियल कोशिकाएं केंद्र की ओर प्रवास और प्रसार कर सकती हैं। लगभग 75% में कॉर्निया पारदर्शिता 14)।
ROCK अवरोधक आई ड्रॉप: पश्चात में रिपासुडिल का उपयोग करने से अप्रतिक्रियाशील मामलों में भी पारदर्शिता बढ़ती है 14)।
| संकेतक | DMEK | UT-DSAEK | स्रोत |
|---|---|---|---|
| 12 महीने BCVA (logMAR अंतर) | −0.06 (DMEK श्रेष्ठ) | — | Sela 2023 मेटा-विश्लेषण3) |
| 20/25 या उससे बेहतर प्राप्ति दर | 66% | 33% (p=0.02) | Dunker 2020 RCT4) |
| री-बबलिंग का OR | — | 2.76 (DSAEK के पक्ष में) | Sela 20233) |
| 12 महीने का ECD | कोई अंतर नहीं | कोई अंतर नहीं | Dunker 20204) |
| ग्राफ्ट मोटाई <70 μm | — | DMEK से दृष्टि में कोई अंतर नहीं | Sela 20233) |
Sela एट अल. (2023) के मेटा-विश्लेषण (8 अध्ययन, 376 आंखें) में, 12 महीने में BCVA DMEK में काफी बेहतर था (−0.06 logMAR)3)। Dunker एट अल. (2020) के बहुकेंद्रीय RCT में भी DMEK में UT-DSAEK की तुलना में 20/25 या उससे अधिक प्राप्त करने की दर अधिक थी (66% बनाम 33%, p=0.02)4)। हालांकि, 70 μm से कम मोटाई वाले UT-DSAEK ग्राफ्ट में DMEK के साथ अंतर कम हो गया3)।
क्योटो विश्वविद्यालय समूह (Kinoshita 2018) ने ROCK अवरोधक (Y-27632) के साथ संवर्धित स्वस्थ दाता कॉर्नियल एंडोथेलियल कोशिकाओं को पूर्वकाल कक्ष में इंजेक्ट करने की एक चिकित्सा विकसित की13)।
ROCK अवरोधक एंडोथेलियल कोशिका आसंजन को बढ़ावा देकर, एपोप्टोसिस को रोककर और कोशिका चक्र प्रगति को उत्तेजित करके प्रभाव डालता है13)।
FECD में मोतियाबिंद का सह-अस्तित्व आम है, इसलिए सर्जरी के समय और विधि के चयन पर ध्यान देने की आवश्यकता है।
DMEK, अपने बहुत पतले ग्राफ्ट (लगभग 15 μm) के कारण, तेजी से दृष्टि सुधार और कम पोस्टऑपरेटिव अपवर्तक परिवर्तन प्रदान करता है। मेटा-विश्लेषणों में भी 12 महीने में BCVA DMEK में बेहतर पाया गया3)। दूसरी ओर, DSAEK ग्राफ्ट को संभालना थोड़ा आसान है, सर्जन के लिए सीखने की अवधि कम है, और जापान में व्यापक रूप से किया जाता है। अल्ट्रा-थिन DSAEK (<70 μm) के साथ DMEK के लगभग बराबर दृश्य परिणाम प्राप्त होने की रिपोर्टें हैं3)। चयन सर्जन के अनुभव, संस्थान के अनुभव और रोगी के कॉर्नियल स्थिति के आधार पर किया जाता है। दोनों प्रक्रियाएं जापान में 2016 (DMEK) या 2009 (DSAEK) से बीमा द्वारा कवर की जाती हैं।
सामान्य कॉर्नियल एंडोथीलियल कोशिकाएं पूर्वकाल कक्ष में कोशिका विभाजन नहीं करती हैं। जब एंडोथीलियम में दोष होता है, तो आसन्न कोशिकाएं फैलकर और स्थानांतरित होकर दोष को भरती हैं, जिससे उम्र के साथ कोशिका घनत्व अपरिवर्तनीय रूप से कम हो जाता है। 400-500 कोशिकाएं/मिमी² से नीचे, कॉर्निया की पारदर्शिता बनाए रखना मुश्किल हो जाता है।
FECD में, अध:पतित एंडोथीलियल कोशिकाएं डेसीमेट झिल्ली की पिछली सतह पर असामान्य कोलेजन जैसे पदार्थों का उत्पादन और जमाव करती हैं, जिससे गुट्टे (guttae) बनते हैं। डेसीमेट झिल्ली मोटी और अनियमित हो जाती है, जिससे एंडोथीलियल कार्य और बाधित होता है और एक दुष्चक्र स्थापित होता है।
उम्र बढ़ना, यूवी जोखिम और धूम्रपान सभी ऑक्सीडेटिव तनाव को बढ़ाते हैं और दुष्चक्र के प्रवेश द्वार के रूप में कार्य करते हैं2)।
कॉर्नियल एंडोथेलियम का पंप फंक्शन Na⁺/K⁺-ATPase पर निर्भर करता है। जब एंडोथेलियल कोशिकाएं क्षतिग्रस्त हो जाती हैं, तो निम्नलिखित मार्गों से एडिमा उत्पन्न होती है।
यदि कॉर्नियल स्ट्रोमा की सूजन दबाव से अधिक अंतःनेत्र दबाव (उच्च अंतःनेत्र दबाव) में वृद्धि होती है, तो एंडोथेलियम अपेक्षाकृत स्वस्थ होने पर भी उपकला एडिमा हो सकती है, जिस पर ध्यान देने की आवश्यकता है।
जापानियों में TCF4 रिपीट विस्तार का योगदान अपेक्षाकृत छोटा होने के कारण8), जापानियों के लिए विशिष्ट आनुवंशिक और पर्यावरणीय पृष्ठभूमि का स्पष्टीकरण भविष्य का एक महत्वपूर्ण मुद्दा है।
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.