Grade 0-1 (없음 ~ 경증)
소견: 중심부에 12개 이하(Grade 0) 또는 12개 초과의 비융합성 구타(Grade 1)
증상: 일반적으로 무증상. 스페큘러 현미경에서 암점(dark spot)으로 검출됩니다.

푹스 각막내피이영양증(FECD)은 각막내피세포가 양안성으로 이상을 일으키는 진행성 질환입니다. 1910년 Ernst Fuchs가 13예를 “dystrophia epithelialis corneae”로 처음 보고했으며, 이후 내피 질환임이 밝혀져 현재의 이름이 되었습니다 1).
각막 중심부 내피면에 구타에(guttae/guttata)가 나타나고 점차 주변으로 퍼집니다. 내피세포의 장벽 및 펌프 기능(Na⁺/K⁺-ATPase)이 저하되면 각막 실질 부종이 발생하고, 상피 부종 및 수포 형성으로 진행됩니다. Descemet막이 두꺼워지고 불규칙해지면서 각막 투명성이 소실됩니다.
IC3D(국제 각막 이영양증 분류) 제2판(Weiss 2015)에서 FECD는 ‘각막 내피 이영양증’ 범주로 분류됩니다15). 발병 시기에 따라 다음과 같은 두 가지 유형으로 크게 나뉩니다.
| 지표 | 수치 | 출처 |
|---|---|---|
| 백내장 수술 전 환자의 각막 내피 소적 빈도 | 1.2% | 국내 다기관 조사 |
| 일본 Kumejima 연구 40세 이상 유병률 | 4.1% | Higa 20117) |
| 일본 여성 유병률(40세 이상) | 5.8% | Higa 20117) |
| 일본: 남성 유병률 (40세 이상) | 2.4% | Higa 20117) |
| 아이슬란드: 레이캬비크 안 연구, 55세 이상 | 여성 11%, 남성 7% | Zoega 200610) |
| 성비 (국제) | 2.5:1 ~ 3.5:1 (여성 우세) | Matthaei 20191) |
| 일본인에서 TCF4 반복 확장 빈도 | 47예 중 12예 (26%) | Nakano 20158) |
황인종인 일본인은 백인종 및 흑인종에 비해 FECD 발병률이 낮은 경향이 있습니다. 그러나 일본에서도 고령화 사회가 진행됨에 따라 앞으로 더 증가할 것으로 예상됩니다. 일본인은 백인에 비해 각막 내피 세포 밀도가 높기 때문에 상대적으로 발병이 늦은 것으로 생각됩니다.
좁은 전방각이 많은 일본인에서는 레이저 홍채 절개술(LI) 후 내피 세포가 감소하는 증례가 적지 않으며, FECD의 조기 발견에 주의가 필요합니다.
오키나와 구메지마에서 수행된 주민 연구(Kumejima Study)에서 40세 이상의 4.1%에서 각막 구타(corneal guttae)가 검출되었습니다. 여성은 5.8%, 남성은 2.4%였습니다7). 백내장 수술 전 검사를 받은 환자의 1.2%에서 적상 각막(cornea guttata)이 관찰되었다는 국내 데이터도 있습니다. 일본인은 서양인보다 빈도가 낮은 것으로 알려져 있지만, 고령화 사회와 함께 증가 추세에 있습니다.
일반적으로 50세 이하에서는 무증상으로 경과합니다. 증상은 부종의 정도와 상관관계를 가지며 서서히 진행됩니다.
세극등 현미경 검사가 기본입니다. 직접 조명, 후방 산란 조명, 경면 반사법을 조합하여 관찰합니다.
Grade 0-1 (없음 ~ 경증)
소견: 중심부에 12개 이하(Grade 0) 또는 12개 초과의 비융합성 구타(Grade 1)
증상: 일반적으로 무증상. 스페큘러 현미경에서 암점(dark spot)으로 검출됩니다.
2-3등급 (중등증)
소견: 중심부 1~5mm에 융합성 구타(guttae). 경도의 두드린 금속판 모양(beaten-metal appearance).
증상: 아침에 시야가 흐림. 경면현미경에서 내피상이 불선명해짐.
4등급 (중증)
소견: 중심부 5mm 초과의 광범위 융합성 구타. 색소침착을 동반한 두드린 금속판 모양.
증상: 아침부터 낮까지 지속적인 시야 흐림 및 눈부심.
4등급+부종 (최중증)
소견: 실질부종, 상피부종, 수포 형성. 각막 혼탁이 현저함.
증상: 하루 종일 심한 시력 저하, 안통, 눈물. 삶의 질이 현저히 저하됨.
이 임상적 병기 분류는 Krachmer 등(1978년)의 수정 분류에 기반합니다5).
세극등 소견 상세:
건강한 각막은 내피세포가 지속적으로 수분을 전방으로 펌프질하여 투명성을 유지합니다. FECD에서는 내피의 펌프 기능이 저하되어 잠을 자는 동안(눈을 감고 있는 동안) 증발에 의한 수분 배출도 중단되어 아침에 각막 부종이 가장 심하고 시야가 흐려집니다. 눈을 뜨고 있으면 각막 표면에서 수분이 증발하여 낮 동안 부종이 어느 정도 개선되어 시력이 회복됩니다. 질환이 진행되면 이러한 일중 변동이 사라지고 하루 종일 시야가 흐려집니다.
FECD는 주로 상염색체 우성 유전이지만 침투율과 표현도에 변이가 있어 가족력이 명확하지 않은 경우도 있습니다.
주요 원인 유전자:
일본인에서는 TCF4 반복 확장의 빈도가 서양보다 낮기 때문에 다른 유전적 배경에 대한 규명이 필요합니다8).
FECD는 주로 상염색체 우성 유전 패턴으로 유전됩니다. 이론적으로 아이에게 유전될 확률은 50%입니다. 그러나 발병 시기와 중증도에는 큰 변이가 있으며(불완전 침투), 유전자를 물려받아도 평생 매우 경미한 증상만 보이는 경우가 많습니다. 특히 일본인에서는 서양에서 가장 흔한 원인인 TCF4 유전자 이상의 비율이 낮아8) 유전적 배경이 다를 수 있습니다. 걱정되시면 유전 전문의와 상담하시기를 권장합니다.
일본에는 통일된 진단 기준이 없지만, 다음 검사를 조합하여 임상 진단을 내립니다.
FECD 진단 및 경과 관찰에 가장 중요한 검사입니다.
| 매개변수 | 정상값 | 이상 역치 |
|---|---|---|
| 내피세포 밀도 (신생아기) | 3,500~4,000 cells/mm² | — |
| 내피세포 밀도 (20대) | 2,700 cells/mm² | — |
| 내피세포 밀도 (70세 이상) | 평균 2,200 cells/mm² | — |
| 투명성 유지 한계 | — | 400~500 cells/mm² 이하 |
| CV값 (변동계수) | 0.2~0.3 | ≥ 0.35 |
| 육각형 세포 출현율 (hexagonality) | 60~70% | ≤ 50% |
| 질환 | 감별 포인트 |
|---|---|
| 후부 다형성 각막 이영양증 (PPCD) | 상염색체 우성 유전, 양안성, 데스메막의 띠 모양 및 수포 모양 혼탁. 유전자: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| 선천성 유전성 각막 내피 이영양증 (CHED) | 상염색체 열성 유전 (SLC4A11 변이), 출생 시~영아기 발병, 출생 시부터 각막 부종 및 혼탁 |
| 인공수정체성 수포성 각막병증 (PBK) | 백내장 수술 후 내피 손상. 구타 없음, 수술 병력 있음 |
| 가성 박리 증후군 각막병증 | PEX 물질 침착, 안압 상승, 수정체 전낭의 PEX 물질이 감별의 핵심 |
| 홍채각막내피 (ICE) 증후군 | 단안성, 홍채 위축, 전방 유착 및 녹내장 동반. 구타 없음 |
| 협우각안의 내피 변화 | 각막 구타 유사 소견이 나타날 수 있음. 안압 및 전방각 형태로 감별 |
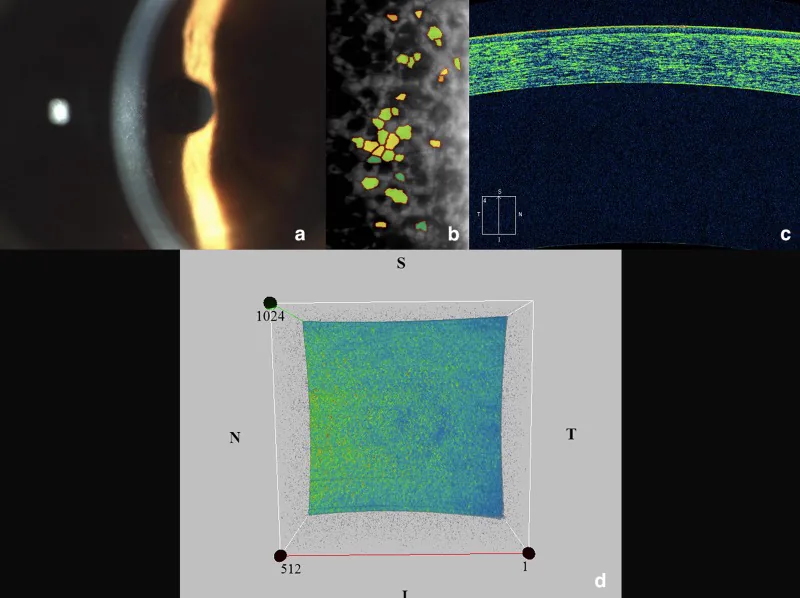
스페큘러 현미경(경면 반사형 내피 세포 촬영 장치)은 특수한 빛 반사를 이용하여 각막 최내층의 내피 세포를 비침습적으로 촬영하고 측정하는 장치입니다. 검사에서는 내피 세포 수(세포 밀도), 크기 변이(CV 값), 형태의 균일성(육각형 세포 비율) 등을 측정합니다. FECD에서는 구타(guttae) 부분이 검은 점(dark spot)으로 나타나 병기 평가에 도움이 됩니다. 촬영은 수 분 내에 끝나며 통증이 없습니다.
치료 목표는 각막 투명성 회복과 시력 유지입니다. 병기에 따라 대증요법에서 수술요법까지 선택합니다.
수술 적응 전 증상 완화를 목적으로 합니다. 내피세포 수 회복이나 병세 진행 억제 효과는 없습니다.
DMEK (데스메막 각막내피이식술)
이식편: Descemet막 + 내피만 (두께 약 15 μm)
특징: 2006년 Melles가 처음 보고11). 시력 회복이 빠르고 거부율이 낮습니다. 숙련된 술자가 필요합니다.
일본 보험 적용: 2016년~
DSAEK (데스메막벗김 자동기기 보조 각막내피이식술)
PKP (전층 각막 이식)
DSO (내피 각막 이식 없는 Descemet막 절제술)
술기: 중심 4 mm Descemet막만 선택적으로 박리. 이식편 불필요.
적응증: 잔여 주변부 내피 세포가 중심으로 이동 및 증식할 수 있는 증례. 약 75%에서 각막 투명화 14).
ROCK 억제제 점안액: 리파수딜을 수술 후 병용하면 불응 증례에서도 투명화가 촉진됨 14).
| 지표 | DMEK | UT-DSAEK | 출처 |
|---|---|---|---|
| 12개월 BCVA (logMAR 차이) | −0.06 (DMEK 우위) | — | Sela 2023 메타분석 3) |
| 20/25 이상 달성률 | 66% | 33%(p=0.02) | Dunker 2020 RCT4) |
| 재기포의 OR | — | 2.76(DSAEK 우세) | Sela 20233) |
| 12개월 ECD | 차이 없음 | 차이 없음 | Dunker 20204) |
| 이식편 두께 <70 μm | — | DMEK와 시력 차이 없음 | Sela 20233) |
Sela 등(2023년)의 메타분석(8개 연구, 376안)에서 12개월 시점의 BCVA는 DMEK에서 유의하게 우수했습니다(−0.06 logMAR)3). Dunker 등(2020년)의 다기관 RCT에서도 DMEK가 UT-DSAEK보다 20/25 이상 달성률이 높았습니다(66% vs 33%, p=0.02)4). 그러나 이식편 두께가 70 μm 미만인 UT-DSAEK에서는 DMEK와의 차이가 줄어들었습니다3).
교토 대학 그룹(Kinoshita 2018)은 배양된 건강한 공여자 각막 내피 세포를 ROCK 억제제(Y-27632)와 함께 전방 내에 주입하는 치료법을 개발했습니다13).
ROCK 억제제는 내피 세포 부착 촉진, 세포자멸사 억제, 세포 주기 진행을 촉진하여 효과를 발휘합니다13).
FECD에서는 백내장이 동반되는 경우가 많아 수술 시기와 방법 선택에 주의가 필요합니다.
DMEK는 가장 얇은 이식편(약 15 μm)을 사용하여 시력 회복이 빠르고 수술 후 굴절 변화가 적은 장점이 있습니다. 메타분석에서도 12개월 BCVA가 DMEK에서 우월했습니다3). 반면 DSAEK는 이식편 조작이 다소 용이하고 술자의 학습 곡선이 짧으며 국내에서도 널리 시행되고 있습니다. 초박형 DSAEK(<70 μm)에서는 DMEK와 거의 동등한 시력 결과를 얻을 수 있다는 보고도 있습니다3). 담당 의사의 경험, 시설의 경험, 환자의 각막 상태를 종합적으로 판단하여 선택합니다. 두 수술 모두 2016년(DMEK) 또는 2009년(DSAEK)부터 국내에서 보험 적용되고 있습니다.
정상 각막 내피세포는 전방 내에서 세포 분열이 일어나지 않습니다. 내피가 결손되면 인접 세포가 확대 및 이동하여 결손 부위를 보충하므로, 세포 밀도는 노화와 함께 비가역적으로 감소합니다. 400~500 cells/mm² 미만으로 떨어지면 각막 투명성 유지가 어려워집니다.
FECD에서는 변성된 내피세포가 비정상적인 콜라겐 유사 물질을 Descemet막 후면에 생성 및 침착시켜 guttae를 형성합니다. Descemet막은 비후 및 불규칙해지며, 내피 기능을 더욱 손상시키는 악순환이 성립됩니다.
노화, 자외선 노출, 흡연은 모두 산화 스트레스를 증가시켜 악순환의 입구가 됩니다 2).
각막 내피의 펌프 기능은 Na⁺/K⁺-ATPase에 의존합니다. 내피 세포가 손상되면 다음과 같은 경로로 부종이 발생합니다.
각막 실질의 팽윤압을 초과하는 안압 상승 (고안압)이 있는 경우, 내피가 비교적 건강하더라도 상피 부종이 발생할 수 있으므로 주의가 필요합니다.
일본인에서는 TCF4 반복 확장의 기여가 상대적으로 작기 때문에8), 일본인 특유의 유전적·환경적 배경을 규명하는 것이 향후 중요한 과제이다.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.