Độ 0-1 (không đến nhẹ)
Dấu hiệu: 12 hạt hoặc ít hơn ở trung tâm (Độ 0) hoặc hơn 12 hạt không hợp nhất (Độ 1)
Triệu chứng: Thường không có triệu chứng. Được phát hiện dưới dạng đốm đen trên kính hiển vi nội mô.

Chứng loạn dưỡng nội mô giác mạc Fuchs (FECD) là một bệnh tiến triển ảnh hưởng đến tế bào nội mô giác mạc ở cả hai mắt. Năm 1910, Ernst Fuchs đã báo cáo 13 trường hợp là “dystrophia epithelialis corneae”, và sau đó được xác định là bệnh nội mô, dẫn đến tên gọi hiện tại 1).
Các hạt guttae (guttata) xuất hiện trên bề mặt nội mô ở trung tâm giác mạc và dần dần lan ra ngoại vi. Khi chức năng hàng rào và bơm (Na⁺/K⁺-ATPase) của tế bào nội mô suy giảm, xảy ra phù nề nhu mô giác mạc, sau đó là phù biểu mô và hình thành bọng nước. Màng Descemet dày lên và trở nên không đều, dẫn đến mất độ trong suốt của giác mạc.
Trong IC3D (Phân loại Loạn dưỡng Giác mạc Quốc tế) phiên bản thứ 2 (Weiss 2015), FECD được xếp vào nhóm “loạn dưỡng nội mô giác mạc” 15). Dựa vào thời điểm khởi phát, được chia thành hai loại chính:
| Chỉ số | Giá trị | Nguồn |
|---|---|---|
| Tần suất guttae giác mạc ở bệnh nhân trước phẫu thuật đục thủy tinh thể | 1,2% | Khảo sát đa trung tâm trong nước |
| Tỷ lệ hiện mắc tại Nhật Bản (Nghiên cứu Kumejima) tuổi ≥40 | 4,1% | Higa 20117) |
| Tỷ lệ hiện mắc ở nữ giới Nhật Bản (tuổi ≥40) | 5,8% | Higa 20117) |
| Nhật Bản - Tỷ lệ mắc bệnh ở nam giới (trên 40 tuổi) | 2,4% | Higa 20117) |
| Iceland - Nghiên cứu Mắt Reykjavik trên 55 tuổi | Nữ 11%, Nam 7% | Zoega 200610) |
| Tỷ lệ giới tính (quốc tế) | 2,5:1 đến 3,5:1 (nữ chiếm ưu thế) | Matthaei 20191) |
| Tần suất mở rộng lặp TCF4 ở người Nhật | 12 trong số 47 trường hợp (26%) | Nakano 20158) |
Người Nhật, thuộc chủng tộc da vàng, có xu hướng mắc FECD thấp hơn so với chủng tộc da trắng và da đen. Tuy nhiên, tại Nhật Bản, số ca dự kiến sẽ tăng khi xã hội già hóa. Người Nhật có mật độ tế bào nội mô giác mạc cao hơn người da trắng, do đó khởi phát bệnh được cho là tương đối muộn hơn.
Ở người Nhật thường có góc tiền phòng hẹp, không hiếm trường hợp giảm tế bào nội mô sau phẫu thuật cắt mống mắt bằng laser (LI), do đó cần chú ý phát hiện sớm FECD.
Trong một nghiên cứu dân số thực hiện tại Okinawa/Đảo Kumejima (Nghiên cứu Kumejima), các hạt giác mạc (corneal guttae) được phát hiện ở 4,1% người từ 40 tuổi trở lên. Ở nữ giới là 5,8%, ở nam giới là 2,4% 7). Cũng có dữ liệu trong nước cho thấy 1,2% bệnh nhân được kiểm tra trước phẫu thuật đục thủy tinh thể có giác mạc dạng hạt. Người Nhật được cho là có tần suất thấp hơn so với người châu Âu/Mỹ, nhưng tỷ lệ này có xu hướng gia tăng cùng với xã hội già hóa.
Thông thường, không có triệu chứng ở người dưới 50 tuổi. Các triệu chứng tiến triển chậm tương quan với mức độ phù nề.
Khám cơ bản bằng đèn khe. Kết hợp chiếu sáng trực tiếp, chiếu sáng tán xạ ngược và phương pháp phản xạ gương để quan sát.
Độ 0-1 (không đến nhẹ)
Dấu hiệu: 12 hạt hoặc ít hơn ở trung tâm (Độ 0) hoặc hơn 12 hạt không hợp nhất (Độ 1)
Triệu chứng: Thường không có triệu chứng. Được phát hiện dưới dạng đốm đen trên kính hiển vi nội mô.
Cấp độ 2-3 (Trung bình)
Dấu hiệu: Guttae hợp lưu trung tâm 1-5 mm. Hình ảnh beaten-metal nhẹ.
Triệu chứng: Mờ mắt buổi sáng. Hình ảnh nội mô không rõ khi soi gương.
Cấp độ 4 (Nặng)
Dấu hiệu: Guttae hợp lưu rộng >5 mm trung tâm. Hình ảnh beaten-metal kèm sắc tố.
Triệu chứng: Mờ mắt dai dẳng và sợ ánh sáng từ sáng đến trưa.
Cấp độ 4+ Phù (Rất nặng)
Dấu hiệu: Phù nhu mô và biểu mô, hình thành bọng nước. Đục giác mạc rõ rệt.
Triệu chứng: Giảm thị lực nghiêm trọng suốt ngày, đau mắt, chảy nước mắt. Chất lượng cuộc sống giảm sút đáng kể.
Phân loại lâm sàng này dựa trên phân loại sửa đổi của Krachmer và cộng sự (1978)5).
Chi tiết dấu hiệu trên đèn khe:
Giác mạc khỏe mạnh duy trì độ trong suốt nhờ các tế bào nội mô liên tục bơm nước ra tiền phòng. Trong FECD, chức năng bơm của nội mô suy giảm, do đó khi ngủ (khi nhắm mắt), sự bay hơi nước cũng ngừng lại, và giác mạc phù nề nhiều nhất vào buổi sáng, gây mờ mắt nghiêm trọng. Khi mở mắt, nước bay hơi khỏi bề mặt giác mạc, phù nề cải thiện phần nào vào ban ngày, giúp phục hồi thị lực. Khi bệnh tiến triển, sự thay đổi trong ngày này biến mất và tình trạng mờ mắt kéo dài suốt cả ngày.
FECD chủ yếu di truyền trội trên nhiễm sắc thể thường, nhưng có sự khác biệt về độ thâm nhập và mức độ biểu hiện, và tồn tại các trường hợp không có tiền sử gia đình rõ ràng.
Các gen nguyên nhân chính:
Ở người Nhật, tần suất mở rộng đoạn lặp TCF4 thấp hơn so với phương Tây, do đó cần làm sáng tỏ các nền tảng di truyền khác8).
FECD chủ yếu di truyền theo kiểu trội trên nhiễm sắc thể thường. Về mặt lý thuyết, xác suất di truyền cho con là 50%. Tuy nhiên, có sự khác biệt lớn về thời điểm khởi phát và mức độ nghiêm trọng (tính thâm nhập không hoàn toàn), và nhiều người mang gen này sống suốt đời với các triệu chứng rất nhẹ. Đặc biệt ở người Nhật, tỷ lệ bất thường gen TCF4, nguyên nhân phổ biến nhất ở phương Tây, thấp 8), cho thấy nền tảng di truyền khác nhau. Nếu bạn lo lắng, nên tham khảo ý kiến bác sĩ di truyền.
Không có tiêu chuẩn chẩn đoán thống nhất ở Nhật Bản, nhưng chẩn đoán lâm sàng được thực hiện bằng cách kết hợp các xét nghiệm sau.
Đây là xét nghiệm quan trọng nhất để chẩn đoán và theo dõi FECD.
| Thông số | Giá trị bình thường | Ngưỡng bất thường |
|---|---|---|
| Mật độ tế bào nội mô (giai đoạn sơ sinh) | 3.500–4.000 tế bào/mm² | — |
| Mật độ tế bào nội mô (tuổi 20) | 2.700 tế bào/mm² | — |
| Mật độ tế bào nội mô (70 tuổi trở lên) | Trung bình 2.200 tế bào/mm² | — |
| Ngưỡng duy trì độ trong suốt | — | 400–500 tế bào/mm² hoặc thấp hơn |
| Giá trị CV (hệ số biến thiên) | 0,2–0,3 | ≥ 0,35 |
| Tỷ lệ tế bào hình lục giác (hexagonality) | 60-70% | ≤ 50% |
| Bệnh | Điểm phân biệt |
|---|---|
| Loạn dưỡng giác mạc đa hình thái sau (PPCD) | Di truyền trội, hai mắt, đục dạng dải hoặc bọng nước ở màng Descemet. Gen: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| Loạn dưỡng nội mô giác mạc bẩm sinh di truyền (CHED) | Di truyền lặn (đột biến SLC4A11), khởi phát lúc sinh hoặc trẻ nhỏ, phù và đục giác mạc từ khi sinh |
| Bệnh giác mạc bọng nước giả thể thủy tinh (PBK) | Rối loạn nội mô sau phẫu thuật đục thủy tinh thể. Không có guttae, có tiền sử phẫu thuật |
| Bệnh giác mạc do hội chứng bong tróc giả | Lắng đọng chất PEX, tăng nhãn áp, chất PEX trên mặt trước thể thủy tinh là chìa khóa chẩn đoán phân biệt |
| Hội chứng ICE (Mống mắt-Giác mạc-Nội mô) | Một mắt, kèm teo mống mắt, dính trước và glôcôm. Không có guttae |
| Thay đổi nội mô ở mắt góc hẹp | Đôi khi có biểu hiện giống guttae giác mạc. Phân biệt bằng nhãn áp và hình thái góc tiền phòng |
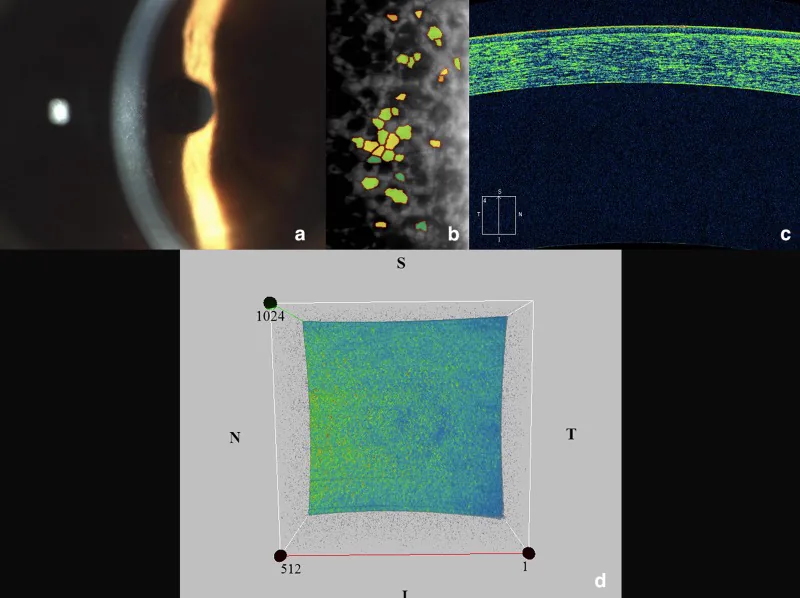
Kính hiển vi đặc biệt (thiết bị chụp ảnh tế bào nội mô bằng phản xạ gương) là thiết bị chụp và đo các tế bào nội mô ở lớp trong cùng của giác mạc một cách không xâm lấn bằng cách sử dụng phản xạ ánh sáng đặc biệt. Xét nghiệm đo số lượng tế bào nội mô (mật độ tế bào), độ biến thiên kích thước (giá trị CV) và độ đồng nhất về hình dạng (tỷ lệ tế bào hình lục giác). Trong FECD, các guttae hiện ra dưới dạng chấm đen (điểm tối), giúp đánh giá giai đoạn bệnh. Việc chụp ảnh chỉ mất vài phút và không gây đau.
Mục tiêu điều trị là phục hồi độ trong suốt của giác mạc và duy trì thị lực. Liệu pháp điều trị triệu chứng hoặc phẫu thuật được lựa chọn tùy theo giai đoạn bệnh.
Nhằm giảm nhẹ triệu chứng trước khi phẫu thuật. Không có tác dụng phục hồi số lượng tế bào nội mô hoặc làm chậm tiến triển bệnh.
DMEK (Ghép nội mô giác mạc màng Descemet)
Mảnh ghép: Chỉ màng Descemet + nội mô (độ dày khoảng 15 μm)
Đặc điểm: Được Melles báo cáo lần đầu năm 2006 11). Phục hồi thị lực nhanh, tỷ lệ thải ghép thấp. Cần bác sĩ phẫu thuật có tay nghề cao.
Bảo hiểm y tế tại Nhật Bản: Từ năm 2016
DSAEK (Ghép nội mô giác mạc có hỗ trợ bóc tách màng Descemet tự động)
PKP (Ghép giác mạc toàn bộ)
Mảnh ghép: Giác mạc toàn bộ độ dày (đường kính 7,0–8,5 mm)
Đặc điểm: Lựa chọn cổ điển. Các thách thức bao gồm khâu, quản lý loạn thị và nguy cơ thải ghép lâu dài. Trong lĩnh vực FECD, đang dần được thay thế bằng ghép nội mô.
DSO (Bóc màng Descemet không ghép nội mô)
Kỹ thuật: Bóc tách chọn lọc phần trung tâm màng Descemet đường kính 4 mm. Không cần mảnh ghép.
Chỉ định: Các trường hợp tế bào nội mô ngoại vi còn lại có thể di chuyển và tăng sinh vào trung tâm. Khoảng 75% giác mạc trở nên trong suốt14).
Thuốc nhỏ mắt ức chế ROCK: Sử dụng ripasudil sau phẫu thuật thúc đẩy sự trong suốt ngay cả ở những trường hợp không đáp ứng14).
| Chỉ số | DMEK | UT-DSAEK | Nguồn |
|---|---|---|---|
| BCVA 12 tháng (chênh lệch logMAR) | −0,06 (DMEK ưu thế) | — | Sela 2023 phân tích tổng hợp3) |
| Tỷ lệ đạt 20/25 trở lên | 66% | 33% (p=0,02) | Dunker 2020 RCT4) |
| Tỷ số chênh lệch của tái bơm hơi | — | 2,76 (DSAEK ưu thế) | Sela 20233) |
| ECD 12 tháng | Không khác biệt | Không khác biệt | Dunker 20204) |
| Độ dày mảnh ghép <70 μm | — | Không khác biệt thị lực với DMEK | Sela 20233) |
Phân tích tổng hợp của Sela và cộng sự (2023) (8 nghiên cứu, 376 mắt) cho thấy BCVA ở 12 tháng tốt hơn đáng kể ở DMEK (−0,06 logMAR) 3). Thử nghiệm lâm sàng ngẫu nhiên đa trung tâm của Dunker và cộng sự (2020) cũng cho thấy DMEK có tỷ lệ đạt 20/25 trở lên cao hơn so với UT-DSAEK (66% so với 33%, p=0,02) 4). Tuy nhiên, UT-DSAEK có độ dày mảnh ghép <70 μm đã thu hẹp khoảng cách với DMEK 3).
Nhóm Đại học Kyoto (Kinoshita 2018) đã phát triển liệu pháp tiêm tế bào nội mô giác mạc từ người hiến khỏe mạnh được nuôi cấy cùng với chất ức chế ROCK (Y-27632) vào tiền phòng 13).
Chất ức chế ROCK hoạt động bằng cách thúc đẩy sự bám dính của tế bào nội mô, ức chế apoptosis và thúc đẩy tiến trình chu kỳ tế bào 13).
Trong FECD, thường có đục thủy tinh thể kèm theo, cần lựa chọn cẩn thận thời điểm và phương pháp phẫu thuật.
DMEK có mảnh ghép mỏng nhất (khoảng 15 μm), do đó phục hồi thị lực nhanh hơn và ít thay đổi khúc xạ sau phẫu thuật. Phân tích tổng hợp cũng cho thấy BCVA 12 tháng vượt trội ở DMEK 3). Mặt khác, DSAEK dễ thao tác mảnh ghép hơn một chút và có đường cong học tập ngắn hơn, được thực hiện rộng rãi trong nước. DSAEK siêu mỏng (<70 μm) được báo cáo cho kết quả thị lực gần tương đương với DMEK 3). Việc lựa chọn dựa trên đánh giá toàn diện về kinh nghiệm của bác sĩ phẫu thuật, kinh nghiệm của cơ sở và tình trạng giác mạc của bệnh nhân. Cả hai thủ thuật đều được bảo hiểm y tế trong nước từ năm 2016 (DMEK) hoặc 2009 (DSAEK).
Tế bào nội mô giác mạc bình thường không phân chia trong tiền phòng. Khi nội mô bị tổn thương, các tế bào lân cận phì đại và di chuyển để bù đắp, do đó mật độ tế bào giảm không hồi phục theo tuổi tác. Dưới 400-500 tế bào/mm², việc duy trì độ trong suốt của giác mạc trở nên khó khăn.
Trong FECD, các tế bào nội mô thoái hóa sản xuất và lắng đọng chất collagen bất thường ở mặt sau màng Descemet, tạo thành các guttae. Màng Descemet dày lên và trở nên không đều, tạo ra một vòng luẩn quẩn làm suy giảm thêm chức năng nội mô.
Lão hóa, tiếp xúc với tia UV và hút thuốc đều làm tăng stress oxy hóa và là cửa ngõ của vòng luẩn quẩn 2).
Chức năng bơm của nội mô giác mạc phụ thuộc vào Na⁺/K⁺-ATPase. Khi tế bào nội mô bị tổn thương, phù nề xảy ra qua các con đường sau.
Nếu có tăng nhãn áp vượt quá áp lực trương nở của nhu mô giác mạc, phù biểu mô có thể xảy ra ngay cả khi nội mô tương đối khỏe mạnh, và cần chú ý điều này.
Vì sự đóng góp của sự mở rộng lặp TCF4 tương đối nhỏ ở người Nhật8), việc làm sáng tỏ nền tảng di truyền và môi trường đặc thù của người Nhật là vấn đề quan trọng trong tương lai.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.