Evre 0-1 (yok veya hafif)
Bulgular: Merkezde 12 veya daha az gutta (Evre 0) veya 12’den fazla birleşmemiş gutta (Evre 1)
Belirtiler: Genellikle asemptomatik. Speküler mikroskopta koyu noktalar olarak tespit edilir.

Fuchs Endotelyal Kornea Distrofisi (FECD), kornea endotel hücrelerini iki taraflı olarak etkileyen ilerleyici bir hastalıktır. 1910’da Ernst Fuchs, 13 vakayı “dystrophia epithelialis corneae” olarak tanımlamış, daha sonra endotel hastalığı olduğu anlaşılarak bugünkü adını almıştır 1).
Kornea merkezindeki endotel yüzeyinde guttae (damla şeklinde çıkıntılar) belirir ve yavaşça çevreye yayılır. Endotel hücrelerinin bariyer ve pompa fonksiyonu (Na⁺/K⁺-ATPaz) azaldığında kornea stroma ödemi, ardından epitel ödemi ve bül oluşumu gelişir. Descemet membranı kalınlaşır ve düzensizleşir, kornea saydamlığını kaybeder.
IC3D (Uluslararası Kornea Distrofisi Sınıflandırması) 2. baskısında (Weiss 2015), FECD «kornea endotel distrofisi» kategorisinde sınıflandırılır15). Başlangıç zamanına göre aşağıdaki iki tipe ayrılır:
| Gösterge | Değer | Kaynak |
|---|---|---|
| Katarakt ameliyatı öncesi hastalarda guttata sıklığı | %1,2 | Yurt içi çok merkezli çalışma |
| Japonya Kumejima Çalışması’nda 40 yaş üstü prevalansı | %4,1 | Higa 20117) |
| Japonya’da kadın prevalansı (40 yaş üstü) | %5,8 | Higa 20117) |
| Japonya’da erkeklerde görülme sıklığı (40 yaş üstü) | %2.4 | Higa 20117) |
| İzlanda - Reykjavik Göz Çalışması, 55 yaş üstü | Kadınlarda %11, erkeklerde %7 | Zoega 200610) |
| Cinsiyet oranı (uluslararası) | 2.5:1 ila 3.5:1 (kadın baskın) | Matthaei 20191) |
| Japonlarda TCF4 tekrar uzaması sıklığı | 47 vakada 12 (%26) | Nakano 20158) |
Sarı ırk olan Japonlar, beyaz ve siyah ırklara kıyasla FECD görülme sıklığında daha düşük bir eğilim gösterir. Ancak ülkemizde yaşlanan nüfusla birlikte gelecekte daha da artması beklenmektedir. Japonların beyazlara göre daha yüksek kornea endotel hücre yoğunluğuna sahip olması nedeniyle hastalığın nispeten daha geç ortaya çıktığı düşünülmektedir.
Dar açılı gözlerin sık görüldüğü Japonlarda, lazer iridotomi (LI) sonrası endotel hücre kaybı nadir değildir ve FECD’nin erken teşhisinde dikkatli olunmalıdır.
Okinawa, Kumejima’da yapılan bir toplum çalışmasında (Kumejima Çalışması), 40 yaş ve üzeri bireylerin %4,1’inde korneal guttae tespit edilmiştir. Kadınlarda bu oran %5,8, erkeklerde ise %2,4’tür7). Ayrıca, katarakt ameliyatı öncesi muayene edilen hastaların %1,2’sinde damla kornea görüldüğüne dair ulusal veriler de mevcuttur. Japonların bu hastalığa Batılılardan daha az sıklıkta yakalandığı söylenmektedir, ancak yaşlanan toplumla birlikte sıklık artış eğilimindedir.
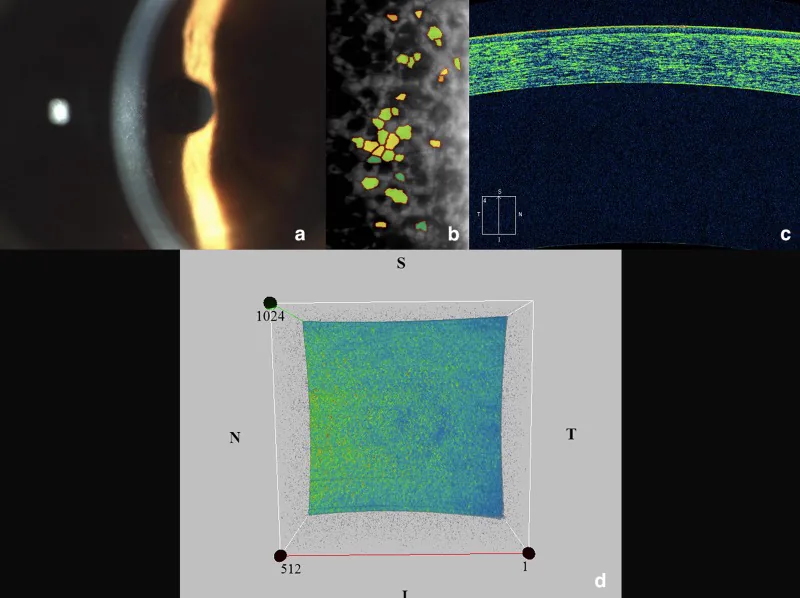
Genellikle 50 yaş altında asemptomatiktir. Belirtiler, ödemin şiddetiyle ilişkili olarak yavaşça ilerler.
Yarık lamba mikroskobu temeldir. Doğrudan aydınlatma, arkadan saçılım aydınlatması ve ayna yansıması yöntemleri kombine edilerek incelenir.
Evre 0-1 (yok veya hafif)
Bulgular: Merkezde 12 veya daha az gutta (Evre 0) veya 12’den fazla birleşmemiş gutta (Evre 1)
Belirtiler: Genellikle asemptomatik. Speküler mikroskopta koyu noktalar olarak tespit edilir.
Derece 2-3 (Orta)
Bulgular: Merkezde 1-5 mm çapında birleşik guttae. Hafif dövülmüş metal görünümü.
Semptomlar: Sabah bulanık görme. Speküler mikroskopta endotel görüntüsü net değildir.
Derece 4 (Şiddetli)
Bulgular: Merkezde 5 mm’den geniş yaygın birleşik guttae. Pigmentasyonla birlikte dövülmüş metal görünümü.
Semptomlar: Sabahtan gün içine kadar sürekli bulanık görme ve fotofobi.
Derece 4+ Ödem (En Şiddetli)
Bulgular: Stromal ödem, epitelyal ödem, bül oluşumu. Belirgin kornea bulanıklığı.
Semptomlar: Gün boyu ciddi görme azalması, göz ağrısı, sulanma. Yaşam kalitesi belirgin şekilde düşer.
Bu klinik evreleme, Krachmer ve ark. (1978) tarafından yapılan modifiye sınıflandırmaya dayanmaktadır5).
Yarık lamba bulgularının detayları:
Sağlıklı bir kornea, endotel hücrelerinin sürekli olarak suyu ön odaya pompalayarak şeffaflığını korur. FECD’de endotel pompa fonksiyonu azaldığından, uyku sırasında (göz kapakları kapalıyken) buharlaşma yoluyla su atılımı da durur ve sabahları kornea en ödemli halde olup bulanık görme en şiddetli düzeye ulaşır. Gözler açıkken kornea yüzeyinden su buharlaşır ve gün içinde ödem bir miktar azalarak görme geri döner. Hastalık ilerledikçe bu gün içi değişkenlik kaybolur ve tüm gün boyunca bulanık görme devam eder.
FECD çoğunlukla otozomal dominant kalıtım gösterir, ancak penetrans ve ekspresivitede değişkenlik vardır ve aile öyküsü net olmayan vakalar da mevcuttur.
Başlıca genler:
Japonlarda TCF4 tekrar genişlemesinin sıklığı Avrupa ve Amerika’ya göre daha düşük olduğundan, diğer genetik arka planların aydınlatılması gerekmektedir8).
FECD çoğunlukla otozomal dominant kalıtım gösterir. Teorik olarak çocuğa geçme olasılığı %50’dir. Ancak başlangıç zamanı ve şiddeti büyük farklılıklar gösterir (tam olmayan penetrans) ve geni taşıyan birçok kişi hayatı boyunca çok hafif semptomlarla yaşar. Özellikle Japonlarda, Batı’da en sık neden olan TCF4 gen anormalliğinin oranı düşüktür8) ve genetik arka plan farklı olabilir. Endişeleniyorsanız bir genetik uzmanına danışmanız önerilir.
Japonya’da birleşik bir tanı kriteri yoktur, ancak aşağıdaki testlerin kombinasyonu ile klinik tanı konur.
FECD tanı ve takibinde en önemli testtir.
| Parametre | Normal değer | Anormal eşik |
|---|---|---|
| Endotel hücre yoğunluğu (yenidoğan dönemi) | 3.500–4.000 hücre/mm² | — |
| Endotel hücre yoğunluğu (20’li yaşlar) | 2.700 hücre/mm² | — |
| Endotel hücre yoğunluğu (70 yaş ve üzeri) | Ortalama 2.200 hücre/mm² | — |
| Saydamlığı koruma sınırı | — | 400–500 hücre/mm² veya altı |
| CV (varyasyon katsayısı) | 0,2–0,3 | ≥ 0,35 |
| Altıgen hücre oranı (hexagonality) | %60-70 | ≤ %50 |
| Hastalık | Ayırıcı tanı noktaları |
|---|---|
| Arka Polimorf Kornea Distrofisi (PPCD) | AD kalıtım, iki taraflı, Descemet membranında bant benzeri ve büllöz opasiteler. Genler: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| Konjenital Herediter Kornea Endotel Distrofisi (CHED) | AR kalıtım (SLC4A11 mutasyonu), doğumdan bebekliğe başlangıç, doğumdan itibaren kornea ödemi ve opasitesi |
| Psödofakik Büllöz Keratopati (PBK) | Katarakt cerrahisi sonrası endotel hasarı. Guttae yok, cerrahi öyküsü var |
| Psödoeksfoliasyon Sendromu Keratopatisi | PEX maddesi birikimi, göz içi basıncı artışı, lens ön yüzünde PEX maddesi ayırıcı tanıda anahtar |
| ICE (İris-Kornea-Endotel) Sendromu | Tek taraflı, iris atrofisi, ön sineşi ve glokom eşlik eder. Guttae yok |
| Dar açılı gözde endotel değişiklikleri | Gutta benzeri bulgular görülebilir. Göz içi basıncı ve açı morfolojisi ile ayırt edilir |
Speküler mikroskop (ayna yansımalı endotel hücre görüntüleme cihazı), korneanın en iç tabakasındaki endotel hücrelerini özel ışık yansıması kullanarak non-invaziv olarak görüntüleyen ve ölçen bir cihazdır. Muayenede endotel hücre sayısı (hücre yoğunluğu), boyut değişkenliği (CV değeri) ve şekil homojenliği (altıgen hücre yüzdesi) ölçülür. FECD’de guttae koyu noktalar (karanlık nokta) olarak görünür ve hastalık evresinin değerlendirilmesine yardımcı olur. Görüntüleme birkaç dakika sürer ve ağrısızdır.
Tedavinin amacı kornea şeffaflığını geri kazanmak ve görme keskinliğini korumaktır. Hastalık evresine göre semptomatik tedaviden cerrahi tedaviye kadar seçenekler mevcuttur.
Amaç, cerrahi endikasyon öncesi semptomları hafifletmektir. Endotel hücre sayısını artırmaz veya hastalığın ilerlemesini durdurmaz.
DMEK (Descemet Membran Endotelyal Keratoplasti)
Greft: Sadece Descemet membranı + endotel (yaklaşık 15 μm kalınlık)
Özellikler: İlk kez 2006’da Melles tarafından bildirilmiştir11). Hızlı görme iyileşmesi ve düşük red oranı. Deneyimli cerrah gerektirir.
Japonya’da sigorta kapsamı: 2016’dan itibaren
DSAEK (Descemet Soyma Otomatik Cihaz Destekli Endotelyal Keratoplasti)
PKP (Tam Kat Kornea Nakli)
Greft: Tam kat kornea (çap 7.0-8.5 mm)
Özellikler: Klasik seçenek. Dikiş, astigmat yönetimi ve uzun dönem red riski zorluklardır. FECD alanında giderek endotel nakli ile yer değiştirmektedir.
DSO (Descemetorheksis Endotel Keratoplastisi Olmadan)
Yöntem: Sadece santral 4 mm Descemet membranının seçici olarak soyulması. Greft gerekmez.
Endikasyon: Periferik endotel hücrelerinin merkeze göç edip çoğalabildiği olgular. Yaklaşık %75’inde kornea şeffaflaşması 14).
ROCK inhibitörü damla: Ripasudil’in ameliyat sonrası kullanımı, yanıtsız olgularda bile şeffaflaşmayı artırır 14).
| Gösterge | DMEK | UT-DSAEK | Kaynak |
|---|---|---|---|
| 12 aylık BCVA (logMAR farkı) | −0.06 (DMEK üstün) | — | Sela 2023 meta-analizi 3) |
| 20/25 veya daha iyi başarı oranı | %66 | %33 (p=0,02) | Dunker 2020 RCT4) |
| Rebubbling OR’si | — | 2,76 (DSAEK lehine) | Sela 20233) |
| 12 aylık ECD | Fark yok | Fark yok | Dunker 20204) |
| Greft kalınlığı <70 μm | — | DMEK ile görme farkı yok | Sela 20233) |
Sela ve ark. (2023) tarafından yapılan meta-analizde (8 çalışma, 376 göz), 12. ayda BCVA, DMEK’te anlamlı olarak daha iyiydi (−0.06 logMAR)3). Dunker ve ark. (2020) çok merkezli RKÇ’sinde de DMEK, UT-DSAEK’ye göre 20/25 veya daha iyi görme keskinliğine ulaşma oranında daha yüksekti (%66’ya karşı %33, p=0.02)4). Ancak, 70 μm’den ince greftli UT-DSAEK’te DMEK ile fark azaldı3).
Kyoto Üniversitesi grubu (Kinoshita 2018), kültüre edilmiş sağlıklı donör kornea endotel hücrelerinin ROCK inhibitörü (Y-27632) ile birlikte ön kamaraya enjekte edildiği bir tedavi yöntemi geliştirdi13).
ROCK inhibitörü, endotel hücre adezyonunu artırarak, apoptozu inhibe ederek ve hücre döngüsünü ilerleterek etki gösterir13).
FECD’de katarakt sık görülür ve cerrahi zamanlaması ile yöntem seçiminde dikkatli olunmalıdır.
DMEK, en ince greft (yaklaşık 15 μm) sayesinde hızlı görme iyileşmesi ve daha az postoperatif refraktif değişiklik avantajına sahiptir. Meta-analizde de 12. ayda BCVA DMEK’te üstündü3). Öte yandan DSAEK, greft manipülasyonu nispeten daha kolay ve cerrahın öğrenme eğrisi daha kısadır ve ülke içinde de yaygın olarak yapılmaktadır. Ultra-ince DSAEK’in (<70 μm) DMEK ile neredeyse eşdeğer görme sonuçları sağladığı bildirilmiştir3). Seçim, sorumlu cerrahın deneyimi, merkezin deneyimi ve hastanın kornea durumu kapsamlı olarak değerlendirilerek yapılır. Her iki yöntem de 2016 (DMEK) veya 2009 (DSAEK) yılından itibaren ülke içinde sigorta kapsamındadır.
Normal kornea endotel hücreleri ön kamarada hücre bölünmesi geçirmez. Endotel hasar gördüğünde, komşu hücreler genişleyip göç ederek hasarı telafi eder, bu nedenle hücre yoğunluğu yaşla birlikte geri dönüşümsüz olarak azalır. 400-500 hücre/mm²’nin altına düştüğünde kornea şeffaflığını korumak zorlaşır.
FECD’de, dejenere olmuş endotel hücreleri anormal kollajen benzeri maddeleri Descemet membranının arka yüzeyinde üretip biriktirerek guttae oluşturur. Descemet membranı kalınlaşır ve düzensizleşir, bu da endotel fonksiyonunu daha da bozan bir kısır döngü oluşturur.
Yaşlanma, UV maruziyeti ve sigara içimi oksidatif stresi artırarak kısır döngüye giriş sağlar2).
Kornea endotelinin pompa fonksiyonu Na⁺/K⁺-ATPaz’a bağımlıdır. Endotel hücreleri hasar gördüğünde, aşağıdaki yollarla ödem oluşur.
Kornea stromasının şişme basıncını aşan göz içi basıncı (yüksek göz tansiyonu) varlığında, endotel nispeten sağlıklı olsa bile epitelyal ödem oluşabilir; bu duruma dikkat edilmelidir.
Japonlarda TCF4 tekrar uzamasının katkısı nispeten küçük olduğundan 8), Japonlara özgü genetik ve çevresel faktörlerin aydınlatılması gelecekte önemli bir konudur.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.