الدرجة 0-1 (لا شيء إلى خفيف)
العلامات: 12 نتوءًا أو أقل في المركز (الدرجة 0) أو أكثر من 12 نتوءًا غير مندمجة (الدرجة 1)
الأعراض: عادةً لا توجد أعراض. يتم اكتشافها كنقاط داكنة في المجهر المرآوي.

ضمور بطانة القرنية لفوكس (FECD) هو مرض تقدمي يصيب الخلايا البطانية للقرنية في كلتا العينين. في عام 1910، أبلغ إرنست فوكس عن 13 حالة تحت اسم “dystrophia epithelialis corneae”، وتبين لاحقاً أنه مرض بطيني، مما أدى إلى الاسم الحالي 1).
تظهر نتوءات (guttae/guttata) على السطح البطاني في وسط القرنية وتنتشر تدريجياً نحو المحيط. عندما تنخفض وظيفة الحاجز والمضخة (Na⁺/K⁺-ATPase) للخلايا البطانية، يحدث وذمة في سدى القرنية، ثم وذمة ظهارية وتشكل فقاعات. يثخن غشاء ديسميه ويصبح غير منتظم، مما يفقد القرنية شفافيتها.
في التصنيف الدولي الثالث لضمور القرنية (IC3D) الإصدار الثاني (Weiss 2015)، يُصنف FECD ضمن فئة “ضمور بطانة القرنية” 15). ويُقسم إلى نوعين رئيسيين حسب وقت الظهور:
| المؤشر | القيمة | المصدر |
|---|---|---|
| تكرار تغوط القرنية لدى مرضى ما قبل جراحة الساد | 1.2% | مسح متعدد المراكز محلي |
| معدل الانتشار في اليابان (دراسة Kumejima) للأعمار ≥40 سنة | 4.1% | Higa 20117) |
| معدل الانتشار لدى النساء في اليابان (الأعمار ≥40 سنة) | 5.8% | Higa 20117) |
| اليابان - معدل انتشار الذكور (فوق 40 سنة) | 2.4% | Higa 20117) |
| آيسلندا - دراسة ريكيافيك للعين فوق 55 سنة | الإناث 11%، الذكور 7% | Zoega 200610) |
| نسبة الجنس (دولي) | 2.5:1 إلى 3.5:1 (غلبة الإناث) | Matthaei 20191) |
| تكرار توسع تكرار TCF4 لدى اليابانيين | 12 من 47 حالة (26%) | Nakano 20158) |
اليابانيون، وهم من العرق الأصفر، يميلون إلى انخفاض معدل الإصابة بـ FECD مقارنة بالعرق الأبيض والأسود. ومع ذلك، من المتوقع أن يزداد العدد في اليابان مع تقدم المجتمع في العمر. يُعتقد أن اليابانيين لديهم كثافة أعلى لخلايا البطانة القرنية مقارنة بالبيض، مما يؤخر ظهور المرض نسبيًا.
في اليابانيين الذين لديهم زاوية ضيقة في العين، ليس من النادر أن تنخفض خلايا البطانة بعد بضع القزحية بالليزر (LI)، لذلك يجب توخي الحذر للكشف المبكر عن FECD.
في دراسة سكانية أجريت في أوكيناوا/كوميجيما (Kumejima Study)، تم اكتشاف نتوءات القرنية (corneal guttae) لدى 4.1% من الأشخاص الذين تبلغ أعمارهم 40 عامًا أو أكثر. كانت النسبة 5.8% لدى النساء و2.4% لدى الرجال 7). هناك أيضًا بيانات محلية تشير إلى أن 1.2% من المرضى الذين خضعوا لفحص ما قبل جراحة إعتام عدسة العينة يعانون من قرنية نقطية. يُعتقد أن اليابانيين أقل عرضة للإصابة مقارنة بالأوروبيين والأمريكيين، لكن معدل الإصابة في ازدياد مع تقدم المجتمع في العمر.
عادةً، لا تظهر أعراض لدى الأشخاص الذين تقل أعمارهم عن 50 عامًا. تتطور الأعراض ببطء بالتوازي مع شدة الوذمة.
الفحص الأساسي هو باستخدام المصباح الشقي. يتم الجمع بين الإضاءة المباشرة، والإضاءة الخلفية المنتشرة، وطريقة الانعكاس المرآوي للمراقبة.
الدرجة 0-1 (لا شيء إلى خفيف)
العلامات: 12 نتوءًا أو أقل في المركز (الدرجة 0) أو أكثر من 12 نتوءًا غير مندمجة (الدرجة 1)
الأعراض: عادةً لا توجد أعراض. يتم اكتشافها كنقاط داكنة في المجهر المرآوي.
الدرجة 2-3 (متوسطة)
العلامات: غُتَّا (guttae) متموجة بقطر 1-5 مم في المركز. مظهر معدني مطروق خفيف.
الأعراض: ضبابية الرؤية صباحًا. صعوبة رؤية البطانة بالمرآة.
الدرجة 4 (شديدة)
العلامات: غُتَّا متموجة واسعة الانتشار تتجاوز 5 مم في المركز. مظهر معدني مطروق مع تصبغ.
الأعراض: ضبابية رؤية مستمرة وحساسية للضوء من الصباح حتى النهار.
الدرجة 4 + وذمة (شديدة جدًا)
العلامات: وذمة السدى والظهارة وتشكل الفقاعات. عتامة القرنية واضحة.
الأعراض: انخفاض حاد في الرؤية طوال اليوم، ألم في العين، دموع. تدهور كبير في جودة الحياة.
يعتمد هذا التصنيف السريري على التصنيف المعدل لـ Krachmer وآخرون (1978)5).
تفاصيل فحص المصباح الشقي:
القرنية السليمة تحافظ على شفافيتها عن طريق ضخ الخلايا البطانية للماء باستمرار إلى الغرفة الأمامية. في حالة ضمور فوكس البطاني للقرنية، تنخفض وظيفة المضخة البطانية، لذلك أثناء النوم (عند إغلاق الجفون) يتوقف تبخر الماء، وتكون القرنية أكثر انتفاخًا في الصباح مع ضبابية رؤية شديدة. عند فتح العينين، يتبخر الماء من سطح القرنية، وتتحسن الوذمة إلى حد ما خلال النهار، مما يؤدي إلى استعادة الرؤية. مع تقدم المرض، يختفي هذا التغير النهاري، وتستمر ضبابية الرؤية طوال اليوم.
ضمور فوكس البطاني للقرنية هو في الغالب وراثة جسمية سائدة، ولكن هناك تباين في النفاذية والتعبيرية، وتوجد حالات لا يكون فيها التاريخ العائلي واضحًا.
الجينات الرئيسية المسببة:
في اليابانيين، تواتر توسع تكرار TCF4 أقل منه في الغرب، لذلك هناك حاجة لتوضيح الخلفيات الوراثية الأخرى8).
يورث FECD بشكل أساسي بنمط وراثي جسمي سائد. نظريًا، احتمال انتقاله إلى الطفل هو 50%. ومع ذلك، هناك تباين كبير في وقت ظهور المرض وشدته (نفاذية غير كاملة)، حيث يعيش العديد من الأشخاص الذين يرثون الجين طوال حياتهم مع أعراض خفيفة جدًا. خاصة في اليابانيين، فإن نسبة تشوهات جين TCF4، وهو السبب الأكثر شيوعًا في الغرب، منخفضة 8)، مما يشير إلى خلفية وراثية مختلفة. إذا كنت قلقًا، نوصي باستشارة طبيب وراثة.
لا توجد معايير تشخيصية موحدة في اليابان، ولكن يتم التشخيص السريري من خلال مجموعة من الفحوصات التالية.
هذا هو الفحص الأكثر أهمية لتشخيص ومتابعة FECD.
| المعلمة | القيمة الطبيعية | عتبة الشذوذ |
|---|---|---|
| كثافة الخلايا البطانية (فترة حديثي الولادة) | 3,500–4,000 خلية/مم² | — |
| كثافة الخلايا البطانية (العقد الثاني من العمر) | 2,700 خلية/مم² | — |
| كثافة الخلايا البطانية (70 سنة فأكثر) | متوسط 2,200 خلية/مم² | — |
| الحد الأدنى للحفاظ على الشفافية | — | 400–500 خلية/مم² أو أقل |
| قيمة CV (معامل الاختلاف) | 0.2–0.3 | ≥ 0.35 |
| معدل ظهور الخلايا السداسية (hexagonality) | 60-70% | ≤ 50% |
| المرض | نقاط التفريق |
|---|---|
| حثل القرنية متعدد الأشكال الخلفي (PPCD) | وراثة سائدة، ثنائي العينين، عتامة شريطية أو فقاعية في غشاء دسميه. الجينات: PPCD1 (20p11.2-q11.2)، PPCD2 (COL8A2)، PPCD3 (ZEB1) |
| حثل القرنية البطاني الخلقي الوراثي (CHED) | وراثة متنحية (طفرة SLC4A11)، ظهور عند الولادة أو في مرحلة الرضاعة، وذمة وعتامة القرنية منذ الولادة |
| اعتلال القرنية الفقاعي الكاذب (PBK) | خلل بطاني بعد جراحة الساد. لا توجد غوتا، تاريخ جراحة موجود |
| اعتلال القرنية الناتج عن متلازمة التقشر الكاذب | ترسبات مادة PEX، ارتفاع ضغط العين، مادة PEX على السطح الأمامي للعدسة هي مفتاح التشخيص التفريقي |
| متلازمة ICE (القزحية القرنية البطانية) | أحادي العين، مصحوب بضمور القزحية، التصاقات أمامية، والزرق. لا توجد غوتا |
| تغيرات بطانية في العين ذات الزاوية الضيقة | قد تظهر مظاهر تشبه غوتا القرنية. يتم التفريق بقياس ضغط العين وتقييم زاوية الغرفة الأمامية |
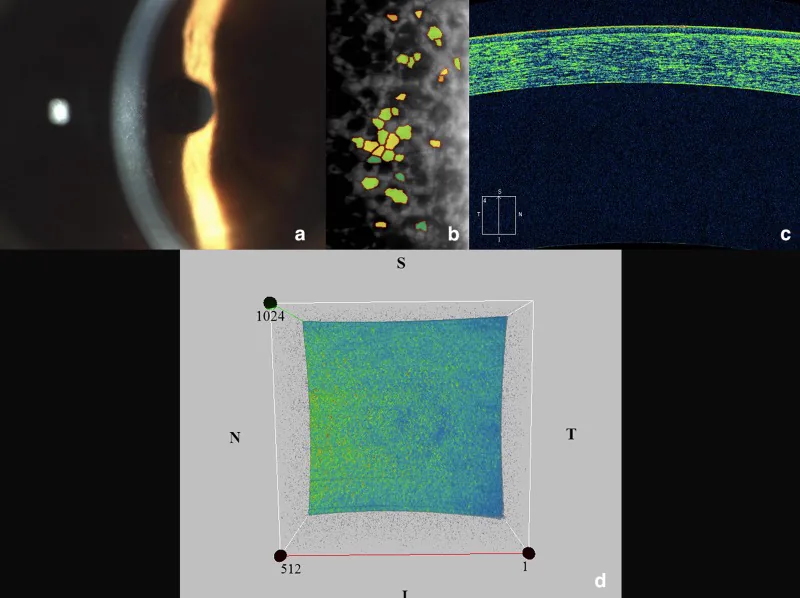
المجهر المرآوي (جهاز تصوير الخلايا البطانية بالانعكاس المرآوي) هو جهاز يصور ويقيس الخلايا البطانية في الطبقة الداخلية للقرنية بطريقة غير باضعة باستخدام انعكاس ضوئي خاص. يقيس الفحص عدد الخلايا البطانية (الكثافة الخلوية)، تباين الأحجام (قيمة CV)، وتجانس الأشكال (نسبة الخلايا السداسية). في حثل فوكس البطاني، تظهر الغوتا كنقاط سوداء (بقع داكنة) مما يساعد في تقييم مرحلة المرض. يستغرق التصوير بضع دقائق ولا يسبب ألمًا.
الهدف من العلاج هو استعادة شفافية القرنية والحفاظ على الرؤية. يتم اختيار العلاج العرضي أو الجراحي حسب مرحلة المرض.
يهدف إلى تخفيف الأعراض قبل الجراحة. لا يوجد تأثير على استعادة عدد الخلايا البطانية أو إبطاء تقدم المرض.
DMEK (زراعة الغشاء الداخلي للقرنية)
الطعم: غشاء ديسيميت + البطانة فقط (سمك حوالي 15 ميكرومتر)
الميزات: تم الإبلاغ عنها لأول مرة بواسطة Melles في 2006 11). استعادة سريعة للرؤية، معدل رفض منخفض. يتطلب جراحًا متمرسًا.
التغطية التأمينية في اليابان: منذ 2016
DSAEK (زراعة البطانة بمساعدة جهاز تشريح الغشاء الداخلي)
PKP (زرع القرنية كامل السمك)
الطعم: قرنية كامل السمك (قطر 7.0-8.5 مم)
الميزات: خيار تقليدي. التحديات تشمل الخياطة، إدارة اللابؤرية، وخطر الرفض طويل الأمد. في مجال ضمور فوكس البطاني، يتم استبداله تدريجياً بزرع البطانة.
DSO (استئصال الغشاء الديسيميتي بدون زرع البطانة)
الإجراء: تقشير انتقائي فقط للجزء المركزي من غشاء ديسيميه بقطر 4 مم. لا حاجة لطعم.
المؤشرات: الحالات التي يمكن فيها للخلايا البطانية المحيطية المتبقية أن تهاجر وتتكاثر نحو المركز. حوالي 75% تصبح القرنية شفافة14).
قطرات مثبط ROCK: استخدام ريباسوديل بعد الجراحة يعزز الشفافية حتى في الحالات غير المستجيبة14).
| المؤشر | DMEK | UT-DSAEK | المصدر |
|---|---|---|---|
| BCVA عند 12 شهرًا (فرق logMAR) | −0.06 (DMEK أفضل) | — | Sela 2023 تحليل تلوي3) |
| معدل تحقيق 20/25 أو أفضل | 66% | 33% (p=0.02) | Dunker 2020 RCT4) |
| نسبة الأرجحية لإعادة التعبئة | — | 2.76 (DSAEK أفضل) | Sela 20233) |
| ECD عند 12 شهرًا | لا فرق | لا فرق | Dunker 20204) |
| سمك الطعم <70 ميكرومتر | — | لا فرق في حدة البصر مع DMEK | Sela 20233) |
أظهر التحليل التلوي الذي أجراه Sela وآخرون (2023) (8 دراسات، 376 عين) أن أفضل حدة بصرية مصححة (BCVA) عند 12 شهرًا كانت أفضل بشكل ملحوظ في DMEK (−0.06 logMAR) 3). كما أظهرت تجربة عشوائية متعددة المراكز أجراها Dunker وآخرون (2020) أن DMEK حقق نسبة أعلى من 20/25 أو أفضل مقارنة بـ UT-DSAEK (66% مقابل 33%, p=0.02) 4). ومع ذلك، فإن UT-DSAEK بسماكة طعم أقل من 70 ميكرومتر قلص الفرق مع DMEK 3).
طورت مجموعة جامعة كيوتو (Kinoshita 2018) علاجًا يتضمن حقن الخلايا البطانية القرنية من متبرع سليم مزروعة مع مثبط ROCK (Y-27632) في الغرفة الأمامية 13).
يعمل مثبط ROCK عن طريق تعزيز التصاق الخلايا البطانية، وتثبيط الاستماتة، وتعزيز تقدم دورة الخلية 13).
في FECD، غالبًا ما يكون هناك ساد مصاحب، مما يتطلب اختيارًا دقيقًا لتوقيت وطريقة الجراحة.
يتميز DMEK بأرق طعم (حوالي 15 ميكرومتر)، مما يؤدي إلى استعادة بصر أسرع وتغير انكساري أقل بعد الجراحة. أظهر التحليل التلوي أيضًا تفوق DMEK في BCVA عند 12 شهرًا 3). من ناحية أخرى، فإن DSAEK أسهل قليلاً في التعامل مع الطعم ومنحنى تعلم أقصر للجراح، ويُمارس على نطاق واسع محليًا. هناك تقارير تفيد بأن DSAEK فائق الرقة (<70 ميكرومتر) يحقق نتائج بصرية مماثلة تقريبًا لـ DMEK 3). يتم الاختيار بناءً على تقييم شامل لخبرة الجراح، وخبرة المنشأة، وحالة قرنية المريض. كلا الإجراءين مشمولان بالتأمين الصحي محليًا منذ 2016 (DMEK) أو 2009 (DSAEK).
الخلايا البطانية الطبيعية للقرنية لا تنقسم في الحجرة الأمامية. عندما يحدث نقص في البطانة، تتوسع الخلايا المجاورة وتهاجر لتعويض النقص، وبالتالي تنخفض كثافة الخلايا بشكل لا رجعة فيه مع تقدم العمر. عندما تقل الكثافة عن 400-500 خلية/مم²، يصبح الحفاظ على شفافية القرنية صعبًا.
في FECD، تنتج الخلايا البطانية المتدهورة مواد كولاجينية غير طبيعية وتترسب على السطح الخلفي لغشاء ديسيميه، مكونة نتوءات (guttae). يزداد سمك غشاء ديسيميه ويصبح غير منتظم، مما يخلق حلقة مفرغة تزيد من إعاقة وظيفة البطانة.
الشيخوخة والتعرض للأشعة فوق البنفسجية والتدخين تزيد جميعها من الإجهاد التأكسدي، وتشكل مدخلًا للحلقة المفرغة 2).
تعتمد وظيفة مضخة البطانة القرنية على Na⁺/K⁺-ATPase. عند تلف الخلايا البطانية، يحدث الوذمة عبر المسارات التالية.
إذا كان هناك ارتفاع في ضغط العين يتجاوز ضغط انتفاخ سدى القرنية، فقد تحدث وذمة ظهارية حتى لو كانت البطانة سليمة نسبيًا، ويجب الانتباه لذلك.
نظرًا لأن مساهمة تكرار توسع TCF4 صغيرة نسبيًا لدى اليابانيين8)، فإن توضيح الخلفيات الوراثية والبيئية الخاصة باليابانيين يعد قضية مهمة في المستقبل.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.