Grado 0-1 (Ninguno a Leve)
Hallazgos: 12 o menos gutas centrales (Grado 0) o más de 12 gutas no confluentes (Grado 1)
Síntomas: Generalmente asintomático. Se detectan como puntos oscuros en la microscopía especular.

La distrofia endotelial corneal de Fuchs (FECD) es una enfermedad progresiva en la que las células endoteliales corneales se vuelven anormales bilateralmente. En 1910, Ernst Fuchs informó por primera vez 13 casos como “dystrophia epithelialis corneae”, y posteriormente se identificó como una enfermedad endotelial, lo que llevó a su nombre actual 1).
Aparecen guttas (guttata) en la superficie endotelial de la córnea central y se extienden gradualmente hacia la periferia. Cuando las funciones de barrera y bomba (Na⁺/K⁺-ATPasa) de las células endoteliales disminuyen, se desarrolla edema del estroma corneal, progresando a edema epitelial y formación de ampollas. El engrosamiento e irregularidad de la membrana de Descemet provocan la pérdida de transparencia corneal.
En la segunda edición de la IC3D (Clasificación Internacional de Distrofias Corneales) (Weiss 2015), la FECD se clasifica en la categoría de “Distrofias endoteliales corneales” 15). Se divide ampliamente en los siguientes dos tipos según la edad de inicio.
| Indicador | Valor | Fuente |
|---|---|---|
| Frecuencia de gotas corneales en pacientes preoperatorios de cataratas | 1.2% | Encuesta multicéntrica nacional |
| Prevalencia en Japón (Estudio Kumejima, ≥40 años) | 4.1% | Higa 20117) |
| Prevalencia en mujeres japonesas (≥40 años) | 5.8% | Higa 20117) |
| Japón: Prevalencia en hombres (mayores de 40 años) | 2.4% | Higa 20117) |
| Islandia: Estudio Ocular de Reikiavik, mayores de 55 años | Mujeres 11%, hombres 7% | Zoega 200610) |
| Proporción de sexos (internacional) | 2.5:1 a 3.5:1 (predominio femenino) | Matthaei 20191) |
| Frecuencia de expansión repetitiva de TCF4 en japoneses | 12 de 47 casos (26%) | Nakano 20158) |
Los japoneses, como raza amarilla, tienden a tener una menor incidencia de FECD en comparación con las razas blanca y negra. Sin embargo, con el envejecimiento de la sociedad en Japón, se espera que los casos aumenten aún más. Los japoneses tienen una mayor densidad de células endoteliales corneales que los blancos, lo que se cree que retrasa la aparición de la enfermedad.
En los japoneses, que a menudo tienen ángulos estrechos, la iridotomía con láser (LI) frecuentemente conduce a una disminución de las células endoteliales, por lo que se necesita atención cuidadosa para la detección temprana de FECD.
En un estudio poblacional realizado en la isla Kumejima de Okinawa (Estudio Kumejima), se detectaron gutas corneales en el 4.1% de las personas de 40 años o más. La prevalencia fue del 5.8% en mujeres y del 2.4% en hombres 7). También hay datos nacionales que muestran que el 1.2% de los pacientes sometidos a examen preoperatorio de cataratas presentaban córnea guttata. Aunque se informa que la frecuencia es menor en japoneses que en poblaciones occidentales, está aumentando con la sociedad envejecida.
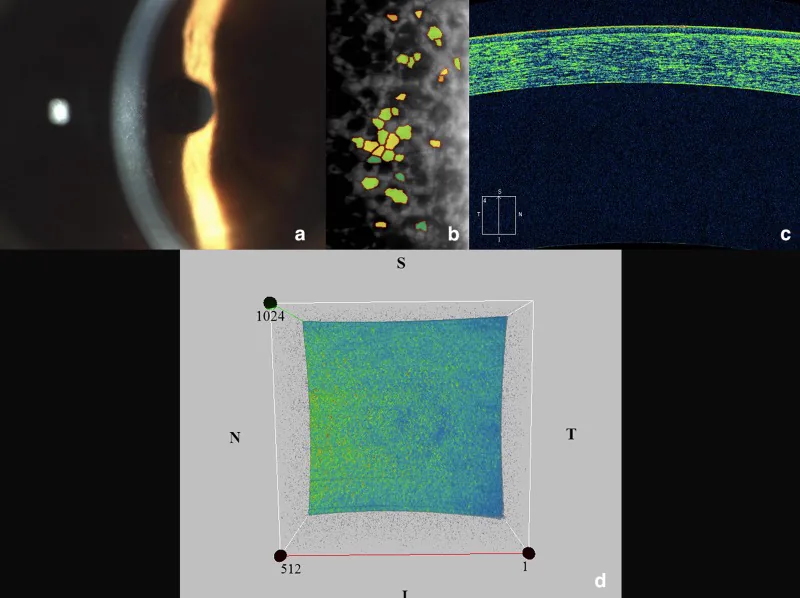
Por lo general, los pacientes menores de 50 años son asintomáticos. Los síntomas progresan lentamente, correlacionándose con el grado de edema.
La microscopía con lámpara de hendidura es fundamental. La observación se realiza mediante una combinación de iluminación directa, retroiluminación y reflexión especular.
Grado 0-1 (Ninguno a Leve)
Hallazgos: 12 o menos gutas centrales (Grado 0) o más de 12 gutas no confluentes (Grado 1)
Síntomas: Generalmente asintomático. Se detectan como puntos oscuros en la microscopía especular.
Grado 2-3 (Moderado)
Hallazgos: Guttata confluentes en el área central de 1 a 5 mm. Aspecto de metal batido leve.
Síntomas: Visión borrosa matutina. La imagen endotelial se vuelve poco clara en la microscopía especular.
Grado 4 (Grave)
Hallazgos: Guttata confluentes extensas >5 mm centralmente. Aspecto de metal batido con pigmentación.
Síntomas: Visión borrosa persistente y fotofobia desde la mañana hasta el día.
Grado 4+ Edema (Muy grave)
Hallazgos: Edema estromal, edema epitelial y formación de ampollas. Opacidad corneal marcada.
Síntomas: Pérdida severa de visión, dolor ocular y lagrimeo durante todo el día. Calidad de vida significativamente reducida.
Esta clasificación clínica por etapas se basa en la clasificación modificada de Krachmer et al. (1978)5).
Detalles de los hallazgos con lámpara de hendidura:
En una córnea sana, las células endoteliales bombean constantemente agua hacia la cámara anterior para mantener la transparencia. En la FECD, debido a que la función de bomba endotelial está reducida, la evaporación del agua también se detiene mientras se duerme (con los ojos cerrados), por lo que la córnea está más edematosa por la mañana y la visión borrosa empeora. Cuando los ojos están abiertos, el agua se evapora de la superficie corneal y durante el día el edema mejora hasta cierto punto, por lo que la visión se recupera. A medida que la enfermedad progresa, esta variación diurna desaparece y la visión borrosa persiste todo el día.
La FECD es principalmente autosómica dominante, pero hay variabilidad en la penetrancia y expresividad, y algunos casos no tienen antecedentes familiares claros.
Genes causantes principales:
En pacientes japoneses, la frecuencia de la expansión de repetición de TCF4 es menor que en poblaciones occidentales, por lo que se necesita dilucidar otros antecedentes genéticos8).
La FECD se hereda principalmente con un patrón autosómico dominante. Teóricamente, la probabilidad de transmitirlo a un hijo es del 50%. Sin embargo, existe una gran variabilidad en la edad de inicio y la gravedad (penetrancia incompleta); muchas personas que heredan el gen viven toda su vida con síntomas muy leves. En particular, la proporción de anomalías en el gen TCF4, que es la causa más común en los países occidentales, es baja en los japoneses8), lo que sugiere posibles diferencias en el trasfondo genético. Si le preocupa, recomendamos consultar a un especialista en genética.
Aunque no existen criterios diagnósticos unificados en Japón, el diagnóstico clínico se realiza combinando las siguientes exploraciones.
Esta es la exploración más importante para diagnosticar y monitorizar la FECD.
| Parámetro | Valor Normal | Umbral Anormal |
|---|---|---|
| Densidad de células endoteliales (período neonatal) | 3,500–4,000 cells/mm² | — |
| Densidad de células endoteliales (20 años) | 2,700 cells/mm² | — |
| Densidad de células endoteliales (70 años o más) | Promedio 2,200 cells/mm² | — |
| Límite para mantener la transparencia | — | 400–500 cells/mm² o menos |
| CV (coeficiente de variación) | 0.2–0.3 | ≥ 0.35 |
| Hexagonalidad (porcentaje de células hexagonales) | 60–70% | ≤ 50% |
| Enfermedad | Puntos clave para el diagnóstico diferencial |
|---|---|
| Distrofia corneal polimorfa posterior (PPCD) | Herencia AD, bilateral, opacidades en banda y vesiculares de la membrana de Descemet. Genes: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| Distrofia endotelial hereditaria congénita (CHED) | Herencia AR (mutación SLC4A11), inicio al nacer o en la infancia, edema y opacidad corneal desde el nacimiento |
| Queratopatía bullosa pseudofáquica (PBK) | Daño endotelial tras cirugía de cataratas. Sin gutas, antecedente quirúrgico |
| Queratopatía por síndrome de pseudoexfoliación | Depósito de material PEX, elevación de la presión intraocular, material PEX en la cápsula anterior del cristalino es clave para el diagnóstico diferencial |
| Síndrome iridocorneal endotelial (ICE) | Unilateral, con atrofia del iris, sinequias anteriores y glaucoma. Sin gutas |
| Cambios endoteliales en ojos de ángulo estrecho | Pueden presentar hallazgos similares a la cornea guttata. Se diferencian por la presión intraocular y la morfología del ángulo |
El microscopio especular (cámara de células endoteliales de reflexión especular) es un dispositivo que fotografía y mide de forma no invasiva las células endoteliales de la capa más interna de la córnea mediante un reflejo de luz especial. La prueba mide el número de células endoteliales (densidad celular), la variación del tamaño (valor CV) y la uniformidad de la forma (porcentaje de células hexagonales). En la FECD, las gutas aparecen como puntos negros (manchas oscuras), lo que ayuda a evaluar el estadio de la enfermedad. La toma de imágenes dura unos minutos y es indolora.
El objetivo del tratamiento es restaurar la transparencia corneal y mantener la visión. Según la etapa de la enfermedad, se selecciona terapia sintomática o quirúrgica.
Dirigida al alivio de síntomas antes de la cirugía. No restaura el recuento de células endoteliales ni suprime la progresión de la enfermedad.
DMEK (queratoplastia endotelial de la membrana de Descemet)
Injerto: Solo membrana de Descemet + endotelio (espesor aproximado 15 μm)
Características: Reportado por primera vez por Melles en 2006 11). Recuperación visual rápida, baja tasa de rechazo. Requiere un cirujano experimentado.
Cobertura del seguro en Japón: Desde 2016
DSAEK (queratoplastia endotelial automatizada con pelado de la membrana de Descemet)
PKP (Queratoplastia Penetrante)
Injerto: Córnea de espesor total (diámetro 7.0–8.5 mm)
Características: Opción clásica. Desafíos incluyen sutura, manejo del astigmatismo y riesgo de rechazo a largo plazo. En FECD, está siendo reemplazado gradualmente por queratoplastia endotelial.
DSO (Descemetorrexis sin Queratoplastia Endotelial)
Procedimiento: Desprendimiento selectivo solo de los 4 mm centrales de la membrana de Descemet. No se requiere injerto.
Indicaciones: Casos donde las células endoteliales periféricas residuales pueden migrar y proliferar hacia el centro. Aproximadamente el 75% logra aclaramiento corneal 14).
Gotas inhibidoras de ROCK: El uso postoperatorio de ripasudil promueve el aclaramiento incluso en casos no respondedores 14).
| Parámetro | DMEK | UT-DSAEK | Fuente |
|---|---|---|---|
| BCVA a 12 meses (diferencia logMAR) | −0.06 (DMEK superior) | — | Metanálisis de Sela 2023 3) |
| Tasa de logro de 20/25 o mejor | 66% | 33% (p=0.02) | Dunker 2020 RCT4) |
| OR de reinyección de burbuja | — | 2.76 (favoreciendo DSAEK) | Sela 20233) |
| ECD a 12 meses | Sin diferencia | Sin diferencia | Dunker 20204) |
| Grosor del injerto <70 μm | — | Sin diferencia en agudeza visual con DMEK | Sela 20233) |
En un metanálisis de Sela et al. (2023) de 8 estudios (376 ojos), la BCVA a los 12 meses fue significativamente mejor con DMEK (−0.06 logMAR)3). Un ECA multicéntrico de Dunker et al. (2020) también mostró una mayor tasa de alcanzar 20/25 o mejor con DMEK en comparación con UT-DSAEK (66% vs 33%, p=0.02)4). Sin embargo, para UT-DSAEK con un grosor del injerto inferior a 70 μm, la diferencia con DMEK se redujo3).
El grupo de la Universidad de Kioto (Kinoshita 2018) desarrolló un método de tratamiento en el que se inyectan células endoteliales corneales de donante sano cultivadas en la cámara anterior junto con un inhibidor de ROCK (Y-27632)13).
Los inhibidores de ROCK ejercen su efecto promoviendo la adhesión de las células endoteliales, suprimiendo la apoptosis y avanzando el ciclo celular13).
La FECD a menudo se asocia con cataratas, y se requiere una consideración cuidadosa sobre el momento y el método de la cirugía.
DMEK utiliza el injerto más delgado (aproximadamente 15 μm), ofreciendo una recuperación visual más rápida y menos cambios refractivos postoperatorios. Los metanálisis también muestran una BCVA superior a los 12 meses con DMEK3). Por otro lado, la manipulación del injerto en DSAEK es algo más fácil, con una curva de aprendizaje más corta para los cirujanos, y se realiza ampliamente en Japón. Se ha informado que el DSAEK ultrafino (<70 μm) logra resultados visuales casi equivalentes a DMEK3). La elección se basa en una evaluación integral de la experiencia del cirujano, la experiencia del centro y la condición corneal del paciente. Ambos procedimientos están cubiertos por el seguro en Japón desde 2016 (DMEK) o 2009 (DSAEK).
Las células endoteliales corneales normales no se dividen en la cámara anterior. Cuando el endotelio se pierde, las células adyacentes se agrandan y migran para cubrir el defecto, por lo que la densidad celular disminuye irreversiblemente con la edad. Cuando cae por debajo de 400–500 células/mm², mantener la transparencia corneal se vuelve difícil.
En la FECD, las células endoteliales degeneradas producen y depositan material similar al colágeno anormal en la superficie posterior de la membrana de Descemet, formando guttae. La membrana de Descemet se engrosa y se vuelve irregular, estableciendo un círculo vicioso que deteriora aún más la función endotelial.
El envejecimiento, la exposición a los rayos UV y el tabaquismo aumentan el estrés oxidativo y sirven como puntos de entrada para el círculo vicioso 2).
La función de bomba del endotelio corneal depende de la Na⁺/K⁺-ATPasa. Cuando las células endoteliales se dañan, se produce edema a través de las siguientes vías.
Si hay un aumento de la presión intraocular (hipertensión ocular) que supera la presión de hinchazón del estroma corneal, puede ocurrir edema epitelial incluso si el endotelio está relativamente sano. Se requiere precaución.
Dado que la contribución de la expansión de repeticiones TCF4 es relativamente pequeña en los japoneses8), dilucidar los antecedentes genéticos y ambientales específicos de los japoneses es un tema importante para el futuro.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.