Grau 0-1 (nenhum a leve)
Achados: 12 guttae ou menos no centro (Grau 0) ou mais de 12 guttae não confluentes (Grau 1)
Sintomas: Geralmente assintomáticos. Detectados como pontos escuros no microscópio especular.

A Distrofia Endotelial da Córnea de Fuchs (FECD) é uma doença progressiva que afeta bilateralmente as células endoteliais da córnea. Em 1910, Ernst Fuchs relatou 13 casos como “dystrophia epithelialis corneae”, e posteriormente foi identificada como uma doença endotelial, resultando no nome atual 1).
Guttae (guttata) aparecem na superfície endotelial central da córnea e se espalham gradualmente para a periferia. Quando a função de barreira e bomba (Na⁺/K⁺-ATPase) das células endoteliais diminui, ocorre edema do estroma corneano, seguido de edema epitelial e formação de bolhas. A membrana de Descemet torna-se espessada e irregular, resultando na perda de transparência da córnea.
Na 2ª edição da IC3D (Classificação Internacional de Distrofias da Córnea) (Weiss 2015), a FECD é classificada na categoria “distrofia endotelial da córnea” 15). De acordo com a idade de início, divide-se em dois tipos principais:
| Indicador | Valor | Fonte |
|---|---|---|
| Frequência de guttae corneanas em pacientes pré-cirurgia de catarata | 1,2% | Pesquisa multicêntrica nacional |
| Prevalência no Japão (Estudo Kumejima) idade ≥40 anos | 4,1% | Higa 20117) |
| Prevalência em mulheres no Japão (idade ≥40 anos) | 5,8% | Higa 20117) |
| Japão - Prevalência em homens (40 anos ou mais) | 2,4% | Higa 20117) |
| Islândia - Reykjavik Eye Study com 55 anos ou mais | Mulheres 11%, Homens 7% | Zoega 200610) |
| Razão entre sexos (internacional) | 2,5:1 a 3,5:1 (predomínio feminino) | Matthaei 20191) |
| Frequência da expansão de repetição TCF4 em japoneses | 12 de 47 casos (26%) | Nakano 20158) |
Os japoneses, que são da raça amarela, tendem a ter uma incidência menor de FECD em comparação com as raças branca e negra. No entanto, no Japão, espera-se que o número aumente com o envelhecimento da sociedade. Acredita-se que os japoneses tenham uma densidade de células endoteliais da córnea maior do que os brancos, retardando relativamente o início da doença.
Em japoneses, que frequentemente têm ângulo estreito, não é raro ocorrer diminuição das células endoteliais após iridectomia a laser (LI), sendo necessária atenção para a detecção precoce de FECD.
Em um estudo populacional realizado em Okinawa/Ilha de Kumejima (Kumejima Study), guttae corneanas foram detectadas em 4,1% dos indivíduos com 40 anos ou mais. Em mulheres, foi de 5,8%, e em homens, 2,4% 7). Há também dados nacionais mostrando que 1,2% dos pacientes submetidos a exame pré-operatório de catarata apresentavam córnea guttata. Acredita-se que os japoneses tenham menor frequência em comparação com europeus/americanos, mas a prevalência tende a aumentar com o envelhecimento da população.
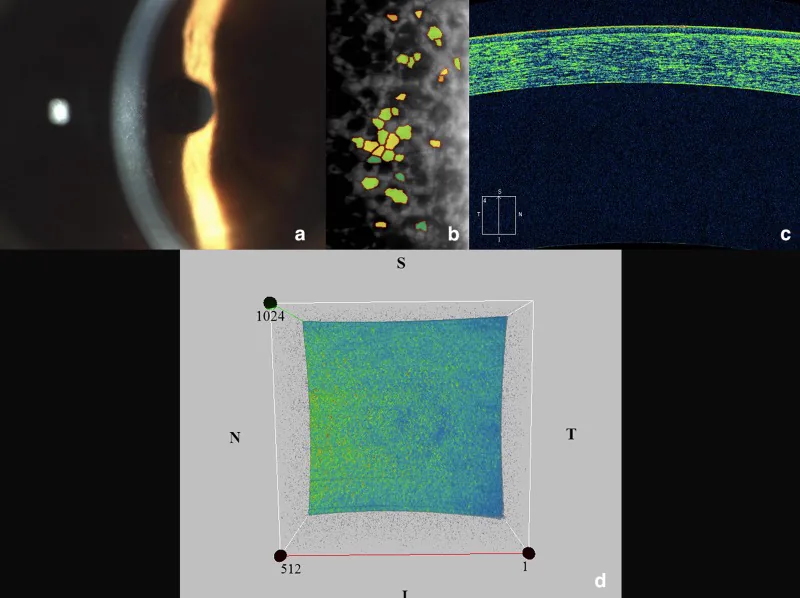
Normalmente, não há sintomas em indivíduos com menos de 50 anos. Os sintomas progridem lentamente em correlação com a gravidade do edema.
O exame básico é com lâmpada de fenda. Combine iluminação direta, iluminação por retrodispersão e método de reflexão especular para observação.
Grau 0-1 (nenhum a leve)
Achados: 12 guttae ou menos no centro (Grau 0) ou mais de 12 guttae não confluentes (Grau 1)
Sintomas: Geralmente assintomáticos. Detectados como pontos escuros no microscópio especular.
Grau 2-3 (Moderado)
Achados: Guttae confluentes centrais de 1-5 mm. Aspecto de metal batido leve.
Sintomas: Visão turva matinal. Imagem endotelial pouco nítida ao especular.
Grau 4 (Grave)
Achados: Guttae confluentes extensas >5 mm centrais. Aspecto de metal batido com pigmentação.
Sintomas: Visão turva persistente e fotofobia da manhã ao dia.
Grau 4+ Edema (Muito Grave)
Achados: Edema estromal e epitelial, formação de bolhas. Opacidade corneana acentuada.
Sintomas: Baixa acuidade visual grave o dia todo, dor ocular, lacrimejamento. Qualidade de vida drasticamente reduzida.
Esta classificação clínica baseia-se na classificação modificada por Krachmer et al. (1978)5).
Detalhes dos achados à lâmpada de fenda:
A córnea saudável mantém sua transparência porque as células endoteliais bombeiam constantemente água para a câmara anterior. Na FECD, a função de bomba endotelial está reduzida, portanto, durante o sono (com as pálpebras fechadas), a evaporação da água também cessa, e a córnea fica mais edemaciada pela manhã, com visão turva intensa. Com os olhos abertos, a água evapora da superfície da córnea e o edema melhora durante o dia, restaurando a visão. Com a progressão da doença, essa variação diurna desaparece e a visão turva persiste o dia todo.
A FECD é principalmente de herança autossômica dominante, mas há variação na penetrância e expressividade, e existem casos sem história familiar clara.
Principais genes causadores:
Em japoneses, a frequência da expansão da repetição do TCF4 é menor que no Ocidente, portanto, outros contextos genéticos precisam ser elucidados8).
A FECD é herdada principalmente em um padrão autossômico dominante. Teoricamente, a probabilidade de transmissão para uma criança é de 50%. No entanto, há grande variação no momento de início e gravidade (penetrância incompleta), e muitas pessoas que herdam o gene vivem a vida inteira com sintomas muito leves. Especialmente em japoneses, a proporção de anormalidades no gene TCF4, a causa mais comum no Ocidente, é baixa 8), sugerindo uma base genética diferente. Se estiver preocupado, recomenda-se consultar um geneticista.
Não existem critérios diagnósticos uniformes no Japão, mas o diagnóstico clínico é feito por uma combinação dos seguintes exames.
Este é o exame mais importante para o diagnóstico e acompanhamento da FECD.
| Parâmetro | Valor Normal | Limiar Anormal |
|---|---|---|
| Densidade de células endoteliais (período neonatal) | 3.500–4.000 células/mm² | — |
| Densidade de células endoteliais (20 anos) | 2.700 células/mm² | — |
| Densidade de células endoteliais (70 anos ou mais) | Média de 2.200 células/mm² | — |
| Limite para manutenção da transparência | — | 400–500 células/mm² ou menos |
| Valor de CV (coeficiente de variação) | 0,2–0,3 | ≥ 0,35 |
| Taxa de células hexagonais (hexagonality) | 60-70% | ≤ 50% |
| Doença | Pontos de diferenciação |
|---|---|
| Distrofia polimorfa posterior da córnea (PPCD) | Herança AD, bilateral, opacidades em faixa ou bolhosas na membrana de Descemet. Genes: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| Distrofia endotelial hereditária congênita da córnea (CHED) | Herança AR (mutação SLC4A11), início ao nascimento ou na infância, edema e opacidade corneana desde o nascimento |
| Ceratopatia bolhosa pseudofácica (PBK) | Disfunção endotelial após cirurgia de catarata. Sem guttae, histórico cirúrgico presente |
| Ceratopatia da síndrome de pseudoexfoliação | Depósitos de material PEX, aumento da pressão intraocular, material PEX na superfície anterior do cristalino é a chave para o diagnóstico diferencial |
| Síndrome ICE (Iridocorneal Endotelial) | Unilateral, acompanhada de atrofia da íris, sinéquias anteriores e glaucoma. Sem guttae |
| Alterações endoteliais em olhos com ângulo estreito | Podem apresentar achados semelhantes a guttae corneanos. Diferenciados pela pressão intraocular e morfologia do ângulo |
O microscópio especular (dispositivo de imagem de células endoteliais por reflexão especular) é um aparelho que fotografa e mede as células endoteliais da camada mais interna da córnea de forma não invasiva, utilizando reflexão de luz especial. O exame mede o número de células endoteliais (densidade celular), a variação de tamanho (valor CV) e a uniformidade da forma (porcentagem de células hexagonais). Na FECD, as guttae aparecem como pontos escuros (dark spots), auxiliando na avaliação do estágio da doença. A captura de imagem leva alguns minutos e é indolor.
O objetivo do tratamento é restaurar a transparência da córnea e manter a visão. A terapia sintomática ou cirúrgica é escolhida de acordo com o estágio da doença.
Visa aliviar os sintomas antes da cirurgia. Não há efeito na recuperação do número de células endoteliais ou na desaceleração da progressão da doença.
DMEK (Ceratoplastia Endotelial com Membrana de Descemet)
Enxerto: Membrana de Descemet + endotélio apenas (espessura de aproximadamente 15 μm)
Características: Primeiro relato por Melles em 2006 11). Recuperação visual rápida, baixa taxa de rejeição. Requer cirurgião experiente.
Cobertura do seguro no Japão: Desde 2016
DSAEK (Ceratoplastia Endotelial Automatizada com Remoção da Membrana de Descemet)
PKP (Transplante de Córnea Total)
Enxerto: Córnea de espessura total (diâmetro 7,0–8,5 mm)
Características: Opção clássica. Desafios incluem sutura, gerenciamento de astigmatismo e risco de rejeição a longo prazo. No campo da FECD, está sendo gradualmente substituído pelo transplante endotelial.
DSO (Descemetorrexe sem Ceratoplastia Endotelial)
Procedimento: Remoção seletiva apenas da parte central da membrana de Descemet com 4 mm. Sem necessidade de enxerto.
Indicações: Casos em que as células endoteliais periféricas remanescentes podem migrar e proliferar para o centro. Cerca de 75% apresentam clareamento corneano14).
Colírio inibidor de ROCK: O uso de ripasudil no pós-operatório promove clareamento mesmo em casos não responsivos14).
| Indicador | DMEK | UT-DSAEK | Fonte |
|---|---|---|---|
| BCVA em 12 meses (diferença logMAR) | −0,06 (DMEK superior) | — | Sela 2023 meta-análise3) |
| Taxa de alcance de 20/25 ou melhor | 66% | 33% (p=0,02) | Dunker 2020 RCT4) |
| Odds ratio de reborbulhamento | — | 2,76 (DSAEK superior) | Sela 20233) |
| ECD em 12 meses | Sem diferença | Sem diferença | Dunker 20204) |
| Espessura do enxerto <70 μm | — | Sem diferença na acuidade visual com DMEK | Sela 20233) |
A metanálise de Sela et al. (2023) (8 estudos, 376 olhos) mostrou que a BCVA em 12 meses foi significativamente melhor no DMEK (−0,06 logMAR) 3). O ECR multicêntrico de Dunker et al. (2020) também mostrou que o DMEK teve maior taxa de atingir 20/25 ou melhor em comparação com UT-DSAEK (66% vs 33%, p=0,02) 4). No entanto, UT-DSAEK com espessura do enxerto <70 μm reduziu a diferença em relação ao DMEK 3).
O grupo da Universidade de Kyoto (Kinoshita 2018) desenvolveu uma terapia que injeta células endoteliais da córnea de doador saudável cultivadas juntamente com um inibidor de ROCK (Y-27632) na câmara anterior 13).
O inibidor de ROCK atua promovendo a adesão das células endoteliais, inibindo a apoptose e promovendo a progressão do ciclo celular 13).
Na FECD, a catarata é frequentemente concomitante, exigindo seleção cuidadosa do momento e método cirúrgico.
O DMEK possui o enxerto mais fino (cerca de 15 μm), proporcionando recuperação visual mais rápida e menos alteração refrativa pós-operatória. A metanálise também mostrou BCVA superior em 12 meses para DMEK 3). Por outro lado, o DSAEK é um pouco mais fácil de manusear o enxerto e tem curva de aprendizado mais curta, sendo amplamente realizado no país. O DSAEK ultrafino (<70 μm) relatou resultados visuais quase equivalentes ao DMEK 3). A escolha é feita com base na avaliação abrangente da experiência do cirurgião, experiência da instituição e condição da córnea do paciente. Ambos os procedimentos são cobertos pelo seguro de saúde no país desde 2016 (DMEK) ou 2009 (DSAEK).
As células endoteliais corneanas normais não se dividem na câmara anterior. Quando o endotélio é danificado, as células adjacentes aumentam e migram para cobrir o defeito, de modo que a densidade celular diminui irreversivelmente com a idade. Abaixo de 400-500 células/mm², torna-se difícil manter a transparência da córnea.
Na FECD, as células endoteliais degeneradas produzem e depositam material colágeno anormal na superfície posterior da membrana de Descemet, formando guttae. A membrana de Descemet torna-se espessada e irregular, criando um ciclo vicioso que prejudica ainda mais a função endotelial.
Envelhecimento, exposição a UV e tabagismo aumentam o estresse oxidativo e servem como porta de entrada para o ciclo vicioso 2).
A função de bomba do endotélio da córnea depende da Na⁺/K⁺-ATPase. Quando as células endoteliais são danificadas, o edema ocorre através das seguintes vias.
Se houver aumento da pressão intraocular que exceda a pressão de inchaço do estroma da córnea, pode ocorrer edema epitelial mesmo que o endotélio esteja relativamente saudável, e isso requer atenção.
Como a contribuição da expansão de repetição TCF4 é relativamente pequena em japoneses8), a elucidação dos antecedentes genéticos e ambientais específicos dos japoneses é uma questão importante para o futuro.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.