درجه 0-1 (بدون تا خفیف)
یافتهها: 12 یا کمتر گوتا در ناحیه مرکزی (درجه 0) یا بیش از 12 گوتای غیرهمجوار (درجه 1)
علائم: معمولاً بدون علامت. در میکروسکوپ اسپکولار به صورت نقاط تیره تشخیص داده میشود.

دیستروفی اندوتلیال قرنیه فوکس (Fuchs Endothelial Corneal Dystrophy; FECD) یک بیماری پیشرونده دوطرفه است که سلولهای اندوتلیال قرنیه را تحت تأثیر قرار میدهد. در سال ۱۹۱۰، ارنست فوکس ۱۳ مورد را با عنوان «dystrophia epithelialis corneae» گزارش کرد و بعداً مشخص شد که این بیماری اندوتلیال است و به نام فعلی تغییر یافت 1).
گوتا (guttae/guttata) در سطح اندوتلیال مرکز قرنیه ظاهر شده و به تدریج به سمت محیط گسترش مییابد. با کاهش عملکرد سد و پمپ سلولهای اندوتلیال (Na⁺/K⁺-ATPase)، ادم استروما و سپس ادم اپیتلیوم و تشکیل تاول رخ میدهد. ضخیم شدن و نامنظمی غشای دسمه منجر به از دست رفتن شفافیت قرنیه میشود.
در ویرایش دوم IC3D (طبقهبندی بینالمللی دیستروفیهای قرنیه) (Weiss 2015)، FECD در رده «دیستروفی اندوتلیال قرنیه» طبقهبندی میشود15). بر اساس زمان شروع، به دو نوع زیر تقسیم میشود:
| شاخص | مقدار | منبع |
|---|---|---|
| فراوانی گوتاتای قرنیه در بیماران قبل از جراحی آب مروارید | ۱٫۲٪ | بررسی چندمرکزی داخلی |
| شیوع در افراد ۴۰ سال و بالاتر در مطالعه Kumejima ژاپن | ۴٫۱٪ | Higa 20117) |
| شیوع در زنان ژاپنی (۴۰ سال و بالاتر) | ۵٫۸٪ | Higa 20117) |
| شیوع در مردان ژاپنی (بالای 40 سال) | 2.4% | Higa 20117) |
| ایسلند - مطالعه چشم ریکیاویک، بالای 55 سال | زنان 11٪، مردان 7٪ | Zoega 200610) |
| نسبت جنسی (بینالمللی) | 2.5:1 تا 3.5:1 (غلبه زنان) | Matthaei 20191) |
| فراوانی تکرار TCF4 در ژاپنیها | 12 مورد از 47 مورد (26%) | Nakano 20158) |
ژاپنیها به عنوان نژاد زرد، نسبت به نژاد سفید و سیاه، تمایل به بروز کمتر FECD دارند. با این حال، با افزایش جمعیت سالمند در کشور ما، پیشبینی میشود که در آینده بیشتر افزایش یابد. تصور میشود که ژاپنیها به دلیل تراکم بالاتر سلولهای اندوتلیال قرنیه نسبت به سفیدپوستان، دیرتر به این بیماری مبتلا میشوند.
در ژاپنیها که اغلب زاویه باریک دارند، موارد کاهش سلولهای اندوتلیال پس از ایریدوتومی لیزری (LI) غیرمعمول نیست و تشخیص زودهنگام FECD نیاز به توجه دارد.
در مطالعهای بر روی ساکنان جزیره کومهجیما در اوکیناوا (مطالعه کومهجیما)، گوتای قرنیه در 4.1% از افراد 40 سال و بالاتر تشخیص داده شد. این میزان در زنان 5.8% و در مردان 2.4% بود7). همچنین دادههای داخلی نشان میدهد که 1.2% از بیمارانی که تحت معاینه قبل از عمل آب مروارید قرار گرفتند، قرنیه قطرهای داشتند. گفته میشود که فراوانی این بیماری در ژاپنیها کمتر از اروپاییها و آمریکاییها است، اما با افزایش سن جمعیت، روند افزایشی دارد.
معمولاً در افراد زیر 50 سال بدون علامت است. علائم به تدریج و متناسب با شدت ادم پیشرفت میکنند.
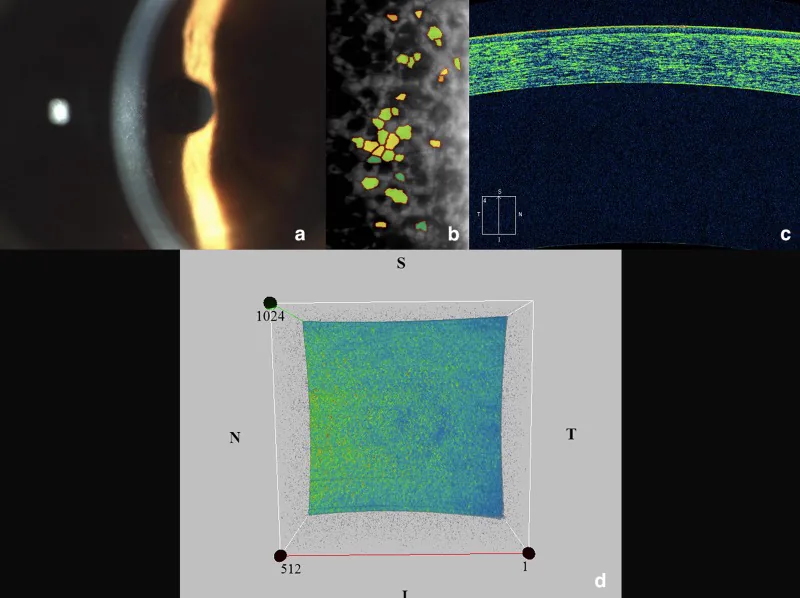
معاینه با لامپ شکاف اساسی است. از روشهای روشنایی مستقیم، روشنایی پراکنده عقبی و بازتاب آینهای به صورت ترکیبی استفاده میشود.
درجه 0-1 (بدون تا خفیف)
یافتهها: 12 یا کمتر گوتا در ناحیه مرکزی (درجه 0) یا بیش از 12 گوتای غیرهمجوار (درجه 1)
علائم: معمولاً بدون علامت. در میکروسکوپ اسپکولار به صورت نقاط تیره تشخیص داده میشود.
درجه ۲-۳ (متوسط)
یافتهها: گوتاهای همجوار به قطر ۱-۵ میلیمتر در مرکز. ظاهر فلز کوبیده شده خفیف.
علائم: تاری دید صبحگاهی. تصویر اندوتلیوم در اسپکولار نامشخص میشود.
درجه ۴ (شدید)
یافتهها: گوتاهای همجوار گسترده به قطر بیش از ۵ میلیمتر در مرکز. ظاهر فلز کوبیده شده همراه با رسوب رنگدانه.
علائم: تاری دید و حساسیت به نور مداوم از صبح تا روز.
درجه ۴+ ادم (بسیار شدید)
یافتهها: ادم استروما، ادم اپیتلیوم، تشکیل تاول. کدورت قرنیه قابل توجه.
علائم: کاهش شدید بینایی در تمام روز، درد چشم، اشکریزش. کیفیت زندگی به شدت کاهش مییابد.
این طبقهبندی بالینی بر اساس طبقهبندی اصلاحشده توسط Krachmer و همکاران (۱۹۷۸) است5).
جزئیات یافتههای لامپ شکافی:
قرنیه سالم به دلیل پمپاژ مداوم آب به سمت اتاق قدامی توسط سلولهای اندوتلیال، شفاف باقی میماند. در FECD، عملکرد پمپ اندوتلیال کاهش مییابد، بنابراین در طول خواب (زمانی که پلکها بسته هستند) دفع آب از طریق تبخیر نیز متوقف میشود و صبحها قرنیه بیشترین ادم را داشته و تاری دید شدیدتر است. با باز بودن چشمها، آب از سطح قرنیه تبخیر میشود و در طول روز ادم تا حدودی بهبود یافته و بینایی بازمیگردد. با پیشرفت بیماری، این نوسان روزانه از بین رفته و تاری دید در تمام طول روز ادامه مییابد.
FECD عمدتاً به صورت اتوزومال غالب به ارث میرسد، اما نفوذ و بیانپذیری متغیر است و مواردی با سابقه خانوادگی نامشخص نیز وجود دارد.
ژنهای اصلی:
در ژاپنیها، فراوانی گسترش تکرار TCF4 کمتر از اروپا و آمریکا است، بنابراین نیاز به کشف سایر زمینههای ژنتیکی وجود دارد8).
FECD عمدتاً به صورت اتوزومال غالب به ارث میرسد. از نظر تئوری، احتمال انتقال به کودک ۵۰٪ است. با این حال، زمان شروع و شدت بیماری بسیار متغیر است (نفوذ ناقص) و بسیاری از افراد حتی با داشتن ژن، علائم بسیار خفیفی در طول زندگی دارند. به ویژه در ژاپنیها، نسبت ناهنجاری ژن TCF4 که شایعترین علت در غرب است، پایین است8) و ممکن است زمینه ژنتیکی متفاوتی داشته باشند. در صورت نگرانی، مشاوره با متخصص ژنتیک توصیه میشود.
معیار تشخیصی یکپارچه در ژاپن وجود ندارد، اما تشخیص بالینی با ترکیب آزمایشهای زیر انجام میشود.
مهمترین آزمایش برای تشخیص و پیگیری FECD است.
| پارامتر | مقدار طبیعی | آستانه غیرطبیعی |
|---|---|---|
| تراکم سلولهای اندوتلیال (دوره نوزادی) | ۳,۵۰۰ تا ۴,۰۰۰ سلول بر میلیمتر مربع | — |
| تراکم سلولهای اندوتلیال (دهه ۲۰ سالگی) | ۲,۷۰۰ سلول بر میلیمتر مربع | — |
| تراکم سلولهای اندوتلیال (۷۰ سال و بالاتر) | میانگین ۲,۲۰۰ سلول بر میلیمتر مربع | — |
| حداقل تراکم برای حفظ شفافیت | — | ۴۰۰ تا ۵۰۰ سلول بر میلیمتر مربع یا کمتر |
| ضریب تغییرات (CV) | ۰.۲ تا ۰.۳ | ≥ ۰.۳۵ |
| درصد سلولهای ششضلعی (hexagonality) | 60-70% | ≤ 50% |
| بیماری | نکات افتراقی |
|---|---|
| دیستروفی پلیمورف خلفی قرنیه (PPCD) | وراثت AD، دوطرفه، کدورتهای نواری و تاولی غشای دسمه. ژنها: PPCD1 (20p11.2-q11.2)، PPCD2 (COL8A2)، PPCD3 (ZEB1) |
| دیستروفی اندوتلیال ارثی مادرزادی قرنیه (CHED) | وراثت AR (جهش SLC4A11)، شروع از بدو تولد تا شیرخوارگی، ادم و کدورت قرنیه از بدو تولد |
| کراتوپاتی تاولی شبهآفاکیک (PBK) | آسیب اندوتلیال پس از جراحی آب مروارید. بدون گوتا، سابقه جراحی |
| کراتوپاتی سندرم شبهلایهبرداری | رسوب مواد PEX، افزایش فشار چشم، مواد PEX روی سطح قدامی عدسی کلید تشخیص افتراقی |
| سندرم ICE (عنبیه-قرنیه-اندوتلیوم) | یکطرفه، همراه با آتروفی عنبیه، چسبندگی قدامی و گلوکوم. بدون گوتا |
| تغییرات اندوتلیال در چشم با زاویه باریک | ممکن است یافتههای شبه گوتا ظاهر شود. تشخیص با فشار چشم و مورفولوژی زاویه |
اسپکولار میکروسکوپ (دستگاه تصویربرداری سلولهای اندوتلیال با بازتاب آینهای) دستگاهی است که با استفاده از بازتاب ویژه نور، سلولهای اندوتلیال داخلیترین لایه قرنیه را به صورت غیرتهاجمی تصویربرداری و اندازهگیری میکند. در این آزمایش، تعداد سلولهای اندوتلیال (تراکم سلولی)، تنوع اندازه (ضریب CV) و یکنواختی شکل (درصد سلولهای ششضلعی) اندازهگیری میشود. در FECD، گوتاها به صورت نقاط تیره (لکه تیره) ظاهر میشوند و به ارزیابی مرحله بیماری کمک میکنند. تصویربرداری چند دقیقه طول میکشد و بدون درد است.
هدف درمان، بازگرداندن شفافیت قرنیه و حفظ بینایی است. بسته به مرحله بیماری، از درمان علامتی تا جراحی انتخاب میشود.
هدف، تسکین علائم قبل از اندیکاسیون جراحی است. این درمان باعث افزایش تعداد سلولهای اندوتلیال یا مهار پیشرفت بیماری نمیشود.
DMEK (پیوند غشای دسمه و اندوتلیوم قرنیه)
پیوند: فقط غشای دسمه + اندوتلیوم (ضخامت حدود ۱۵ میکرومتر)
ویژگیها: اولین گزارش توسط Melles در سال ۲۰۰۶11). بهبود بینایی سریع و نرخ رد پیوند پایین. نیاز به جراح ماهر دارد.
پوشش بیمه در ژاپن: از سال ۲۰۱۶
DSAEK (پیوند اندوتلیوم قرنیه با کمک دستگاه خودکار جداسازی غشای دسمه)
PKP (پیوند قرنیه تماملایه)
گرافت: قرنیه تماملایه (قطر ۷.۰ تا ۸.۵ میلیمتر)
ویژگیها: گزینه کلاسیک. چالشها شامل بخیه، مدیریت آستیگماتیسم و خطر رد طولانیمدت. در زمینه FECD به تدریج با پیوند اندوتلیال جایگزین میشود.
DSO (Descemetorhexis بدون پیوند اندوتلیال قرنیه)
روش: فقط برداشت انتخابی ۴ میلیمتر مرکزی غشای دسمه. بدون نیاز به گرافت.
موارد مناسب: مواردی که سلولهای اندوتلیال محیطی باقیمانده میتوانند به مرکز مهاجرت و تکثیر کنند. حدود ۷۵٪ شفافیت قرنیه 14).
قطره مهارکننده ROCK: استفاده از ریپاسودیل پس از جراحی باعث افزایش شفافیت حتی در موارد مقاوم میشود 14).
| شاخص | DMEK | UT-DSAEK | منبع |
|---|---|---|---|
| BCVA ۱۲ ماهه (تفاوت logMAR) | ۰.۰۶- (برتری DMEK) | — | Sela 2023 متاآنالیز 3) |
| نرخ دستیابی به 20/25 یا بهتر | 66% | 33% (p=0.02) | Dunker 2020 RCT4) |
| نسبت شانس ریبابلینگ | — | 2.76 (به نفع DSAEK) | Sela 20233) |
| ECD 12 ماهه | بدون تفاوت | بدون تفاوت | Dunker 20204) |
| ضخامت گرافت <70 میکرومتر | — | بدون تفاوت بینایی با DMEK | Sela 20233) |
در متاآنالیز Sela و همکاران (2023) روی 376 چشم از 8 مطالعه، BCVA در 12 ماه در DMEK به طور معنیداری بهتر بود (۰.۰۶- logMAR)3). در کارآزمایی بالینی تصادفی چندمرکزی Dunker و همکاران (2020) نیز DMEK نرخ دستیابی به 20/25 یا بهتر را نسبت به UT-DSAEK بالاتر نشان داد (66% در مقابل 33%، p=0.02)4). با این حال، در UT-DSAEK با ضخامت گرافت کمتر از 70 میکرومتر، تفاوت با DMEK کاهش یافت3).
گروه دانشگاه کیوتو (Kinoshita 2018) روشی را توسعه دادند که در آن سلولهای اندوتلیال قرنیه اهداکننده سالم کشتشده همراه با مهارکننده ROCK (Y-27632) به داخل اتاق قدامی تزریق میشود13).
مهارکننده ROCK با افزایش چسبندگی سلولهای اندوتلیال، مهار آپوپتوز و پیشبرد چرخه سلولی اثر خود را اعمال میکند13).
در FECD، آب مروارید شایع است و انتخاب زمان و روش جراحی نیاز به دقت دارد.
DMEK به دلیل نازکترین گرافت (حدود 15 میکرومتر) مزایای بهبود سریعتر بینایی و تغییرات انکساری کمتر پس از عمل را دارد. متاآنالیز نیز BCVA در 12 ماه را در DMEK برتر نشان داد3). از سوی دیگر، DSAEK دستکاری گرافت نسبتاً آسانتر و منحنی یادگیری جراح کوتاهتر است و در داخل کشور نیز به طور گسترده انجام میشود. گزارش شده است که DSAEK فوقنازک (کمتر از 70 میکرومتر) نتایج بینایی تقریباً معادل DMEK دارد3). انتخاب با توجه به تجربه جراح معالج، تجربه مرکز و وضعیت قرنیه بیمار به صورت جامع انجام میشود. هر دو روش از سال 2016 (DMEK) یا 2009 (DSAEK) در داخل کشور تحت پوشش بیمه هستند.
سلولهای اندوتلیال قرنیه طبیعی در اتاق قدامی تقسیم سلولی ندارند. هنگامی که اندوتلیوم دچار نقص میشود، سلولهای مجاور بزرگ شده و مهاجرت میکنند تا نقص را جبران کنند، بنابراین تراکم سلولی با افزایش سن به طور غیرقابل برگشتی کاهش مییابد. هنگامی که تراکم به زیر ۴۰۰-۵۰۰ سلول در میلیمتر مربع میرسد، حفظ شفافیت قرنیه دشوار میشود.
در FECD، سلولهای اندوتلیال تخریب شده مواد کلاژن مانند غیرطبیعی را در سطح پشتی غشای دسمه تولید و رسوب میدهند و گوتا تشکیل میدهند. غشای دسمه ضخیم و نامنظم میشود و یک چرخه معیوب ایجاد میکند که عملکرد اندوتلیال را بیشتر مختل میکند.
افزایش سن، قرار گرفتن در معرض اشعه ماوراء بنفش و سیگار کشیدن همگی استرس اکسیداتیو را افزایش میدهند و به عنوان ورودی چرخه معیوب عمل میکنند2).
عملکرد پمپ اندوتلیوم قرنیه به Na⁺/K⁺-ATPase وابسته است. هنگامی که سلولهای اندوتلیال آسیب میبینند، ادم از طریق مسیرهای زیر ایجاد میشود.
در صورت افزایش فشار داخل چشم (فشار بالا) که از فشار تورمی استرومای قرنیه فراتر رود، حتی اگر اندوتلیوم نسبتاً سالم باشد، ممکن است ادم اپیتلیال رخ دهد که نیاز به توجه دارد.
از آنجایی که سهم تکرارهای TCF4 در ژاپنیها نسبتاً کم است 8)، روشنسازی زمینههای ژنتیکی و محیطی خاص ژاپنیها یک موضوع مهم آینده است.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.