Grado 0-1 (assente o lieve)
Segni: 12 o meno guttae non confluenti (Grado 0) o più di 12 guttae non confluenti (Grado 1) nell’area centrale.
Sintomi: Di solito asintomatico. Rilevato come macchie scure al microscopio speculare.

La distrofia endoteliale corneale di Fuchs (FECD) è una malattia progressiva caratterizzata da un’anomalia bilaterale delle cellule endoteliali corneali. Nel 1910 Ernst Fuchs riportò per la prima volta 13 casi come «dystrophia epithelialis corneae», e successivamente si scoprì che si trattava di una malattia endoteliale, da cui il nome attuale 1).
Sulla superficie endoteliale centrale della cornea compaiono gocce (guttae/guttata) che si estendono gradualmente verso la periferia. Quando la funzione di barriera e pompa (Na⁺/K⁺-ATPasi) delle cellule endoteliali diminuisce, si verifica edema dello stroma corneale, seguito da edema epiteliale e formazione di bolle. La membrana di Descemet si ispessisce e diventa irregolare, portando alla perdita di trasparenza della cornea.
Nella 2ª edizione dell’IC3D (Classificazione Internazionale delle Distrofie Corneali) (Weiss 2015), la FECD è classificata nella categoria «Distrofie endoteliali corneali» 15). In base all’età di insorgenza, si distinguono due tipi principali.
| Indicatore | Valore | Fonte |
|---|---|---|
| Frequenza di cornea guttata nei pazienti prima dell’intervento di cataratta | 1,2% | Indagine multicentrica nazionale |
| Prevalenza in Giappone (studio Kumejima) nei ≥40 anni | 4,1% | Higa 20117) |
| Prevalenza nelle donne giapponesi (≥40 anni) | 5,8% | Higa 20117) |
| Prevalenza maschile in Giappone (40 anni e oltre) | 2,4% | Higa 20117) |
| Islanda - Reykjavik Eye Study, 55 anni e oltre | Donne 11%, uomini 7% | Zoega 200610) |
| Rapporto maschi/femmine (internazionale) | 2,5:1 - 3,5:1 (predominanza femminile) | Matthaei 20191) |
| Frequenza dell’espansione di ripetizione TCF4 nei giapponesi | 12 casi su 47 (26%) | Nakano 20158) |
I giapponesi, come razza gialla, tendono ad avere un’incidenza di FECD inferiore rispetto ai caucasici e ai neri. Tuttavia, con l’invecchiamento della società in Giappone, si prevede un ulteriore aumento. Si ritiene che i giapponesi abbiano una densità di cellule endoteliali corneali più elevata rispetto ai caucasici, ritardando relativamente l’insorgenza della malattia.
In molti giapponesi con angolo stretto, la diminuzione delle cellule endoteliali dopo iridotomia laser (LI) non è rara, ed è necessaria attenzione per la diagnosi precoce della FECD.
Nello studio di popolazione condotto a Okinawa, isola di Kumejima (Kumejima Study), le guttae corneali sono state rilevate nel 4,1% delle persone di età pari o superiore a 40 anni. Nelle donne era il 5,8%, negli uomini il 2,4% 7). Esistono anche dati nazionali che mostrano una cornea guttata nell’1,2% dei pazienti esaminati prima di un intervento di cataratta. La frequenza è considerata più bassa nei giapponesi rispetto agli europei o americani, ma è in aumento con l’invecchiamento della società.
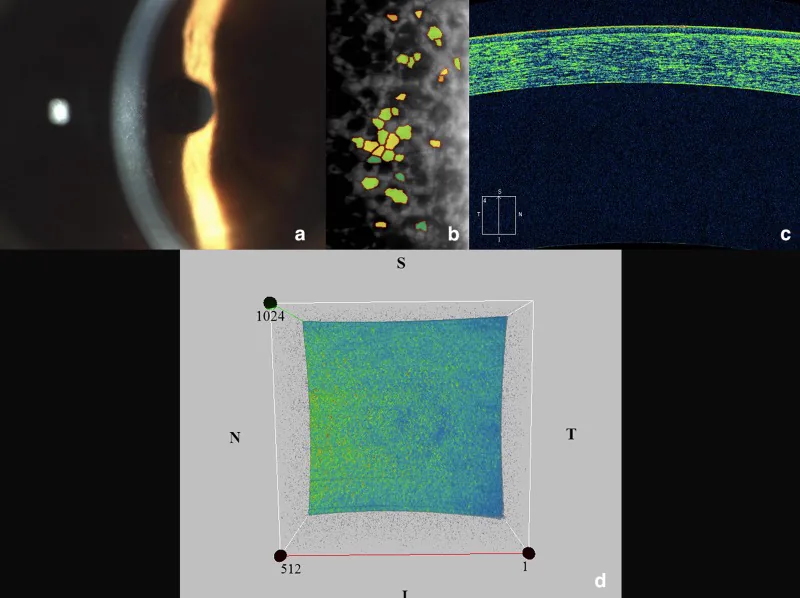
Di solito, prima dei 50 anni la malattia è asintomatica. I sintomi progrediscono lentamente in correlazione con il grado di edema.
L’esame con lampada a fessura è fondamentale. Si combinano illuminazione diretta, retroilluminazione e riflessione speculare.
Grado 0-1 (assente o lieve)
Segni: 12 o meno guttae non confluenti (Grado 0) o più di 12 guttae non confluenti (Grado 1) nell’area centrale.
Sintomi: Di solito asintomatico. Rilevato come macchie scure al microscopio speculare.
Grado 2-3 (moderato)
Reperti: Guttae confluenti centrali di 1-5 mm. Lieve aspetto a metallo battuto.
Sintomi: Visione offuscata mattutina. L’endotelio appare poco nitido alla microscopia speculare.
Grado 4 (grave)
Reperti: Guttae confluenti estese > 5 mm centrali. Aspetto a metallo battuto con pigmentazione.
Sintomi: Visione offuscata persistente dal mattino al giorno, fotofobia.
Grado 4+ edema (gravissimo)
Reperti: Edema stromale, edema epiteliale, formazione di bolle. Opacità corneale marcata.
Sintomi: Grave riduzione della vista per tutto il giorno, dolore oculare, lacrimazione. Qualità della vita notevolmente ridotta.
Questa stadiazione clinica si basa sulla classificazione modificata di Krachmer et al. (1978)5).
Dettagli dei reperti alla lampada a fessura:
In una cornea sana, le cellule endoteliali pompano costantemente acqua verso la camera anteriore per mantenere la trasparenza. Nella FECD, la funzione di pompa endoteliale è ridotta, quindi durante il sonno (palpebre chiuse) anche l’evaporazione dell’acqua si ferma, e la cornea è più edematosa al mattino, con visione offuscata aumentata. Quando gli occhi sono aperti, l’acqua evapora dalla superficie corneale e durante il giorno l’edema migliora in una certa misura, consentendo il recupero della vista. Con il progredire della malattia, questa variazione diurna scompare e la visione offuscata persiste per tutto il giorno.
La FECD è principalmente a trasmissione autosomica dominante, ma ci sono variazioni nella penetranza e nell’espressività, e alcuni casi non hanno una chiara storia familiare.
Geni principali responsabili :
Nei giapponesi, la frequenza dell’espansione della ripetizione TCF4 è inferiore rispetto all’Occidente, quindi è necessaria la chiarificazione di altri background genetici8).
La FECD si eredita principalmente con un pattern autosomico dominante. Teoricamente, la probabilità di trasmissione a un figlio è del 50%. Tuttavia, l’età di insorgenza e la gravità variano notevolmente (penetranza incompleta); molte persone che ereditano il gene presentano sintomi molto lievi per tutta la vita. In particolare nei giapponesi, la proporzione di anomalie del gene TCF4, la causa più comune negli occidentali, è bassa8), suggerendo un diverso background genetico. In caso di preoccupazione, si consiglia una consulenza con un genetista.
Non esistono criteri diagnostici unificati in Giappone, ma la diagnosi clinica viene effettuata combinando i seguenti esami.
Questo è l’esame più importante per la diagnosi e il follow-up della FECD.
| Parametro | Valore normale | Soglia di anomalia |
|---|---|---|
| Densità delle cellule endoteliali (periodo neonatale) | 3.500–4.000 cellule/mm² | — |
| Densità delle cellule endoteliali (20 anni) | 2.700 cellule/mm² | — |
| Densità delle cellule endoteliali (70 anni e oltre) | Media 2.200 cellule/mm² | — |
| Soglia di mantenimento della trasparenza | — | 400–500 cellule/mm² o meno |
| Valore CV (coefficiente di variazione) | 0,2–0,3 | ≥ 0,35 |
| Percentuale di esagonalità (hexagonality) | 60–70% | ≤ 50% |
| Malattia | Punti chiave per la diagnosi differenziale |
|---|---|
| Distrofia corneale polimorfa posteriore (PPCD) | Ereditarietà AD, bilaterale, opacità a bande e vescicolari della membrana di Descemet. Geni: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| Distrofia endoteliale corneale ereditaria congenita (CHED) | Ereditarietà AR (mutazione SLC4A11), esordio alla nascita o nell’infanzia, edema e opacità corneale dalla nascita |
| Cheratopatia bollosa pseudofachica (PBK) | Danno endoteliale dopo chirurgia della cataratta. Assenza di guttae, anamnesi chirurgica |
| Cheratopatia da sindrome pseudoesfoliativa | Depositi di sostanza PEX, aumento della pressione intraoculare, sostanza PEX sulla superficie anteriore del cristallino come chiave per la diagnosi differenziale |
| Sindrome ICE (irido-corneo-endoteliale) | Unilaterale, associata ad atrofia dell’iride, sinechie anteriori e glaucoma. Assenza di guttae |
| Alterazioni endoteliali in occhi con angolo stretto | Può presentare aspetti simili a gocce corneali. Diagnosi differenziale tramite pressione intraoculare e morfologia dell’angolo |
Il microscopio speculare (apparecchio per la fotografia delle cellule endoteliali a riflessione speculare) è un dispositivo che fotografa e misura in modo non invasivo le cellule endoteliali dello strato più interno della cornea utilizzando una speciale riflessione della luce. L’esame misura il numero di cellule endoteliali (densità cellulare), la variabilità delle dimensioni (coefficiente di variazione) e l’uniformità della forma (percentuale di cellule esagonali). Nella FECD, le guttae appaiono come punti neri (macchie scure), aiutando a valutare lo stadio della malattia. La fotografia richiede pochi minuti ed è indolore.
L’obiettivo del trattamento è ripristinare la trasparenza corneale e mantenere l’acuità visiva. A seconda dello stadio della malattia, si sceglie una terapia sintomatica o chirurgica.
Ha lo scopo di alleviare i sintomi prima dell’indicazione chirurgica. Non ha effetto sul recupero del numero di cellule endoteliali né sulla progressione della malattia.
DMEK (cheratoplastica endoteliale con membrana di Descemet)
Innesto: solo membrana di Descemet + endotelio (spessore circa 15 μm)
Caratteristiche: prima descrizione da Melles nel 2006 11). Recupero visivo rapido, basso tasso di rigetto. Richiede un chirurgo esperto.
Copertura assicurativa in Giappone: dal 2016
DSAEK (cheratoplastica endoteliale automatizzata con stripping della membrana di Descemet)
PKP (cheratoplastica perforante)
Innesto: cornea a tutto spessore (diametro 7,0–8,5 mm)
Caratteristiche: opzione classica. Sfide: suture, gestione dell’astigmatismo, rischio di rigetto a lungo termine. Nel campo della FECD, gradualmente sostituita dal trapianto endoteliale.
DSO (Descemetorhexis Without Endothelial Keratoplasty)
Procedura: rimozione selettiva solo della membrana di Descemet centrale di 4 mm. Nessun innesto necessario.
Indicazioni: casi in cui le cellule endoteliali periferiche residue possono migrare e proliferare verso il centro. Circa il 75% di trasparenza corneale 14).
Collirio inibitore di ROCK: l’uso postoperatorio di ripasudil promuove la trasparenza anche nei casi refrattari 14).
| Indicatore | DMEK | UT-DSAEK | Fonte |
|---|---|---|---|
| BCVA a 12 mesi (differenza logMAR) | −0,06 (DMEK superiore) | — | Sela 2023 meta-analisi3) |
| Tasso di raggiungimento di 20/25 o migliore | 66% | 33% (p=0,02) | Dunker 2020 RCT4) |
| OR di re-bubbling | — | 2,76 (favorevole a DSAEK) | Sela 20233) |
| ECD a 12 mesi | Nessuna differenza | Nessuna differenza | Dunker 20204) |
| Spessore del graft <70 μm | — | Nessuna differenza visiva con DMEK | Sela 20233) |
In una meta-analisi di Sela et al. (2023) su 8 studi (376 occhi), la BCVA a 12 mesi era significativamente migliore con DMEK (−0,06 logMAR)3). Anche lo studio randomizzato multicentrico di Dunker et al. (2020) ha mostrato un tasso più elevato di ≥20/25 con DMEK rispetto a UT-DSAEK (66% vs 33%, p=0,02)4). Tuttavia, con innesti UT-DSAEK di spessore inferiore a 70 μm, la differenza con DMEK si è ridotta3).
Il gruppo dell’Università di Kyoto (Kinoshita 2018) ha sviluppato una terapia che prevede l’iniezione di cellule endoteliali corneali di donatore sano coltivate nella camera anteriore insieme a un inibitore di ROCK (Y-27632)13).
L’inibitore di ROCK agisce promuovendo l’adesione delle cellule endoteliali, inibendo l’apoptosi e stimolando la progressione del ciclo cellulare13).
Nella FECD è frequente la coesistenza di cataratta, pertanto è necessario prestare attenzione alla scelta del momento e del metodo chirurgico.
La DMEK, grazie al suo innesto molto sottile (circa 15 μm), offre un recupero visivo più rapido e minori cambiamenti refrattivi post-operatori. Anche le meta-analisi mostrano una BCVA a 12 mesi superiore per la DMEK3). D’altra parte, la DSAEK è leggermente più facile da maneggiare, ha una curva di apprendimento più breve per il chirurgo ed è ampiamente praticata in Giappone. Esistono segnalazioni che la DSAEK ultra-sottile (<70 μm) ottiene risultati visivi quasi equivalenti alla DMEK3). La scelta dipende dall’esperienza del chirurgo, dall’esperienza della struttura e dalle condizioni corneali del paziente. Entrambe le procedure sono coperte dall’assicurazione in Giappone dal 2016 (DMEK) o dal 2009 (DSAEK).
Le cellule endoteliali corneali normali non subiscono divisione cellulare nella camera anteriore. Quando l’endotelio è difettoso, le cellule adiacenti si allargano e migrano per coprire il difetto, quindi la densità cellulare diminuisce irreversibilmente con l’età. Al di sotto di 400-500 cellule/mm², diventa difficile mantenere la trasparenza corneale.
Nella FECD, le cellule endoteliali degenerate producono e depositano sostanze anomale simili al collagene sulla superficie posteriore della membrana di Descemet, formando guttae. La membrana di Descemet si ispessisce e diventa irregolare, creando un circolo vizioso che compromette ulteriormente la funzione endoteliale.
L’invecchiamento, l’esposizione ai UV e il fumo aumentano tutti lo stress ossidativo e fungono da porta d’ingresso nel circolo vizioso2).
La funzione di pompa dell’endotelio corneale dipende dalla Na⁺/K⁺-ATPasi. Quando le cellule endoteliali sono danneggiate, l’edema si verifica attraverso le seguenti vie.
In caso di aumento della pressione intraoculare (ipertensione oculare) che supera la pressione di rigonfiamento dello stroma corneale, può verificarsi edema epiteliale anche se l’endotelio è relativamente sano, e ciò richiede attenzione.
Poiché il contributo dell’espansione delle ripetizioni TCF4 è relativamente piccolo nei giapponesi8), la chiarificazione dei background genetici e ambientali specifici dei giapponesi è una questione importante per il futuro.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.