Grade 0-1 (ไม่มีถึงเล็กน้อย)
อาการแสดง: guttae 12 จุดหรือน้อยกว่าที่ศูนย์กลาง (Grade 0) หรือมากกว่า 12 จุดที่ไม่รวมกัน (Grade 1)
อาการ: โดยปกติไม่มีอาการ ตรวจพบเป็นจุดดำในกล้องจุลทรรศน์ specular

โรคเสื่อมของเยื่อบุผิวดวงตาชั้นในของฟุคส์ (FECD) เป็นโรคที่ลุกลามซึ่งส่งผลต่อเซลล์เยื่อบุผิวดวงตาชั้นในทั้งสองข้าง ในปี 1910 Ernst Fuchs รายงานผู้ป่วย 13 รายในชื่อ “dystrophia epithelialis corneae” และต่อมาพบว่าเป็นโรคของเยื่อบุผิวชั้นใน จึงได้ชื่อปัจจุบัน 1)
Guttae (guttata) ปรากฏบนพื้นผิวเยื่อบุผิวชั้นในบริเวณกลางกระจกตาและค่อยๆ แพร่กระจายไปยังส่วนรอบนอก เมื่อการทำงานของสิ่งกีดขวางและปั๊ม (Na⁺/K⁺-ATPase) ของเซลล์เยื่อบุผิวลดลง จะเกิดอาการบวมน้ำของสโตรมากระจกตา ตามด้วยอาการบวมน้ำของเยื่อบุผิวและการเกิดตุ่มพอง เยื่อ Descemet หนาขึ้นและไม่สม่ำเสมอ ทำให้กระจกตาสูญเสียความใส
ใน IC3D (การจำแนกโรคกระจกตาเสื่อมระหว่างประเทศ) ฉบับที่ 2 (Weiss 2015) FECD จัดอยู่ในหมวด “โรคกระจกตาเสื่อมชนิดเยื่อบุผิวนอก” 15) แบ่งออกเป็น 2 ชนิดหลักตามอายุที่เริ่มมีอาการ:
| ตัวชี้วัด | ค่า | แหล่งอ้างอิง |
|---|---|---|
| ความถี่ของ guttae กระจกตาในผู้ป่วยก่อนผ่าตัดต้อกระจก | 1.2% | การสำรวจหลายศูนย์ในประเทศ |
| ความชุกในญี่ปุ่น (การศึกษา Kumejima) อายุ ≥40 ปี | 4.1% | Higa 20117) |
| ความชุกในผู้หญิงญี่ปุ่น (อายุ ≥40 ปี) | 5.8% | Higa 20117) |
| ญี่ปุ่น - ความชุกในเพศชาย (อายุ 40 ปีขึ้นไป) | 2.4% | Higa 20117) |
| ไอซ์แลนด์ - การศึกษาดวงตาเรคยาวิก อายุ 55 ปีขึ้นไป | หญิง 11%, ชาย 7% | Zoega 200610) |
| อัตราส่วนเพศ (นานาชาติ) | 2.5:1 ถึง 3.5:1 (หญิงเด่น) | Matthaei 20191) |
| ความถี่ของการขยายซ้ำ TCF4 ในคนญี่ปุ่น | 12 จาก 47 ราย (26%) | Nakano 20158) |
คนญี่ปุ่นซึ่งเป็นเชื้อชาติเอเชีย มีแนวโน้มอุบัติการณ์ของ FECD ต่ำกว่าเมื่อเทียบกับเชื้อชาติผิวขาวและผิวดำ อย่างไรก็ตาม ในญี่ปุ่น คาดว่าจำนวนผู้ป่วยจะเพิ่มขึ้นตามสังคมสูงอายุ คนญี่ปุ่นมีความหนาแน่นของเซลล์เยื่อบุผิวจอประสาทตาสูงกว่าคนผิวขาว จึงเชื่อว่าการเกิดโรคจะช้ากว่า
ในคนญี่ปุ่นซึ่งมักมีมุมแคบ ไม่ใช่เรื่องแปลกที่เซลล์เยื่อบุผิวจะลดลงหลังการตัดม่านตาด้วยเลเซอร์ (LI) ดังนั้นจึงต้องระวังในการตรวจพบ FECD ตั้งแต่เนิ่นๆ
ในการศึกษาประชากรที่ดำเนินการในโอกินาว่า/เกาะคูเมจิมะ (Kumejima Study) พบ corneal guttae ใน 4.1% ของผู้ที่มีอายุ 40 ปีขึ้นไป ในเพศหญิง 5.8% และเพศชาย 2.4% 7) นอกจากนี้ยังมีข้อมูลในประเทศที่แสดงว่า 1.2% ของผู้ป่วยที่ได้รับการตรวจก่อนการผ่าตัดต้อกระจกมีกระจกตาแบบ guttata ชาวญี่ปุ่นถือว่ามีความถี่ต่ำกว่าชาวยุโรป/อเมริกา แต่แนวโน้มเพิ่มขึ้นตามสังคมผู้สูงอายุ
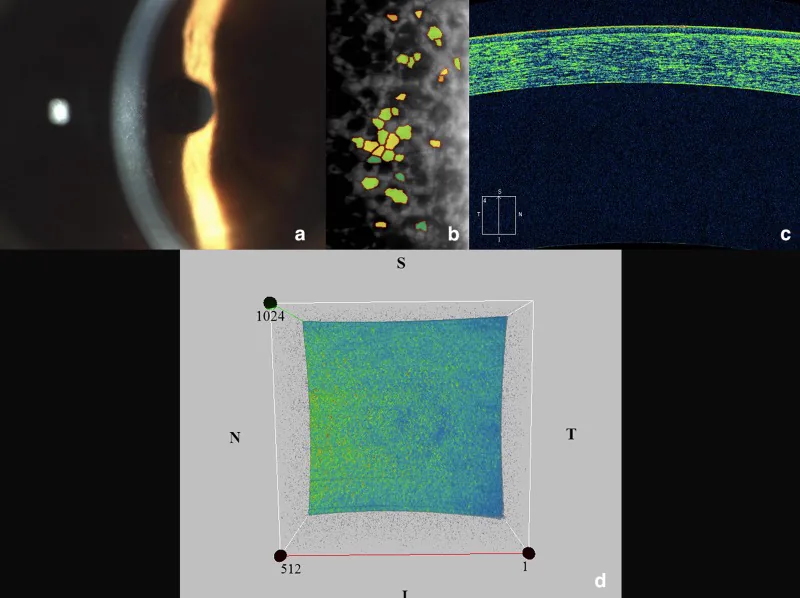
โดยปกติแล้ว ไม่มีอาการในผู้ที่มีอายุต่ำกว่า 50 ปี อาการจะค่อยๆ ดำเนินไปตามความรุนแรงของอาการบวมน้ำ
การตรวจพื้นฐานคือการใช้ slit-lamp ใช้การส่องสว่างโดยตรง การส่องสว่างแบบกระเจิงกลับ และวิธีสะท้อนแบบ specular เพื่อสังเกต
Grade 0-1 (ไม่มีถึงเล็กน้อย)
อาการแสดง: guttae 12 จุดหรือน้อยกว่าที่ศูนย์กลาง (Grade 0) หรือมากกว่า 12 จุดที่ไม่รวมกัน (Grade 1)
อาการ: โดยปกติไม่มีอาการ ตรวจพบเป็นจุดดำในกล้องจุลทรรศน์ specular
ระดับ 2-3 (ปานกลาง)
สิ่งที่พบ: Guttae รวมตัวกันตรงกลาง 1-5 มม. ลักษณะ beaten-metal เล็กน้อย
อาการ: มองเห็นไม่ชัดในตอนเช้า ภาพเยื่อบุผิวยังไม่ชัดเจนเมื่อใช้กล้องส่อง
ระดับ 4 (รุนแรง)
สิ่งที่พบ: Guttae รวมตัวกันกว้าง >5 มม. ตรงกลาง ลักษณะ beaten-metal ร่วมกับเม็ดสี
อาการ: มองเห็นไม่ชัดต่อเนื่องและกลัวแสงตั้งแต่เช้าถึงกลางวัน
ระดับ 4+ บวมน้ำ (รุนแรงมาก)
สิ่งที่พบ: อาการบวมน้ำของสโตรมาและเยื่อบุผิว การเกิดตุ่มน้ำ กระจกตาขุ่นอย่างชัดเจน
อาการ: การมองเห็นลดลงอย่างรุนแรงตลอดวัน ปวดตา น้ำตาไหล คุณภาพชีวิตลดลงอย่างมาก
การจำแนกทางคลินิกนี้ขึ้นอยู่กับการจำแนกที่ปรับปรุงโดย Krachmer และคณะ (1978)5)
รายละเอียดการตรวจด้วย Slit-lamp:
กระจกตาที่แข็งแรงจะคงความใสไว้ได้เนื่องจากเซลล์เอนโดทีเลียมจะสูบน้ำออกไปยังช่องหน้าม่านตาอย่างต่อเนื่อง ใน FECD การทำงานของปั๊มเอนโดทีเลียมลดลง ดังนั้นระหว่างนอนหลับ (เมื่อหลับตา) การระเหยของน้ำก็หยุดลง และกระจกตาจะบวมมากที่สุดในตอนเช้า ทำให้ตามัวอย่างรุนแรง เมื่อลืมตา น้ำจะระเหยจากผิวกระจกตา และอาการบวมจะดีขึ้นบ้างในตอนกลางวัน ทำให้การมองเห็นกลับคืนมา เมื่อโรคดำเนินไป ความผันแปรในแต่ละวันนี้จะหายไป และตามัวจะคงอยู่ตลอดทั้งวัน
FECD ส่วนใหญ่ถ่ายทอดทางพันธุกรรมแบบออโตโซมอลโดมิแนนต์ แต่มีความแปรปรวนในการแทรกซึมและการแสดงออก และมีกรณีที่ประวัติครอบครัวไม่ชัดเจน
ยีนหลักที่ทำให้เกิดโรค:
ในคนญี่ปุ่น ความถี่ของการขยายตัวซ้ำของ TCF4 ต่ำกว่าในตะวันตก ดังนั้นจึงจำเป็นต้องอธิบายพื้นฐานทางพันธุกรรมอื่นๆ8)
FECD ถ่ายทอดทางพันธุกรรมแบบ autosomal dominant เป็นหลัก ตามทฤษฎีแล้ว ความน่าจะเป็นในการถ่ายทอดสู่เด็กคือ 50% อย่างไรก็ตาม มีความแปรปรวนอย่างมากในระยะเวลาเริ่มต้นและความรุนแรง (penetrance ไม่สมบูรณ์) และหลายคนที่ได้รับยีนนี้ใช้ชีวิตทั้งชีวิตโดยมีอาการเพียงเล็กน้อย โดยเฉพาะในคนญี่ปุ่น สัดส่วนของความผิดปกติของยีน TCF4 ซึ่งเป็นสาเหตุที่พบบ่อยที่สุดในตะวันตกนั้นต่ำ 8) แสดงให้เห็นถึงพื้นฐานทางพันธุกรรมที่แตกต่างกัน หากคุณกังวล แนะนำให้ปรึกษาแพทย์ผู้เชี่ยวชาญด้านพันธุศาสตร์
ไม่มีเกณฑ์การวินิจฉัยที่เป็นมาตรฐานในญี่ปุ่น แต่การวินิจฉัยทางคลินิกทำได้โดยการตรวจหลายอย่างร่วมกันดังต่อไปนี้
นี่คือการตรวจที่สำคัญที่สุดสำหรับการวินิจฉัยและติดตาม FECD
| พารามิเตอร์ | ค่าปกติ | เกณฑ์ความผิดปกติ |
|---|---|---|
| ความหนาแน่นของเซลล์เยื่อบุผิวดวงตา (ช่วงทารกแรกเกิด) | 3,500–4,000 เซลล์/ตร.มม. | — |
| ความหนาแน่นของเซลล์เยื่อบุผิวดวงตา (อายุ 20 ปี) | 2,700 เซลล์/ตร.มม. | — |
| ความหนาแน่นของเซลล์เยื่อบุผิวดวงตา (อายุ 70 ปีขึ้นไป) | เฉลี่ย 2,200 เซลล์/ตร.มม. | — |
| ขีดจำกัดในการคงความใส | — | 400–500 เซลล์/ตร.มม. หรือน้อยกว่า |
| ค่า CV (สัมประสิทธิ์ความแปรปรวน) | 0.2–0.3 | ≥ 0.35 |
| อัตราการปรากฏของเซลล์รูปหกเหลี่ยม (hexagonality) | 60-70% | ≤ 50% |
| โรค | จุดที่ใช้แยกโรค |
|---|---|
| โรคกระจกตาเสื่อมชนิดพอลิมอร์ฟัสส่วนหลัง (PPCD) | ถ่ายทอดทางพันธุกรรมแบบ AD, เป็นทั้งสองข้าง, ความขุ่นแบบแถบหรือตุ่มน้ำที่เยื่อเดสเซเมท (Descemet membrane) ยีน: PPCD1 (20p11.2-q11.2), PPCD2 (COL8A2), PPCD3 (ZEB1) |
| โรคกระจกตาเสื่อมชนิดเยื่อบุผนังชั้นในแต่กำเนิด (CHED) | ถ่ายทอดทางพันธุกรรมแบบ AR (การกลายพันธุ์ของ SLC4A11), เริ่มมีอาการตั้งแต่แรกเกิดถึงวัยทารก, มีอาการบวมน้ำและขุ่นของกระจกตาตั้งแต่แรกเกิด |
| โรคกระจกตาพุพองเทียม (PBK) | ความผิดปกติของเยื่อบุผนังชั้นในหลังการผ่าตัดต้อกระจก ไม่มี guttae มีประวัติการผ่าตัด |
| โรคกระจกตาจากกลุ่มอาการเทียมลอก (pseudoexfoliation syndrome) | การสะสมของสาร PEX, ความดันลูกตาสูง, สาร PEX ที่ผิวหน้าของเลนส์ตาเป็นกุญแจสำคัญในการวินิจฉัยแยกโรค |
| กลุ่มอาการ ICE (ม่านตา-กระจกตา-เยื่อบุผนังชั้นใน) | เป็นข้างเดียว, ร่วมกับม่านตาฝ่อ, การยึดเกาะด้านหน้า, และต้อหิน ไม่มี guttae |
| การเปลี่ยนแปลงของเยื่อบุผนังชั้นในในตาที่มีมุมแคบ | บางครั้งอาจมีลักษณะคล้าย guttae ของกระจกตา แยกโรคโดยใช้ความดันลูกตาและลักษณะของมุมห้องหน้า |
กล้องจุลทรรศน์สเปคคูลาร์ (เครื่องถ่ายภาพเซลล์เยื่อบุผนังชั้นในกระจกตาแบบสะท้อนแสง) เป็นอุปกรณ์ที่ถ่ายภาพและวัดเซลล์เยื่อบุผนังชั้นในของกระจกตาชั้นในสุดแบบไม่รุกล้ำ โดยใช้การสะท้อนแสงพิเศษ การตรวจวัดจำนวนเซลล์เยื่อบุผนังชั้นใน (ความหนาแน่นของเซลล์), ความแปรผันของขนาด (ค่า CV), และความสม่ำเสมอของรูปร่าง (เปอร์เซ็นต์ของเซลล์รูปหกเหลี่ยม) ในโรค FECD guttae จะปรากฏเป็นจุดดำ (dark spot) ซึ่งช่วยในการประเมินระยะของโรค การถ่ายภาพใช้เวลาไม่กี่นาทีและไม่เจ็บปวด
เป้าหมายของการรักษาคือการฟื้นฟูความใสของกระจกตาและรักษาการมองเห็น การรักษาตามอาการหรือการผ่าตัดจะถูกเลือกตามระยะของโรค
มีเป้าหมายเพื่อบรรเทาอาการก่อนการผ่าตัด ไม่มีผลต่อการฟื้นฟูจำนวนเซลล์เอนโดทีเลียมหรือชะลอการดำเนินของโรค
DMEK (การปลูกถ่ายเยื่อบุผิวดิสเซเมท)
กราฟต์: เยื่อดิสเซเมท + เยื่อบุผิวเท่านั้น (ความหนาประมาณ 15 ไมครอน)
ลักษณะเด่น: รายงานครั้งแรกโดย Melles ในปี 2006 11) ฟื้นฟูการมองเห็นเร็ว อัตราการปฏิเสธต่ำ ต้องใช้ศัลยแพทย์ที่มีความชำนาญ
การครอบคลุมของประกันในญี่ปุ่น: ตั้งแต่ปี 2016
DSAEK (การปลูกถ่ายเยื่อบุผิวกระจกตาด้วยเครื่องลอกเยื่อดิสเซเมทอัตโนมัติ)
PKP (การปลูกถ่ายกระจกตาทั้งชั้น)
กราฟต์: กระจกตาทั้งชั้น (เส้นผ่านศูนย์กลาง 7.0–8.5 มม.)
ลักษณะ: ทางเลือกแบบดั้งเดิม ความท้าทาย ได้แก่ การเย็บ การจัดการสายตาเอียง และความเสี่ยงต่อการปฏิเสธในระยะยาว ในสาขา FECD กำลังถูกแทนที่ด้วยการปลูกถ่ายเยื่อบุผนังกระจกตาชั้นในอย่างค่อยเป็นค่อยไป
DSO (การลอกเยื่อเดสเซเม็ทโดยไม่ปลูกถ่ายเยื่อบุผนังกระจกตา)
ขั้นตอน: ลอกเฉพาะส่วนกลางของเยื่อเดสเซเม็ทขนาด 4 มม. โดยเลือก ไม่ต้องใช้กราฟต์
ข้อบ่งชี้: กรณีที่เซลล์เยื่อบุผนังกระจกตาส่วนปลายที่เหลือสามารถเคลื่อนย้ายและเพิ่มจำนวนไปยังส่วนกลางได้ ประมาณ 75% กระจกตาใสขึ้น14)
ยาหยอดตายับยั้ง ROCK: การใช้ ripasudil หลังผ่าตัดช่วยส่งเสริมความใสแม้ในกรณีที่ไม่ตอบสนอง14)
| ตัวชี้วัด | DMEK | UT-DSAEK | แหล่งอ้างอิง |
|---|---|---|---|
| BCVA ที่ 12 เดือน (ความแตกต่าง logMAR) | −0.06 (DMEK เหนือกว่า) | — | Sela 2023 การวิเคราะห์อภิมาน3) |
| อัตราการบรรลุ 20/25 หรือดีกว่า | 66% | 33% (p=0.02) | Dunker 2020 RCT4) |
| Odds ratio ของการรีบับเบิล | — | 2.76 (DSAEK เหนือกว่า) | Sela 20233) |
| ECD ที่ 12 เดือน | ไม่แตกต่าง | ไม่แตกต่าง | Dunker 20204) |
| ความหนาของกราฟต์ <70 μm | — | ไม่แตกต่างด้านการมองเห็นกับ DMEK | Sela 20233) |
การวิเคราะห์อภิมานโดย Sela และคณะ (2023) (8 การศึกษา 376 ตา) พบว่า BCVA ที่ 12 เดือนดีขึ้นอย่างมีนัยสำคัญใน DMEK (−0.06 logMAR) 3) การทดลองแบบสุ่มที่มีกลุ่มควบคุมหลายศูนย์โดย Dunker และคณะ (2020) ยังพบว่า DMEK มีอัตราการบรรลุ 20/25 หรือดีกว่าสูงกว่า UT-DSAEK (66% เทียบกับ 33%, p=0.02) 4) อย่างไรก็ตาม UT-DSAEK ที่มีความหนาของกราฟต์ <70 μm ทำให้ความแตกต่างกับ DMEK ลดลง 3)
กลุ่มมหาวิทยาลัยเกียวโต (Kinoshita 2018) ได้พัฒนาการบำบัดโดยการฉีดเซลล์เยื่อบุผิวก้อนกระจกตาจากผู้บริจาคที่มีสุขภาพดีซึ่งเพาะเลี้ยงร่วมกับสารยับยั้ง ROCK (Y-27632) เข้าไปในช่องหน้าม่านตา 13)
สารยับยั้ง ROCK ออกฤทธิ์โดยส่งเสริมการยึดเกาะของเซลล์เยื่อบุผิวก้อน ยับยั้งการตายของเซลล์แบบอะพอพโทซิส และส่งเสริมการดำเนินไปของวัฏจักรเซลล์ 13)
ใน FECD มักมีต้อกระจกร่วมด้วย จึงต้องเลือกเวลาและวิธีการผ่าตัดอย่างระมัดระวัง
DMEK มีกราฟต์ที่บางที่สุด (ประมาณ 15 μm) จึงฟื้นฟูการมองเห็นได้เร็วกว่าและมีการเปลี่ยนแปลงค่าสายตาหลังผ่าตัดน้อยกว่า การวิเคราะห์อภิมานยังแสดงให้เห็นว่า BCVA ที่ 12 เดือนดีกว่าใน DMEK 3) ในทางกลับกัน DSAEK จัดการกราฟต์ได้ง่ายกว่าเล็กน้อยและมีช่วงการเรียนรู้ที่สั้นกว่า และมีการทำอย่างแพร่หลายในประเทศ DSAEK แบบบางพิเศษ (<70 μm) มีรายงานว่าให้ผลการมองเห็นใกล้เคียงกับ DMEK 3) การเลือกขึ้นอยู่กับการประเมินอย่างครอบคลุมถึงประสบการณ์ของศัลยแพทย์ ประสบการณ์ของสถานพยาบาล และสภาพกระจกตาของผู้ป่วย ทั้งสองหัตถการได้รับการคุ้มครองโดยประกันสุขภาพในประเทศตั้งแต่ปี 2016 (DMEK) หรือ 2009 (DSAEK)
เซลล์เอนโดทีเลียมกระจกตาปกติจะไม่แบ่งตัวในช่องหน้าม่านตา เมื่อเอนโดทีเลียมบกพร่อง เซลล์ข้างเคียงจะขยายใหญ่และเคลื่อนที่เพื่อชดเชยส่วนที่ขาด ทำให้ความหนาแน่นของเซลล์ลดลงอย่างถาวรตามอายุ เมื่อต่ำกว่า 400-500 เซลล์/ตร.มม. การรักษาความใสของกระจกตาจะทำได้ยาก
ใน FECD เซลล์เอนโดทีเลียมที่เสื่อมสภาพจะผลิตและสะสมสารคล้ายคอลลาเจนที่ผิดปกติบนผิวด้านหลังของเยื่อหุ้มเดสเซเมท เกิดเป็น guttae เยื่อหุ้มเดสเซเมทหนาขึ้นและไม่สม่ำเสมอ สร้างวงจรอุบาทว์ที่ทำให้การทำงานของเอนโดทีเลียมบกพร่องยิ่งขึ้น
ความชรา การได้รับรังสี UV และการสูบบุหรี่ล้วนเพิ่มความเครียดออกซิเดชัน และเป็นประตูสู่วงจรอุบาทว์ 2)
การทำงานของปั๊มของเอ็นโดทีเลียมกระจกตาขึ้นอยู่กับ Na⁺/K⁺-ATPase เมื่อเซลล์เอ็นโดทีเลียมเสียหาย อาการบวมน้ำจะเกิดขึ้นผ่านทางเดินต่อไปนี้
หากมีความดันลูกตาสูงเกินกว่าความดันพองตัวของสโตรมากระจกตา อาจเกิดอาการบวมน้ำที่เยื่อบุผิวได้แม้ว่าเอ็นโดทีเลียมจะค่อนข้างปกติ และต้องให้ความสนใจกับสิ่งนี้
เนื่องจากผลของการขยายซ้ำ TCF4 ค่อนข้างน้อยในคนญี่ปุ่น8) การอธิบายพื้นฐานทางพันธุกรรมและสิ่งแวดล้อมเฉพาะของคนญี่ปุ่นจึงเป็นประเด็นสำคัญในอนาคต
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Ong Tone S, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: The vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. Br J Ophthalmol. 2023.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet Membrane Endothelial Keratoplasty versus Ultrathin Descemet Stripping Automated Endothelial Keratoplasty: A Multicenter Randomized Controlled Clinical Trial. Ophthalmology. 2020;127(9):1152-1159.
Krachmer JH, Purcell JJ Jr, Young CW, Bucher KD. Corneal endothelial dystrophy. A study of 64 families. Arch Ophthalmol. 1978;96(11):2036-2039.
Gain P, Jullienne R, He Z, et al. Global Survey of Corneal Transplantation and Eye Banking. JAMA Ophthalmol. 2016;134(2):167-173.
Higa A, Sakai H, Sawaguchi S, et al. Prevalence of and risk factors for cornea guttata in a population-based study in a southwestern island of Japan: the Kumejima study. Arch Ophthalmol. 2011;129(3):332-336.
Nakano M, Okumura N, Nakagawa H, et al. Trinucleotide repeat expansion in the TCF4 gene in Fuchs’ endothelial corneal dystrophy in Japanese. Invest Ophthalmol Vis Sci. 2015;56(8):4865-4869.
Wieben ED, Aleff RA, Tosakulwong N, et al. A common trinucleotide repeat expansion within the transcription factor 4 (TCF4) gene predicts Fuchs corneal dystrophy. PLoS One. 2012;7(11):e49083.
Zoega GM, Fujisawa A, Sasaki H, et al. Prevalence and risk factors for cornea guttata in the Reykjavik Eye Study. Ophthalmology. 2006;113(4):565-569.
Melles GR, Ong TS, Ververs B, van der Wees J. Descemet membrane endothelial keratoplasty (DMEK). Cornea. 2006;25(8):987-990.
Price MO, Feng MT, Price FW Jr. Endothelial Keratoplasty Update 2020. Cornea. 2021;40(5):541-547.
Kinoshita S, Koizumi N, Ueno M, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.
Moloney G, Petsoglou C, Ball M, et al. Descemetorhexis Without Grafting for Fuchs Endothelial Dystrophy-Supplementation With Topical Ripasudil. Cornea. 2017;36(6):642-648.
Weiss JS, Møller HU, Aldave AJ, et al. IC3D classification of corneal dystrophies—edition 2. Cornea. 2015;34(2):117-159.
Seitzman GD, Gottsch JD, Stark WJ. Cataract surgery in patients with Fuchs’ corneal dystrophy: expanding recommendations for cataract surgery without simultaneous keratoplasty. Ophthalmology. 2005;112(3):441-446.