การตัดม่านตา ส่วนปลายด้วยเลเซอร์ (laser peripheral iridotomy : LPI ) เป็นหัตถการที่สร้างรูบนม่านตา ส่วนปลายด้วยเลเซอร์ เพื่อสร้างทางให้ aqueous humor ไหลจากช่องหลังตาสู่ช่องหน้าตาโดยตรง ซึ่งจะช่วยแก้ไข pupil block, ขจัดความแตกต่างของความดันระหว่างช่องหน้าและช่องหลังตา และทำให้มุมเปิดกว้างขึ้น 3)
ในปี ค.ศ. 1857 Albrecht von Graefe รายงานการตัดม่านตา ด้วยการผ่าตัดผ่านแผลที่กระจกตา ในทศวรรษ 1970 เลเซอร์อาร์กอนทำให้สามารถตัดม่านตา แบบไม่รุกรานได้ ในทศวรรษ 1980 มีการนำเลเซอร์ Nd:YAG แบบ Q-switch มาใช้ ซึ่งทำงานโดยการทำลายด้วยแสงโดยไม่ขึ้นกับปริมาณเมลานินในม่านตา ทำให้สามารถเจาะทะลุได้อย่างมีประสิทธิภาพในทุกสีของม่านตา ปัจจุบันเลเซอร์ Nd:YAG เป็นมาตรฐานสำหรับการตัดม่านตา
ในการศึกษา Tajimi ในชาวญี่ปุ่นอายุ 40 ปีขึ้นไป รายงานความชุกของ suspected primary angle closure (PACS) อยู่ที่ 0.2%, primary angle closure (PAC) อยู่ที่ 0.5% และ primary angle closure glaucoma (PACG ) อยู่ที่ 0.6% ปัจจัยโน้มนำ ได้แก่ ผู้หญิงสูงอายุ, แกนตา สั้น, และสายตายาว
ปัจจัยที่อาจกระตุ้นให้เกิด acute angle closure attack ได้แก่:
ยาต้านโคลิเนอร์จิก : ยาก่อนส่องกล้องกระเพาะอาหาร, ยานอนหลับ, ยารักษาโรคจิตยาขยายม่านตา : ยาหยอดตาที่มี tropicamide และ phenylephrineยาแก้ซึมเศร้า : ยาแก้ซึมเศร้ากลุ่ม tricyclic, SSRI 11) ยาลดน้ำมูก : ยาแก้หวัดที่ซื้อเองได้ซึ่งมี phenylephrine 11) อื่นๆ : การก้มศีรษะเป็นเวลานาน, การขยายม่านตา ตามธรรมชาติในเวลากลางคืน
ผู้ป่วยที่มีปัจจัยโน้มนำให้มุมตาแคบควรได้รับข้อมูลเกี่ยวกับความเสี่ยงในการใช้ยาเหล่านี้
ข้อบ่งชี้หลัก
โรคต้อหินมุมปิด เฉียบพลันปฐมภูมิ (APAC) : ทำทันทีหลังวินิจฉัย LPI จำเป็นสำหรับตาอีกข้างด้วย หากไม่รักษา 50% จะมีอาการชักที่ตาอีกข้างภายใน 5 ปี
โรคต้อหินมุมปิดปฐมภูมิ (PAC) และโรคต้อหินมุมปิดปฐมภูมิ (PACG ) : ผู้ป่วยทุกรายจำเป็นต้องแก้ไขการอุดตันของรูม่านตา หากพังผืดม่านตา ส่วนปลายน้อยกว่า 50% LPI อาจเพียงพอ
สงสัยโรคต้อหินมุมปิดปฐมภูมิ (PACS) : ในการทดลอง ZAP ความเสี่ยงในการลุกลามเป็น PAC ลดลง 47% ใน 6 ปี และ 69% ใน 14 ปี 2) อย่างไรก็ตาม ไม่แนะนำให้ทำ LPI ป้องกันเป็นประจำ 2) 3)
ข้อบ่งชี้อื่นๆ
ม่านตา บวม (iris bombé) จากการยึดติดของม่านตา ด้านหลังรูม่านตา ทุติยภูมิที่เกี่ยวข้องกับม่านตาอักเสบ
ม่านตา แบบที่ราบสูง (plateau iris)LPI เพื่อกำจัดองค์ประกอบการอุดตันของรูม่านตา อย่างไรก็ตาม หลัง LPI ประมาณ 1 ใน 3 ยังคงมี ITC 7)
กลุ่มอาการกระจายเม็ดสี (pigment dispersion syndrome) : ทำเพื่อแก้ไขการอุดตันของรูม่านตา แบบกลับด้าน แต่หลักฐานประสิทธิภาพยังไม่เพียงพอ
การไหลของ aqueous misdirection (ต้อหิน ร้าย) : LPI สำคัญในการแยกแยะความเป็นไปได้ของการอุดตันของรูม่านตา
ข้อห้าม ได้แก่ ความขุ่นของสื่อ (กระจกตาบวมน้ำ , การอักเสบในช่องหน้าตา), ช่องหน้าตาตื้นมากจนไม่สามารถทำหัตถการได้อย่างปลอดภัย, และผู้ป่วยที่ไม่ให้ความร่วมมือ 3) ในกรณีที่ความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา น้อยกว่า 2000 เซลล์/ตร.มม. ให้พิจารณาการตัดม่านตา ส่วนปลายหรือการสร้างเลนส์ใหม่
Q
ควรทำ LPI เพื่อป้องกันหรือไม่?
A
ไม่แนะนำให้ทำ LPI ป้องกันเป็นประจำสำหรับทุกมุมแคบ การทดลอง ZAP แสดงผลการป้องกันของ LPI ในผู้ที่สงสัยโรคต้อหินมุมปิดปฐมภูมิ (PACS) แต่อัตราการเกิดโรคต่ำ (4-8 ต่อ 1,000 ตาต่อปี) และจำนวนที่ต้องรักษา (NNT) ใน 6 ปีคือ 44 คำแนะนำปัจจุบันคือให้พิจารณา LPI ป้องกันเฉพาะในตาที่มีความเสี่ยงสูง (มุมแคบมาก, ช่องหน้าตาตื้น, แนวโน้มความดันลูกตา สูง)
หยอดพิโลคาร์พีน 1-2% ทุก 15 นาที จำนวน 2-4 ครั้ง เริ่ม 1 ชั่วโมงก่อนทำหัตถการเพื่อทำให้รูม่านตา หด 3) อย่างไรก็ตาม ในกรณีที่ความดันลูกตา สูงมาก (≥40 มิลลิเมตรปรอท) กล้ามเนื้อหูรูดของรูม่านตา อาจเป็นอัมพาตจากการขาดเลือด และอาจไม่ได้ผลในการหดรูม่านตา จากพิโลคาร์พีน ในกรณีนั้น ให้ลดความดันลูกตา ก่อนด้วยยาที่เพิ่มแรงดันออสโมซิส จากนั้นจึงใช้ยาหดรูม่านตา เพื่อป้องกันความดันลูกตา สูงหลังผ่าตัด ให้หยอดอะพราโคลนิดีน 1 ชั่วโมงก่อนและทันทีหลังทำหัตถการ 3) ทำการระงับความรู้สึกเฉพาะที่ด้วยออกซีบูโปรเคน ไฮโดรคลอไรด์ หากมีอาการบวมน้ำที่กระจกตา ให้ปรับปรุงความใสของกระจกตา ด้วยกลีเซอรีน 10% หยอดตา หรือให้ทางระบบ (อะเซตาโซลาไมด์ , แมนนิทอล 1.0-3.0 กรัม/กิโลกรัม ฉีดเข้าหลอดเลือดดำนาน 30-45 นาที) 2) ระวังการใช้แมนนิทอลในผู้ป่วยที่มีการทำงานของไตบกพร่อง
ใส่คอนแทคเลนส์สำหรับผ่าม่านตา (Abraham, Wise, Goldmann three-mirror) 3) เลือกตำแหน่งฉายแสงในจตุภาคบนระหว่าง 11 ถึง 1 นาฬิกา บริเวณม่านตา ที่บาง เช่น ร่องม่านตา 2) หลีกเลี่ยงทิศทาง 12 นาฬิกาเพราะฟองอากาศมักจะรวมตัวกันที่นั่น หลีกเลี่ยงหลอดเลือดม่านตา และเลือกตำแหน่งที่ถูกปิดด้วยเปลือกตาบนอย่างสมบูรณ์ 2)
พารามิเตอร์ เลเซอร์ Nd:YAG เลเซอร์อาร์กอน (ขั้นที่ 1) เลเซอร์อาร์กอน (ขั้นที่ 2) กำลัง 1-6 มิลลิจูล 200-600 มิลลิวัตต์ 800-1,500 มิลลิวัตต์ ขนาดจุด 50-70 ไมโครเมตร 200-500 ไมโครเมตร 50 ไมโครเมตร เวลา — 0.2–0.6 วินาที 0.02 วินาที
จำนวนการยิงเลเซอร์อาร์กอนทั้งหมดควรน้อยกว่า 100 ครั้งเพื่อหลีกเลี่ยงความเสียหายต่อเอ็นโดทีเลียมกระจกตา
วิธีเลเซอร์ Nd:YAG เพียงอย่างเดียว : ยิง 1–3 พัลส์ด้วยพลังงาน 1–6 mJ 2) 4) โฟกัสลำแสงภายในสโตรมาของม่านตา หากเกิน 2 mJ มีความเสี่ยงต่อความเสียหายของแคปซูลเลนส์ 2) ใช้การยิงหลายครั้งพลังงานต่ำ (10–30 ครั้ง) หรือการยิงน้อยครั้งพลังงานสูง (2–3 ครั้ง) 2)
วิธีผสมอาร์กอน + Nd:YAG : แนะนำสำหรับม่านตา สีเข้ม 3) 4) ขั้นที่ 1: ยืดม่านตา ; ขั้นที่ 2: เตรียมการเจาะ (มีผลการจับตัวเป็นลิ่มเพื่อห้ามเลือด); ขั้นที่ 3: ทำให้การเจาะสมบูรณ์ด้วยเลเซอร์ Nd:YAG (2–4 mJ) 3)
การเจาะทะลุเต็มความหนาถือว่าเกิดขึ้นเมื่อเห็นน้ำอารมณ์ที่มีเม็ดสีไหลจากช่องหลังไปยังช่องหน้า 2) หลังการเจาะ รูจะขยายในแนวนอนจนถึงประมาณ 200 ไมโครเมตร การส่องผ่าน (transillumination) ไม่ใช่ตัวบ่งชี้ความโปร่งที่เชื่อถือได้ 2)
วัดความดันลูกตา 1–3 ชั่วโมงหลังหัตถการเพื่อตรวจสอบความดันลูกตา ที่สูงขึ้นชั่วคราว 3) หากจำเป็น ให้ยับยั้งเอนไซม์คาร์บอนิกแอนไฮเดรสหรือยาออสโมติก 3) สั่งยาหยอดตาสเตียรอยด์ คอร์ติโคสเตียรอยด์ 3–4 ครั้งต่อวันเป็นเวลา 4–7 วัน หลังจากหนึ่งสัปดาห์ ประเมินความลึกของช่องหน้าและการเปิดของมุมด้วย OCT ส่วนหน้าของลูกตา
หากความดันลูกตา ยังคงสูง อาจมีการอุดตันเรื้อรังเนื่องจากการยึดติดของม่านตาส่วนปลายด้านหน้า (PAS ) และควรพิจารณาส่งต่อทันทีไปยังสถานพยาบาลที่สามารถทำการผ่าตัดสลายต้อกระจก ได้ หากตาอีกข้างมีความเสี่ยงต่อการปิดมุม ให้พิจารณาการทำเลเซอร์ม่านตา เพื่อป้องกันหรือการผ่าตัดสลายต้อกระจก ตั้งแต่เนิ่นๆ 10) รูม่านตา ขยายแบบอัมพาตอาจคงอยู่หลังการโจมตี
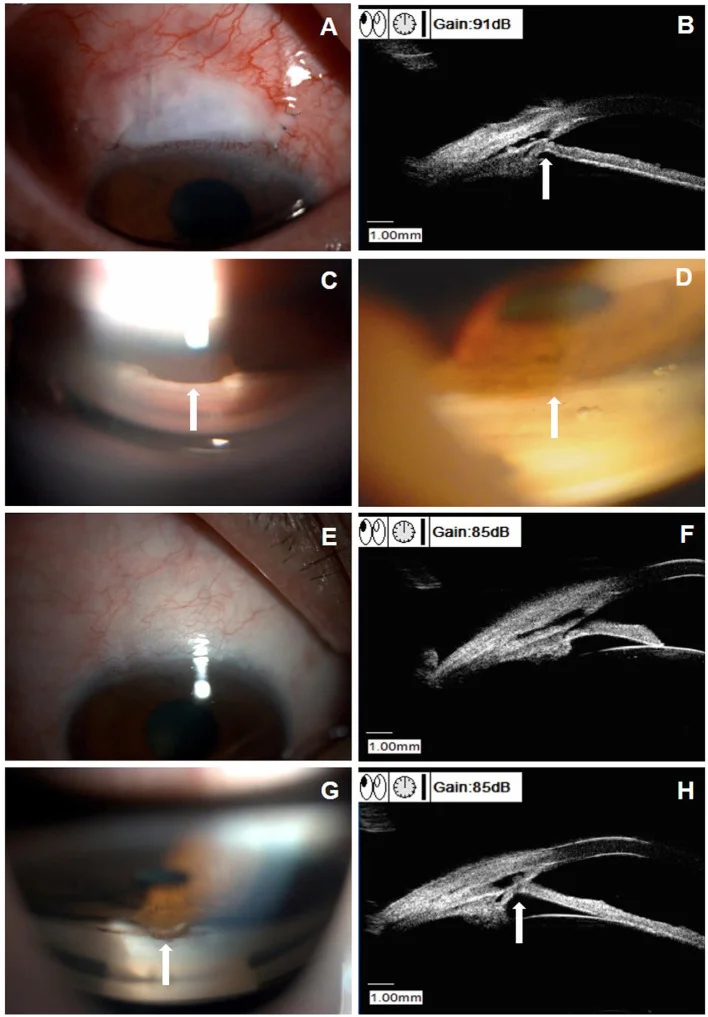
แผงภาพหลายภาพของการยึดติดของม่านตาส่วนปลายด้านหน้า (PAS) ในกล้องจุลทรรศน์หลอดกรีด, UBM และกล้องตรวจมุมตา Babak Esfandiari; Hamed Esfandiari; et al. Complications of
MIGS . Front Med (Lausanne). 2021 Dec 24;8:806734. Figure 3. PM
CI D: PMC8740123. License: CC BY.
แผงหลายภาพแสดง PAS ในกล้องจุลทรรศน์หลอดกรีด (A), UBM (B) และกล้องตรวจมุมตา (C) และการหดตัวของม่านตา หลังการปลดการยึดติดด้วยเลเซอร์ Nd:YAG (D) สอดคล้องกับการปิดม่านตา ส่วนปลายที่เกี่ยวข้องกับ PAS และการปิดซ้ำของม่านตา แบบที่ราบสูงที่กล่าวถึงในหัวข้อ “4. ภาวะแทรกซ้อน”
โรคกระจกตาพุพอง (Bullous keratopathy) เป็นภาวะแทรกซ้อนที่ร้ายแรงที่สุดของ LPI ซึ่งสัมพันธ์กับสภาพของเซลล์บุผนังกระจกตา และพลังงานเลเซอร์ทั้งหมด ควรตรวจเซลล์บุผนังกระจกตา ก่อนการผ่าตัดและหลีกเลี่ยงการฉายแสงมากเกินไป 3) .
ความดันลูกตา สูงชั่วคราว3) มีรายงานการเพิ่มขึ้น ≥8 มิลลิเมตรปรอทจากค่าพื้นฐานใน 6-10% ของกรณี ป้องกันโดยการให้ยาตัวรับ α2 ก่อนและหลังผ่าตัด
เลือดออกในช่องหน้าลูกตา : เลือดออกจากบริเวณที่ตัดม่านตา ส่วนใหญ่ไม่รุนแรง สามารถห้ามเลือดได้โดยการกดเบาๆ ด้วยคอนแทคเลนส์ ไม่จำเป็นต้องหยุดยาต้านการแข็งตัวของเลือดหรือยาต้านเกล็ดเลือด
ม่านตาอักเสบ หลังผ่าตัดสเตียรอยด์ 3) .
โรคกระจกตาพุพอง กระจกตา ที่มีอยู่ก่อน (รวมถึงกระจกตา guttata) ประวัติการเกิดโรคต้อหินมุมปิด เฉียบพลัน และโรคเบาหวาน 3) มีรายงานว่ามากกว่า 40% ของกรณีต้องผ่าตัดต้อกระจก ภายใน 3 ปีหลัง LPI
ความผิดปกติทางการมองเห็น จากแสง (LIVD) : มีรายงานอาการตาพร่า เห็นแสงเป็นวงกลม และเงาเป็นเส้นใน 2-16% ของกรณี 10) ไม่มีความแตกต่างอย่างมีนัยสำคัญในอัตราการเกิดตามตำแหน่ง LPI (ด้านบนหรือด้านขมับ) ส่วนใหญ่เป็นชั่วคราวและหายไปเองภายใน 6 เดือน 10) .
การฉายแสงผิดไปที่จอประสาทตา : ภาวะแทรกซ้อนที่เลเซอร์ไปถึงจอประสาทตา ผ่านม่านตา ซึ่งรวมอยู่ในรายการภาวะแทรกซ้อน 3) ป้องกันโดยการเลือกตำแหน่งฉายแสงและการปรับโฟกัส
อาการบวมของจานประสาทตา ชั่วคราว : อาจเกิดอาการบวมของจานประสาทตา ชั่วคราวเนื่องจากการลดลงอย่างรวดเร็วของความดันลูกตา หลัง LPI สำหรับการรักษาโรคต้อหินมุมปิด เฉียบพลัน 5) มีรายงานกรณีหญิงอายุ 65 ปีที่มีอาการบวมของจานประสาทตา หลังจากความดันลดลงจาก 54 มิลลิเมตรปรอทเป็น 9 มิลลิเมตรปรอท และดีขึ้นภายใน 4 สัปดาห์ 5) กลไกที่สงสัยคือการรั่วจากเส้นเลือดฝอยคอรอยด์ หรือการฟื้นฟูการไหลของแอกซอน 5) .
จอประสาทตา ผิดปกติจากการลดความดัน (ODR)จอประสาทตา กระจาย อาการบวมของจานประสาทตา และอาการบวมของจุดรับภาพหลัง LPI 6) มีรายงานกรณีหญิงอายุ 56 ปีที่การมองเห็น ลดลงเหลือ 20/400 หลัง LPI จากความดันลูกตา 46 มิลลิเมตรปรอท และดีขึ้นเป็น 20/40 หลังจาก 1 เดือน 6) การตรวจฟลูออเรสซีน แองจิโอกราฟี (FA ) และ OCT มีประโยชน์ในการแยกความแตกต่างจากภาวะหลอดเลือดดำจอประสาทตาส่วนกลางอุดตัน 6) .
การหลุดลอกของซิลิอารีบอดี และคอรอยด์ ชนิดเซรุ่ม : มีรายงานกรณีชายอายุ 78 ปีที่มีการหลุดลอกของซิลิอารีบอดี และคอรอยด์ เป็นบริเวณกว้างร่วมกับอาการบวมของจุดรับภาพหลัง LPI ด้วย Nd:YAG 8) ดีขึ้นด้วยสเตียรอยด์ ทั้งระบบและเฉพาะที่ 8) รายงานด้วย Nd:YAG พบน้อยกว่าเลเซอร์อาร์กอน แต่สงสัยว่ามีหลายปัจจัยร่วมกัน รวมถึงการเปลี่ยนแปลงของความดันลูกตา การอักเสบ และภาวะเลือดคั่งในหลอดเลือด 8) .
การอุดตันซ้ำเนื่องจากกลุ่มอาการม่านตา แบน : การปิดมุมอาจเกิดขึ้นเมื่อขยายม่านตา แม้ว่า LPI จะเปิดแล้วก็ตาม 7) มีรายงานกรณีหญิงอายุ 41 ปีที่เกิดการปิดมุมเฉียบพลันหลังขยายม่านตา แม้ LPI จะเปิด และในที่สุดต้องได้รับการผ่าตัด trabeculectomy + ผ่าตัดต้อกระจก 7) การประเมินม่านตา แบนด้วย UBM มีความสำคัญ 7)
Q
LPI เจ็บปวดหรือไม่? ภาวะแทรกซ้อนมีมากหรือไม่?
A
เนื่องจาก LPI ทำภายใต้การหยดยาชา จึงแทบไม่มีอาการปวดรุนแรง อาจรู้สึกกดเบาๆ หรือปวดชั่วขณะขณะฉายแสง ภาวะแทรกซ้อนส่วนใหญ่เป็นความดันลูกตา สูงชั่วคราวหรือม่านตาอักเสบ เล็กน้อยที่หายได้เอง ภาวะแทรกซ้อนที่ร้ายแรงที่สุดคือโรคกระจกตาพุพอง แต่สามารถป้องกันได้โดยการประเมินเซลล์บุผนังกระจกตา ก่อนผ่าตัดและการควบคุมกำลังเลเซอร์ที่เหมาะสม
การทดลองแบบสุ่มและมีกลุ่มควบคุมแบบหลายศูนย์ในผู้ป่วย 419 รายอายุ 50 ปีขึ้นไปที่มี PAC (ความดันลูกตา ≥30 mmHg) หรือ PACG 2) เปรียบเทียบผลลัพธ์ 3 ปีระหว่างกลุ่มผ่าตัดเลนส์แก้วตา (CLE) และกลุ่ม LPI
รายการ กลุ่ม CLE กลุ่ม LPI ความแตกต่างของความดันลูกตา เฉลี่ย ต่ำกว่า 1.18 mmHg ค่าอ้างอิง อัตราการใช้ยา 21% 61% จำนวนการผ่าตัดเพิ่มเติม 1 ราย 24 ราย
กลุ่ม CLE เหนือกว่ากลุ่ม LPI ทั้งในด้านคุณภาพชีวิตและการควบคุมความดันลูกตา 2) การทำ CLE ได้รับการสนับสนุนให้เป็นการรักษาเบื้องต้นสำหรับ PAC/PACG ที่มีความดันสูงในผู้ป่วยอายุ 50 ปีขึ้นไป 2) อย่างไรก็ตาม ควรทราบว่าการถอดเลนส์แก้วตา เป็นเทคนิคที่ยาก 2) การวิเคราะห์ความคุ้มทุนในสหราชอาณาจักรพบว่า CLE มีความคุ้มทุนที่ 3 ปี และประมาณการว่าประหยัดต้นทุนที่ 10 ปี 10) .
การทำ LPI เพียงอย่างเดียวอาจไม่เพียงพอในระยะยาว มีรายงานว่าผู้ป่วยที่ได้รับการทำ LPI หลังการโจมตีเฉียบพลันมากถึง 58% จะพัฒนาเป็นต้อหินมุมปิด เรื้อรัง (CACG) ซึ่งจำเป็นต้องได้รับการแทรกแซงเพิ่มเติม เช่น การรักษาด้วยยา การตัด trabeculectomy หรือการถอดเลนส์แก้วตา 11) การถอดเลนส์แก้วตา ตั้งแต่เนิ่นๆ อาจลดการดำเนินไปสู่ CACG ลดการพึ่งพายา และนำไปสู่ผลลัพธ์ระยะยาวที่ดีขึ้น 11) ช่วงเวลาที่เหมาะสมในการถอดเลนส์แก้วตา คือ 1–3 เดือนหลังการโจมตี 11) .
เป็นการทดลองแบบสุ่มที่มีกลุ่มควบคุมในผู้ป่วย PACS ชาวจีน 889 ราย โดยตาข้างหนึ่งได้รับการทำ LPI และอีกข้างไม่ได้รับการรักษา 2) 3) ที่ 6 ปี การดำเนินไปสู่ PAC คือ 19 ตาในกลุ่ม LPI เทียบกับ 36 ตาในกลุ่มไม่ได้รับการรักษา (4.19 เทียบกับ 7.97 ต่อ 1,000 ตาต่อปี) ความแตกต่างมีนัยสำคัญ 2) 3) ในการติดตามผลเพิ่มเติม 14 ปี กลุ่ม LPI แสดง 33 ตาเทียบกับ 105 ตาในกลุ่มควบคุม ลดความเสี่ยงสัมพัทธ์ 69% 2) อย่างไรก็ตาม อัตราการเกิดโรคต่ำ NNT=44 3) ไม่ทราบว่าสามารถสรุปไปยังเชื้อชาติอื่นที่ไม่ใช่ชาวจีนได้หรือไม่ 2) .
เมื่อการทำ LPI ทำได้ยากในระหว่างการโจมตี APAC ทางเลือกอื่นรวมถึงการทำ iridoplasty รอบนอกด้วยเลเซอร์อาร์กอน (ALPI ) หรือการเจาะห้องหน้า 1) สามารถทำ ALPI ได้แม้มีกระจกตา บวม และสามารถลดความดันลูกตา ได้เร็วเกือบเท่ากับการรักษาทางยา 1) .
Q
วิธีไหนดีกว่า LPI หรือการผ่าตัดต้อกระจก?
A
จากผลการทดลอง EAGLE การถอดเลนส์แก้วตา (การผ่าตัดต้อกระจก ) เหนือกว่า LPI ในการควบคุมความดันลูกตา และความจำเป็นในการรักษาเพิ่มเติมในผู้ป่วยอายุ 50 ปีขึ้นไปที่มีความดันสูงใน primary angle closure หรือ primary angle closure glaucoma อย่างไรก็ตาม ไม่ใช่ทุกกรณีของ angle closure ที่อยู่ในกลุ่มนี้ และการตัดสินใจควรเป็นรายบุคคล โดยพิจารณาจากอายุ ความดันลูกตา ขอบเขตของ peripheral anterior synechiae และการมีต้อกระจก
เมื่อความต้านทานการไหลของ aqueous humor ระหว่างม่านตา และเลนส์แก้วตา เพิ่มขึ้น pupillary block สัมพัทธ์จะเพิ่มขึ้น ความดันในห้องหลังที่เพิ่มขึ้นทำให้ม่านตา โป่งไปข้างหน้า และม่านตา ส่วนรอบปิดกั้นมุม การทำ LPI โดยการสร้างรูในม่านตา ส่วนรอบจะสร้างทางเดินโดยตรงของ aqueous humor จากห้องหลังไปยังห้องหน้า ซึ่งช่วยลดความแตกต่างของความดันระหว่างห้องหน้าและห้องหลัง ม่านตา แบนราบ และมุมเปิดกว้างขึ้น 3) .
ในม่านตา แบบที่ราบสูง (plateau iris) ซิลิอารีบอดี ้จะเคลื่อนไปข้างหน้าและดันโคนม่านตา ไปข้างหน้า ดังนั้นการแก้ไขการอุดตันของรูม่านตา โดย LPI เพียงอย่างเดียวไม่สามารถแก้ไขการปิดมุมได้ 7) หลังจาก LPI ให้ประเมินว่ามีม่านตา แบบที่ราบสูงหรือไม่ และหากจำเป็น ให้เพิ่มเลเซอร์ทำมุม (laser iridoplasty)
มีการรายงานข้อมูลการติดตามผลเพิ่มเติม 14 ปีของการทดลอง ZAP ซึ่งยืนยันว่าผลการป้องกันของ LPI คงอยู่นาน 2) ในกลุ่ม LPI เกิดอาการเฉียบพลันเพียง 1 ตา ในขณะที่กลุ่มควบคุมเกิด 5 ตา 2) ความดันลูกตา สูง ความลึกของช่องหน้าม่านตาตื้น และมุมแคบถูกระบุเป็นตัวบ่งชี้สำหรับการระบุ PACS ที่มีความเสี่ยงสูง 2)
มีรายงานกรณีผู้พักอาศัยในสถานดูแลอายุ 97 ปีที่ตรวจพบมุมปิดระหว่างการเยี่ยมบ้านและได้รับการทำ LPI 9) โดยใช้ slit lamp แบบพกพาและเครื่องวัดความดันลูกตา iCare เพื่อติดตามผลทางไกล ทำให้สามารถควบคุมความดันลูกตา ได้ดีนานถึง 102 วันหลังผ่าตัด 9) รายงานนี้แสดงให้เห็นถึงความเป็นไปได้ของการดูแลตาที่บ้านในสังคมผู้สูงอายุ 9)
นอกเหนือจากการรักษาด้วยยาแบบดั้งเดิม วิธีการลดความดันลูกตา อย่างรวดเร็ว เช่น ALPI , การเจาะช่องหน้าม่านตา (anterior chamber paracentesis) และเลเซอร์ทำรูม่านตา (laser pupilloplasty ) กำลังถูกพิจารณาเป็นแนวทางทางเลือก 1) วิธีการเหล่านี้มีประโยชน์อย่างยิ่งเมื่อการทำ LPI ทำได้ยากเนื่องจากกระจกตา บวม 1) หากสามารถลดความดันลูกตา ได้อย่างรวดเร็ว การรักษาแบบรุนแรง (LPI หรือการถอดเลนส์แก้วตา ) จะสามารถทำได้ในสภาวะที่ปลอดภัยยิ่งขึ้น 1)
Chan PP, Zhang X, Tham CCY. Acute Primary Angle-Closure Attack: Management and Prevention. Asia Pac J Ophthalmol. 2025;14:100223.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. PubliComm; 2025.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
Tsuchiya S, Makino S. Transient Optic Disc Swelling After Laser Iridotomy for the Treatment of Acute Angle Closure Glaucoma. Cureus. 2024;16:e55765.
Ersan S, Zhang C, Sieminski SF. Visually significant ocular decompression retinopathy following laser peripheral iridotomy in a patient with primary acute angle-closure glaucoma. Am J Ophthalmol Case Rep. 2024;36:102215.
Sen S, Das M, Singh Chugh TM. Angle Closure with Patent Laser Peripheral Iridotomy - An Unusual Complication. Int J App Basic Med Res. 2021;11:270-272.
Betsch D, Zaki A, Murphy J, Lakosha H, Gupta RR. Extensive serous ciliochoroidal detachments and macular subretinal and intraretinal fluid following laser peripheral iridotomy . Am J Ophthalmol Case Rep. 2022;26:101483.
Nishimura H, Khemukani RJ, Yokoiwa R, Nakayama S, Shimizu E. Primary Angle Closure Observed During a House Visit: A Case Treated With Laser Iridotomy. Cureus. 2024;16:e66321.
American Academy of Ophthalmology Glaucoma Panel. Primary Angle-Closure Disease Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2025.
Chan PP, Zhang X, Tham CCY, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA ) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Prog Retin Eye Res. 2025;100:100223.