โรคต้อหินมุมปิดปฐมภูมิ (PACG ) เป็นโรคที่ความดันลูกตา สูงขึ้นเนื่องจากการปิดมุมปฐมภูมิซึ่งเกิดจากการเปลี่ยนแปลงของสัณฐานวิทยาของส่วนหน้าของตาจากปัจจัยทางพันธุกรรมหรือความชรา โดยไม่มีปัจจัยอื่น และได้ทำให้เกิดโรคเส้นประสาทตา จากต้อหิน แล้ว1) โรคต้อหินมุมปิดปฐมภูมิ (PAC) เป็นภาวะที่ความดันลูกตา สูงขึ้นเนื่องจากการปิดมุมปฐมภูมิ หรือเกิดการยึดติดของม่านตาส่วนปลายด้านหน้า (PAS ) แต่ยังไม่เกิดโรคเส้นประสาทตา จากต้อหิน 1) ผู้สงสัยโรคต้อหินมุมปิดปฐมภูมิ (PACS) เป็นภาวะที่มีการปิดมุมปฐมภูมิ แต่ไม่มีความดันลูกตา สูงหรือ PAS ที่เป็นโครงสร้าง และยังไม่เกิดโรคเส้นประสาทตา จากต้อหิน 1)
คำว่า โรคมุมปิดปฐมภูมิ (primary angle closure disease: PACD) ถูกใช้เป็นคำครอบคลุมที่รวมสามระยะนี้ รวมถึงโรคต้อหินมุมปิดปฐมภูมิ เฉียบพลัน (acute PACG ) และมุมปิดปฐมภูมิเฉียบพลัน (acute PAC)1) 2) ความสำคัญของการใช้คำครอบคลุม PACD คือการเน้นว่าสภาพพยาธิสภาพของบุคคลเดียวกันนั้นเป็นสเปกตรัมต่อเนื่องที่สามารถเปลี่ยนจาก PACS ไปเป็น PAC และต่อไปเป็น PACG เมื่อระยะดำเนินไป ส่งเสริมการติดตามผลอย่างต่อเนื่องและการแทรกแซงตั้งแต่เนิ่นๆ1) 2)
เกณฑ์การวินิจฉัยโดยกล้องส่องมุมตาดังนี้2) 12) :
ระยะ การสัมผัสระหว่างม่านตา และ trabecular meshwork (ITC) ≥ 180 องศา ความดันลูกตา สูงหรือ PAS โรคเส้นประสาทตา จากต้อหิน PACS มี ไม่มี ไม่มี PAC มี มี ไม่มี PACG มี มี มี
ในการจำแนกประเภทของ Foster ปี 2002 PACS ถูกกำหนดให้เป็น ITC ≥3 ควอดแรนต์ (270 องศา) แต่ปัจจุบัน ตามการจำแนกประเภท Preferred Practice Pattern ของสหรัฐอเมริกาตั้งแต่ปี 2021 ใช้ ITC ≥180 องศาเป็นเกณฑ์2) 12) .
PACG และ PAC มีทั้งชนิดเฉียบพลันและเรื้อรัง ในโรคต้อหินมุมปิดปฐมภูมิ เฉียบพลันหรือภาวะมุมปิดปฐมภูมิเฉียบพลัน ความดันลูกตา มักจะสูงขึ้นอย่างรุนแรงถึง 40-80 มิลลิเมตรปรอท ทำให้เกิดอาการต่างๆ เช่น การมองเห็น ลดลง มองเห็นไม่ชัด เห็นแสงเป็นวงกลม ปวดตา ปวดศีรษะ คลื่นไส้ อาเจียน และปฏิกิริยารูม่านตา ต่อแสงลดลงหรือหายไป1) 2) ในทางกลับกัน โรคต้อหินมุมปิดปฐมภูมิ เรื้อรัง (CACG) ไม่มีประวัติความดันลูกตา สูงเฉียบพลัน และความดันลูกตา สูงระดับปานกลาง (20-30 มิลลิเมตรปรอท) จะดำเนินไปอย่างช้าๆ1) .
การศึกษา Tajimi รายงาน PACS 0.2%, PAC 0.5% และ PACG 0.6% ในผู้ที่มีอายุ 40 ปีขึ้นไป13) ในประชากรญี่ปุ่นอีกกลุ่มหนึ่ง ความชุกของ PACG ในผู้ที่มีอายุมากกว่า 40 ปีอยู่ระหว่าง 0.34% ถึง 0.6%2) ทั่วโลก ประมาณ 0.7% ของผู้ที่มีอายุ 40 ปีขึ้นไปเป็นโรคต้อหินมุมปิด คาดว่ามี 20.2 ล้านคนในปี 2013 โดย 15.5 ล้านคนกระจุกตัวอยู่ในเอเชีย2) 11) ภายในปี 2040 คาดว่าจำนวนผู้ป่วยจะเพิ่มขึ้นประมาณ 50% เป็น 32 ล้านคน และมากกว่า 5 ล้านคนอาจตาบอด2) .
ความแตกต่างทางเชื้อชาติชัดเจน: 2.5-3.8% ในชาวอินูอิต, 3.0% ในไต้หวัน, 1.5% ในกวางโจว ประเทศจีน, 1.2% ในปักกิ่ง, 1.1% ในสิงคโปร์, 1.4% ในมองโกเลีย, 0.9% ในไทย, 0.5-0.87% ในอินเดียใต้, 0.4% ในบังกลาเทศ2) ในชาวยุโรป อัตราต่ำ (0-0.6%)2) ในบางภูมิภาคของเอเชีย PACG มีความถี่เทียบเท่ากับโรคต้อหินมุมเปิดปฐมภูมิ (POAG )2) 11) เมื่อเทียบกับ POAG แล้ว PACG มีอัตราการตาบอดข้างเดียวสูงกว่าเมื่อมาพบครั้งแรก และความเสี่ยงต่อความบกพร่องทางการมองเห็น อย่างรุนแรงทั้งสองข้างสูงกว่าประมาณ 3 เท่า2) .
นอกจากนี้ อายุที่เริ่มเป็น PACG มักสูงกว่า POAG และความเสี่ยงในการเกิดโรคเพิ่มขึ้นอย่างชัดเจนในผู้หญิงอายุมากกว่า 50 ปี2) เมื่อดูอัตราส่วนเพศของ PACG และ POAG พบว่า POAG มีความแตกต่างทางเพศเพียงเล็กน้อย ในขณะที่ PACG พบในผู้หญิงมากกว่าผู้ชาย 2-4 เท่า2) ในผู้หญิง ความลึกของช่องหน้าม่านตาตื้น กว่าและความยาวแกนลูกตา สั้นกว่าผู้ชาย ซึ่งเป็นปัจจัยทางกายวิภาคที่เอื้อต่อการเกิดโรค2) ในญี่ปุ่น คาดว่าจำนวนผู้ป่วย PACG จะเพิ่มขึ้นตามการสูงอายุของประชากร ดังนั้นการเสริมสร้างระบบการดูแลสุขภาพและการเพิ่มการตรวจคัดกรองมุมแคบในการดูแลปฐมภูมิจึงเป็นความท้าทาย2) 11)
Q
หากได้รับการวินิจฉัยว่าเป็น PACS ฉันจำเป็นต้องได้รับการผ่าตัดทันทีหรือไม่?
A
ไม่ใช่ทุกรายของ PACS ที่จำเป็นต้องได้รับการรักษาด้วยเลเซอร์ อย่างสม่ำเสมอ ในการทดลอง Zhongshan Angle Closure Prevention (ZAP) ในประเทศจีน การดำเนินโรคของตา PACS ที่ไม่ได้รับการรักษาไปเป็น PAC หรือภาวะเฉียบพลันอยู่ที่ประมาณ 4% ใน 6 ปี และ 12% ใน 14 ปี และการลดความเสี่ยงสัมพัทธ์ด้วยการผ่าตัดเปิดม่านตา ด้วยเลเซอร์เชิงป้องกันคือ 47% ใน 6 ปี และ 70% ใน 14 ปี แต่ประโยชน์สัมบูรณ์มีน้อย3) การทดลอง ANA-LIS ในสิงคโปร์ก็แสดงแนวโน้มที่คล้ายกัน โดยมีอัตราการดำเนินโรค 9.4% ใน 5 ปี และการลดความเสี่ยง 45% ด้วย LPI 4) จากผลลัพธ์เหล่านี้ แนวทางของสมาคมต้อหิน ยุโรปฉบับที่ 6 ไม่แนะนำให้ทำ LPI เป็นประจำในตา PACS ที่แข็งแรง และควรพิจารณา LPI เฉพาะในกรณีที่มีความเสี่ยงสูง เช่น สายตายาว สูง กรณีที่ต้องขยายม่านตา บ่อย หรือการเข้าถึงการรักษาที่ยาก5) แนวทางปฏิบัติทางคลินิกโรคต้อหิน ฉบับที่ 5 ระบุว่าข้อบ่งชี้ในการผ่าตัดรวมถึงกรณีที่ผลบวกต่อการทดสอบในห้องมืดหรือการทดสอบก้มหน้า กรณีที่ตรวจติดตามเป็นประจำได้ยาก กรณีที่ไม่สามารถมาพบแพทย์ได้ทันทีเมื่อเกิดภาวะเฉียบพลัน กรณีที่มีประวัติครอบครัวเป็นบวก และกรณีที่ต้องขยายม่านตา บ่อย เช่น จอประสาทตาเสื่อมจากเบาหวาน 1)
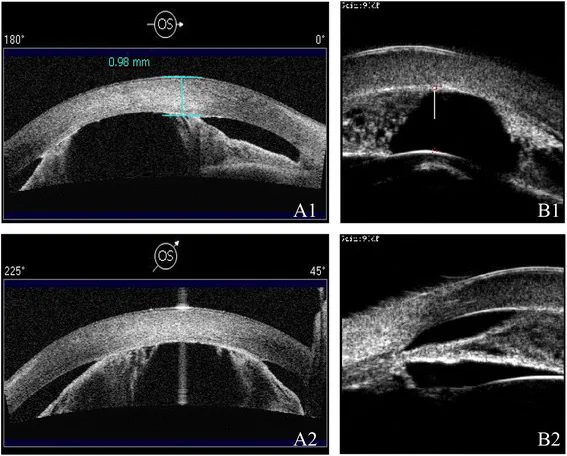
ภาพ OCT และ UBM ส่วนหน้าของตาในโรคต้อหินมุมปิดปฐมภูมิ แสดงช่องหน้าม่านตาตื้น มุมแคบ และการยึดเกาะของม่านตาส่วนปลายด้านหน้า Ni W, et al. A novel histopathologic finding in the Descemet’s membrane of a patient with Peters Anomaly: a case-report and literature review. BMC Ophthalmol. 2015. Figure 2. PM
CI D: PMC4619091. License: CC BY.
ในภาพตัดขวาง
OCT และ
UBM ส่วนหน้า
ช่องหน้าม่านตาตื้น และมุมแคบลงอย่างมาก นอกจากนี้ยังพบสิ่งบ่งชี้ถึงการยึดเกาะของ
ม่านตา ส่วนปลายด้านหน้า ซึ่งเป็นลักษณะทางกายวิภาคของ PACS/
PACG ใน PACS และ PACG เรื้อรัง อาการที่ผู้ป่วยรับรู้ได้มีน้อย และมักผู้ป่วยจะสังเกตเห็นการมองเห็น ลดลงหรือข้อบกพร่องของลานสายตาในระยะท้าย1) 2) ในระยะเรื้อรัง ความดันลูกตา สูงขึ้นอย่างช้าๆ ดังนั้นความเสียหายของเส้นประสาทตา อาจดำเนินไปโดยที่ผู้ป่วยไม่รู้ตัว1) นอกจากนี้ ในภาวะความดันลูกตาสูง ระยะสั้นเนื่องจากการอุดตันของรูม่านตา เล็กน้อย (มุมปิดเป็นระยะ) อาจมีอาการคลุมเครือ เช่น ตาพร่า ในที่มืดหรือรู้สึกหนักศีรษะเล็กน้อยเกิดขึ้นซ้ำๆ และการซักประวัติเพื่อค้นหาอาการเหล่านี้เป็นสิ่งสำคัญ2)
ในทางกลับกัน อาการในภาวะเฉียบพลันจะรุนแรงมาก ได้แก่ การมองเห็น ลดลง ตาพร่า มองเห็นแสงเป็นวงสีรุ้ง (halo) รอบดวงไฟ ปวดตา อย่างรุนแรงร่วมกับปวดศีรษะข้างเดียวกัน และอาการทางระบบประสาทเวกัส เช่น คลื่นไส้ อาเจียน 1) 2) การมองเห็น แสงเป็นวงสีรุ้งเกิดจากความผิดปกติของการหักเหแสงเนื่องจากกระจกตา บวม ผู้ป่วยจะเห็นวงสีรอบหลอดไฟหรือไฟถนน อาการปวดศีรษะและคลื่นไส้อาจเด่นชัด ทำให้ผู้ป่วยถูกส่งต่อไปยังอายุรกรรมระบบประสาทหรือระบบทางเดินอาหาร ดังนั้น ผู้ป่วยทุกรายที่มีอาการปวดศีรษะรุนแรงโดยไม่ทราบสาเหตุร่วมกับอาการทางตาควรได้รับการประเมินทางจักษุวิทยา 2) 7) นอกจากนี้ยังมีภาวะเฉียบพลันแบบกึ่งเฉียบพลัน (subacute attack) ซึ่งความดันลูกตา สูงคงอยู่โดยไม่มีอาการปวดชัดเจน และการทำลายเส้นประสาทตา ดำเนินไป ดังนั้นจึงไม่ควรละเลยการประเมินจอตาและมุมของช่องหน้าม่านตา 1) 2)
อาการแสดงในภาวะเฉียบพลัน
ความดันลูกตา 1) 2)
กระจกตา
เยื่อบุตา เยื่อบุตา อย่างรุนแรง
ช่องหน้าม่านตา : ตื้นตรงกลาง ตื้นมากบริเวณรอบนอก
รูม่านตา
มุมของช่องหน้าม่านตา : อุดตันเป็นบริเวณกว้างเนื่องจากม่านตา สัมผัสกับ trabecular meshwork
เลนส์แก้วตา ต้อหิน (glaukomflecken, เนื้อตายขาดเลือดใต้แคปซูลด้านหน้า) เป็นอาการแสดงที่บ่งชี้ถึงภาวะเฉียบพลันที่เคยเกิดขึ้น 2)
อาการแสดงของ PACG เรื้อรัง
ความดันลูกตา
ส่วนหน้าของลูกตา : ช่องหน้าม่านตาตื้น แกนลูกตาสั้น เลนส์แก้วตา หนาและอยู่ด้านหน้า
มุมของช่องหน้าม่านตา : การอุดตันแบบอินทรีย์จาก PAS และการอุดตันเชิงหน้าที่ (appositional closure) ปนกัน
เส้นประสาทตา จานประสาทตา จากต้อหิน ขอบจานประสาทตา บางลง
ลานสายตา : ความบกพร่องของลานสายตา ที่ดำเนินไปคล้ายกับโรคต้อหินมุมเปิดปฐมภูมิ
อาการ : มักไม่มีอาการ เฉพาะในรายที่ลุกลามแล้วผู้ป่วยจะสังเกตเห็นความผิดปกติของการมองเห็น หรือลานสายตา
ลักษณะของม่านตาแบบที่ราบสูง
ช่องหน้าม่านตา : ความลึกส่วนกลางเกือบปกติ
ม่านตา ส่วนกลาง
โคนม่านตา : งอไปด้านหลังเป็นมุมแหลมคล้ายสี่เหลี่ยมคางหมู มุมรอบนอกแคบมาก
กonioสโคปแบบกด : เครื่องหมาย double hump (ม่านตา ถูกกดเป็นสองยอด)
UBM ซิลิอารีบอดี การหายไปของซิลิอารีซัลคัส การหนาตัวของโคนม่านตา 14)
การวินิจฉัยที่แน่นอน : หากหลังทำ LPI แล้ว การขยายม่านตา ยังทำให้เกิดการปิดมุมและความดันลูกตา สูงขึ้น
Q
อาการที่เกิดขึ้นในภาวะต้อหินเฉียบพลันมีอะไรบ้าง?
A
ในภาวะต้อหินมุมปิดปฐมภูมิ เฉียบพลัน ความดันลูกตา จะสูงขึ้นอย่างรวดเร็วถึง 40–80 มิลลิเมตรปรอทภายในระยะเวลาสั้น ทำให้เกิดอาการปวดตา อย่างรุนแรงและปวดศีรษะข้างเดียวกัน การมองเห็น ลดลง ตาพร่า มองเห็นแสงเป็นวงสีรุ้งรอบดวงไฟ (halo) คลื่นไส้และอาเจียน1) 2) ตาแดง กระจกตา ขุ่น และม่านตา ขยายปานกลางที่ตรึงอยู่เป็นลักษณะทั่วไป1) 2) อาการทางระบบมักเด่นชัดกว่าและอาจถูกวินิจฉัยผิดว่าเป็นโรคทางเดินอาหารหรือไมเกรน 2) 7) หากปล่อยไว้นานเกินสองสามชั่วโมง อาจทำให้เกิดความเสียหายต่อเส้นประสาทตา อย่างถาวร ดังนั้นเมื่อสงสัยควรรีบไปพบจักษุแพทย์ทันที2) 7) .
PACG เกิดจากปัจจัยทางพันธุกรรมและกายวิภาคร่วมกับการเปลี่ยนแปลงตามอายุ1) 2) ด้านล่างคือปัจจัยเสี่ยงหลัก
หมวดหมู่ ปัจจัย สรุป ค่าสายตา สายตายาว ช่องหน้าตาแคบร่วมกับแกนตา สั้น 1) 2) กายวิภาค ความยาวแกนตา สั้น ภาวะตาจิ๋ว (nanophthalmos) ที่มีความยาวแกน <20 มม. มีความเสี่ยงสูงมาก 2) กายวิภาค ช่องหน้าตาแคบ ความลึกช่องหน้าตาส่วนกลาง <2.0–2.2 มม. มีความเสี่ยงสูง 2) กายวิภาค ความหนาเลนส์และตำแหน่งด้านหน้า เพิ่มขึ้นตามอายุและส่งเสริมการอุดตันของรูม่านตา 1) 2) 10) กายวิภาค เส้นผ่านศูนย์กลางกระจกตา เล็ก เส้นผ่านศูนย์กลางแนวนอน <11 มม. เพิ่มความเสี่ยง 2) อายุ ≥50 ปี ความชุกเพิ่มขึ้นตามอายุ1) 2) เพศ หญิง พบบ่อยในเพศหญิง1) 2) เชื้อชาติ ชาวเอเชีย / อินูอิต สูงกว่าชาวยุโรปหลายเท่าถึงหลายสิบเท่า ขึ้นอยู่กับภูมิภาค2) 11) ประวัติครอบครัว มีประวัติครอบครัวเป็น PACD ในญาติสายตรง ปัจจัยทางพันธุกรรม2) ยาที่กระตุ้น ยาต้านโคลิเนอร์จิก, ยาขยายรูม่านตา , ยากระตุ้นซิมพาเทติก ยาก่อนส่องกล้องกระเพาะอาหาร, ยานอนหลับ, ยารักษาโรคจิต, ยาแก้หวัด, ยาต้านเศร้ากลุ่มไตรไซคลิก, SSRI, สเปรย์พ่นจมูกสำหรับโรคจมูกอักเสบ, ยาสูดพ่นบางชนิด เป็นต้น2) 7)
โรคต้อหินมุมปิดปฐมภูมิ และโรคมุมปิดปฐมภูมิมักเกิดจากหลายกลไกร่วมกัน ไม่ใช่กลไกเดียว 1) 2) 10) .
การอุดตันของรูม่านตา แบบสัมพัทธ์ (relative pupillary block) : พื้นผิวด้านหลังของม่านตา และพื้นผิวด้านหน้าของเลนส์ตาขัดขวางการไหลของอารมณ์ขันจากช่องหลังไปยังช่องหน้า ทำให้ความดันในช่องหลังเพิ่มขึ้น ส่งผลให้ม่านตา โป่งไปข้างหน้าและปิดทับ trabecular meshwork เป็นกลไกที่พบบ่อยที่สุดของ PACD 1) 2) ม่านตา แบบที่ราบสูง (plateau iris)ซิลิอารีบอดี ้ดันโคนม่านตา ไปข้างหน้า ทำให้ปิดมุมโดยตรงเมื่อม่านตา ขยาย 1) 14) ปัจจัยจากเลนส์ตา : ความหนาของเลนส์ตาเพิ่มขึ้นตามอายุ การเลื่อนของเลนส์ตาไปข้างหน้า พบเด่นชัดในกรณีต้อกระจก ที่ลุกลาม 1) 10) ปัจจัยหลังเลนส์ตา : ความผิดปกติของรูปร่างซิลิอารีบอดี ้ คอรอยด์ และวุ้นตา ทำให้กะบังม่านตา -เลนส์ตาเคลื่อนไปข้างหน้า 1)
ปัจจัยในชีวิตประจำวันที่กระตุ้นให้เกิดอาการเฉียบพลัน ได้แก่ การอ่านหนังสือในที่มืด ดูหนัง การก้มตัวเป็นเวลานาน (งานสวน การผ่าตัด ขับรถทางไกล) การขยายม่านตา ตามธรรมชาติในเวลากลางคืน การรับประทาน/สูดดม/พ่นยาต้านโคลิเนอร์จิก ผลของการตรวจขยายม่านตา และความเครียดรุนแรง 2) 7) โดยเฉพาะอย่างยิ่งการให้ยาก่อนส่องกล้องกระเพาะอาหารในหญิงสูงอายุ ยาจิตเวช ยารักษาโรคพาร์กินสัน และยาสูดพ่นต้านโคลิเนอร์จิกสำหรับโรคหอบหืด/COPD มักถูกมองข้าม การร่วมมือกับแพทย์ผู้สั่งยาจึงสำคัญ 2) 7) ผู้ป่วยที่มีปัจจัยเสี่ยงต่อ PAC ควรได้รับคำแนะนำให้ปรึกษาจักษุแพทย์ก่อนใช้ยารักษาไข้หวัด ยาแก้คัดจมูก ยาแก้เมารถ และยาแก้แพ้ที่ซื้อได้เอง 2) นอกจากนี้ หากผู้ป่วยสายตายาว อายุมากกว่า 50 ปีเลื่อนการผ่าตัดต้อกระจก ความเสี่ยงต่ออาการเฉียบพลันจะเพิ่มขึ้นตามความหนาของเลนส์ตาที่เพิ่มขึ้นตามอายุ ดังนั้นการพิจารณาผ่าตัดต้อกระจก จึงอาจเป็นการแทรกแซงเชิงป้องกัน 6) 10) .
การตรวจ Gonioscopy เป็นการตรวจที่สำคัญที่สุดในการวินิจฉัยโรคมุมปิดปฐมภูมิ และเป็นมาตรฐานทองคำ 1) 2) 5) หลังจากหยดยาชา ขั้นแรกให้ทำการตรวจ gonioscopy แบบสถิตในท่าปกติโดยไม่กด ใช้ลำแสงกรีดสั้นและบาง ระวังไม่ให้ม่านตา หดตัวเนื่องจากลำแสง ประเมินโครงสร้างทางกายวิภาคของพื้นมุม (เส้น Schwalbe, trabecular meshwork, scleral spur, ciliary band) และ PAS ขนาดเล็ก รวมถึงการสะสมของเม็ดสีที่มุม 2) จากนั้นทำการตรวจ gonioscopy แบบไดนามิก/กดเพื่อแยกความแตกต่างระหว่างการอุดตันเชิงหน้าที่และการอุดตันเชิงโครงสร้าง (PAS ) ตามการจำแนกของ Shaffer-Kanski ระดับ 2 หรือน้อยกว่า (มุม 20 องศาหรือน้อยกว่า) บ่งชี้ถึงความเป็นไปได้ของการปิดมุม ระดับ 1 หรือน้อยกว่าบ่งชี้ถึงความเสี่ยงสูงต่อการปิดมุม
เป็นวิธีการตรวจคัดกรองอย่างง่ายที่ทำได้โดยใช้กล้องจุลทรรศน์ชีวภาพเพียงอย่างเดียว โดยฉายแสงกรีดที่ขอบกระจกตา ด้านขมับด้วยมุม 60 องศา และประเมินจากอัตราส่วนของความลึกของช่องหน้าม่านตา ส่วนปลายต่อความหนาของกระจกตา เมื่อความลึกน้อยกว่าหนึ่งในสี่ของความหนากระจกตา (เกรด 1–2) มีความเป็นไปได้สูงที่จะเกิดการอุดตันของมุมตา และต้องทำการตรวจ gonioscopy เพิ่มเติมเสมอ 2)
การตรวจ ลักษณะเฉพาะ บทบาทใน PACD OCT ส่วนหน้าตาไม่สัมผัส รวดเร็ว ถ่ายภาพทั้งสี่จตุภาคพร้อมกัน ประเมินเชิงปริมาณ AO D500, พื้นที่ร่องมุม, ดัชนี ITC 2) การวัดปริมาณการอุดตันของมุมตาอย่างเป็นกลาง เปรียบเทียบตามเวลา ประเมินแบบพลวัตในที่มืด/สว่าง กล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ (UBM )แบบสัมผัส ความลึกทะลุเนื้อเยื่อสูง สามารถมองเห็นจนถึงเลนส์ปรับตา 2) 14) การวินิจฉัยม่านตา แบบที่ราบสูง (การเคลื่อนของเลนส์ปรับตาไปข้างหน้า การหายไปของร่องเลนส์ปรับตา) การแยกโรคต้อหินชนิดร้าย กล้องมุมตาแบบรอบวง ถ่ายภาพ 360 องศาพร้อมกันด้วยกระจกหลายบาน 16 บาน การคัดกรองและติดตามข้อมูลมุมช่องหน้าม่านตา การวัดความยาวแกน ความยาวแกน <20 มม. บ่งชี้ภาวะตาลูกเล็ก (nanophthalmos) เส้นผ่านศูนย์กลางกระจกตา แนวนอน <11 มม. บ่งชี้ภาวะตาลูกเล็ก ส่วนหน้าสัมพัทธ์ 2) การระบุตาที่มีความเสี่ยงสูง การวางแผนการผ่าตัด การตรวจเซลล์เยื่อบุผิวดวงตา กล้องจุลทรรศน์สเปกคิวลาร์ ประเมินการลดลงของเซลล์เยื่อบุผิวดวงตาในตาที่เกิดอาการ ตัดสินความปลอดภัยของ LPI
OCT ส่วนหน้าสามารถประเมินเชิงปริมาณได้อย่างรวดเร็วและไม่ต้องสัมผัส และยังใช้ทำนายการดำเนินโรคตามยาวได้อีกด้วย การวิเคราะห์ STAR ใน CASIA2 สามารถวิเคราะห์ AO D500 ได้โดยอัตโนมัติ 360 องศา มีประโยชน์ในการคัดกรองมุมแคบ 2) อย่างไรก็ตาม เนื่องจากยากต่อการแยกแยะข้อมูลสีหรือการอุดตันเชิงโครงสร้าง จึงไม่ใช่การทดแทนการตรวจ gonioscopy แต่เป็นส่วนเสริม 2) 5) UBM ต้องใช้เวลาและสัมผัส แต่เหนือกว่า OCT ส่วนหน้าในการวิเคราะห์ซิลิอารีบอดี และผิวด้านหลังของม่านตา และจำเป็นอย่างยิ่งในการวินิจฉัยม่านตา แบบราบ 2) 14)
การทดสอบกระตุ้น เช่น การทดสอบในห้องมืด การทดสอบก้มหน้า และการทดสอบขยายรูม่านตา มีขีดจำกัดในการตรวจพบ การศึกษา ZAP รายงานว่าการทดสอบในห้องมืดร่วมกับการก้มหน้าไม่สามารถแยกกลุ่มเสี่ยงสูงต่อการดำเนินโรคได้ 3) ดังนั้น การวินิจฉัยจึงทำโดยการประเมินผลการตรวจทางคลินิก ผลการตรวจ gonioscopy และผลการตรวจภาพรวมกัน
ควรคำนึงถึงการวินิจฉัยแยกโรคต่อไปนี้เสมอ 1) 2) :
มุมปิดทุติยภูมิ: ต้อกระจก บวม, เลนส์เคลื่อนบางส่วน, ม่านตาติด หลังเนื่องจากม่านตาอักเสบ , โรค Vogt-Koyanagi-Harada, เนื้องอกในลูกตา, เลือดออกในคอรอยด์ , ยากลุ่มซัลโฟนาไมด์ เช่น โทพิราเมต 2)
ต้อหินชนิดร้าย (ความผิดปกติของการไหลของอารมณ์ขันน้ำ)ต้อหินจากเส้นเลือดใหม่ , ต้อหิน ชนิดผลัดเซลล์ 1) กลุ่มอาการไอริสคอร์เนียลเอนโดทีเลียล (ICE)
การโป่งของคอรอยด์ ด้านหน้าที่สัมพันธ์กับจอประสาทตา อักเสบชนิดเซรุ่มส่วนกลางหรือเยื่อบุตาอักเสบ ส่วนหลัง
ใน PACD ซึ่งโดยหลักการแล้วเป็นทั้งสองข้าง หากตาอีกข้างมีช่องหน้าม่านตา ลึกและมุมกว้าง ให้สงสัยสาเหตุทุติยภูมิอย่างมาก 2) 7) โดยเฉพาะในกรณีเฉียบพลันข้างเดียวที่มีประวัติเลนส์เคลื่อนบางส่วนหรือการบาดเจ็บ ให้สงสัยเลนส์เคลื่อนจากบาดเจ็บ ในกรณีเฉียบพลันสองข้างในผู้ป่วยอายุน้อย ให้สงสัยสาเหตุจากยา เช่น โทพิราเมต 2) ในต้อหินจากเส้นเลือดใหม่ ให้ตรวจหาหลอดเลือดใหม่ที่ม่านตา และประวัติโรคส่วนหลัง (จอประสาทตา เบาหวาน, หลอดเลือดดำจอประสาทตาส่วนกลางอุดตัน ) 1)
ในการวินิจฉัย PACG จำเป็นต้องมีหลักฐานของโรคเส้นประสาทตา จากต้อหิน 1) 2) ในระยะเฉียบพลัน การตรวจอวัยวะภายในตาอย่างละเอียดทำได้ยากเนื่องจากกระจกตา บวม แต่การใช้ OCT จอประสาทตา และเส้นประสาทตา แทนการตรวจด้วยกล้องตรวจตาทางอ้อมหรือ OCT ส่วนหน้า สามารถประเมินหัวประสาทตา ชั้นใยประสาทจอประสาทตา (RNFL ) และกลุ่มเซลล์ปมประสาทจอประสาทตา บริเวณจุดรับภาพ (GCC) โดยไม่ต้องขยายม่านตา 2) ในระหว่างการกำเริบ RNFL จะหนาขึ้นชั่วคราวเนื่องจากแอกซอนบวม หลังจากนั้นหนึ่งเดือนจะกลับสู่ค่าปกติ และหลังจากสามเดือนจะบางลง ดังนั้นจึงจำเป็นต้องประเมินตามเวลา 2) การตรวจลานสายตา จะทำหลังจากอาการกำเริบสงบลง โดยใช้ Humphrey 24-2 SITA หรือการทดสอบลานสายตาคงที่อัตโนมัติเชิงปริมาณที่เทียบเท่า และติดตามการดำเนินโรคเช่นเดียวกับ POAG 1) 5)
Q
จะแยกการใช้ OCT ส่วนหน้าและกล้องจุลทรรศน์อัลตราซาวนด์ (UBM) อย่างไร?
A
OCT ส่วนหน้าสามารถประเมินมุมช่องหน้าตาในเชิงปริมาณ 360 องศาได้ในเวลาอันสั้นโดยไม่ต้องสัมผัส เหมาะสำหรับการคัดกรองผู้ป่วยนอกและการเปรียบเทียบตามเวลา ในการวิเคราะห์ STAR ของ CASIA2 จะวิเคราะห์ AO D500 โดยอัตโนมัติจากภาพตัดขวาง 16 ทิศทาง และสามารถแสดงพื้นที่ ITC เป็นแผนที่สี 2) ในทางกลับกัน UBM ต้องใช้เวลาและเป็นแบบสัมผัส แต่เนื่องจากใช้อัลตราซาวนด์ จึงสามารถมองเห็นซิลิอารีบอดี และพื้นผิวด้านหลังของม่านตา ซึ่งจำเป็นสำหรับการวินิจฉัยม่านตา แบบที่ราบสูง ซึ่งมีลักษณะเฉพาะคือการเคลื่อนของซิลิอารีบอดี ไปข้างหน้าและการหายไปของร่องซิลิอารี 2) 14) UBM ยังเป็นตัวเลือกแรกเมื่อสงสัยว่าต้อหินชนิดร้าย เนื้องอกซิลิอารีบอดี หรือรอยโรคอินทรีย์หลังเลนส์ ในทางปฏิบัติทางคลินิก OCT ส่วนหน้าใช้สำหรับการคัดกรองและการประเมินตามเวลา ในขณะที่ UBM ใช้สำหรับการประเมินซิลิอารีบอดี การยืนยันม่านตา แบบที่ราบสูง และการวินิจฉัยแยกโรค 2) 5)
เป้าหมายการรักษาคือการแก้ไขการอุดตันของมุมตา การควบคุมความดันลูกตา ในระยะยาว และการป้องกันความเสียหายของเส้นประสาทตา 1) 2) 5) กลยุทธ์การรักษาแตกต่างกันไปตามระยะ (PACS/PAC/PACG ) และชนิดเฉียบพลันหรือเรื้อรัง
PACS ส่วนใหญ่ไม่ดำเนินไปสู่ PAC หรือ PACG แต่มีสัดส่วนหนึ่งที่ดำเนินไป ดังนั้นจึงแนะนำให้จัดการตามความเสี่ยง 1) 2) 3)
ความเสี่ยง การจัดการที่แนะนำ ความเสี่ยงต่ำ (ไม่ใช่ผู้หญิงสูงอายุ ไม่มีประวัติครอบครัว การเข้าถึงบริการสุขภาพดี) สังเกตอาการ 2) 3) 5) ความเสี่ยงปานกลางถึงสูง (สายตายาว มาก ประวัติครอบครัว PACG จำเป็นต้องขยายม่านตา บ่อย เข้าถึงบริการสุขภาพยาก ใช้ยาต้านโคลิเนอร์จิกเป็นประจำ) พิจารณา LPI 1) 2) 5) กรณีที่มีต้อกระจก ร่วม การถอดเลนส์ก็เป็นทางเลือกหนึ่ง 1) 6)
ในกรณีที่มีความเสี่ยง ยาที่ซื้อได้โดยไม่ต้องมีใบสั่งแพทย์ซึ่งมีฤทธิ์ต้านโคลิเนอร์จิก เช่น ยารักษาโรคจมูกอักเสบ ยานอนหลับ และยาแก้เมารถ อาจกระตุ้นให้เกิดอาการเฉียบพลันได้ ดังนั้น การให้ความรู้แก่ผู้ป่วยและคำแนะนำให้ไปพบแพทย์ฉุกเฉินเมื่อมีอาการจึงเป็นสิ่งสำคัญ2) 7)
แนวทางปฏิบัติทางคลินิกสำหรับโรคต้อหิน ฉบับที่ 5 แนะนำให้แก้ไข pupillary block โดยการทำเลเซอร์ตัดม่านตา (laser iridotomy) หรือการผ่าตัดเลนส์แก้วตา เป็นทางเลือกแรก (ระดับคำแนะนำ 1A)1) เนื่องจากกรณีส่วนใหญ่เป็นทั้งสองตา หากพบ PACG หรือ PAC ในตาข้างเดียว ควรทำ LPI เชิงป้องกัน (1A) หรือการผ่าตัดเลนส์แก้วตา (1A) สำหรับมุมแคบของตาอีกข้างหนึ่ง1)
เลเซอร์ตัดม่านตา (LPI ) : ทำโดยใช้ Nd:YAG เพียงอย่างเดียว หรือใช้ร่วมกับเลเซอร์อาร์กอน + Nd:YAG การฉายแสงอาร์กอนเพียงอย่างเดียวไม่แนะนำเนื่องจากมีความเสี่ยงสูงต่อความเสียหายของเอ็นโดทีเลียม1) ภาวะแทรกซ้อน ได้แก่ ความดันลูกตา สูงชั่วคราว เลือดออกในช่องหน้าลูกตา ต้อกระจก เฉพาะที่ ความเสียหายของเอ็นโดทีเลียมกระจกตา โรคกระจกตาพุพอง ทุติยภูมิ และอาการทางสายตา เช่น แสงจ้าและรัศมี2) การผ่าตัดเลนส์แก้วตา (การสลายเลนส์ด้วยคลื่นเสียงความถี่สูง + การใส่เลนส์แก้วตาเทียม ) : แก้ไข pupillary block อย่างถาวร เพิ่มความลึกของช่องหน้าลูกตา และเปิดมุม1) 10) ในการทดลอง EAGLE ได้เปรียบเทียบการผ่าตัดเลนส์แก้วตา ใสในระยะแรกกับ LPI ในผู้ป่วยอายุ ≥50 ปีที่มี PAC แบบมีอาการ (IOP ≥30 mmHg) หรือ PACG และหลังจาก 3 ปี กลุ่มผ่าตัดเลนส์แก้วตา แสดงความเหนือกว่าในด้านคุณภาพชีวิต (EQ-5D) และการควบคุม IOP โดยมีโอกาสรักษาการควบคุม IOP โดยไม่ต้องใช้ยาหยอดตาสูงกว่าประมาณ 10 เท่า6) การวิเคราะห์ต้นทุนในสหราชอาณาจักรแสดงให้เห็นถึงความคุ้มค่าที่ดีใน 3 ปี และประมาณการประหยัดต้นทุนใน 10 ปี2) 6) แนวทางของสมาคมต้อหิน ยุโรปฉบับที่ 6 แนะนำอย่างยิ่งให้ผ่าตัดเลนส์แก้วตา หรือ LPI สำหรับ PAC และ PACG ในผู้ป่วยอายุ ≥50 ปี5) การตัดม่านตา ส่วนปลาย (Peripheral iridectomy) : เป็นทางเลือกสำหรับกรณีที่ทำ LPI ได้ยากเนื่องจากกระจกตา ขุ่น เป็นต้น1) เนื่องจากเป็นหัตถการผ่าตัดแบบเปิด จึงมีความเสี่ยงต่อภาวะแทรกซ้อนจากการผ่าตัดภายในลูกตา แต่สามารถฟื้นฟูการไหลของอารมณ์ขันในน้ำได้อย่างน่าเชื่อถือ1) การเลือกตำแหน่ง LPI : แม้ว่ารายงานก่อนหน้านี้จะแนะนำตำแหน่ง 12 นาฬิกา แต่รายงานต่อเนื่องเกี่ยวกับอาการทางสายตา (dysphotopsia) นำไปสู่การเปรียบเทียบระหว่างการวางในตำแหน่งขมับด้านบนหรือแนวนอน (3 หรือ 9 นาฬิกา) ผลการทดลองแบบสุ่มไม่สอดคล้องกัน แต่การวางรูในจตุภาคด้านบนเพื่อให้เปลือกตาบนปิดทับอย่างดี หรือตำแหน่งแนวนอน ขึ้นอยู่กับนโยบายของแต่ละสถาบัน2) อาการ dysphotopsia หลังผ่าตัดส่วนใหญ่ (แสงจ้า มองเห็นภาพซ้อน เส้นแสง) จะดีขึ้นเองภายใน 6 เดือน2)
Q
เหตุใดการผ่าตัดเลนส์แก้วตาในการทดลอง EAGLE จึงได้รับความสนใจ?
A
การทดลอง EAGLE (ประสิทธิผลของการสกัดเลนส์ในโรคต้อหินมุมปิด ) เป็นการทดลองแบบสุ่มที่มีกลุ่มควบคุมแบบ multicenter ซึ่งส่วนใหญ่ดำเนินการในสหราชอาณาจักร โดยสุ่มผู้ป่วย PAC ที่มีอาการ (ความดันลูกตา ≥30 mmHg) หรือ PACG จำนวน 419 รายที่มีอายุ 50 ปีขึ้นไป เข้ารับการสกัดเลนส์ใสระยะแรก (CLE) หรือ LPI 6) ที่ระยะเวลา 3 ปี กลุ่ม CLE แสดงผลลัพธ์ที่ดีกว่าในตัวชี้วัดคุณภาพชีวิต (EQ-5D) การควบคุมความดันลูกตา และความจำเป็นในการรักษาเพิ่มเติม โดยความน่าจะเป็นในการรักษาความดันลูกตา เป้าหมายโดยไม่ใช้ยาสูงกว่ากลุ่ม LPI ประมาณ 10 เท่า6) การวิเคราะห์ต้นทุนในสหราชอาณาจักรแสดงให้เห็นความคุ้มค่าที่ 3 ปี และประมาณการประหยัดต้นทุนที่ 10 ปี2) 6) เพื่อตอบสนองต่อสิ่งนี้ แนวทางปฏิบัติที่พึงประสงค์สำหรับโรคมุมปิดปฐมภูมิของ AAO สหรัฐอเมริกา ก็ได้เสนอการสกัดเลนส์ระยะแรกเป็นทางเลือกการรักษาเริ่มต้นสำหรับ PAC และ PACG ที่มีความดันลูกตา สูง แม้ในกรณีที่ไม่มีต้อกระจก ที่ส่งผลต่อการมองเห็น 2) แนวทางของสมาคมต้อหิน ยุโรป ฉบับที่ 6 ก็แนะนำการสกัดเลนส์และ LPI ด้วยความแรงเท่ากันสำหรับ PAC และ PACG ในผู้ป่วยอายุ 50 ปีขึ้นไป5) แนวทางปฏิบัติโรคต้อหิน ของญี่ปุ่น ฉบับที่ 5 ก็ระบุว่าเป็นทางเลือกแรกควบคู่กับ LPI ด้วยระดับคำแนะนำ 1A1)
ภาวะเฉียบพลันเป็นภาวะฉุกเฉินทางจักษุวิทยา การลดความดันลูกตา ตั้งแต่เนิ่นๆ และการแก้ไขภาวะปิดกั้นรูม่านตา จะเป็นตัวกำหนดพยากรณ์การมองเห็น 1) 2) 7) แนวทางปฏิบัติโรคต้อหิน ของญี่ปุ่น ฉบับที่ 5 แนะนำการรักษาแบบเป็นขั้นตอนดังนี้1) :
การรักษาด้วยยาเริ่มต้น :
ยาที่เพิ่มแรงดันออสโมซิส : D-mannitol 20% 1.0-2.0 กรัม/กิโลกรัม ให้ทางหลอดเลือดดำใน 30-60 นาที ความดันลูกตา จะถึงจุดต่ำสุด 60-90 นาทีหลังจากเริ่มให้ยา และผลคงอยู่นาน 4-6 ชั่วโมง ใช้ด้วยความระมัดระวังในผู้ป่วยไตวายหรือหัวใจล้มเหลว1) Glycerol 300-500 มล. ให้ทางหลอดเลือดดำใน 45-90 นาที และติดตามระดับน้ำตาลในเลือดในผู้ป่วยเบาหวาน1) ยาทำให้ม่านตา หด : ยาหยอดตา pilocarpine hydrochloride 1% หรือ 2% หยอด 2-3 ครั้งต่อชั่วโมง1) อย่างไรก็ตาม หากความดันลูกตา สูงมากและกล้ามเนื้อหูรูดม่านตา ขาดเลือดจนสูญเสียรีเฟล็กซ์ต่อแสง จะไม่สามารถคาดหวังผลการหดตัวของม่านตา ได้ และการเคลื่อนตัวไปข้างหน้าของกล้ามเนื้อซิลิอารีอาจทำให้ภาวะปิดกั้นรูม่านตา แย่ลง ดังนั้นควรหลีกเลี่ยงการหยอดบ่อยครั้ง1) การยับยั้งการผลิตอารมณ์ขันในลูกตา : Acetazolamide 10 มก./กก. ทางหลอดเลือดดำหรือรับประทาน ยาหยอดตากลุ่ม beta-blocker ยาหยอดตากลุ่ม α2 agonist และยาหยอดตากลุ่ม carbonic anhydrase inhibitor ใช้ร่วมกัน1) ต้านการอักเสบ : ระงับการอักเสบของส่วนหน้าด้วยยาหยอดสเตียรอยด์ เช่น betamethasone1)
การรักษาด้วยการผ่าตัด :
ในแนวทางปฏิบัติทางคลินิกโรคต้อหิน ฉบับที่ 5 แนะนำให้ผ่าตัดสร้างเลนส์ใหม่เป็นทางเลือกแรกสำหรับโรคต้อหินมุมปิดปฐมภูมิ เฉียบพลันและภาวะมุมปิดปฐมภูมิเฉียบพลัน 1) หากไม่สามารถผ่าตัดฉุกเฉินได้ในวันเดียวกัน ให้ลดความดันลูกตา ด้วยการรักษาด้วยยาก่อน จากนั้นเมื่อกระจกตา ใสแล้วจึงทำ LPI 1) ตัวอย่างการตั้งค่าเลเซอร์สำหรับ LPI : ขั้นแรก ยืดม่านตา ด้วยเลเซอร์อาร์กอนขนาดจุด 200–400 ไมครอน 200 มิลลิวัตต์ 0.2 วินาที จากนั้นทำให้บางจนเกือบทะลุด้วยจุด 50 ไมครอน 800–1,000 มิลลิวัตต์ 0.02 วินาที สุดท้าย ยิงทะลุ 1–2 ครั้งด้วยเลเซอร์ Nd:YAG 2.0–4.0 มิลลิจูล จำนวนครั้งทั้งหมดควรน้อยกว่า 100 ครั้งเพื่อป้องกันเยื่อบุกระจกตา 1) ในกรณีที่กระจกตา ขุ่น ให้พิจารณาเปลี่ยนเป็นการตัดม่านตา ส่วนปลายแบบผ่าตัด
ในฉันทามติปี 2025 โดยสมาคมต้อหิน เอเชียแปซิฟิก (APGS) และ Academy of Asia-Pacific Professors of Ophthalmology เกี่ยวกับภาวะมุมปิดปฐมภูมิเฉียบพลัน (APACA ) เสนอให้พิจารณาการรักษาทางเลือกต่อไปนี้อย่างจริงจัง เนื่องจากการรักษาด้วยยาแบบเดิมเพียงอย่างเดียวออกฤทธิ์ช้าในกรณีที่มีความดันลูกตา >50 มิลลิเมตรปรอทหลังเริ่มมีอาการ และยังมีความเสี่ยงต่อภาวะแทรกซ้อนทางระบบ7)
การทำม่านตา ส่วนปลายด้วยเลเซอร์อาร์กอน (ALPI ) : หัตถการที่ใช้เลเซอร์กำลังต่ำ ระยะเวลานาน จุดขนาดใหญ่ เพื่อหดม่านตา ส่วนปลายและเปิดมุมเชิงกล การทดลองแบบสุ่มมีกลุ่มควบคุมแสดงให้เห็นว่าความดันลูกตา เฉลี่ยลดลงเหลือ 30.8 มิลลิเมตรปรอทภายใน 15 นาทีหลัง ALPI และ 24.1 มิลลิเมตรปรอทภายใน 30 นาที ซึ่งถึงความดันลูกตา เป้าหมายได้เร็วกว่าการรักษาด้วยยาแบบเดิม7) การทำรูม่านตา ด้วยเลเซอร์ (LPP) : ใช้เลเซอร์ 532 นาโนเมตรเพื่อหดและพลิกขอบรูม่านตา ปลดบล็อกรูม่านตา สามารถทำได้แม้กระจกตา ขุ่นเล็กน้อย และใช้ร่วมกับ ALPI 7) การเจาะช่องหน้าลูกตา (ACP) : หัตถการลดความดันในช่องหน้าด้วยเข็ม 30 G หรือมีด 15 องศา ซึ่งช่วยลดความดันลูกตา ได้ทันที สามารถทำได้ในสถานที่ที่ไม่มีเลเซอร์อาร์กอน7)
ด้วยการรักษาทางเลือกเหล่านี้ แนะนำให้หลีกเลี่ยงการผ่าตัด trabeculectomy ฉุกเฉินหรือการผ่าตัดสลายต้อกระจก ฉุกเฉินในตาที่มีอาการ “ร้อนและฉุนเฉียว” ซึ่งก่อนหน้านี้เคยหลีกเลี่ยง7) หลังจากอาการเฉียบพลันสงบลง การผ่าตัดสลายต้อกระจก ในระยะแรกอาจพิจารณาเป็นทางเลือกเพื่อป้องกันความเสียหายเพิ่มเติมต่อเซลล์ปมประสาทจอประสาทตา 7)
การจัดการตาข้างตรงข้าม :
ประมาณครึ่งหนึ่งของตาข้างตรงข้ามหลัง APAC อาจเกิดอาการเฉียบพลันภายใน 5 ปีหากไม่ได้รับการทำ LPI เพื่อป้องกัน2) โดยหลักการแล้ว ควรทำ LPI เพื่อป้องกันทันที และระหว่างรอ ให้เริ่มใช้ยาหยอดตากลุ่มทำให้รูม่านตา หด (พิโลคาร์พีน)2) 7) อย่างไรก็ตาม การใช้พิโลคาร์พีนระยะยาวสัมพันธ์กับการขยายรูม่านตา ไม่ดี การยึดติดของม่านตา ด้านหลัง การดำเนินของต้อกระจก ความเสี่ยงต่อจอประสาทตาลอก ดังนั้นจึงไม่เหมาะสมเป็นการรักษาเรื้อรัง และใช้เป็นเพียงการเชื่อมต่อจนกว่าจะทำ LPI 2) แม้จะทำ LPI เพื่อป้องกันในตาข้างตรงข้าม ก็มีรายงานกรณีที่อาจเกิด PACG ภายใน 5-6 ปี จึงจำเป็นต้องติดตามผลระยะยาว2)
สำหรับความดันลูกตา สูงเรื้อรังที่เหลืออยู่ (ต้อหิน ตกค้าง) หลังจากแก้ไขการอุดตันของรูม่านตา ให้ทำการรักษาด้วยยา เลเซอร์ และการผ่าตัดตามแนวทางของต้อหินมุมเปิด ปฐมภูมิ1)
การรักษาด้วยยา : ยากลุ่มพรอสตาแกลนดิน /พรอสตาโนด์เป็นทางเลือกแรก1) 5) หากจำเป็น ให้เพิ่มยาเบต้าบล็อกเกอร์ ยากระตุ้นอัลฟา-2 ยายับยั้ง Rho kinase ยายับยั้งคาร์บอนิกแอนไฮเดรสการผ่าตัดเลนส์แก้วตา : มีประสิทธิภาพทั้งในการแก้ไขการอุดตันของรูม่านตา และการเปิดมุม และมีฤทธิ์ลดความดันลูกตา เพียงอย่างเดียว (ระดับคำแนะนำ 1A)1) อย่างไรก็ตาม ในกรณีที่มี PAS กว้าง (>50% ของมุม) ผลการลดความดันลูกตา จะจำกัด1) 10) การผ่าตัดแกะพังผืดยึดมุมตา : เหมาะในกรณีที่มี PAS กว้าง และเมื่อใช้ร่วมกับการผ่าตัดเลนส์แก้วตา สามารถป้องกันการยึดติดซ้ำและลดความดันลูกตา ได้1) การผ่าตัดเปิดทrabeculum : ใช้กับส่วนที่เปิดของ trabeculum และใช้เพื่อวัตถุประสงค์ในการปลด PAS ด้วย1) การผ่าตัด Trabeculectomy : เหมาะในกรณีที่ควบคุมความดันลูกตา ด้วยยาไม่เพียงพอ กรณี PAS เป็นเวลานาน หรือกรณีที่มองเห็นมุมได้ยาก ในตาที่มีมุมแคบ มีความเสี่ยงต่อภาวะแทรกซ้อน เช่น ช่องหน้าหายไปหลังผ่าตัด จอประสาทตาลอก ต้อหินร้ายแรง จึงจำเป็นต้องจัดการอย่างเข้มงวด1) 9) แนวทางของสมาคมต้อหิน ยุโรปฉบับที่ 6 แนะนำให้ Trabeculectomy เป็นการผ่าตัดทางเลือกแรกสำหรับ PACG ในตาปลอม5) การผ่าตัดต้อหิน แบบรุกรานน้อยที่สุด (MIGS ) : MIGS ในตาที่มีมุมปิดแต่เดิมเป็นข้อห้าม แต่การร่วมกับ phaco ช่วยให้เข้าถึงมุมได้ ดังนั้นข้อบ่งชี้จึงขยายออกไปในช่วงไม่กี่ปีที่ผ่านมา ในการวิเคราะห์อภิมานจาก 23 การศึกษาที่มี 875 ราย ความดันลูกตา หลัง 1 ปีลดลงเฉลี่ย 7.71 มม.ปรอท (95% CI 5.16–10.26) และยาหยอดตาต้อหิน ลดลงเฉลี่ย 1.57 หยด (95% CI 1.17–1.96) หลัง MIGS (ร่วมกับหรือไม่ร่วม phaco)8) การตัด trabeculotomy ภายใน (AIT ) ดีกว่าการจี้เลนส์ปรับเลนส์ด้วยกล้องส่องและ iStent และ phaco-MIGS มีประสิทธิภาพในการลดยามากกว่า phaco เพียงอย่างเดียว8) อัตราภาวะแทรกซ้อนคือ 16% ส่วนใหญ่เป็นเลือดออกในช่องหน้าตา เล็กน้อยชั่วคราว8) ใน PACG ระดับเล็กน้อยถึงปานกลางที่มีต้อกระจก phaco + MIGS ถือเป็นทางเลือกก่อนที่จะเปลี่ยนไปทำ trabeculectomy8)
ในม่านตา แบบที่ราบสูง การแก้ไขการอุดตันของรูม่านตา เพียงอย่างเดียวอาจไม่สามารถควบคุมความดันลูกตา ได้1) 14)
ยาหยอดพิโลคาร์พีน : ทำให้ม่านตา ส่วนปลายยืดออกและเปิดมุม แต่ผลไม่แน่นอน และการใช้ระยะยาวอาจทำให้รูม่านตา ขยายไม่ดี ม่านตาติด ด้านหลัง และต้อกระจก ดำเนินไป1) การทำเลเซอร์โกนิโอพลาสตี้ (LGP ) : ใช้เลนส์อับราฮัม เลเซอร์อาร์กอนขนาดจุด 500 ไมโครเมตร ระยะเวลา 0.2–0.5 วินาที กำลัง 200 มิลลิวัตต์เป็นเกณฑ์ กำหนด 15 นัดต่อหนึ่งจตุรัส บนครึ่งหรือรอบทั้งหมดของม่านตา ส่วนปลาย1) ในกรณีที่มีการอุดตันของรูม่านตา ร่วม ให้ทำเลเซอร์เปิดม่านตา (LPI ) ก่อน แล้วจึงเพิ่ม LGP 1) การนำเลนส์ออก : เมื่อเลนส์ถูกแทนที่ด้วยเลนส์แก้วตาเทียม ความลึกของช่องหน้าตาจะเพิ่มขึ้น และในตาที่มีมุมปิด ซีเลียรี โพรเซสจะเคลื่อนไปทางด้านหลังมากขึ้นหลังผ่าตัด ทำให้มุมเปิดกว้างขึ้น จึงถูกเลือกเป็นวิธีการเปิดมุมที่เชื่อถือได้1) 6) 14) การติดตามผล : ข้อมูลประสิทธิภาพระยะยาวมีจำกัด และควรหยอดพิโลคาร์พีนต่อเนื่องหลังผ่าตัด รวมถึงประเมินมุมเป็นระยะด้วย UBM 1) 14) การนำเลนส์ออกร่วมกับการจี้เลนส์ปรับเลนส์ด้วยกล้องส่อง (ECP ) : ในรายงานผู้ป่วยกลุ่มเล็ก มีรายงานว่าส่งผลต่อสัณฐานของซีเลียรี โพรเซส และอาจช่วยควบคุมความดันลูกตา ได้ดีขึ้น2) ในการทดลองเปรียบเทียบไปข้างหน้า ไม่มีความแตกต่างอย่างมีนัยสำคัญในความดันลูกตา หลังผ่าตัดเมื่อเทียบกับ phaco เพียงอย่างเดียว แต่การวัดด้วย OCT ส่วนหน้าพบว่ามุมเปิดกว้างกว่า2) การให้ความรู้ผู้ป่วย : อธิบายให้ผู้ป่วยทราบล่วงหน้าว่า iris plateau ไม่สามารถแก้ไขได้อย่างถาวรด้วย LPI และแจ้งว่ายังมีความเสี่ยงที่จะเกิดอาการกำเริบซ้ำจากการกระตุ้นให้ม่านตา ขยายแม้หลังทำ LPI แล้ว1) 14)
PACD ส่วนใหญ่มีกลไกพื้นฐานคือการอุดตันรูม่านตา แบบสัมพัทธ์1) 2) การสัมผัสระหว่างม่านตา และเลนส์ในบริเวณรูม่านตา ทำให้ความต้านทานการไหลของอารมณ์ขันจากช่องหลังไปยังช่องหน้าเพิ่มขึ้น เมื่อความดันในช่องหลังค่อนข้างสูง ม่านตา จะโป่งไปข้างหน้าและปกคลุม trabecular meshwork ในส่วนรอบนอกเกือบทั้งหมด ทำให้เกิดการอุดตันของมุมตาในเชิงหน้าที่ ในภาวะเฉียบพลัน สภาวะนี้จะรวมกับการเคลื่อนที่ของเลนส์ไปข้างหน้าและอาการบวมน้ำของ stroma ม่านตา ซึ่งทำให้การอุดตันรูม่านตา รุนแรงขึ้น และนำไปสู่วงจรอุบาทว์ของความดันลูกตา ที่เพิ่มขึ้นอย่างรวดเร็ว1) 2)
การอุดตันรูม่านตา มักจะรุนแรงที่สุดเมื่อรูม่านตา อยู่ในตำแหน่งขยายปานกลาง นี่คือสาเหตุที่การอ่านหนังสือในที่มืด การตื่นนอนตอนกลางคืน ยาที่มีฤทธิ์ต้านโคลิเนอร์จิก และท่าก้มตัวสามารถกระตุ้นให้เกิดอาการชักได้2) 7)
ใน iris plateau ซิลิอารีบอดี ้จะอยู่ในตำแหน่งด้านหน้า ดันรากม่านตา ไปข้างหน้าในเชิงกล ความลึกของช่องหน้าส่วนกลางค่อนข้างคงที่จึงดูปกติ แต่เมื่อม่านตา ขยาย ม่านตา ส่วนรอบนอกจะปีนขึ้นไปบนซิลิอารี โพรเซส และปิดกั้นมุมตาโดยตรง1) 14) ลักษณะเฉพาะใน UBM คือ การเบี่ยงเบนไปข้างหน้าของซิลิอารีบอดี ้ การหายไปของซิลิอารี ซัลคัส รากม่านตา ที่หนาและโค้งไปข้างหน้า และฐานมุมที่แคบ14)
ปัจจัยจากเลนส์มีส่วนผ่านการเพิ่มความหนาของเลนส์ตามอายุและการเคลื่อนที่ไปข้างหน้า เมื่อเลนส์หนาขึ้น พื้นที่สัมผัสระหว่างม่านตา และเลนส์จะขยายออก ทำให้การอุดตันรูม่านตา เพิ่มขึ้น1) 10) นอกจากนี้ เลนส์ที่หนาขึ้นยังทำให้ช่องหน้าตื้นขึ้น ซึ่งทำให้ปัจจัยทางกายวิศาสตร์เด่นชัดยิ่งขึ้น2) 10) นี่คือพื้นฐานทางทฤษฎีของผลการเปิดมุมตาหลังการผ่าตัดเลนส์6) 10)
การสัมผัสระหว่างม่านตา และ trabecular meshwork เป็นเวลานานหรือซ้ำๆ ทำให้เกิดความผิดปกติที่ไม่สามารถกลับคืนได้ใน trabecular meshwork เอง นำไปสู่การเกิด peripheral anterior synechiae (PAS )1) 2) ดังนั้นแม้หลังจากการปลดปล่อยการอุดตันรูม่านตา แล้ว ผู้ป่วยบางส่วนยังคงมีความดันลูกตา สูงเรื้อรัง ซึ่งเรียกว่า residual glaucoma1) ตามฉันทามติของ APGS แม้หลัง LPI ที่ประสบความสำเร็จหลังการชักเฉียบพลัน ผู้ป่วยมากถึง 58% อาจเปลี่ยนเป็น PACG เรื้อรัง7) มีการเสนอหลายกลไกรวมถึงความเสียหายเชิงกลต่อเซลล์ trabecular meshwork การเกี่ยวข้องของสารสื่อกลางการอักเสบ และการยุบตัวของคลอง Schlemm แต่ความเข้าใจพยาธิสรีรวิทยาอย่างสมบูรณ์ยังไม่บรรลุผล7) 10)
หลังการเกิดภาวะเฉียบพลัน ชั้นเส้นใยประสาทจอตา (RNFL ) จะหนาขึ้นชั่วคราวเนื่องจากอาการบวมของแอกซอนทันทีหลังการเกิดภาวะ กลับสู่ค่าปกติหลังจากประมาณ 1 เดือน และหลังจาก 3 เดือนจะเริ่มบางลง 2) ซึ่งบ่งชี้ว่าอาการบวมของแอกซอนและการเสื่อมสภาพทุติยภูมิเกิดขึ้นแยกกันตามเวลา และติดตามได้ด้วยการประเมินตามยาวด้วย OCT ในการศึกษาที่ติดตามผลระยะยาวของผู้ป่วย APAC ที่ไม่ได้รับการรักษาเป็นเวลา 4–10 ปี รายงานว่า 18% กลายเป็นตาบอดตามกฎหมาย และ 58% มีค่าการมองเห็น น้อยกว่า 20/40 2) ความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา ก็ลดลงตามสัดส่วนของระยะเวลาการเกิดภาวะ ทำให้เกิดความหลากหลายทางสัณฐาน (การแปรผัน) และความหลากหลายของขนาด (anisocytosis) ของเซลล์ 2) ผลกระทบของความดันลูกตา สูงและภาวะขาดเลือดยังขยายไปถึงการไหลเวียนเลือดของซิลิอารีบอดี ทำให้การผลิตอารมณ์ขันน้ำลดลงชั่วคราว ซึ่งอาจทำให้การตอบสนองต่อการรักษาด้วยยาแย่ลง 7)
ความดันลูกตา ที่เพิ่มขึ้นอย่างมากในระหว่างการเกิดภาวะเฉียบพลันทำให้การไหลเวียนเลือดไปยังจานประสาทตา และจอตาบกพร่อง และหลังจากภาวะคลี่คลาย จะเกิดภาวะเครียดออกซิเดชัน และการผลิตไซโตไคน์อักเสบในระหว่างการไหลเวียนกลับ 7) การบาดเจ็บจากภาวะขาดเลือด-การไหลเวียนกลับนี้ทำให้การสูญเสียเซลล์ปมประสาทจอตา (RGC ) ดำเนินต่อไปอีกระยะหนึ่งแม้หลังจากความดันลูกตา ลดลง ดังที่การศึกษาในสัตว์และการศึกษาตามยาวในมนุษย์ชี้ให้เห็น 7) ความรู้นี้สนับสนุนความสำคัญของการลดความดันลูกตา “อย่างรวดเร็ว” ในระหว่างการเกิดภาวะ และเป็นพื้นฐานทางทฤษฎีสำหรับคำแนะนำของ APGS เกี่ยวกับการรักษาทางเลือก (ALPI , LPP, ACP) เพื่อลดความดันลูกตา อย่างรวดเร็ว 7)
การทดลอง ZAP ให้ข้อมูลพื้นฐานสำหรับการจัดการ PACS ในฐานะการทดลองแบบสุ่มขนาดใหญ่ในประชากรเอเชีย และกระตุ้นให้มีการพิจารณาทบทวนการบ่งชี้ตามปกติของ LPI เชิงป้องกัน 3) การทดลอง ANA-LIS ของสิงคโปร์ก็สนับสนุนสิ่งนี้เช่นกัน 4) ในทางกลับกัน การทดลอง EAGLE แสดงให้เห็นถึงความเหนือกว่าของการผ่าตัดเลนส์แก้วตา เร็วสำหรับ PAC และ PACG และได้รับการนำมาใช้ในแนวทางหลักปัจจุบันของสหรัฐอเมริกา ยุโรป และญี่ปุ่น 1) 2) 5) 6) จากผลลัพธ์เหล่านี้ Preferred Practice Pattern สำหรับโรคมุมปิดปฐมภูมิฉบับปี 2026 ระบุอย่างชัดเจนว่าการผ่าตัดเลนส์แก้วตา เป็นทางเลือกการรักษาเริ่มต้นที่แข็งแกร่งสำหรับ PAC และ PACG 2)
ในฉันทามติ APGS/AAPPO ปี 2025 ได้เสนอแนวทางการรักษาที่รวมถึงการลดความดันลูกตา อย่างรวดเร็วด้วยเทคนิคทางเลือก เช่น ALPI , LPP และ ACP รวมถึงการผ่าตัดสลายต้อกระจก ในระยะแรกหลังจากระงับอาการเฉียบพลัน เนื่องจากการรักษาด้วยยาแบบดั้งเดิมเพียงอย่างเดียวออกฤทธิ์ช้าและมีความเสี่ยงต่อผลข้างเคียงทั้งระบบในผู้สูงอายุและผู้ป่วยที่มีโรคร่วม 7) นอกจากนี้ยังมีความสำคัญจากมุมมองของการยับยั้งการบาดเจ็บจากภาวะขาดเลือด-กลับมาเลือดไหล ซึ่งอาจดำเนินต่อไปหลังจากการโจมตีเฉียบพลัน ทำให้สูญเสียเซลล์ปมประสาทจอประสาทตา 7)
การวิเคราะห์ตามยาวของ OCT ส่วนหน้าพบว่าการเพิ่มขึ้นของ anterior lens vault และการลดลงของ angle width เป็นปัจจัยทำนายการดำเนินของ PACD ใน 3–6 ปี 2) ในอนาคต คาดว่าการตัดสินใจทำ LPI หรือการนำเลนส์ออกจะขึ้นอยู่กับการประเมินความเสี่ยงรายบุคคลโดยใช้ตัวชี้วัดทางชีวมิติเหล่านี้ การศึกษาในประเทศจีนที่ใช้การวินิจฉัยอัตโนมัติด้วย AI และแบบจำลอง Markov แสดงให้เห็นว่าการคัดกรองประชากรในผู้ที่มีอายุ 65 ปีขึ้นไปสามารถยับยั้งการดำเนินของ PACG ได้ แต่การคืนทุนค่าคัดกรองยังคงเป็นความท้าทาย 2)
MIGS ถูกห้ามใช้ใน PACG ในตอนแรก แต่กลายเป็นทางเลือกที่มีการรุกรานน้อยที่สุดสำหรับ PACG ระดับเล็กน้อยถึงปานกลางเมื่อใช้ร่วมกับ phaco ซึ่งช่วยให้เข้าถึงมุมตาได้ 8) การวิเคราะห์อภิมานแสดงให้เห็นความเหนือกว่าของ AIT แต่จำนวนการทดลองและระยะเวลาติดตามผลมีจำกัด จึงจำเป็นต้องมีการตรวจสอบเพิ่มเติมเกี่ยวกับผลลัพธ์ระยะยาวและความคุ้มค่า 8) เนื่องจากความเสี่ยงของภาวะแทรกซ้อนที่เกี่ยวข้องกับ bleb และการติดเชื้อ bleb ต่ำกว่าการผ่าตัด trabeculectomy จึงอาจส่งผลกระทบอย่างมากต่อการเลือกวิธีการผ่าตัดสำหรับ PACG ที่มีต้อกระจก ร่วม 8)
ในช่วงไม่กี่ปีที่ผ่านมา มีการระบุความหลากหลายทางพันธุกรรม (เช่น PLEKHA7, COL11A1, PCMTD1-ST18) ที่เพิ่มความเสี่ยงของ PACD ผ่านการศึกษา association ทั่วทั้งจีโนม ซึ่งช่วยเพิ่มความเข้าใจเกี่ยวกับความโน้มเอียงทางกายวิภาคและการประเมินความเสี่ยงรายบุคคล 2) ในอนาคต อาจมีการกำหนดกลยุทธ์การคัดกรองที่รวมข้อมูลทางพันธุกรรมและข้อมูลชีวมิติสำหรับบุคคลที่มีประวัติครอบครัวเป็นบวกหรือกลุ่มชาติพันธุ์ที่มีความเสี่ยงสูง 2)
จากมุมมองการให้คำแนะนำผู้ป่วย สิ่งสำคัญคือต้องให้ความรู้แก่ผู้ที่มีความเสี่ยงต่อ PACD เกี่ยวกับอาการของการโจมตีเฉียบพลันและความจำเป็นในการไปพบแพทย์ทันที ให้ข้อมูลเพื่อหลีกเลี่ยงยา (ทั้งที่จำหน่ายหน้าเคาน์เตอร์และที่ต้องสั่งโดยแพทย์) ที่ทำให้รูม่านตา ขยาย และสนับสนุนให้สมาชิกในครอบครัว (โดยเฉพาะญาติสายตรง) ตรวจตาเพื่อรักษาการทำงานของการมองเห็น ในระยะยาว 2)
日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
American Academy of Ophthalmology. Primary Angle-Closure Disease Preferred Practice Pattern®. San Francisco: American Academy of Ophthalmology; 2025.
He M, Jiang Y, Huang S, et al. Laser peripheral iridotomy for the prevention of angle closure: a single-centre, randomised controlled trial (Zhongshan Angle Closure Prevention Trial). Lancet. 2019;393(10181):1609-1618.
Baskaran M, Kumar RS, Friedman DS, et al. The Singapore Asymptomatic Narrow Angles Laser Iridotomy Study: Five-Year Results of a Randomized Controlled Trial. Ophthalmology. 2022;129(2):147-158.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Azuara-Blanco A, Burr J, Ramsay C, et al. Effectiveness of early lens extraction for the treatment of primary angle-closure glaucoma (EAGLE): a randomised controlled trial. Lancet. 2016;388(10052):1389-1397.
Chan PP, Zhang X, Aung T, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA ) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Asia Pac J Ophthalmol. 2025.
Paik B, Chua CH, Yip LW, Yip VCH. Outcomes and Complications of Minimally Invasive Glaucoma Surgeries (MIGS ) in Primary Angle Closure and Primary Angle Closure Glaucoma: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2024;18:1573-1588.
Song BJ, Ramanathan M, Morales E, et al. Trabeculectomy and combined phacoemulsification-trabeculectomy: outcomes and risk factors for failure in primary angle closure glaucoma. J Glaucoma. 2016;25(9):763-769.
Tarongoy P, Ho CL, Walton DS. Angle-closure glaucoma: the role of the lens in the pathogenesis, prevention, and treatment. Surv Ophthalmol. 2009;54(2):211-225.
Quigley HA, Broman AT. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophthalmol. 2006;90(3):262-267.
Foster PJ, Buhrmann R, Quigley HA, Johnson GJ. The definition and classification of glaucoma in prevalence surveys. Br J Ophthalmol. 2002;86(2):238-242.
Yamamoto T, Iwase A, Araie M, et al. The Tajimi Study report 2: prevalence of primary angle closure and secondary glaucoma in a Japanese population. Ophthalmology. 2005;112(10):1661-1669.
Kumar RS, Baskaran M, Chew PT, et al. Prevalence of plateau iris in primary angle closure suspects: an ultrasound biomicroscopy study. Ophthalmology. 2008;115(3):430-434.