การผ่าตัดเปิดท่อระบายน้ำ (trabeculotomy) คือการผ่าตัดที่กรีดเนื้อเยื่อบุผนังข้างคลอง Schlemm ซึ่งเป็นตำแหน่งที่มีความต้านทานการไหลของอารมณ์ขันน้ำสูงที่สุด เพื่อปรับปรุงการอุดตันของการไหลของอารมณ์ขันน้ำและลดความดันลูกตา เมื่อเทียบกับการผ่าตัดกรอง (trabeculectomy) ภาวะแทรกซ้อนระหว่างและหลังผ่าตัดน้อยกว่า แต่ผลการลดความดันลูกตา ด้อยกว่าการผ่าตัดกรอง
ตามธรรมเนียม การผ่าตัดเปิดท่อระบายน้ำต้องกรีดเยื่อบุตา และสร้างแผ่นตาขาว (วิธีภายนอกตา ab externo) ในช่วงไม่กี่ปีที่ผ่านมา เทคนิครุกรานน้อยที่สุดที่เรียกว่าการผ่าตัดต้อหิน แบบรุกรานน้อยที่สุด (MIGS ) ได้ถูกนำมาใช้ในทางคลินิก และทำในระยะที่เร็วกว่าข้อบ่งชี้ของการผ่าตัด trabeculectomy1) MIGS เป็นกลุ่มเทคนิคภายในตา (ab interno) ที่ไม่สร้างตุ่มกรอง ลดการรุกรานต่อกายวิภาคและสรีรวิทยาปกติ3)
ลักษณะเฉพาะที่กำหนดของ MIGS สรุปได้ในห้าข้อต่อไปนี้3) :
ความปลอดภัยสูง : ความเสี่ยงต่ำต่อภาวะแทรกซ้อนรุนแรง เช่น ความดันลูกตาต่ำ และจอประสาทตาลอก รุกรานกายวิภาคปกติน้อยที่สุด : เสริมสร้างกลไกการระบายตามสรีรวิทยาแนวทาง Ab interno : ดำเนินการจากภายในตาผ่านแผลที่กระจกตา ประสิทธิผล : ทำให้ความดันลูกตา ลดลงอย่างน้อย 20% หรือลดยาลง 1 ชนิดฟื้นตัวเร็ว : ระยะเวลาพักฟื้นเพิ่มเติมน้อยที่สุด
ในบริบทของการผ่าตัดต้อหิน การผ่าตัดสร้างทางระบายอารมณ์ขันน้ำ (trabeculotomy / MIGS ) มีข้อบ่งใช้ในกรณีที่การรักษาด้วยยาหรือเลเซอร์ไม่สามารถลดความดันลูกตา ได้เพียงพอ 1) ชนิดโรคหลักที่มุ่งเป้าคือ ต้อหินมุมเปิด ปฐมภูมิ ต้อหิน ความดันปกติ ต้อหิน ชนิดผลัดเซลล์ ต้อหินจากสเตียรอยด์ และต้อหิน ในเด็ก (ต้อหิน เด็ก) ในต้อหิน ชนิดผลัดเซลล์และต้อหินจากสเตียรอยด์ จะได้ผลการลดความดันลูกตา ที่สูงกว่าต้อหินมุมเปิด ปฐมภูมิ
การรักษาต้อหิน จะดำเนินการเป็นขั้นตอน: การรักษาด้วยยา (ทางเลือกแรก) → การรักษาด้วยเลเซอร์ (เช่น SLT ) → การผ่าตัดแบบเปิด 1) ในบรรดาการผ่าตัดแบบเปิด การตัดเนื้อเยื่อ trabecular (trabeculectomy) เป็นการผ่าตัดกรอง ที่ทำกันอย่างแพร่หลายที่สุด แต่การผ่าตัดสร้างทางระบาย (trabeculotomy / MIGS ) มีข้อได้เปรียบที่สำคัญคือสามารถแทรกแซงได้เร็วกว่าข้อบ่งชี้ของการตัดเนื้อเยื่อ trabecular 1) ในกรณีต้อหิน ระยะลุกลามหรือกรณีที่ความดันลูกตา เป้าหมายต่ำ ยังคงจำเป็นต้องตัดเนื้อเยื่อ trabecular หรือผ่าตัดใส่ท่อระบาย
อุปกรณ์ที่สร้างตุ่มน้ำใต้เยื่อบุตา (เช่น XEN Gel Stent, PreserFlo MicroShunt ) มีโปรไฟล์ความปลอดภัยและประสิทธิผลที่แตกต่างกัน ดังนั้นจึงจัดเป็น MIBS (การผ่าตัดตุ่มน้ำแบบ minimally invasive) ไม่ใช่ MIGS 3)
ประวัติการอนุมัติ stent ภายในตาที่ใช้ร่วมกับการผ่าตัดต้อกระจก มีดังนี้ 2)
iStent iStent inject WHydrus
ตามธรรมเนียม สำหรับต้อหินมุมเปิด ระยะต้นถึงระยะกลาง การผ่าตัดพร้อมกันกับการผ่าตัดต้อกระจก จะดำเนินการโดยวิธีภายนอกโดยใช้ trabeculotome (หัววัดโลหะ) 2) อย่างไรก็ตาม วิธีภายนอกจำเป็นต้องกรีดเยื่อบุตา ซึ่งอาจทำให้เกิดแผลเป็นที่เยื่อบุตา และขัดขวางการผ่าตัดกรอง เพิ่มเติม เช่น การตัดเนื้อเยื่อ trabecular หากจำเป็น 2) เพื่อแก้ปัญหานี้ จึงได้พัฒนาการผ่าตัดสร้างทางระบายจากด้านหน้าช่องลูกตาโดยใช้ gonioscopy (ด้วยไนลอน, handpiece, ตะขอ, ใบมีด ฯลฯ) ทำให้สามารถผ่าตัดได้โดยไม่ทิ้งแผลเป็นจากการผ่าตัดที่เยื่อบุตา 2)
ในสหภาพยุโรป iStent ได้รับการอนุมัติในปี 2004, iStent inject W ในปี 2010 และ Hydrus ในปี 2011 ในขณะที่ FDA ของสหรัฐอเมริกาอนุมัติ iStent ในปี 2012, iStent inject W และ Hydrus ในปี 20182)
Q
MIGS แตกต่างจากการผ่าตัดต้อหินแบบดั้งเดิมอย่างไร?
A
MIGS ทำจากภายในตา (ab interno) ผ่านแผลขนาดเล็ก จึงฟื้นตัวเร็วและมีความเสี่ยงต่อภาวะแทรกซ้อนต่ำ ในทางกลับกัน การผ่าตัดแบบดั้งเดิม เช่น การตัดท่อระบายน้ำ (trabeculectomy) สามารถลดความดันลูกตา ได้มากกว่า แต่มีความเสี่ยงต่อภาวะแทรกซ้อนร้ายแรง เช่น ความดันลูกตาต่ำ และการติดเชื้อ MIGS เหมาะสำหรับต้อหิน ระดับเล็กน้อยถึงปานกลาง และช่วยรักษาเยื่อบุตา ไว้ จึงไม่ส่งผลต่อความสำเร็จของการผ่าตัดกรอง ในอนาคต สำหรับต้อหิน ระยะลุกลามที่ต้องการความดันลูกตา เป้าหมายต่ำ จะเลือกการผ่าตัดแบบดั้งเดิม ปรึกษาแพทย์ของคุณ
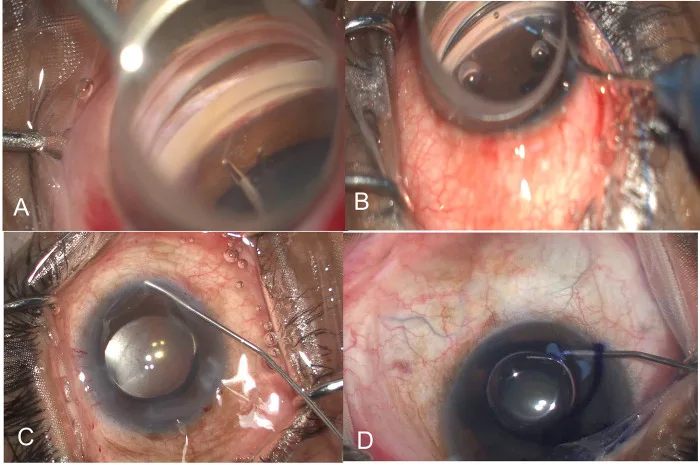
สี่ขั้นตอนระหว่างการผ่าตัด: การลอก trabecular meshwork ด้วยไมโครฟอร์เซป, การสอดไหม GATT, ปรากฏการณ์ blanching, การย้อม trabecular meshwork ด้วย trypan blue Rao A, Mukherjee S. Intraoperative predictors for clinical outcomes after microinvasive glaucoma surgery. PLoS One. 2023;18(11):e0293212. Figure 1. PM
CI D: PMC10635545. License: CC BY 4.0.
A แสดงขั้นตอนการลอก trabecular meshwork ด้วยไมโครฟอร์เซปใน micro MIGS (trabeculectomy แบบแถบ), B แสดงขั้นตอนการสอดไหม Prolene เข้าไปในคลอง Schlemm ใน GAT T (trabeculotomy ผ่านคลองภายใต้การส่องกล้องมุมตา), C แสดงปรากฏการณ์ blanching ของท่อรวบรวมหลังเปิดคลอง Schlemm, D แสดงการย้อม trabecular meshwork ด้วย trypan blue ขั้นตอนเหล่านี้สอดคล้องกับขั้นตอนย่อยของการจัดการมุมช่องหน้าม่านตา ใน GAT T และวิธีภายในตาที่กล่าวถึงในหัวข้อ “การจำแนกประเภทและเทคนิคการผ่าตัด”
การผ่าตัดต้อหิน แบ่งออกเป็นสี่ประเภทหลัก: การผ่าตัดกรอง , การสร้างทางระบายอารมณ์ขันน้ำใหม่, การผ่าตัดแก้ไขการอุดตันของรูม่านตา , และการทำลายซิลิอารีบอดี 1) การผ่าตัดที่อยู่ใน การสร้างทางระบายอารมณ์ขันน้ำใหม่ แบ่งออกเป็นสามกลุ่มตามแนวทางและเครื่องมือที่ใช้
Trabeculotomy (วิธีภายนอกตา) : วิธีดั้งเดิมที่ใส่ trabeculotome เข้าไปในคลอง Schlemm และหมุนเข้าไปในช่องหน้าม่านตา Trabeculotomy (วิธีภายในตา) : MIGS ที่กรีด trabecular meshwork โดยใช้ไมโครฮุค, KDB, Trabectome หรือไหมภายใต้การมองเห็น โดยตรงผ่าน gonioscopeการระบายภายในตาร่วมกับการผ่าตัดต้อกระจก : MIGS แบบ stent ที่ใส่ iStent inject W หรือ Hydrus เข้าไปในคลอง Schlemm
วิธีภายนอกตา (trabeculotome)
แนวทาง : ab externo (กรีดเยื่อบุตา , สร้างแผ่นตาขาว )
เทคนิค : หลังจากหยอด pilocarpine เพื่อทำให้ม่านตา หด, กรีดเยื่อบุตา บริเวณลิมบัส และเผยให้เห็นตาขาว สร้างแผ่นตาขาว ขนาด 4 มม., ระบุคลอง Schlemm และกรีดผนังด้านนอก ใส่หัววัดโลหะรูปตัวยู (trabeculotome, เส้นผ่านศูนย์กลางโค้ง 13-17 มม.) เข้าไปในคลอง Schlemm และหมุนเพื่อกรีดผนังด้านในของคลอง Schlemm และ trabecular meshwork เย็บแผ่นตาขาว และเยื่อบุตา ด้วยไหมไนลอน 10-0
ลักษณะเฉพาะ : บางสถานที่ใช้วิธีแผ่นตาขาว สองชั้น การทำพร้อมกันกับการผ่าตัดต้อกระจก ช่วยปรับปรุงผลลัพธ์ เนื่องจากต้องกรีดเยื่อบุตา จึงอาจส่งผลต่อการผ่าตัดกรอง ในอนาคต
การผ่าตัดภายในลูกตา (การสร้างทางระบายน้ำแบบ MIGS)
แนวทาง : ผ่านทางด้านใน (กรีดกระจกตา เล็ก, รักษาเยื่อบุตา )
เทคนิค : หลังผ่าตัดต้อกระจก ฉีดสารหนืดหยุ่น เอียงใบหน้าผู้ป่วย 35° ไปทางตรงข้ามศัลยแพทย์ เอียงกล้องจุลทรรศน์ 35° ภายใต้กล้องโกนิโอสโคป ระบุตำแหน่ง trabecular meshwork และสอดไมโครฮุค (μ-hook) หรือ KDB เข้าไปในช่องหน้าม่านตา ใช้ scleral spur เป็นตัวนำ กรีด trabecular meshwork ประมาณ 120° กำจัดเลือดที่ไหลย้อนกลับจากคลอง Schlemm ด้วย I/A สร้างช่องหน้าม่านตา และสิ้นสุด
ลักษณะเด่น : ไม่สร้างแผลเป็นผ่าตัดที่เยื่อบุตา ทำให้สามารถผ่าตัดกรองได้ในภายหลัง เนื่องจากมองเห็นโดยตรงจึงมีความแม่นยำและปลอดภัยสูง1)
ท่อระบายภายในลูกตา (MIGS แบบสเตนต์)
แนวทาง : ผ่านทางด้านใน (กรีดกระจกตา , รักษาเยื่อบุตา )
เทคนิค (iStent inject W) : สอดอุปกรณ์ใส่สเตนต์ผ่านแผลกรีดกระจกตา กด trocar เข้ากับ trabecular meshwork กดปุ่มปล่อยเพื่อปล่อยสเตนต์ไทเทเนียมรูปกระสุนสองอัน ยืนยันเลือดออกย้อนกลับ2)
เทคนิค (Hydrus ) : วางอุปกรณ์ไนตินอลรูปพระจันทร์เสี้ยวขนาด 8 มม. เข้าไปในคลอง Schlemm ประมาณ 90° โดยใช้ระบบนำส่ง ทำหน้าที่เป็นโครงค้ำยันขยายคลอง Schlemm 4-5 เท่า9)
ลักษณะเด่น : โดยทั่วไปทำร่วมกับผ่าตัดต้อกระจก แต่ iStent inject W ได้รับอนุมัติให้ผ่าตัดเดี่ยวตั้งแต่เดือนกรกฎาคม 20242)
เทคนิคการผ่าตัด เครื่องมือที่ใช้ ขอบเขตการกรีด/การวาง การรักษาเยื่อบุตา ทำพร้อมกับการผ่าตัดต้อกระจก การผ่าตัดเปิดท่อระบายน้ำออกทางภายนอก อุปกรณ์เปิดท่อระบายน้ำ (หัววัดโลหะ) ประมาณ 120° ไม่สามารถ สามารถ ไมโครฮุค (μ-hook/TMH) ไมโครฮุค ab interno ของ Yato ประมาณ 120° สามารถ โดยปกติจำเป็น KDB (Kahook Dual Blade) ใบมีดสองคม 3-5 ชั่วโมง สามารถ สามารถ (สามารถทำเดี่ยวได้) Trabectome หัวมือจับอิเล็กโทรดความถี่สูง สูงสุด 180° ได้ ได้ (สามารถทำเดี่ยวได้) GAT Tสายสวน/ไหมเย็บ สูงสุด 360° ได้ ได้ (สามารถทำเดี่ยวได้) OMNI ไมโครคาเทเตอร์แบบยืดหยุ่น 360° (ขยายด้วยสารหนืดยืดหยุ่น + กรีด) ได้ ได้ ABiC (การผ่าตัดคลองชเลมม์ ทางด้านใน) สายสวนไมโคร iTrack ขยายด้วยสารหนืดยืดหยุ่น 360° ได้ ได้ iStent inject Wขดลวดไทเทเนียมรูปกระสุน ×2 วางใน 2 ตำแหน่ง ได้ ปกติทำพร้อมกัน/ทำเดี่ยวได้ Hydrus รูปพระจันทร์เสี้ยวจากไนตินอล คลองชเลมม์ 90°ได้ ปกติทำพร้อมกัน
เป็นหัตถการที่ใช้อิเล็กโทรดความถี่สูงในการจี้และตัดผนังด้านในของคลอง Schlemm และเนื้อเยื่อ trabecular (ได้รับการอนุมัติจาก FDA ในปี 2004) หัวมือถือที่มีระบบชลประทานและดูดในตัวถูกสอดผ่านแผลที่กระจกตา ขนาด 1.6 มม. โดยมีแผ่นรองเท้าปกป้องเนื้อเยื่อข้างเคียง เริ่มให้กำลังไฟฟ้าที่ 0.8 mW และจัดการ trabecular ได้สูงสุด 180° การนำความร้อนไปยังผนังด้านนอกถูกจำกัดให้เหลือประมาณ 1.2°C ไม่ใช้วัสดุหนืดหยุ่น ผลหลังผ่าตัดเทียบเท่ากับ trabeculotomy และผลลัพธ์ดีขึ้นเมื่อทำร่วมกับการผ่าตัดต้อกระจก การวิเคราะห์อภิมาน (ผู้ป่วย 5,091 ราย) พบอัตราความสำเร็จ 2 ปี 46% สำหรับหัตถการเดี่ยว และ 85% สำหรับการรวมกับ phacoemulsification 4) เลือดออกในช่องหน้าม่านตา เกิดขึ้นได้ถึง 100% แต่ส่วนใหญ่หายไปภายในไม่กี่วันหลังผ่าตัด 5)
เป็นหัตถการที่ใส่ไมโครคาเทเตอร์หรือไหม Prolene เข้าไปในคลอง Schlemm และตัด trabecular ตลอดเส้นรอบวง (360°) รายงานครั้งแรกโดย Fellman และ Grover ในปี 2014 สามารถทำได้ด้วยต้นทุนต่ำโดยใช้ไหมเย็บ
เทคนิค: ขั้นแรก เปิดคลอง Schlemm โดย goniotomy ใส่คาเทเตอร์หรือไหมเข้าไปในคลอง Schlemm และผ่านไปตลอดเส้นรอบวง จากนั้นดึงเข้าหาศูนย์กลางเพื่อตัด trabecular หลังผ่าตัด ต้องรักษาความดันลูกตา ให้สูงกว่า 30 mmHg
การวิเคราะห์อภิมาน (537 ตา) แสดงความดันลูกตา ลดลงเฉลี่ย 9.81 mmHg และยาลดลง 1.67 ชนิด 4) ภาวะแทรกซ้อนรวมถึงเลือดออกในช่องหน้าม่านตา 12.5–80.6%, ความดันลูกตา พุ่งสูง 1.9–32.3%, และความดันลูกตาต่ำ ชั่วคราว 4.5–6.5% 4) พบการหลุดลอกของคอรอยด์ และซิลิอารีบอดี 47.7% ในการตรวจ OCT ส่วนหน้า แต่ส่วนใหญ่ไม่มีอาการและหายเอง 4)
การเปรียบเทียบระหว่างหัตถการ 180° (hemi-GAT T) และ 360° แสดงให้เห็นว่าเกณฑ์การตอบสนองต่อขนาดยาถึงที่ 120–180° โดยมีข้อดีคือส่วนที่เหลือสามารถเก็บไว้สำหรับการแทรกแซงซ้ำในอนาคต ส่วนล่างมีแนวโน้มที่จะมีกิจกรรมของทางระบายสูงกว่า
ใส่ไมโครคาเทเตอร์แบบยืดหยุ่นได้สองครั้ง ครั้งละ 180° และทำการขยายคลอง Schlemm ด้วยวัสดุหนืดหยุ่น (viscodilation) และตัด trabecular ด้วยอุปกรณ์เดียว การศึกษา GEMINI พบว่า 84.2% บรรลุความดันลูกตา ลดลง ≥20% ที่ 1 ปี 4)
เป็นหัตถการที่ใช้ไมโครคาเทเตอร์ iTrack เพื่อขยายคลอง Schlemm และท่อรวบรวม 360° ด้วยวัสดุหนืดหยุ่น ไม่มีการตัด trabecular แต่เป็นการปรับปรุงการเปลี่ยนแปลงทางพยาธิวิทยา (การยุบตัว) ของรูเปิด 4)
Q
ควรเลือกหัตถการใด?
A
การเลือกวิธีการผ่าตัดขึ้นอยู่กับชนิดและความรุนแรงของโรคต้อหิน การผ่าตัดต้อกระจก ร่วมหรือไม่ และประสบการณ์ของศัลยแพทย์ การวิเคราะห์อภิมานพบว่าการผ่าตัด trabeculotomy และ trabeculectomy (เช่น KDB, GAT T) เหนือกว่าชนิด stent (เช่น iStent ) ในการลดความดันลูกตา และลดยา 5) แต่โปรไฟล์ความปลอดภัยก็แตกต่างกันไปตามวิธีการ ผลการผ่าตัดสร้างทางระบายน้ำดีเป็นพิเศษในต้อหินชนิด exfoliation และต้อหินจากสเตียรอยด์ กรุณาปรึกษาจักษุแพทย์ผู้เชี่ยวชาญเพื่อเลือกวิธีการผ่าตัดที่เหมาะสมที่สุด
การรักษาโรคต้อหิน ด้วยการผ่าตัดทำเพื่อลดความดันลูกตา 1) ข้อบ่งชี้รวมถึงกรณีที่ไม่สามารถลดความดันลูกตา ได้เพียงพอด้วยการรักษาด้วยยาหรือเลเซอร์ หรือกรณีที่คาดว่าจะไม่สามารถลดความดันลูกตา ได้เนื่องจากผลข้างเคียงของยาหรือการปฏิบัติตามการรักษา ที่ไม่ดี 1)
การผ่าตัดสร้างทางระบายน้ำ (trabeculotomy, MIGS ) กำลังถูกทำเป็นข้อบ่งชี้ที่เร็วกว่าเมื่อเทียบกับการผ่าตัด trabeculectomy 1)
ต้อหินมุมเปิด ปฐมภูมิและต้อหิน ความดันปกติต้อหินชนิด exfoliation ความดันลูกตา สูงกว่าต้อหินมุมเปิด ปฐมภูมิ และเป็นข้อบ่งชี้ที่ดีเป็นพิเศษต้อหินจากสเตียรอยด์ ความดันลูกตา ที่ดีในระยะยาวต้อหิน เด็กทุติยภูมิต้อหิน เด็กปฐมภูมิต้อหิน พัฒนาการ (ต้อหิน เด็กปฐมภูมิ)ต้อหิน เส้นเลือดใหม่และต้อหินทุติยภูมิ จากม่านตาอักเสบ
ในกรณีผ่าตัดต้อกระจก พร้อมกัน :
ต้อหินมุมเปิด ปฐมภูมิ (ในความหมายกว้าง) หรือต้อหินชนิด exfoliation ระยะต้นถึงระยะกลางที่มีต้อกระจก ร่วมไม่มีประวัติการผ่าตัดภายในลูกตายกเว้นการรักษาด้วยเลเซอร์
มุมเปิดระดับ III ขึ้นไปตามการจำแนกของ Shaffer และไม่มีพังผืดม่านตา ส่วนหน้าแบบรอบนอก
กำลังใช้ยาหยอดตารักษาโรคต้อหิน
เกณฑ์การคัดออก:
มีภาวะเลนส์สั่นหรือเส้นใยยึดเลนส์ฉีกขาด
ไม่สามารถให้ความร่วมมือในการตรวจ gonioscopy หลังผ่าตัดเนื่องจากภาวะสมองเสื่อมหรืออื่นๆ
เด็ก
ความหนาแน่นเซลล์เยื่อบุผนังกระจกตา น้อยกว่า 1500 เซลล์/ตร.มม.
แพ้วัสดุที่ใช้ทำ stent
ข้อบ่งชี้สำหรับการผ่าตัด iStent inject W เพียงอย่างเดียว (ได้รับการอนุมัติเมื่อกรกฎาคม 2024) 2) :
โรคต้อหินมุมเปิดปฐมภูมิ (ในความหมายกว้าง) ระยะต้นถึงระยะกลาง หรือต้อหิน ชนิด exfoliativeไม่มีประวัติการผ่าตัดภายในลูกตายกเว้นการรักษาด้วยเลเซอร์ และการผ่าตัดต้อกระจก
มุมเปิดระดับ III ขึ้นไปตามการจำแนกของ Shaffer ไม่มีพังผืดม่านตา ส่วนหน้าแบบรอบนอก
กำลังใช้ยาหยอดตารักษาโรคต้อหิน
กรณีที่มีต้อกระจก ร่วมด้วยจะถูกคัดออก (เนื่องจากควรทำการผ่าตัดต้อกระจก ร่วมด้วย)
การเลือกวิธีการผ่าตัดต้องทำตามผู้ป่วยแต่ละราย 7) โดยประเมินปัจจัยต่อไปนี้อย่างครอบคลุม
ความดันลูกตา เป้าหมายระยะของโรคและความเร็วในการดำเนินโรค : ระยะต้นถึงระยะกลางเป็นข้อบ่งชี้หลัก ในระยะลุกลามอาจไม่เพียงพอชนิดของต้อหิน : ในต้อหินชนิด exfoliation และต้อหินจากสเตียรอยด์ ผลการผ่าตัดสร้างทางระบายน้ำใหม่ดีเป็นพิเศษความจำเป็นในการสงวนเยื่อบุตา : หากต้องการสงวนการผ่าตัดกรอง ในอนาคต วิธีการในลูกตาหรือชนิด stent ที่ไม่กรีดเยื่อบุตา จะได้เปรียบการมีต้อกระจก : ในกรณีที่มีต้อกระจก ร่วม การทำพร้อมกันเป็นมาตรฐาน และสามารถใช้ท่อระบายในลูกตาได้ประสบการณ์ของศัลยแพทย์ : จำเป็นต้องมีประสบการณ์เพียงพอในการผ่าตัดมุมตา และควรหลีกเลี่ยงการทำอย่างไม่ระมัดระวัง 1) ความทนต่อการมีเลือดออกในช่องหน้าลูกตา : มีรายงานว่า iStent ทำให้เลือดออกในช่องหน้าน้อยกว่าวิธีที่ใช้ใบมีด และในกรณีที่ต้องการหลีกเลี่ยงเลือดออกหลังผ่าตัด ท่อระบายในลูกตาอาจเป็นทางเลือก 2)
ต้อหินมุมปิด 3) )โรคที่มีความดันหลอดเลือดดำอีพิสเกลราสูง (เช่น Sturge-Weber syndrome): ผลของ MIGS ต่อ trabecular meshwork ถูกจำกัดโดยความดันหลอดเลือดดำอีพิสเกลรา จึงเป็นข้อห้ามต้อหิน ที่มีความผิดปกติแต่กำเนิดของมุมตาต้อหิน ชนิด neovascular
ดำเนินการโดยแพทย์ที่มีประสบการณ์ในการผ่าตัดสร้างเลนส์แก้วตา ใหม่มากกว่า 100 ราย และผ่าตัดต้อหิน แบบรุกล้ำมากกว่า 10 ราย และได้เข้ารับการอบรมจากแต่ละบริษัท 2)
Q
สามารถทำพร้อมกับการผ่าตัดต้อกระจกได้หรือไม่?
A
MIGS หลายชนิดสามารถทำพร้อมกับการผ่าตัดต้อกระจก (การสร้างเลนส์แก้วตา ใหม่) และการทำร่วมกันช่วยลดความดันลูกตา ได้ดีกว่าและมีอัตราการผ่าตัดซ้ำต่ำกว่าเมื่อเทียบกับการทำ MIGS เพียงอย่างเดียว 6) โดยหลักการแล้ว iStent inject W และ Hydrus ใช้ร่วมกับการผ่าตัดต้อกระจก แต่ iStent inject W ได้รับอนุมัติให้ทำเดี่ยวตั้งแต่เดือนกรกฎาคม 2024 2) Microhook, KDB, GAT T และ Trabectome สามารถทำเดี่ยวได้ แต่ในกรณีที่มีต้อกระจก ร่วมด้วย การผ่าตัดพร้อมกันเป็นมาตรฐาน โปรดปรึกษาจักษุแพทย์ผู้เชี่ยวชาญ
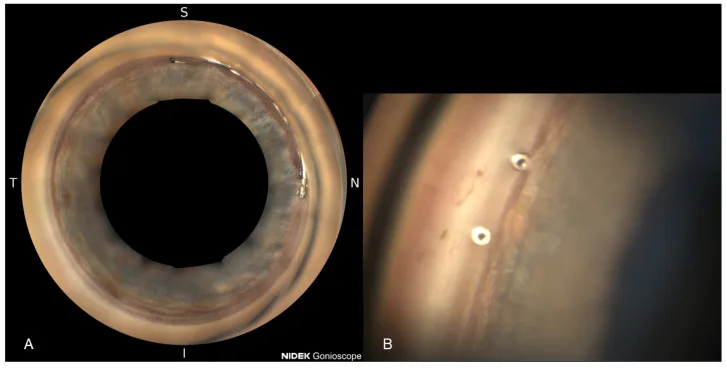
ภาพมุมตา 360° หลังใส่ Hydrus โดยใช้กล้อง Gonioscope NIDEK GS-1 และภาพใกล้ของ iStent inject W Weich C, Zimmermann JA, Storp JJ, Merté R-L, Eter N, Brücher VC. Comparison of the Intraocular Pressure-Lowering Effect of Minimally Invasive Glaucoma Surgery (
MIGS )
iStent Inject W and
Hydrus —The 12-Month Real-Life Data. Diagnostics. 2025;15(4):493. Figure 1. PM
CI D: PMC11854837. License: CC BY 4.0.
A คือภาพ Gonioscopy เต็มรูปแบบ (NIDEK GS-1) หลังใส่
Hydrus แสดงปลายใกล้ของ stent ด้านจมูก และ B คือภาพมุมใกล้ยืนยันช่องเปิดสองช่องของ
iStent inject W ภายใน trabecular meshwork สอดคล้องกับการประเมินตำแหน่งอุปกรณ์และความสำคัญของการตรวจ Gonioscopy หลังผ่าตัดในหัวข้อ “ผลการรักษาและภาวะแทรกซ้อน”
ความดันลูกตา หลังผ่าตัดมักอยู่ในช่วง 16-20 มิลลิเมตรปรอท สำหรับต้อหินมุมเปิด ปฐมภูมิ ความดันลูกตา ที่คาดหวังหลัง Trabeculotomy เพียงอย่างเดียวคือประมาณ 18 มิลลิเมตรปรอทที่ 5 ปี และอัตราการควบคุมต่ำกว่า 20 มิลลิเมตรปรอทประมาณ 50% ที่ 5 ปี เมื่อเทียบกับการผ่าตัด Trabeculectomy ไม่จำเป็นต้องดูแลหลังผ่าตัดอย่างเข้มข้นที่ส่งผลต่อผลลัพธ์ และข้อดีรวมถึงการฟื้นฟูการมองเห็น ที่รวดเร็ว สายตาเอียง น้อย และความคลาดเคลื่อนลำดับสูงต่ำ
เนื่องจากการผ่าตัดพร้อมกันกับการสร้างเลนส์แก้วตา ใหม่ช่วยปรับปรุงผลลัพธ์ของ Trabeculotomy จึงมักเลือกการผ่าตัดพร้อมกันในกรณีที่มีต้อกระจก ร่วมด้วย
ผลลัพธ์ตามชนิดของโรคมีดังนี้:
ต้อหิน ชนิดผลัดเซลล์และต้อหินจากสเตียรอยด์ ความดันลูกตา สูงกว่าต้อหินมุมเปิด ปฐมภูมิ ในต้อหินจากสเตียรอยด์ เป็นวิธีการที่มีประสิทธิภาพมากโดยคาดหวังการควบคุมความดันลูกตา ที่ดีในระยะยาวต้อหิน แต่กำเนิดปฐมภูมิความดันลูกตา ที่คาดหวังคือ 17-18 มิลลิเมตรปรอทที่ 18 ปีหลังผ่าตัด อัตราความสำเร็จ 96% สำหรับการเริ่มต้นหลังอายุ 2 เดือน อย่างไรก็ตาม การพยากรณ์โรคไม่ดีในกรณีที่มีกลุ่มอาการ Axenfeld-Rieger , กลุ่มอาการ Sturge-Weber หรือเส้นผ่านศูนย์กลางกระจกตา >13 มิลลิเมตรต้อหิน ชนิดพัฒนาการโดยรวม
โดยรวมแล้ว MIGS ช่วยลดความดันลูกตา ได้ 15-50% และลดจำนวนยาที่ใช้ลง 0.4-1.8 ชนิด 6) การทำร่วมกับการผ่าตัดต้อกระจก ช่วยลดความดันลูกตา เพิ่มขึ้นอีก 2-2.8 มิลลิเมตรปรอท เมื่อเทียบกับการผ่าตัดต้อกระจก เพียงอย่างเดียว และอัตราการผ่าตัดซ้ำที่ 2 ปีต่ำกว่าอย่างมีนัยสำคัญ (3% เทียบกับ 24%) 6) ในบางชุดการศึกษา ผู้ป่วย 22.6-80% สามารถหยุดยาได้ 6)
ในการวิเคราะห์อภิมาน (875 ตา, 23 การศึกษา) ค่าเฉลี่ยถ่วงน้ำหนักของการลดความดันลูกตา ที่ 1 ปีคือ 7.71 มิลลิเมตรปรอท (95% CI : 5.16-10.26) และการลดจำนวนยาคือ 1.57 ชนิด (95% CI : 1.17-1.96) 5) การวิเคราะห์กลุ่มย่อยพบว่าการผ่าตัดเปิด/ตัด trabecular meshwork (AIT ) เหนือกว่า iStent และการจี้เลเซอร์ปรับเลนส์ผ่านกล้องอย่างมีนัยสำคัญทั้งในด้านการลดความดันลูกตา (p<0.02) และการลดยา (p<0.01) 5)
เนื่องจากการผ่าตัดต้อกระจก เองก็มีผลลดความดันลูกตา จึงเป็นเรื่องยากที่จะแยกผลของ MIGS ออกจากผลของการผ่าตัดต้อกระจก ได้อย่างสมบูรณ์ 3) 7) จากผลการทดลองแบบสุ่มที่มีกลุ่มควบคุม ประมาณว่าสองในสามของการลดความดันลูกตา และการลดยาในกลุ่ม CE-IOL +MIGS เกิดจากผลของ CE-IOL เพียงอย่างเดียว และผลเพิ่มเติมของ MIGS คิดเป็นประมาณหนึ่งในสาม 4)
ผลลัพธ์ของอุปกรณ์ชนิดสเตนต์
iStent inject W + CE-IOL ความดันลูกตา ≥20% (กลุ่ม CE-IOL เพียงอย่างเดียว 61.9%, p=0.005) 8)
Hydrus + CE-IOL (การศึกษา HORIZON)ความดันลูกตา ≥20% (กลุ่ม CE-IOL เพียงอย่างเดียว 57.8%, p<0.001) อัตราการไม่ใช้ยา 78% เทียบกับ 48% 9)
Hydrus เทียบกับ iStent (การศึกษา COMPARE, การผ่าตัดเดี่ยว)ความดันลูกตา ≤18 มิลลิเมตรปรอทคือ Hydrus 35.6% เทียบกับ iStent 10.5% (p=0.001) อัตราการไม่ใช้ยาคือ Hydrus 46.6% เทียบกับ iStent 24.0% 10)
ผลลัพธ์ของการผ่าตัดเปิด/ตัด Trabecular Meshwork
KDB + CE-IOL เทียบกับ iStent + CE-IOL : อัตราความสำเร็จที่ 1 ปี 93.7% เทียบกับ 83.3% (p=0.04) ความดันลูกตา เฉลี่ย 15.4 เทียบกับ 16.1 มิลลิเมตรปรอท 11)
Microhook + CE-IOL เทียบกับ CE-IOL เพียงอย่างเดียว : อัตราการลดความดันลูกตา 51.5% เทียบกับ 20.1% (p<0.001) อัตราความสำเร็จสมบูรณ์ 90.3% เทียบกับ 0% 12)
Trabectome (การวิเคราะห์อภิมาน, ผู้ป่วย 5,091 ราย) : อัตราความสำเร็จคือ 46% สำหรับการผ่าตัดเดี่ยว และ 85% เมื่อทำร่วมกับ CE-IOL (2 ปี) 4)
GAT T (การวิเคราะห์อภิมาน, 537 ตา)ความดันลูกตา ลดลงเฉลี่ย 9.81 มิลลิเมตรปรอท, ลดยาลง 1.67 ชนิด4)
โดยรวมแล้ว MIGS มีโปรไฟล์ภาวะแทรกซ้อนที่ดีกว่าการผ่าตัดกรอง แบบดั้งเดิม5) ในการวิเคราะห์อภิมาน ไม่มีรายงานภาวะความดันลูกตาต่ำ ตาเหล่ หรือการติดเชื้อ และ MIGS ทุกประเภทมีความปลอดภัยสูง5)
ภาวะแทรกซ้อน MIGS โดยรวมวิธีภายนอก GAT THydrus iStent เลือดออกในช่องหน้าตา 24.9%5) เกิดขึ้นแน่นอน (หายใน 2-3 วัน) 12.5-80.6% 0.5-36.0% 1.2-1.9% ความดันลูกตา สูงชั่วคราว4.9%5) อาจคงอยู่นานถึง 3 เดือน 1.9–32.3% 0.5–20% 1–33.3% การอักเสบหลังผ่าตัด 3.31%5) — — — — การอุดตันของอุปกรณ์ — — — 1.1–12.2% 1–13.2% ตำแหน่งอุปกรณ์ผิดปกติ — — — 1.1% 3–18% PAS เฉพาะที่— — — 8.7–20.0% 1.8% เยื่อเดสเซเม็ตลอก — — 0.5% — —
การใส่ trabeculotome ผิดตำแหน่ง : การทะลุเร็วที่เกิดขึ้นเมื่อการใส่เข้าไปในคลอง Schlemm อย่างแม่นยำทำได้ยากการแยกตัวของซิลิอารีบอดี คอรอยด์ การหลุดลอกของเยื่อเดสเซเม็ทและเลือดคั่ง เลือดออกในช่องหน้าม่านตา : เกิดขึ้นแน่นอนเมื่อทะลุผนังด้านในของคลอง Schlemm แต่โดยปกติจะหายเองใน 2-3 วัน หากความดันลูกตา สูงคงที่ อาจเกิดการย้อมสีกระจกตา จากเลือด จำเป็นต้องล้างช่องหน้าม่านตา
ใน Hydrus มีรายงานกลุ่มอาการ UGH (ยูเวียอักเสบ-ต้อหิน -เลือดออกในช่องหน้าม่านตา ) ซึ่งแสดงเป็นม่านตาอักเสบ จอประสาทตา บวมน้ำชนิดซีสตอยด์ เลือดออกในช่องหน้าม่านตา และความดันลูกตา สูงเนื่องจากการวางตำแหน่งที่ไม่เหมาะสม 13) หลังจาก 6 เดือนขึ้นไปหลังการฝัง การนำออกทำได้ยากเนื่องจากการยึดเกาะของเนื้อเยื่อม่านตา ดังนั้นการรับรู้ความผิดปกติตั้งแต่เนิ่นๆ จึงสำคัญ 13) .
มีรายงานผู้ป่วย 2 รายที่มีการหลุดลอกของคอรอยด์ และซิลิอารีบอดี ร่วมกับความดันลูกตาต่ำ เรื้อรัง (1-4 มิลลิเมตรปรอท นานกว่า 2 เดือน) หลังการผ่าตัด trabeculotomy ด้วยไมโครฮุค ทั้งสองรายได้รับการแก้ไขด้วยการผ่าตัดวุ้นตา และการอัดแก๊ส 14) นอกจากนี้ยังมีรายงานผู้ป่วยที่มีการแยกตัวของซิลิอารีบอดี ที่ปิดเองหลังจาก 5 เดือนหลังไมโครฮุค โดยมีความดันลูกตา สูงเฉียบพลัน (42 มิลลิเมตรปรอท) ขณะปิด แล้วกลับสู่ปกติ OCT ส่วนหน้า (AS-OCT ) เหนือกว่า gonioscopy ในการตรวจหาการแยกตัวของซิลิอารีบอดี แสดงให้เห็นประโยชน์ของ AS-OCT ในการประเมินมุมหลังผ่าตัด
MIGS
แม้ว่า MIGS จะปลอดภัยกว่าการผ่าตัดแบบดั้งเดิม แต่ก็ไม่ปราศจากความเสี่ยง ต้องระวังความดันลูกตา ที่สูงขึ้นชั่วคราวหลังผ่าตัด เลือดออกในช่องหน้าม่านตา เป็นภาวะแทรกซ้อนที่พบบ่อยในหลายเทคนิค แต่โดยปกติจะหายเองในไม่กี่วัน หากความดันลูกตา พุ่งสูง (≥30 มิลลิเมตรปรอท) อย่างต่อเนื่อง จะรักษาด้วยยาหยอดพิโลคาร์พีน ยาหยอดเบต้าบล็อคเกอร์ ยาเม็ดอะเซตาโซลาไมด์ หรือการให้แมนนิทอลทางหลอดเลือดดำ หลังผ่าตัด ให้ปฏิบัติตามคำแนะนำของแพทย์และมาตรวจตามนัดอย่างสม่ำเสมอ
Q
ภาวะแทรกซ้อนของ MIGS รุนแรงหรือไม่?
A
ภาวะแทรกซ้อนของ MIGS โดยทั่วไปไม่รุนแรงและเกิดขึ้นชั่วคราว เลือดออกในช่องหน้าม่านตา พบบ่อยที่สุด แต่โดยปกติจะหายเองในไม่กี่วัน ภาวะแทรกซ้อนรุนแรง เช่น ความดันลูกตาต่ำ การติดเชื้อ และภาพซ้อน ซึ่งเป็นข้อกังวลในการผ่าตัดแบบดั้งเดิมนั้นแทบไม่มีรายงานใน MIGS 5) อย่างไรก็ตาม การวางตำแหน่งอุปกรณ์ที่ไม่เหมาะสมอาจต้องผ่าตัดเพิ่มเติม หลังผ่าตัด ให้ปฏิบัติตามคำแนะนำของแพทย์และมาตรวจตามนัดอย่างสม่ำเสมอ
การตรวจ Gonioscopy : จำเป็น ตรวจสอบระดับการเปิดของมุมโดยใช้การจำแนกของ Shaffer และบันทึกผลการตรวจมุมในเวชระเบียน 2) ความหนาแน่นของเซลล์เยื่อบุผิวก่อนกระจกตา : ต้อง ≥ 1500 เซลล์/ตร.มม. 2) การตรวจลานสายตา อัลตราซาวนด์ชีวกล้องจุลทรรศน์ (UBM ) : ประเมินระดับความผิดปกติของมุมในต้อหิน แต่กำเนิดการวัดความดันลูกตา ความดันลูกตา พื้นฐานซ้ำหลายครั้ง 7)
เลือดออกในช่องหน้าลูกตา : เกิดขึ้นแน่นอนเมื่อเจาะผนังด้านในของคลอง Schlemm ทันทีหลังผ่าตัดทำให้การมองเห็น บกพร่อง แต่ส่วนใหญ่จะหายไปใน 2-3 วัน และดูดซึมเองภายใน 2 สัปดาห์ หากเลือดออกทำให้ความดันลูกตา สูงต่อเนื่อง อาจเกิดการย้อมสีกระจกตา ด้วยเลือด (การสะสมของฮีโมโกลบินแบบถาวรในชั้นสโตรมาของกระจกตา ) จึงต้องล้างช่องหน้าลูกตา ความดันลูกตา สูงแบบ Spikeความดันลูกตา ≥ 30 มม.ปรอท อาจคงอยู่นานถึง 3 เดือนหลังผ่าตัด ปรากฏการณ์นี้เรียกว่า “ความดันลูกตา สูงแบบ Spike” การจัดการใช้ยาต่อไปนี้:
ยาหยอดพิโลคาร์พีน 1-2% (เปิดมุมโดยทำให้ม่านตา หด)
ยาหยอดเบต้าบล็อกเกอร์ เช่น ติโมลอล 0.5%
อะเซตาโซลาไมด์ 250 มก. รับประทาน (ยับยั้งคาร์บอนิกแอนไฮเดรส)แมนนิทอล 20% ทางหลอดเลือดดำ (ยาขับปัสสาวะออสโมติก สำหรับฉุกเฉินเฉียบพลัน)
สายตาเอียง ที่เกิดจากผ่าตัดสายตาเอียง อาจเกิดขึ้นจากการสร้างแผ่นตาขาว วิธีภายในลูกตา (MIGS ) มีข้อดีคือทำให้สายตาเอียง น้อยกว่าและเกิดความคลาดเคลื่อนลำดับสูงน้อยกว่ายาหยอดหลังผ่าตัด : ใช้ยาหยอดปฏิชีวนะและสเตียรอยด์ ประมาณ 1-2 เดือน
การดูแลหลังผ่าตัดจะดำเนินการคล้ายกับการผ่าตัดต้อกระจก 1) ไม่จำเป็นต้องดูแลหลังผ่าตัดอย่างเข้มข้นที่ส่งผลต่อผลลัพธ์เหมือนการตัด trabeculum และการฟื้นตัวของการมองเห็น เป็นไปอย่างรวดเร็ว
ยาหยอดตาปฏิชีวนะ เช่น levofloxacin: 3 ครั้งต่อวัน
ยาหยอดตาต้านการอักเสบที่ไม่ใช่สเตียรอยด์ (NSAIDs) เช่น diclofenac: 3 ครั้งต่อวัน
ยาหยอดตาสเตียรอยด์ เช่น betamethasone 0.1%: 3 ครั้งต่อวัน
เลือดออกในช่องหน้าตา เกิดขึ้นเกือบทุกครั้ง แต่ส่วนใหญ่จะดีขึ้นภายใน 1 ถึงไม่กี่วันตรวจติดตามเป็นระยะในวันที่ 1, สัปดาห์ที่ 1, เดือนที่ 1, 3 เดือน, 6 เดือน และ 1 ปีหลังผ่าตัด
ตรวจวัดสายตาและวัดความดันลูกตา เป็นประจำ 2)
ประเมินความปลอดภัยระยะยาวของอุปกรณ์โดยการตรวจจำนวนเซลล์บุผนังกระจกตา (การเปลี่ยนแปลงของเยื่อบุผนังกระจกตา ตามเวลาต้องให้ความสนใจเป็นพิเศษ เช่น กรณีการถอน CyPass Micro-Stent ออกจากตลาด)
ตรวจสอบตำแหน่งของ stent ด้วย gonioscopy (การตรวจพบตำแหน่งผิดปกติตั้งแต่เนิ่นๆ มีความสำคัญ)
แจกบัตรผู้ป่วยและอธิบายความสำคัญของการติดตามผลหลังผ่าตัด
ประเมินการอุดตันของอุปกรณ์หรือการมีเยื่อยึดม่านตา ส่วนปลาย (PAS ) เป็นระยะ
อารมณ์ขันที่เป็นน้ำถูกผลิตขึ้นในซิลิอารีบอดี ไหลจากช่องหลังผ่านรูม่านตา ไปยังช่องหน้า มีเส้นทางหลักสองเส้นทางในการระบายออกจากช่องหน้า
เส้นทาง trabecular (conventional pathway) เป็นเส้นทางหลักที่รับผิดชอบประมาณ 80-90% ของการระบายอารมณ์ขันที่เป็นน้ำทั้งหมด และผ่านโครงสร้างต่อไปนี้ตามลำดับ
Trabecular meshwork : ประกอบด้วยสามชั้น: uveal meshwork, corneoscleral meshwork และ juxtacanalicular tissue ในโรคต้อหินมุมเปิด เมทริกซ์นอกเซลล์ใน juxtacanalicular tissue เพิ่มขึ้น ทำให้ความต้านทานการระบายเพิ่มขึ้นคลอง Schlemm : โครงสร้างคล้ายท่อน้ำเหลืองวงแหวนที่มีเส้นผ่านศูนย์กลางภายในประมาณ 200-400 ไมโครเมตร ความดันลูกตา ที่เพิ่มขึ้นทำให้ลูเมนยุบตัว ยิ่งเพิ่มความต้านทานการระบายท่อรวบรวม : ประมาณ 25-35 ท่อแตกแขนงจากคลอง Schlemm และนำออกไปด้านนอก การกระจายของช่องเปิดของท่อรวบรวมไม่สม่ำเสมอ และความสามารถในการระบายแตกต่างกันตามตำแหน่งหลอดเลือดดำเอพิสเกลอรัล : ในที่สุดจะรวมเข้ากับระบบหลอดเลือดดำ ความดันหลอดเลือดดำเอพิสเกลอรัลประมาณ 8-10 มิลลิเมตรปรอท ซึ่งกำหนดขีดจำกัดล่างทางทฤษฎีของการลดความดันลูกตา ใน MIGS
เส้นทาง uveoscleral (unconventional pathway) เป็นเส้นทางที่ผ่านช่องว่างระหว่างกล้ามเนื้อซิลิอารีไปยังช่องเหนือคอรอยด์ และรับผิดชอบประมาณ 10-20% ของการระบายอารมณ์ขันที่เป็นน้ำทั้งหมด
ความต้านทานการระบายอารมณ์ขันที่เป็นน้ำส่วนใหญ่อยู่ที่ juxtacanalicular tissue และผนังด้านในของคลอง Schlemm ในโรคต้อหินมุมเปิด ความต้านทานในบริเวณนี้เพิ่มขึ้นทางพยาธิวิทยา และเทคนิค MIGS ทั้งหมดลดความต้านทานนี้โดยตรงหรือโดยอ้อมเพื่อลดความดันลูกตา
วิธีภายนอก (Trabeculotome) : ผนังด้านนอกของคลอง Schlemm ถูกเปิดออก และใช้หัววัดเจาะผนังด้านในไปทางช่องหน้าโดยการหมุนเพื่อกรีด trabecular meshwork เป็นวิธีการเข้าถึงคลอง Schlemm ทางกายภาพจากด้านสเกลอรัลวิธีภายใน (Microhook / KDB) : จากด้านช่องหน้า ภายใต้การมองเห็น โดยตรงด้วย gonioscopy trabecular meshwork และผนังด้านในของคลอง Schlemm ถูกกรีดหรือตัดออกเป็นแถบ ตำแหน่งที่มีความต้านทานสูงสุดถูกกำจัดโดยตรงTrabectome : Trabecular meshwork ถูกจี้และกำจัดออกโดยใช้อิเล็กโทรดความถี่สูง ทำให้คลอง Schlemm เปิดออกGAT TStent (iStent inject W) : ขดลวดไทเทเนียมถูกวางไว้ใน trabecular meshwork เพื่อสร้างทางบายพาสจากช่องหน้าไปยังคลอง SchlemmHydrus ABiC : ขยายคลองชเลมม์ และท่อรวบรวม 360° ด้วยสารหนืดยืดหยุ่น ช่วยแก้ไขการยุบตัวของลูเมน ไม่มีการกรีดที่ trabecular meshwork
ผลการลดความดันลูกตา ของ MIGS ที่กำหนดเป้าหมายที่ trabecular meshwork ถูกจำกัดโดยความต้านทานการไหลส่วนปลายจากคลองชเลมม์ และ ความดันหลอดเลือดดำอีพิสเกลอรัล (ประมาณ 8-10 มิลลิเมตรปรอท)3) ดังนั้น จึงพบได้ยากที่ความดันลูกตา หลังผ่าตัดจะลดลงต่ำกว่าช่วงกลางวัยรุ่น (ประมาณ 15 มิลลิเมตรปรอท)3) ตามกฎของฮาเกน-ปัวซอยล์ การไหลภายในลูเมนเป็นสัดส่วนกับกำลังสี่ของเส้นผ่านศูนย์กลางภายในและแปรผกผันกับความยาว ดังนั้น เส้นผ่านศูนย์กลางลูเมนของสเตนต์หรือขอบเขตการกรีด trabecular จึงเป็นปัจจัยสำคัญที่กำหนดการไหล
ในทางกลับกัน การผ่าตัดกรอง (trabeculectomy และ tube shunt) จะระบายอารมณ์ขันน้ำไปยังช่องว่างใต้เยื่อบุตา ดังนั้นจึงไม่ถูกจำกัดโดยความดันหลอดเลือดดำอีพิสเกลอรัลและสามารถบรรลุความดันลูกตา เป้าหมายที่ต่ำกว่า (10 มิลลิเมตรปรอทหรือน้อยกว่า) นี่คือพื้นฐานทางทฤษฎีที่ MIGS ไม่เพียงพอในกรณีต้อหิน ระยะลุกลามที่ต้องการความดันลูกตา เป้าหมายต่ำ
ผลของการผ่า trabeculotomy ขึ้นอยู่กับขอบเขตการกรีด แต่เชื่อกันว่าจะถึงเกณฑ์การตอบสนองต่อขนาดยาเมื่อเกิน 120-180° การไหลของอารมณ์ขันน้ำไม่สม่ำเสมอรอบเส้นรอบวงของมุม โดยมีกิจกรรมของทางเดินระบายสูงกว่าในส่วนจมูกและส่วนล่าง ความหนาแน่นของการกระจายของท่อรวบรวมก็แตกต่างกันไปตามตำแหน่ง และสามารถคาดหวังการลดความดันลูกตา ที่มีประสิทธิภาพโดยการกรีดเฉพาะส่วนที่อุดมไปด้วยทางเดินระบาย ดังนั้น การรักษา 180° (เช่น hemi-GAT T) อาจเพียงพอในบางกรณี
ในการผ่าตัดต้อหิน ทั้งหมดรวมถึง MIGS ผลการลดความดันลูกตา มักจะลดลงเมื่อเวลาผ่านไป3) ในอุปกรณ์สเตนต์ อาจเกิด synechia anterior ส่วนปลายหรือการอุดตันของอุปกรณ์ ในการผ่า trabeculotomy อาจเกิดการตีบซ้ำที่ตำแหน่งกรีดเนื่องจากการสร้างเยื่อ fibrovascular หรือแผลเป็นจากปฏิกิริยาการอักเสบ ดังนั้น ต้อหิน เป็นโรคตลอดชีวิตและไม่สามารถรักษาให้หายขาดได้ด้วยการผ่าตัดเพียงครั้งเดียว3) ข้อได้เปรียบที่สำคัญของ MIGS คือไม่เกี่ยวข้องกับการกรีดเยื่อบุตา ดังนั้นจึงไม่ส่งผลต่อความสำเร็จของการผ่าตัดกรอง ในอนาคต (trabeculectomy หรือ tube shunt)3)
Pilocarpine เป็นหนึ่งในยาลดความดันลูกตา ที่เก่าแก่ที่สุด แต่บางครั้งใช้หลัง MIGS ด้วยความหวังว่าจะคงผลการระบายไว้ และมีบทบาทสำคัญในการจัดการหลังการผ่าตัดต้อหิน แบบรุกรานน้อยที่สุด ยาหยอดตา pilocarpine 1-2% เชื่อว่ารักษามุมให้เปิดในช่วงต้นหลัง MIGS และยังช่วยให้เลือดในช่องหน้าม่านตา หายเร็วขึ้น
วิธีการรายงานจุดสิ้นสุดทางคลินิกในการศึกษา MIGS ไม่ได้เป็นมาตรฐานเดียวกัน ทำให้ยากต่อการเปรียบเทียบระหว่างการศึกษาต่างๆ 4) คณะกรรมการ PPP ของ AAO แนะนำให้ใช้อัตราความสำเร็จสะสมจากการวิเคราะห์การรอดชีวิตแบบ Kaplan-Meier ที่ 2 ปีเป็นจุดสิ้นสุดหลัก 4)
เกณฑ์ความสำเร็จสำหรับ MIGS เดี่ยว : ความดันลูกตา ≤21 มม.ปรอท และลดลง ≥20% จากค่าพื้นฐาน ไม่มีการเพิ่มยารักษาโรคต้อหิน ไม่มีการผ่าตัดเพิ่มเติม ไม่สูญเสียการรับรู้แสง ไม่มีความดันลูกตาต่ำ 4)
เกณฑ์ความสำเร็จสำหรับ MIGS ร่วมกับ CE-IOL : ลดยา ≥1 ชนิด (โดยไม่มีความดันลูกตา เพิ่มขึ้น) หรือความดันลูกตา ≤21 มม.ปรอท และลดลง ≥20% 4)
ความแตกต่างขั้นต่ำที่มีนัยสำคัญทางคลินิก (MCI D) สำหรับอัตราความสำเร็จสะสมที่ 2 ปีถูกเสนอ: ≥50% สำหรับ MIGS เดี่ยว, ≥65% สำหรับ MIGS ร่วมกับ CE-IOL 4)
ตามธรรมเนียมแล้ว โรคต้อหินมุมปิด ถือเป็นข้อห้ามสำหรับ MIGS แต่ในช่วงไม่กี่ปีที่ผ่านมา มุมมองนี้กำลังเปลี่ยนไป โดยเชื่อว่าผู้ป่วยจำนวนมากขึ้นจะได้รับประโยชน์จาก MIGS 3)
การวิจัยเกี่ยวกับผลลัพธ์ที่รายงานโดยผู้ป่วยหลัง MIGS ยังมีจำกัด แต่มีข้อค้นพบเบื้องต้นที่บ่งชี้ถึงการปรับปรุงการมองเห็น คุณภาพชีวิต และสุขภาพผิวตา 6) การลดภาระยาอาจช่วยปรับปรุงผิวตาและการปฏิบัติตามการรักษา 6)
ในการทบทวน 40 การศึกษา ผู้ป่วย 22.6-80% ไม่ต้องใช้ยาหลัง MIGS -phaco ร่วมกัน และเชื่อว่าการลดความผิดปกติของผิวตาที่เกิดจากยาหยอดตา (เช่น ความเสียหายของเยื่อบุกระจกตา ภาวะเยื่อบุตา คั่ง ความผิดปกติของต่อมไมโบเมียน ) ช่วยปรับปรุงคุณภาพชีวิต 6) ผู้ป่วยที่ใช้ยาหลายชนิด (≥3) ได้รับประโยชน์อย่างมากจากการลดยาหลัง MIGS การพัฒนาตัวชี้วัด PRO ที่ได้มาตรฐานและการวิจัยในกลุ่มเชื้อชาติที่หลากหลายเป็นความท้าทายในอนาคต 6)
CyPass Micro-Stent (MIGS เหนือคอรอยด์ ) ถูกถอนออกจากตลาดโดยสมัครใจในปี 2018 หลังจากพบว่าจำนวนเซลล์บุผนังกระจกตา ลดลงหลังจาก 5 ปี 3) โดยทั่วไป การรวบรวมข้อมูลเกี่ยวกับความปลอดภัยระยะยาว ความคุ้มค่า และอัตราการไม่พึ่งพายาสำหรับ MIGS ยังคงเป็นความท้าทายในอนาคต 3) 7)
มีรายงานกรณีที่ทำ KDB สำหรับโรคต้อหินมุมเปิด ในเด็กและเยาวชนที่เกี่ยวข้องกับกลุ่มอาการฟรีแมน-เชลดอน ซึ่งลดความดันลูกตา จาก 40 มม.ปรอท เหลือ 10 มม.ปรอท และคงที่ต่ำกว่า 15 มม.ปรอท นาน 27 เดือน กำลังมีการพิจารณาขยาย MIGS ไปสู่ชนิดพิเศษที่เกินกว่าข้อบ่งชี้ดั้งเดิม
มีรายงานกรณีที่การผ่าตัด trabeculectomy ร่วมกับ KDB และ deep sclerectomy ทำให้ความดันลูกตา หลังผ่าตัดลดลงต่ำกว่าความดันหลอดเลือดดำเหนือตาขาว ส่งผลให้เกิดเลือดออกในช่องหน้าม่านตา จำนวนมากและก้อน fibrin นำไปสู่การยึดติดของม่านตาส่วนปลายด้านหน้า และการอุดตันของท่อรวบรวม การใช้หัตถการที่ลดความดันลูกตา อย่างมากร่วมกันต้องใช้ความระมัดระวัง และมีรายงานว่ากลุ่มที่ใช้ร่วมกันไม่ได้ผลเพิ่มเติมอย่างมีนัยสำคัญเมื่อเทียบกับการลดความดันลูกตา ประมาณ 28.4% ด้วย KDB เพียงอย่างเดียว
ELIOS : เทคโนโลยีใหม่ที่ใช้เลเซอร์ไม่ใช้ความร้อนความแม่นยำสูงเพื่อสร้างไมโครแชนเนล 10 ช่องใน trabecula เลเซอร์เย็นช่วยลดการเกิดพังผืดของเนื้อเยื่อ และมีรายงานการรักษาระดับความดันลูกตา ที่ลดลงนาน 8 ปี หนึ่งปีหลังผ่าตัด ผู้ป่วย 80% สามารถหยุดการใช้ยาได้MIMS (การผ่าตัดเปิดตาขาว ขนาดเล็กแบบบุกรุกน้อยที่สุด) : การผ่าตัดกรอง แบบ ab externo โดยไม่ใช้ stent ซึ่งสร้างท่อระบายตาขาว -กระจกตา อย่างถาวรด้วยเข็มขนาด 600 μm ที่มีใบมีดสามเหลี่ยมขนาด 300 μm ผลลัพธ์มีแนวโน้มดี แต่ยังอยู่ในขั้นตอนการวิจัย
Q
จำเป็นต้องผ่าตัดซ้ำหลัง MIGS หรือไม่?
A
ประสิทธิภาพของ MIGS อาจลดลงเมื่อเวลาผ่านไปเช่นเดียวกับการผ่าตัดต้อหิน ทั้งหมด มีรายงานว่าผู้ป่วยมากถึง 24% จำเป็นต้องผ่าตัดซ้ำภายใน 2 ปีเมื่อทำ MIGS เพียงอย่างเดียว 6) เมื่อทำร่วมกับการผ่าตัดต้อกระจก อัตราการผ่าตัดซ้ำลดลงอย่างมากเหลือ 3% 6) ข้อดีของ MIGS คือการรักษาเยื่อบุตา ไว้ ดังนั้นจึงไม่ลดความสำเร็จของการผ่าตัดเพิ่มเติมในอนาคต เช่น trabeculectomy หรือ tube shunt หากจำเป็น
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
白内障手術併用眼内ドレーン会議. 白内障手術併用眼内ドレーン使用要件等基準(第3版). 日眼会誌. 2024;128:1013-1016.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Gedde SJ, et al. Reporting Clinical Endpoints in Studies of Minimally Invasive Glaucoma Surgery. Ophthalmology. 2025;132(2):143-151.
Paik JM, et al. Outcomes and Complications of Minimally Invasive Glaucoma Surgery: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2025;19:487-503.
Singh A, et al. Minimally Invasive Glaucoma Surgery: A Review of Clinical and Patient-Reported Outcomes. Cureus. 2025;17(7):e87872.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern. 2020.
Samuelson TW, et al. Prospective, randomized, controlled pivotal trial of an ab interno implanted trabecular micro-bypass in primary open-angle glaucoma and cataract: two-year results. Ophthalmology. 2019;126:811-821.
Samuelson TW, et al. A Schlemm canal microstent for intraocular pressure reduction in primary open-angle glaucoma and cataract: the HORIZON Study. Ophthalmology. 2019;126:29-37.
Ahmed IIK , et al. A prospective randomized trial comparing hydrus and iStent microinvasive glaucoma surgery implants for standalone treatment of open-angle glaucoma: the COMPARE Study. Ophthalmology. 2020;127:52-61.
Falkenberry SM, et al. CE-IOL plus KDB vs CE-IOL plus iStent : 1-year multicenter RCT results. Ophthalmology. 2020.
Maheshwari D, et al. CE-IOL plus Tanito Microhook vs CE-IOL alone: a randomized single-center trial. 2023.
Sachdeva N, et al. Early to late explantation of Hydrus microstent MIGS device: A case series. Am J Ophthalmol Case Rep. 2024;36:102105.
Otsuka M, et al. Gas Tamponade Improved Cilio-Choroidal Effusion Induced by an Ab Interno Trabeculotomy with a Microhook: Two Cases. Int Med Case Rep J. 2024;17:479-486.