小梁切开术 (trabeculotomy)是切开房水 流出道中流出阻力最高的近Schlemm管内皮组织,改善房水 流出障碍从而降低眼压 的手术。与滤过手术 (小梁切除术 )相比,术中及术后并发症较少,但降眼压 效果不如滤过手术 。
传统的小梁切开术 是需要结膜 切开和巩膜 瓣制作的眼外法(ab externo)。近年来,被称为微创青光眼手术 (MIGS )的微创技术被引入临床,并在比小梁切除术 适应证更早的阶段进行1) 。MIGS 是从眼内(ab interno)进行的非滤过泡形成技术,最大限度地减少对正常解剖和生理的干扰3) 。
MIGS 的定义特征归纳为以下五点3) 。
高安全性 :低眼压 、脉络膜 脱离等严重并发症风险低对正常解剖的最小干扰 :增强生理性流出机制内路式入路 :通过角膜 切口从眼内进行有效性 :实现至少20%的眼压 降低或减少一种药物快速恢复 :额外停机时间最小化
在青光眼 手术中,房水 流出通道重建术(小梁切开术 /MIGS )适用于药物或激光治疗 无法充分降低眼压 的病例1) 。主要目标疾病类型包括原发性开角型青光眼 、正常眼压性青光眼 、剥脱性青光眼 、类固醇性青光眼 和发育性青光眼 (儿童青光眼 )。剥脱性青光眼 和类固醇性青光眼 的眼压 降低效果优于原发性开角型青光眼 。
青光眼 治疗按步骤进行:药物治疗(首选)→激光治疗 (SLT 等)→侵入性手术1) 。在侵入性手术中,小梁切除术 是最广泛进行的滤过手术 ,但流出通道重建术(小梁切开术 /MIGS )相比小梁切除术 具有更早干预的巨大优势1) 。对于晚期青光眼 或目标眼压 较低的病例,仍需要小梁切除术 或管分流手术。
在结膜 下形成滤过泡的装置(XEN Gel Stent、PreserFlo MicroShunt等)具有不同的安全性和有效性特征,被归类为MIBS(微创滤过泡手术)而非MIGS 3) 。
白内障 手术联合眼内引流装置的批准历程如下2) 。
iStent iStent inject WHydrus
传统上,对于早期至中期开角型青光眼 ,与白内障 手术联合手术采用外路法,使用小梁切开刀(金属探针)2) 。然而,外路法需要切开结膜 ,如果后续需要额外的滤过手术 如小梁切除术 ,结膜 瘢痕常会妨碍手术2) 。为解决此问题,开发了在房角 镜引导下从前房 侧进行的流出通道重建术(使用尼龙线、手柄、钩、刀片等),从而可以在不造成结膜 瘢痕的情况下进行手术2) 。
欧盟于2004年批准iStent ,2010年批准iStent inject W,2011年批准Hydrus ;美国FDA于2012年批准iStent ,2018年批准iStent inject W和Hydrus 2) 。
Q
MIGS与传统青光眼手术有何不同?
A
MIGS 通过眼内小切口(ab interno)进行,因此恢复快、并发症风险低。而传统手术如小梁切除术 可更大幅度降低眼压 ,但存在低眼压 、感染等严重并发症风险。MIGS 适用于轻至中度青光眼 ,且保留结膜 ,不影响未来滤过手术 的成功率。对于需要较低目标眼压 的晚期青光眼 ,则选择传统手术。请咨询您的医生。
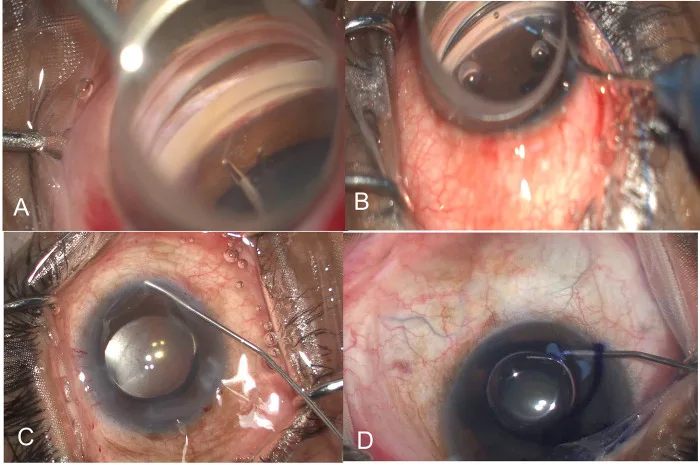
显微镊剥离小梁网、GATT缝线插入、漂白效应、台盼蓝染色的术中四步骤 Rao A, Mukherjee S. Intraoperative predictors for clinical outcomes after microinvasive glaucoma surgery. PLoS One. 2023;18(11):e0293212. Figure 1. PM
CI D: PMC10635545. License: CC BY 4.0.
A为显微
MIGS (小梁带切除术),显微镊剥离
小梁网 ;B为
GAT T(
房角 镜辅助下经腔
小梁切开术 ),Prolene缝线穿过Schlemm管;C为Schlemm管开放后集合管的漂白效应;D为台盼蓝染色显示
小梁网 。这些对应于本文“术式分类与操作技术”部分中
GAT T和眼内法的
前房 角操作步骤。
青光眼 手术大致分为四类:滤过手术 、房水 流出通道重建术、瞳孔阻滞 解除手术和睫状体 破坏手术1) 。房水 流出通道重建术
小梁切开术 (眼外法)前房 旋转的传统方法。小梁切开术 (眼内法)房角 镜直视下使用显微钩、KDB、Trabectome、缝线等切开小梁网 的MIGS 。白内障 手术联合眼内引流管 iStent inject W或Hydrus 植入Schlemm管的支架型MIGS 。
眼外法(小梁切开刀)
入路 :ab externo(结膜 切开、巩膜 瓣制作)
操作技术 :毛果芸香碱滴眼缩瞳后,切开角巩膜 缘结膜 暴露巩膜 。制作4mm巩膜 瓣,识别并切开Schlemm管外壁。将U形金属探针(小梁切开刀,曲率直径13-17mm)插入Schlemm管,旋转切开Schlemm管内壁和小梁网 。用10-0尼龙线缝合巩膜 瓣和结膜 。
特点 :部分机构采用双层巩膜 瓣技术。与白内障 手术同时进行可改善效果。由于需要结膜 切开,可能影响未来滤过手术 。
眼内法(MIGS流出道重建术)
入路 : ab interno(角膜 小切口,保留结膜 )
操作 : 白内障 手术后注入粘弹剂。将患者面部向术者相反方向倾斜35°,显微镜倾斜35°。在房角 镜下确认小梁网 ,将微钩(μ钩)或KDB等插入前房 。以巩膜 突为标志,切开小梁网 约120°。用I/A清除Schlemm管返流血液,形成前房 后结束。
特点 : 结膜 无手术瘢痕,可保留滤过手术 。因直视下操作,可靠性和安全性高1) 。
眼内引流(支架型MIGS)
入路 : ab interno(角膜 切口,保留结膜 )
操作(iStent inject W) : 从角膜 切口插入植入器,将套管针压向小梁网 ,按下释放按钮分离两个子弹形钛支架。确认返流性出血2) 。
操作(Hydrus ) : 用输送系统将8mm新月形镍钛合金装置置入Schlemm管内约90°。作为支架将Schlemm管扩张4~5倍9) 。
特点 : 原则上与白内障 手术联合进行,但iStent inject W自2024年7月起已获批单独手术2) 。
术式 使用器械 切开/留置范围 保留结膜 白内障 同时施行外路小梁切开术 小梁切开刀(金属探针) 约120° 否 是 微钩(μ钩/TMH) 谷户氏ab interno微钩 约120° 是 通常需要 KDB(Kahook双刃刀) 双刃刀片 3至5个钟点 是 是(可单独进行) Trabectome 高频电极手柄 最大180° 可 可(可单独进行) GAT T导管/缝线 最大360° 可 可(可单独进行) OMNI 柔性微导管 360°(粘弹扩张+切开) 可 可 ABiC(内路小梁切开术 ) iTrack微导管 360°粘弹剂扩张 可 可 iStent inject W钛制子弹状支架×2 两处植入 可 通常联合/可单独 Hydrus 镍钛诺新月形 Schlemm管90° 可 通常联合
该术式使用高频电极电凝并切开Schlemm管内壁和小梁网 组织(2004年FDA批准)。将带有灌注和吸引功能的手柄通过1.6mm角膜 切口插入。在足板保护邻近组织的同时,从0.8mW开始输出,处理最大180°的小梁网 。对外壁的热传导被控制在约1.2℃的最小限度。不使用粘弹剂。术后效果与小梁切开术 相当,联合白内障 手术可改善效果。一项荟萃分析(5,091名患者)显示,2年成功率单独为46%,联合CE-IOL 为85%4) 。前房 出血发生率高达100%,但多数在术后数天内消退5) 。
该术式将微导管或Prolene缝线插入Schlemm管,全周(360°)切开小梁网 。2014年由Fellman和Grover报道。使用缝线可低成本实施。
操作步骤:首先通过房角 切开术开放Schlemm管,然后将导管或缝线插入Schlemm管内并使其通过全周。之后向心性牵引以切开小梁网 。术后需将眼压 维持在30mmHg以上。
一项荟萃分析(537眼)显示,平均眼压 降低9.81mmHg,药物减少1.67种4) 。并发症包括前房 出血(12.5-80.6%)、眼压 峰值(1.9-32.3%)和一过性低眼压 (4.5-6.5%)4) 。前节OCT 检测到睫状体 脉络膜 脱离占47.7%,但多数无症状并自行消退4) 。
180°处理(半GAT T)与360°处理的比较表明,剂量反应阈值在120-180°达到,剩余范围可保留用于未来再次干预。下方节段的流出道活性往往更高。
将柔性微导管分两次各插入180°,使用单一设备进行Schlemm管粘弹扩张和小梁切开。GEMINI研究显示,1年时84.2%的患者眼压 下降≥20%4) 。
该术式使用iTrack微导管,用粘弹剂全周(360°)扩张Schlemm管和集合管。不切开小梁网 ,而是改善管腔的病理性改变(塌陷)4) 。
Q
应该选择哪种术式?
A
手术方式的选择取决于青光眼 的类型和严重程度、是否同时进行白内障 手术以及术者的经验。荟萃分析显示,小梁切开/切除术(如KDB、GAT T)在降低眼压 和减少用药方面优于支架型手术(如iStent )5) ,但安全性特征也因术式而异。剥脱性青光眼 和类固醇性青光眼 的流出道重建手术效果尤其良好。请与您的眼科专科医生协商,选择最佳手术方式。
青光眼 的手术治疗是为了降低眼压 1) 。适应症包括药物治疗或激光治疗 后仍无法获得充分眼压 下降的病例,或因药物副作用或依从性差而预计无法获得眼压 下降的病例1) 。
流出道重建手术(小梁切开术 /MIGS )现在比小梁切除术 更早地作为适应症进行1) 。
同时进行白内障 手术时 :
排除标准 :
合并晶状体 震颤或悬韧带断裂
因痴呆等难以配合术后房角镜检查
儿童
角膜内皮细胞密度 低于1,500个/mm²对支架材料过敏
iStent inject W单独手术的适应证2) :
术式的选择需要根据每位患者个体化进行7) 。综合判断以下因素。
目标眼压 :能否接受中等十几毫米汞柱,还是需要低十几毫米汞柱以下。后者需要滤过手术 。病程与进展速度 :主要适用于早期至中期。进展期可能效果不足。青光眼 类型剥脱性青光眼 、类固醇性青光眼 的流出道重建术效果尤其良好。是否需要保留结膜 :如需保留将来滤过手术 的可能性,不切开结膜 的眼内法或支架型更为有利。是否合并白内障 :合并白内障 时,联合手术是标准做法,可使用眼内引流装置。术者经验 :需要充分的房角 手术经验,应严格避免草率进行1) 。对前房 出血的耐受性 :有报告称iStent 比使用刀片的术式前房 出血更少,在希望避免术后前房 出血的病例中,眼内引流装置可作为选择之一2) 。
闭角型青光眼 房角 关闭,不适合流出道重建术(但近年来有扩大适应症的趋势3) )。上巩膜 静脉压升高疾病 (如Sturge-Weber综合征):小梁网 MIGS 的效果受上巩膜 静脉压限制,因此禁忌。伴有房角 先天性异常的青光眼 :房角 结构不清晰,无法保证支架植入的安全性。新生血管性青光眼 小梁网 的新生血管 阻碍流出道重建的效果,有效率低。
由具有100例以上白内障 手术经验和10例以上切开性青光眼 手术经验,并参加过各公司培训课程的医生实施2) 。
Q
可以和白内障手术同时进行吗?
A
许多MIGS 手术可以与白内障 手术(晶状体 重建术)同时进行,联合手术比单独MIGS 能获得更好的眼压 降低和更低的再手术率6) 。iStent inject W和Hydrus 原则上与白内障 手术联合使用,但iStent inject W自2024年7月起也获批单独手术2) 。微钩、KDB、GAT T和Trabectome可以单独进行,但在合并白内障 的病例中,同时手术是标准做法。请咨询您的眼科专科医生。
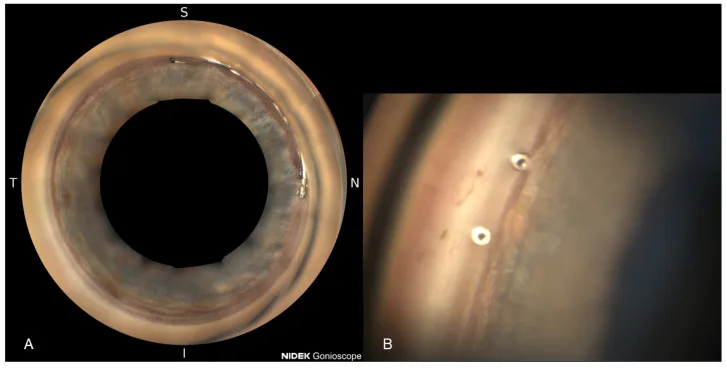
使用NIDEK GS-1全周房角镜的Hydrus植入后360°房角图像和iStent inject W近距图像 Weich C, Zimmermann JA, Storp JJ, Merté R-L, Eter N, Brücher VC. Comparison of the Intraocular Pressure-Lowering Effect of Minimally Invasive Glaucoma Surgery (
MIGS )
iStent Inject W and
Hydrus —The 12-Month Real-Life Data. Diagnostics. 2025;15(4):493. Figure 1. PM
CI D: PMC11854837. License: CC BY 4.0.
A为
Hydrus 植入后的全周
房角 镜(NIDEK GS-1)图像,鼻侧可见支架近端;B为
iStent inject W的两个端口开口位于
小梁网 内的近距
房角 图像。对应本文“治疗结果与并发症”部分讨论的装置位置评估和术后
房角镜检查 的意义。
术后眼压 通常在16至20 mmHg范围内波动。对于原发性开角型青光眼 ,单独小梁切开术 术后5年预期眼压 为18 mmHg,控制在20 mmHg以下的比率约为50%。与小梁切除术 相比,不需要影响预后的集中术后管理,且具有视力 恢复快、诱发散光 少、高阶像差不易发生等优点。
与白内障 手术(晶状体 重建术)同时手术可改善小梁切开术 的效果,因此在合并白内障 的病例中常选择联合手术。
不同疾病类型的结果如下:
剥脱性青光眼 和类固醇性青光眼 眼压 降低效果优于原发性开角型青光眼 。对于类固醇性青光眼 ,这是一种非常有效的手术方式,可期待长期良好的眼压 控制。原发性婴幼儿青光眼 :术后18年预期眼压 为17–18 mmHg。出生后2个月以后发病的成功率为96%。但合并Axenfeld-Rieger综合征 、Sturge-Weber综合征或角膜 直径超过13 mm时预后不良。发育性青光眼 总体房角 切开术成功率为94%。出生后1个月以内或2岁以后发病的成功率降至38%。
总体而言,MIGS 可实现15%至50%的眼压 下降,并减少0.4至1.8种药物使用量6) 。与白内障 手术联合使用时,相比单纯白内障 手术可额外降低眼压 2至2.8 mmHg,且2年时的再手术率显著降低(3%对24%)6) 。部分系列研究中,22.6%至80%的患者实现了免药6) 。
一项荟萃分析(875只眼,23项研究)显示,1年时加权平均眼压 下降为7.71 mmHg(95%CI : 5.16-10.26),药物减少1.57种(95%CI : 1.17-1.96)5) 。亚组分析表明,内路小梁切开术 (AIT )在眼压 下降(p<0.02)和药物减少(p<0.01)两方面均显著优于iStent 和经内镜睫状体 光凝术 5) 。
由于白内障 手术本身也具有降眼压 效果,因此很难完全区分MIGS 的纯效应和白内障 手术的效应3) 7) 。根据RCT结果,CE-IOL +MIGS 组中约三分之二的眼压 下降和药物减少归因于单纯CE-IOL ,MIGS 的附加效应估计约为三分之一4) 。
支架型装置的效果
iStent inject W + CE-IOL 眼压 下降≥20%(单纯CE-IOL 组为61.9%,p=0.005)8)
Hydrus + CE-IOL (HORIZON试验)眼压 下降≥20%(单纯CE-IOL 组为57.8%,p<0.001)。免药率78%对48%9)
Hydrus 对比iStent (COMPARE试验,单独手术)眼压 ≤18 mmHg的累积成功率,Hydrus 为35.6%,iStent 为10.5%(p=0.001)。免药率:Hydrus 46.6%对iStent 24.0%10)
小梁切开/切除术的效果
KDB + CE-IOL 对比iStent + CE-IOL :1年成功率93.7%对83.3%(p=0.04)。平均眼压 15.4对16.1 mmHg11)
微钩 + CE-IOL 对比单纯CE-IOL :眼压 下降率51.5%对20.1%(p<0.001)。完全成功率90.3%对0%12)
Trabectome(荟萃分析,5,091例患者) :成功率:单独手术46%,联合CE-IOL 85%(2年)4)
GAT T(荟萃分析,537眼)眼压 降低9.81 mmHg,药物减少1.67种4)
MIGS 总体上比传统滤过手术 具有更好的并发症谱5) 。荟萃分析未报告低眼压 、复视 或感染,所有类型的MIGS 均安全5) 。
并发症 所有MIGS 眼外法 GAT THydrus iStent 前房积血 24.9%5) 必然发生(2-3天消退) 12.5-80.6% 0.5-36.0% 1.2-1.9% 一过性眼压 升高 4.9%5) 可能持续长达3个月 1.9~32.3% 0.5~20% 1~33.3% 术后炎症 3.31%5) — — — — 设备阻塞 — — — 1.1~12.2% 1~13.2% 设备位置不良 — — — 1.1% 3~18% 局灶性PAS — — — 8.7~20.0% 1.8% Descemet膜脱离 — — 0.5% — —
小梁切开刀误插入 :当难以准确插入Schlemm管时发生的早期穿孔睫状体 脱离脉络膜 上腔Descemet膜下剥离/血肿 前房积血 眼压 持续存在,可能发生角膜血染 ,需进行前房 冲洗。
Hydrus 因位置不良导致虹膜炎 、囊样黄斑水肿 、前房积血 和高眼压 的UGH(葡萄膜炎 -青光眼 -前房积血 )综合征已有报道13) 。植入6个月以上后,虹膜 组织粘连导致取出困难,因此早期识别异常很重要13) 。
微钩小梁切开术 后出现睫状体 脉络膜 脱离和持续性低眼压 (1-4mmHg,持续2个月以上)的2例病例已有报道。两例均通过玻璃体 手术和气体填塞得到缓解14) 。此外,有病例报道微钩后睫状体 脱离在5个月后自行闭合,闭合时出现急性眼压 升高(42mmHg),随后恢复正常。前段OCT (AS-OCT )在检测睫状体 脱离方面优于房角 镜,显示了术后房角 评估中应用AS-OCT 的实用性。
Q
MIGS的并发症严重吗?
A
MIGS 的并发症通常轻微且短暂。前房积血 最常见,但通常在数日内自行消退。传统手术中令人担忧的严重并发症如低眼压 、感染和复视 ,在MIGS 中很少报道5) 。然而,因装置位置不良可能需要再次手术。术后请遵医嘱定期复查。
房角镜检查 房角 开放程度,并在病历中记录房角 所见2) 角膜内皮细胞密度 2) 视野检查 超声生物显微镜 (UBM )发育性青光眼 的房角 发育异常程度眼压测量 眼压 7)
前房积血 视力 障碍,但大多在2-3天内消退,2周内自然吸收。若出血导致持续高眼压 ,可能发生角膜血染 (角膜 实质中血红蛋白沉积的不可逆变化),需进行前房 冲洗眼压 峰值眼压 。这种现象称为“眼压 峰值”。处理使用以下药物:
毛果芸香碱1-2%滴眼液(缩瞳以开放房角 )
0.5%噻吗洛尔等β受体阻滞剂 滴眼液
乙酰唑胺 250 mg口服(碳酸酐酶抑制剂 )20%甘露醇静脉滴注(渗透性利尿剂,急性期紧急处理)
诱发散光 :制作巩膜 瓣可能引起散光 。眼内法(MIGS )具有诱发散光 少、高阶像差不易发生的优点术后滴眼液 :使用抗生素和类固醇 滴眼液约1-2个月
术后管理与白内障 手术类似1) 。不需要像小梁切除术 那样密集的术后管理,视力 恢复较快。
抗生素滴眼液如左氧氟沙星:每日3次
非甾体抗炎药(NSAIDs)滴眼液如双氯芬酸:每日3次
类固醇 滴眼液如0.1%倍他米松:每日3次前房 出血几乎必然发生,但多数病例在次日到数日内改善。术后第1天、1周、1个月、3个月、6个月、1年进行定期检查。
定期进行视力检查 和眼压测量 2) 。
通过角膜内皮 细胞计数评估装置的长期安全性(根据CyPass Micro-Stent退出市场的先例,需特别注意角膜内皮 随时间的变化)。
通过房角 镜确认支架位置(早期发现位置不良很重要)。
发放患者卡,并解释术后随访的重要性。
定期评估装置阻塞或周边虹膜前粘连 (PAS )的存在。
房水 由睫状体 产生,从后房经瞳孔 流入前房 。前房 的流出途径主要有两条。
经小梁网 流出途径(conventional pathway) 是主要途径,承担全部房水 流出的约80-90%,依次通过以下结构。
小梁网 巩膜 网和近管组织三层结构组成。开角型青光眼 中,尤其是近管组织的细胞外基质增加,导致流出阻力升高。Schlemm管 :内径约200-400μm的环形淋巴管样结构。眼压 升高导致管腔塌陷,进一步增加流出阻力。集合管 :从Schlemm管分出约25-35条,向外引导。集合管开口分布不均匀,不同部位的流出能力不同。上巩膜 静脉 :最终汇入静脉系统。上巩膜 静脉压约8-10mmHg,决定了MIGS 降低眼压 的理论下限。
葡萄膜巩膜 流出途径(unconventional pathway) 是通过睫状肌间隙进入脉络膜 上腔的途径,承担全部房水 流出的约10-20%。
房水 流出阻力的大部分存在于近Schlemm管组织(juxtacanalicular tissue) 和Schlemm管内壁。开角型青光眼 中,该部位的阻力病理性增加,所有MIGS 术式通过直接或间接降低该阻力来降低眼压 。
眼外法(小梁切开刀) :暴露Schlemm管外壁,用探头旋转突破内壁进入前房 ,切开小梁网 。这是从巩膜 侧物理进入Schlemm管的方法。眼内法(微钩、KDB) :从前房 侧在房角 镜直视下切开或带状切除小梁网 和Schlemm管内壁。直接去除流出阻力的最大部位。Trabectome :用高频电极烧灼并去除小梁网 ,暴露Schlemm管。GAT T支架(iStent inject W) :在小梁网 内放置钛制支架,形成从前房 到Schlemm管的旁路通道。Hydrus ABiC :使用粘弹性物质将Schlemm管和集合管扩张360°,改善管腔塌陷。不切开小梁网 。
针对小梁网 的MIGS 的眼压 下降效果受到Schlemm管远端流出阻力和上巩膜 静脉压 (约8-10 mmHg)的限制3) 。因此,术后眼压 很少降至mid-teens(约15 mmHg)以下3) 。根据Hagen-Poiseuille定律,管腔内流量与内径的四次方成正比,与长度成反比,因此支架内腔直径和小梁切开范围是决定流量的关键因素。
另一方面,滤过手术 (小梁切除术 、引流阀植入术)将房水 引流至结膜 下腔,不受上巩膜 静脉压的限制,可以达到更低的靶眼压 (≤10 mmHg)。这就是为什么对于需要低靶眼压 的晚期青光眼 ,MIGS 可能不足的理论依据。
小梁切开术 的效果取决于切开范围,但超过120-180°后,剂量反应达到平台期。房水 流出在房角 并非均匀分布,尤其是鼻侧和下方节段的流出通路活性较高。集合管的分布密度也因部位而异,选择性切开流出通路丰富的节段有望实现有效的眼压 下降。因此,180°的处理(如hemi-GAT T)有时也能获得足够的效果。
包括MIGS 在内的所有青光眼 手术,眼压 下降效果都有随时间减弱的趋势3) 。支架型装置可能发生周边虹膜前粘连 或装置阻塞。小梁切开术 可能因炎症反应导致的纤维血管膜形成或瘢痕化,引起切开部位的再狭窄。因此,青光眼 是一种终身疾病,不能通过单一手术治愈3) 。MIGS 不涉及结膜 切开,因此不会损害未来滤过手术 (小梁切除术 或引流阀植入术)的成功率,这是一个重要的优点3) 。
毛果芸香碱是最古老的降眼压 药物之一,但在MIGS 后有时用于维持流出效果,在微创青光眼手术 后的管理中占有重要地位。1-2%毛果芸香碱滴眼液被认为在MIGS 术后早期维持房角 开放,并有助于前房积血 的早期消退。
MIGS 研究中临床终点的报告方法尚未统一,导致不同研究之间的比较困难4) 。AAO 青光眼 PPP委员会建议将2年时Kaplan-Meier生存分析的累积成功率作为主要评价指标4) 。
单独MIGS 的成功标准 :眼压 ≤21 mmHg且较基线下降≥20%,无青光眼 药物增加,无额外手术,无视功能丧失,无低眼压 4)
CE-IOL 联合MIGS 的成功标准 :减少至少一种药物(眼压 不升高),或眼压 ≤21 mmHg且下降≥20%4)
2年累积成功率的最小临床重要差异(MCI D)建议为:单独MIGS ≥50%,CE-IOL 联合MIGS ≥65%4) 。
传统上,闭角型青光眼 被认为是MIGS 的禁忌症,但近年来,基于更多患者可能从MIGS 中获益的观点,这一看法正在改变3) 。
关于MIGS 后患者报告结局的研究有限,但初步发现提示视觉功能、生活质量和眼表健康有所改善6) 。减轻药物负担可能有助于改善眼表和治疗依从性 6) 。
一项对40项研究的综述发现,MIGS 联合超声乳化 术后22.6%至80%的患者不再需要药物,减少滴眼液引起的眼表损伤(如角膜上皮 损伤、结膜 充血 、睑板腺功能障碍 等)被认为有助于改善生活质量6) 。特别是使用多种药物(≥3种)的患者,MIGS 后药物减量的获益更大。开发标准化的患者报告结局指标以及在多样化种族人群中进行研究是未来的挑战6) 。
CyPass Micro-Stent(脉络膜 上腔MIGS )在5年后被发现导致角膜内皮 细胞减少,于2018年自愿退出市场3) 。对于MIGS 整体而言,积累长期安全性、成本效益和无药物率的数据是未来的挑战3) 7) 。
有报道对Freeman-Sheldon综合征合并的青少年开角型青光眼 实施KDB手术,眼压 从40 mmHg降至10 mmHg,并在27个月内稳定在15 mmHg以下。MIGS 正在考虑扩展到传统适应症以外的特殊疾病类型。
在KDB小梁切开联合深层巩膜切除术 中,有报告称术后眼压 降至上巩膜 静脉压以下,导致大量前房积血 和纤维蛋白凝块,进而引起周边虹膜前粘连 和集合管阻塞。联合使用大幅降低眼压 的手术需谨慎;KDB单独使用降压率约28.4%,而联合组未显示出显著的额外效果。
ELIOS :一种使用高精度非热激光在小梁网 中创建10个微通道的新技术。冷激光最大限度地减少组织纤维化,已有报告显示可维持8年的眼压 降低。术后1年时,80%的患者能够停止药物治疗。MIMS (微创迷你巩膜 切开术) :一种无支架的ab externo滤过手术 ,使用带有300μm三角形刀片的600μm针头永久性地创建巩膜 角膜 引流通道。结果令人鼓舞,但仍处于研究阶段。
Q
MIGS后是否需要再次手术?
A
与所有青光眼 手术一样,MIGS 的效果可能随时间减弱。有报告称,单独MIGS 在2年时最多有24%的患者需要再次手术6) 。与白内障 手术联合时,再手术率显著降至3%6) 。MIGS 保留结膜 ,因此未来如果需要额外手术如小梁切除术 或引流管 植入,其成功率不会受到影响。
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
白内障 手術併用眼内ドレーン会議. 白内障 手術併用眼内ドレーン使用要件等基準(第3版). 日眼会誌. 2024;128:1013-1016.European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Gedde SJ, et al. Reporting Clinical Endpoints in Studies of Minimally Invasive Glaucoma Surgery. Ophthalmology. 2025;132(2):143-151.
Paik JM, et al. Outcomes and Complications of Minimally Invasive Glaucoma Surgery: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2025;19:487-503.
Singh A, et al. Minimally Invasive Glaucoma Surgery: A Review of Clinical and Patient-Reported Outcomes. Cureus. 2025;17(7):e87872.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern. 2020.
Samuelson TW, et al. Prospective, randomized, controlled pivotal trial of an ab interno implanted trabecular micro-bypass in primary open-angle glaucoma and cataract: two-year results. Ophthalmology. 2019;126:811-821.
Samuelson TW, et al. A Schlemm canal microstent for intraocular pressure reduction in primary open-angle glaucoma and cataract: the HORIZON Study. Ophthalmology. 2019;126:29-37.
Ahmed IIK , et al. A prospective randomized trial comparing hydrus and iStent microinvasive glaucoma surgery implants for standalone treatment of open-angle glaucoma: the COMPARE Study. Ophthalmology. 2020;127:52-61.
Falkenberry SM, et al. CE-IOL plus KDB vs CE-IOL plus iStent : 1-year multicenter RCT results. Ophthalmology. 2020.
Maheshwari D, et al. CE-IOL plus Tanito Microhook vs CE-IOL alone: a randomized single-center trial. 2023.
Sachdeva N, et al. Early to late explantation of Hydrus microstent MIGS device: A case series. Am J Ophthalmol Case Rep. 2024;36:102105.
Otsuka M, et al. Gas Tamponade Improved Cilio-Choroidal Effusion Induced by an Ab Interno Trabeculotomy with a Microhook: Two Cases. Int Med Case Rep J. 2024;17:479-486.