線維柱帯切開術 (トラベクロトミー )は、房水 流出路のなかで流出抵抗が最も高い傍Schlemm管内皮組織を切開し、房水 流出障害を改善させ眼圧 下降を得る手術である。濾過手術 (線維柱帯切除術 )と比較して術中・術後の合併症が少ない一方、眼圧 下降効果では濾過手術 に劣る。
従来の線維柱帯切開術 は結膜 切開・強膜 弁作製を要する眼外法(ab externo)であった。近年、低侵襲緑内障手術 (minimally invasive glaucoma surgery: MIGS )と呼ばれる低侵襲な手技が臨床に導入され、線維柱帯切除術 の適応より早期を対象として行われるようになった1) 。MIGS はab interno(眼内側)から行う非ブレブ形成手技群であり、正常な解剖・生理への侵襲を最小限に抑える3) 。
MIGS の定義的特徴は以下の5項目に集約される3) 。
高い安全性 : 低眼圧 ・脈絡膜 剥離などの重篤合併症リスクが低い正常解剖への最小侵襲 : 生理的流出機構を強化するAb internoアプローチ : 角膜 切開創から眼内側で施行する有効性 : 少なくとも20%の眼圧 下降または1剤の薬剤減量を達成する迅速な回復 : 追加のダウンタイムが最小限である
緑内障 手術の中での位置づけとして、房水 流出路再建術(線維柱帯切開術 ・MIGS )は、薬物治療やレーザー治療 で十分な眼圧 下降が得られない症例に適応される1) 。主な対象病型は原発開放隅角緑内障 、正常眼圧緑内障 、落屑緑内障 、ステロイド緑内障 、発達緑内障 (小児緑内障 )である。落屑緑内障 やステロイド緑内障 では原発開放隅角緑内障 よりも高い眼圧 下降効果が得られる。
緑内障 治療は薬物治療(第1選択)→レーザー治療 (SLT 等)→観血的手術の順に段階的に行われる1) 。観血的手術のうち、線維柱帯切除術 が最も広く行われる濾過手術 であるが、流出路再建術(線維柱帯切開術 ・MIGS )は線維柱帯切除術 の適応よりも早期に介入できる点が大きな利点である1) 。進行した緑内障 や目標眼圧 が低い症例では、依然として線維柱帯切除術 やチューブシャント 手術が必要となる。
結膜 下にブレブを形成するデバイス(XEN Gel Stent、PreserFlo MicroShuntなど)は安全性・有効性プロファイルが異なるため、MIGS ではなくMIBS(minimally invasive bleb surgery)に分類される3) 。
白内障 手術併用眼内ドレーンの承認経緯は以下のとおりである2) 。
iStent iStent inject WHydrus
従来、初期〜中期の開放隅角緑内障 に対する白内障 手術との同時手術としてはトラベクロトーム(金属プローブ)を用いた眼外法が行われてきた2) 。しかし眼外法では結膜 を切開する必要があり、追加で線維柱帯切除術 などの濾過手術 が必要になった場合に結膜 の瘢痕が手術の支障になることが多かった2) 。この問題を解決するため、隅角 鏡で観察しながら前房 側から行う流出路再建術(ナイロン糸、ハンドピース、フック、ブレード等)が開発され、結膜 に手術瘢痕を作らず手術可能となった2) 。
欧州連合では2004年にiStent 、2010年にiStent inject W、2011年にHydrus が承認されており、米国FDAでは2012年にiStent 、2018年にiStent inject WとHydrus が承認されている2) 。
Q
MIGSと従来の緑内障手術はどう違いますか?
A
MIGS は眼の内側(ab interno)から小さな切開で行うため、回復が早く合併症リスクが低いのが特徴です。一方、線維柱帯切除術 などの従来手術は眼圧 をより大きく下げられますが、低眼圧 や感染などの重篤な合併症リスクがあります。MIGS は軽度〜中等度の緑内障 に適しており、結膜 を温存するため将来の濾過手術 の成功率を損ないません。進行した緑内障 で低い目標眼圧 が必要な場合は従来手術が選択されます。担当医と相談してください。
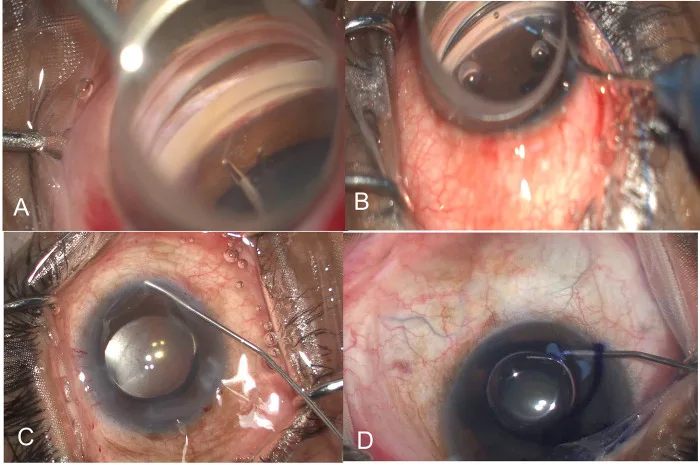
マイクロ鉗子によるTM剥離・GATT縫合糸挿入・blanching効果・トリパンブルー染色の術中4段階 Rao A, Mukherjee S. Intraoperative predictors for clinical outcomes after microinvasive glaucoma surgery. PLoS One. 2023;18(11):e0293212. Figure 1. PM
CI D: PMC10635545. License: CC BY 4.0.
Aはマイクロ
MIGS (
線維柱帯 帯状切除)でマイクロ鉗子が
線維柱帯 を剥離する工程、Bは
GAT T(
隅角 鏡補助下経管腔的
線維柱帯切開術 )でProlene縫合糸をSchlemm管に通す工程、CはSchlemm管開放後の集合管blanching効果、Dはトリパンブルーによる
線維柱帯 染色を示す。本文「術式の分類と手技」の項で扱う
GAT T・眼内法における
前房 角操作の個別ステップに対応する。
緑内障 手術は濾過手術 、房水 流出路再建術、瞳孔ブロック 解消手術、毛様体破壊術 の4つに大別される1) 。房水 流出路再建術
線維柱帯切開術 (眼外法)前房 内へ回旋する従来法線維柱帯切開術 (眼内法)隅角 鏡直視下でマイクロフック・KDB・Trabectome・縫合糸などにより線維柱帯 を切開するMIGS 白内障 手術併用眼内ドレーンiStent inject W・Hydrus をSchlemm管に留置するステント型MIGS
眼外法(トラベクロトーム)
アプローチ : ab externo(結膜 切開・強膜 弁作製)
手技 : ピロカルピン点眼で縮瞳後、輪部 結膜 を切開し強膜 を露出する。4mm強膜 弁を作製し、Schlemm管を同定・外壁切開する。U字型金属プローブ(トラベクロトーム、曲率直径13〜17mm)をSchlemm管に挿入し、回旋させてSchlemm管内壁と線維柱帯 を切開する。10-0ナイロン糸で強膜 弁・結膜 を縫合する。
特徴 : 二重強膜 弁法を用いる施設もある。白内障 手術との同時施行で成績が改善する。結膜 切開が必要なため、将来の濾過手術 に影響しうる。
眼内法(MIGS流出路再建術)
アプローチ : ab interno(角膜 小切開、結膜 温存)
手技 : 白内障 手術後に粘弾性物質 を注入する。患者の顔を術者と反対方向に35°傾け、顕微鏡を35°傾ける。隅角 鏡下に線維柱帯 を確認し、マイクロフック(μフック)またはKDB等を前房 内に挿入する。強膜 岬を指標として線維柱帯 を約120°切開する。Schlemm管からの逆流血をI/Aで除去し、前房 を形成して終了する。
特徴 : 結膜 に手術瘢痕を作らず、濾過手術 を温存できる。直視下操作のため確実性・安全性が高い1) 。
眼内ドレーン(ステント型MIGS)
アプローチ : ab interno(角膜 切開、結膜 温存)
手技(iStent inject W) : 角膜 切開創からインサーターを挿入し、線維柱帯 にトロカールを押しつけ、リリースボタンで弾丸状チタン製ステント2個を切り離す。逆流性出血を確認する2) 。
手技(Hydrus ) : ニチノール製8mm三日月型デバイスをデリバリーシステムでSchlemm管内に約90°にわたり留置する。Schlemm管を4〜5倍に拡張する足場として機能する9) 。
特徴 : 白内障 手術との併用が原則だが、iStent inject Wは2024年7月より単独手術も承認された2) 。
術式 使用器具 切開/留置範囲 結膜 温存白内障 同時施行眼外法トラベクロトミー トラベクロトーム(金属プローブ) 約120° 不可 可 マイクロフック(μフック/TMH) 谷戸氏ab internoマイクロフック 約120° 可 通常必要 KDB(Kahook Dual Blade) 二連刃ブレード 3〜5時間分 可 可(単独も可) Trabectome 高周波電極ハンドピース 最大180° 可 可(単独も可) GAT Tカテーテル/縫合糸 最大360° 可 可(単独も可) OMNI 可撓性マイクロカテーテル 360°(粘弾性拡張+切開) 可 可 ABiC(ab interno canaloplasty) iTrackマイクロカテーテル 360°粘弾性拡張 可 可 iStent inject Wチタン製弾丸状ステント×2 2箇所留置 可 原則同時/単独可 Hydrus ニチノール製三日月型 Schlemm管90° 可 原則同時
高周波電極でSchlemm管内壁と線維柱帯 組織を電気焼灼して切開する術式である(2004年FDA承認)。灌流・吸引を内蔵したハンドピースを1.6mm角膜 切開創から挿入する。フットプレートで隣接組織を保護しながら、0.8mWから出力を開始し、最大180°の線維柱帯 を処理する。外壁への熱伝導は約1.2℃と最小限に抑えられている。粘弾性物質 は不使用。術後成績は線維柱帯切開術 と同等であり、白内障 手術との同時施行で成績が改善する。メタアナリシス(5,091患者)では、2年成功率は単独46%、CE-IOL 併用85%であった4) 。前房出血 は最大100%で生じるが、多くは術後数日で消退する5) 。
マイクロカテーテルまたはProlene縫合糸をSchlemm管に挿入し、全周(360°)にわたり線維柱帯 を切開する術式である。2014年にFellmanとGroverにより報告された。縫合糸を用いれば低コストで実施可能である。
手技は、まず隅角 切開によりSchlemm管を開放し、カテーテルまたは縫合糸をSchlemm管内に挿入して全周を通過させる。その後、求心的に牽引して線維柱帯 を切開する。術後は眼圧 30mmHg以上に維持する管理が求められる。
メタアナリシス(537眼)では、平均眼圧 低下9.81mmHg、薬剤1.67剤減少を示した4) 。合併症は前房出血 12.5〜80.6%、眼圧 スパイク1.9〜32.3%、一過性低眼圧 4.5〜6.5%であった4) 。毛様体 脈絡膜 剥離が前眼部OCT で47.7%に検出されるが、多くは無症候性で自然消退する4) 。
180°処置(ヘミGAT T)と360°処置の比較では、120〜180°で用量反応閾値に達するとされ、残りの範囲を将来の再介入に温存できるという利点がある。下方セグメントの方が流出路活性が高い傾向にある。
可撓性マイクロカテーテルを180°ずつ2回挿入し、粘弾性物質 によるSchlemm管拡張(viscodilation)と線維柱帯 切開を1デバイスで行う。GEMINI Studyでは1年時に84.2%が20%以上の眼圧 下降を達成した4) 。
iTrackマイクロカテーテルを用いてSchlemm管と集合管を360°にわたり粘弾性物質 で拡張する手技である。線維柱帯 の切開は行わず、管腔の病的変化(虚脱)を改善する4) 。
Q
どの術式を選べばよいですか?
A
術式の選択は緑内障 の病型・重症度、白内障 手術の同時施行の有無、術者の経験により異なります。メタアナリシスでは線維柱帯 切開・切除術(KDB、GAT Tなど)がステント型(iStent 等)よりも眼圧 下降・薬剤減少に優れるとされますが5) 、安全性プロファイルも術式ごとに異なります。落屑緑内障 やステロイド緑内障 では流出路再建術の成績が特に良好です。担当の眼科専門医と相談のうえ、最適な術式を選択してください。
緑内障 の手術治療は眼圧 下降のために行う1) 。薬物治療やレーザー治療 によっても十分な眼圧 下降が得られない症例や、薬物による副作用やアドヒアランスが不良で眼圧 下降が得られないと予想される症例が適応となる1) 。
流出路再建術(線維柱帯切開術 ・MIGS )は、線維柱帯切除術 より早期の適応として行われるようになっている1) 。
原発開放隅角緑内障 ・正常眼圧緑内障 落屑緑内障 原発開放隅角緑内障 よりも眼圧 下降効果が高く、特に良好な適応ステロイド緑内障 眼圧 コントロールが期待できる続発小児緑内障 : 原発小児緑内障 と同様に線維柱帯切開術 が適応となる発達緑内障 (原発小児緑内障 )濾過手術 のブレブの術後管理が困難な小児では線維柱帯切開術 が第一選択。生後2か月以降の発症では成功率96%と良好な成績を示す血管新生緑内障 ・ぶどう膜炎続発緑内障 : 線維柱帯 への病的変化が著しく、流出路再建術の奏効率が低いため原則として適応外
白内障 同時手術の場合
除外基準 :
水晶体 振盪またはZinn小帯断裂を合併認知症等で術後隅角鏡検査 の協力が困難
小児
角膜内皮細胞密度 1,500個/mm²未満ステント材質へのアレルギー
iStent inject W単独手術の適応2) :
術式の選択は個々の患者に合わせて行う必要がある7) 。以下の要因を総合的に判断する。
目標眼圧 : mid-teens程度で許容できるか、あるいはlow-teens以下が必要か。後者には濾過手術 が必要病期と進行速度 : 初期〜中期が主な適応。進行期では不十分な可能性がある緑内障 の病型落屑緑内障 ・ステロイド緑内障 では流出路再建術の成績が特に良好結膜 温存の必要性濾過手術 を温存したい場合、結膜 を切開しない眼内法・ステント型が有利白内障 の有無白内障 合併例では同時施行が標準的であり、眼内ドレーンの使用が可能術者の経験 : 十分な隅角 手術の経験が必要であり、安易に行うことは厳に慎むべきとされる1) 前房出血 への許容度iStent はブレードを用いた術式より前房出血 が少ないとの報告があり、術後の前房出血 を避けたい症例では眼内ドレーンが選択肢となりうる2)
閉塞隅角緑内障 隅角 が閉塞しており流出路再建術の対象にならない(ただし近年は適応拡大の動きがある3) )上強膜 静脈圧上昇疾患 (Sturge-Weber症候群など): 線維柱帯 MIGS の効果が上強膜 静脈圧で制限されるため禁忌隅角 に先天異常のある緑内障 隅角 構造が不明瞭でステント留置の安全性が担保できない血管新生緑内障 : 線維柱帯 への新生血管 が流出路再建の効果を阻害し、奏効率が低い
水晶体 再建術を100件以上経験し、かつ観血的緑内障 手術を10件以上経験のある医師で、各社の講習会を受講した医師が施行する2) 。
Q
白内障手術と同時に受けられますか?
A
多くのMIGS は白内障 手術(水晶体 再建術)との同時施行が可能であり、併用により単独MIGS よりも良好な眼圧 下降と低い再手術率が得られます6) 。iStent inject WやHydrus は原則として白内障 手術との併用で使用されますが、iStent inject Wは2024年7月より単独手術も承認されました2) 。マイクロフックやKDB、GAT T、Trabectomeは単独でも施行可能ですが、白内障 合併例では同時施行が標準的です。担当の眼科専門医にご相談ください。
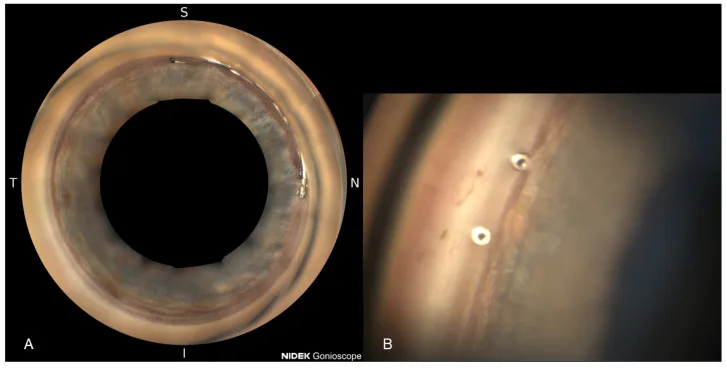
NIDEK GS-1全周ゴニオスコープによるHydrus留置後360°隅角像とiStent inject W近接像 Weich C, Zimmermann JA, Storp JJ, Merté R-L, Eter N, Brücher VC. Comparison of the Intraocular Pressure-Lowering Effect of Minimally Invasive Glaucoma Surgery (
MIGS )
iStent Inject W and
Hydrus —The 12-Month Real-Life Data. Diagnostics. 2025;15(4):493. Figure 1. PM
CI D: PMC11854837. License: CC BY 4.0.
Aは
Hydrus 留置後の全周ゴニオスコープ(NIDEK GS-1)像で鼻側にステント近位端を認め、Bは
iStent inject Wの2ポート開口部を
線維柱帯 内に確認する近接
隅角 像である。本文「治療成績と合併症」の項で扱うデバイス位置評価・術後
隅角鏡検査 の意義に対応する。
術後眼圧 は16〜20mmHgの範囲で推移することが多い。原発開放隅角緑内障 に対する期待眼圧 は、トラベクロトミー 単独で術後5年18mmHg、20mmHg以下へのコントロール率は5年で約50%である。線維柱帯切除術 と比較して術後成績を左右するような集約的な術後管理は必要ではなく、視力 の回復が早く、惹起乱視 が少なく、高次収差が発生しにくいなどの利点がある。
水晶体 再建術との同時手術は線維柱帯切開術 の成績を改善する効果があるため、白内障 を併発している症例では同時手術が選択されることが多い。
病型別の成績は以下のとおりである。
落屑緑内障 ・ステロイド緑内障 原発開放隅角緑内障 よりも眼圧 下降効果が高い。ステロイド緑内障 では長期にわたる良好な眼圧 コントロールが期待できる非常に有効な術式原発小児緑内障 : 期待眼圧 は術後18年で17〜18mmHg。生後2か月以降の発症で成功率96%。ただしAxenfeld-Rieger症候群、Sturge-Weber症候群を合併する場合や、角膜 径が13mmを超える場合は予後が不良発達緑内障 全体隅角 切開術で成功率94%。生後1か月未満や2歳以降の発症例では成功率38%に低下
MIGS 全体では15〜50%の眼圧 下降を達成し、薬剤使用量を0.4〜1.8剤減量させる6) 。白内障 手術との併用は単独白内障 手術と比較して追加2〜2.8mmHgの眼圧 下降をもたらし、2年時の再手術率は3%対24%と大幅に低い6) 。一部のシリーズでは22.6〜80%の患者が薬剤フリーを達成している6) 。
メタアナリシス(875眼、23研究)では、1年時の加重平均眼圧 低下は7.71mmHg(95%CI : 5.16-10.26)、薬剤減少は1.57剤(95%CI : 1.17-1.96)であった5) 。サブグループ解析では、線維柱帯 切開・切除術(AIT)がiStent や内視鏡下毛様体光凝固術 に対して眼圧 下降(p<0.02)・薬剤減少(p<0.01)の両面で有意に優れていた5) 。
白内障 手術自体にも眼圧 下降効果があるため、MIGS の純粋な効果と白内障 手術の効果を完全に分離することは困難である3) 7) 。RCTの結果からは、CE-IOL +MIGS 群における眼圧 下降・薬剤減量の約2/3がCE-IOL 単独の効果であり、MIGS の追加効果は約1/3と推定されている4) 。
ステント型デバイスの成績
iStent inject W + CE-IOL 眼圧 下降を達成(CE-IOL 単独群は61.9%、p=0.005)8)
Hydrus + CE-IOL (HORIZON試験)眼圧 下降を達成(CE-IOL 単独群は57.8%、p<0.001)。無薬物達成率78% vs 48%9)
Hydrus vs iStent (COMPARE試験、単独手術)眼圧 18mmHg以下の累積成功率はHydrus 35.6% vs iStent 10.5%(p=0.001)。薬剤フリー率はHydrus 46.6% vs iStent 24.0%10)
線維柱帯切開・切除術の成績
KDB + CE-IOL vs iStent + CE-IOL : 1年成功率93.7% vs 83.3%(p=0.04)。平均眼圧 15.4 vs 16.1mmHg11)
マイクロフック + CE-IOL vs CE-IOL 単独 : 眼圧 下降率51.5% vs 20.1%(p<0.001)。完全成功率90.3% vs 0%12)
Trabectome(メタ解析、5,091患者) : 成功率は単独46%、CE-IOL 併用85%(2年)4)
GAT T(メタ解析、537眼)眼圧 低下9.81mmHg、薬剤1.67剤減少4)
MIGS は全体として従来の濾過手術 より良好な合併症プロファイルを示す5) 。メタアナリシスでは低眼圧 ・複視 ・感染の報告がなく、全タイプのMIGS が安全性に優れる5) 。
合併症 MIGS 全体眼外法 GAT THydrus iStent 前房出血 24.9%5) 必発(2〜3日消退) 12.5〜80.6% 0.5〜36.0% 1.2〜1.9% 一過性眼圧 上昇 4.9%5) 3ヶ月まで持続しうる 1.9〜32.3% 0.5〜20% 1〜33.3% 術後炎症 3.31%5) — — — — デバイス閉塞 — — — 1.1〜12.2% 1〜13.2% デバイス位置不良 — — — 1.1% 3〜18% 局所性PAS — — — 8.7〜20.0% 1.8% Descemet膜剥離 — — 0.5% — —
トラベクロトームの誤挿入 : Schlemm管への正確な挿入が困難な場合に生じる早期穿孔毛様体解離 脈絡膜 腔に迷入Descemet膜下剥離・血腫 前房出血 眼圧 が持続する場合は角膜血染 症の可能性があるため前房 洗浄を行う
Hydrus では位置不良により虹彩炎 ・嚢胞様黄斑浮腫 ・前房出血 ・高眼圧 を呈するUGH(ぶどう膜炎 -緑内障 -前房出血 )症候群の報告がある13) 。留置後6ヶ月以上経過すると虹彩 組織の癒着により摘出が困難となるため、早期の異常認識が重要である13) 。
マイクロフックトラベクロトミー 後に毛様体 脈絡膜 剥離と遷延性低眼圧 (1〜4mmHg、2ヶ月以上持続)を呈した2症例が報告されている。両症例とも硝子体手術 とガスタンポナーデ により解消された14) 。また、マイクロフック後の毛様体解離 が5ヶ月後に自然閉鎖し、閉鎖時に急性眼圧 上昇(42mmHg)を認めた後に正常化した症例も報告されている。前眼部OCT (AS-OCT )が隅角 鏡よりも毛様体解離 の検出に優れていたとされ、術後の隅角 評価にAS-OCT を活用する有用性が示されている。
Q
MIGSの合併症は重篤ですか?
A
MIGS の合併症は一般的に軽度で一過性です。前房出血 が最も多いですが、通常は数日で自然に消退します。低眼圧 ・感染・複視 といった従来手術で懸念される重篤な合併症はMIGS ではほとんど報告されていません5) 。ただし、デバイスの位置不良により追加手術が必要になる場合があります。術後は担当医の指示に従い定期的に受診してください。
隅角鏡検査 隅角 の開放度を確認し、隅角 所見をカルテに記載する2) 角膜内皮細胞密度 2) 視野検査 超音波生体顕微鏡 (UBM )発達緑内障 では隅角 形成異常の程度を評価眼圧測定 眼圧 の反復測定が推奨される7)
前房出血 視力 障害をきたすが、ほとんどが2〜3日で消退し、2週間以内に自然吸収する。出血により高眼圧 が持続する場合は角膜血染 症(角膜実質 にヘモグロビンが沈着する不可逆的変化)の可能性があるため、前房 洗浄を行う眼圧 スパイク眼圧 が持続することがある。「眼圧 スパイク」と呼ばれる現象である。対処として以下の薬剤を使用する:
ピロカルピン1〜2%点眼(縮瞳により隅角 を開放)
0.5%チモロール等のβ遮断薬 点眼
アセタゾラミド 250mg内服(炭酸脱水酵素阻害薬 )20%マンニトール点滴(浸透圧利尿薬、急性期の緊急対応)
惹起乱視 : 強膜 弁作製に伴い乱視 が生じることがある。眼内法(MIGS )では惹起乱視 が少なく、高次収差も発生しにくいという利点がある術後点眼 : 抗菌薬点眼・ステロイド 点眼を約1〜2ヶ月使用する
白内障 手術に準じた術後管理を行う1) 。線維柱帯切除術 のような術後成績を左右する集約的な術後管理は必要ではなく、視力 の回復が早い。
レボフロキサシン等の抗菌薬点眼:1日3回
ジクロフェナク等の非ステロイド 性抗炎症薬(NSAIDs)点眼:1日3回
0.1%ベタメタゾン等のステロイド 点眼:1日3回
前房出血 はほぼ必発であるが、翌日〜数日で改善する症例が多い術後1日目・1週間後・1ヶ月後・3ヶ月後・6ヶ月後・1年後に定期検査を行う
視力検査 ・眼圧測定 を定期的に実施2) 角膜内皮 細胞数検査でデバイスの長期安全性を評価(CyPass Micro-Stentの市場撤退の前例から、角膜内皮 の経時的変化は特に注意が必要)隅角 鏡でステントの位置を確認(位置不良の早期発見が重要)患者カードを交付し、術後の経過観察の重要性を説明
デバイスの閉塞や周辺虹彩前癒着 (PAS )の有無を定期的に評価する
房水 は毛様体 で産生され、後房から瞳孔 を通り前房 に流入する。前房 からの流出経路は主に2つ存在する。
経線維柱帯 流出路(conventional pathway) が全房水 流出の約80〜90%を担う主経路であり、以下の構造を順に通過する。
線維柱帯 強膜 網・傍管内皮組織の3層構造。開放隅角緑内障 では特に傍管内皮組織の細胞外マトリックスが増加し、流出抵抗が上昇するSchlemm管 : 内径約200〜400μmの環状リンパ管様構造。眼圧 上昇により管腔が虚脱し、さらに流出抵抗が増大する集合管 : Schlemm管から約25〜35本が分岐し外方へ導く。集合管の開口部の分布は不均一であり、部位によって流出能が異なる上強膜 静脈 : 最終的に静脈系へ合流する。上強膜 静脈圧は約8〜10mmHgであり、MIGS の眼圧 下降の理論的下限を規定する
ぶどう膜強膜流出路 (unconventional pathway)毛様体 筋間隙を通り脈絡膜 上腔へ流出する経路で、全房水 流出の約10〜20%を担う。
房水 流出抵抗の大部分は**傍Schlemm管内皮組織(juxtacanalicular tissue)**とSchlemm管内壁に存在する。開放隅角緑内障 ではこの部位の抵抗が病的に増大しており、すべてのMIGS 術式はこの抵抗を直接的あるいは間接的に低減することで眼圧 下降を得る。
眼外法(トラベクロトーム) : Schlemm管外壁を露出し、プローブで内壁を前房 側へ突き破るように回旋して線維柱帯 を切開する。強膜 側からSchlemm管に物理的にアクセスする方法である眼内法(マイクロフック・KDB) : 前房 側から隅角 鏡直視下に線維柱帯 とSchlemm管内壁を切開または帯状切除する。流出抵抗の最大部位を直接除去するTrabectome : 高周波電極で線維柱帯 を焼灼・除去し、Schlemm管を露出させるGAT Tステント(iStent inject W) : 線維柱帯 内にチタン製ステントを留置し、前房 からSchlemm管へのバイパス経路を形成するHydrus ABiC : 粘弾性物質 によりSchlemm管と集合管を360°拡張し、管腔の虚脱を改善する。線維柱帯 の切開は行わない
線維柱帯 を標的とするMIGS の眼圧 下降効果は、Schlemm管から遠位の流出抵抗と上強膜 静脈圧 (約8〜10mmHg)によって制限される3) 。このため、術後眼圧 がmid-teens(15mmHg前後)以下に低下することは稀である3) 。Hagen-Poiseuille則に基づくと、管腔内の流量は内径の4乗に比例し長さに反比例するため、ステントの内腔径や線維柱帯 切開の範囲が流量を決定する重要な因子となる。
一方、濾過手術 (線維柱帯切除術 ・チューブシャント )は房水 を結膜 下腔に排出するため、上強膜 静脈圧の制約を受けず、より低い目標眼圧 (10mmHg以下)を達成できる。このことが、進行緑内障 で低い目標眼圧 が必要な症例にはMIGS が不十分となる理論的根拠である。
線維柱帯切開術 の効果は切開範囲に依存するが、120〜180°を超えると用量反応閾値に達するとされる。房水 流出は隅角 の全周で均一ではなく、特に鼻側・下方セグメントの流出路活性が高い。集合管の分布密度も部位によって異なり、流出路が豊富なセグメントを選択的に切開することで効率的な眼圧 下降が期待できる。このため180°の処置(ヘミGAT T等)でも十分な効果が得られる場合がある。
MIGS を含むすべての緑内障 手術において、眼圧 下降効果は経時的に減弱する傾向がある3) 。ステント型デバイスでは周辺虹彩前癒着 やデバイス閉塞が起こりうる。線維柱帯切開術 では炎症反応に起因する線維血管膜の形成や瘢痕化により、切開部位の再狭窄が生じることがある。このため、緑内障 は生涯にわたる疾患であり、単一の手術で完治するものではない3) 。MIGS は結膜 切開を伴わないため、将来の濾過手術 (線維柱帯切除術 やチューブシャント )の成功率を損なわないという重要な利点がある3) 。
ピロカルピンは最も古い眼圧 下降薬の一つであるが、MIGS 後に流出効果の維持を期待して使用されることがあり、低侵襲緑内障手術 後の管理においても重要な位置づけを占める。1〜2%ピロカルピン点眼はMIGS 後の初期に隅角 の開放を維持し、前房出血 の早期消退にも寄与するとされる。
MIGS 研究における臨床エンドポイントの報告方法は統一されておらず、異なる研究間の比較が困難であった4) 。AAO Glaucoma PPP Committeeは、2年時点のKaplan-Meier生存分析による累積成功率を主要評価項目とすることを推奨している4) 。
単独MIGS の成功基準 : 眼圧 21mmHg以下かつベースラインから20%以上低下、緑内障 薬剤増加なし、追加手術なし、光覚喪失なし、低眼圧 なし4)
CE-IOL 併用MIGS の成功基準 : 薬剤1剤以上の減量(眼圧 上昇なし)、または眼圧 21mmHg以下かつ20%以上低下4)
2年時累積成功率の最小臨床的有意差(MCI D)として、単独MIGS ≥50%、CE-IOL 併用MIGS ≥65%が提案されている4) 。
従来、閉塞隅角緑内障 はMIGS の禁忌とされてきたが、近年はより多くの患者がMIGS の恩恵を受けられるとの考えから、この見解は変化しつつある3) 。
MIGS 後の患者報告アウトカムに関する研究は限られているが、視覚機能・生活の質・眼表面の健康の改善を示唆する予備的知見が得られている6) 。薬剤負担の軽減は患者の眼表面の改善や治療アドヒアランス 向上に寄与する可能性がある6) 。
40研究のレビューでは、MIGS -phaco併用で22.6〜80%の患者が薬剤フリーとなり、点眼薬による眼表面障害(角膜上皮 障害・結膜 充血 ・マイボーム腺機能不全 など)の軽減が生活の質の改善に寄与すると考えられている6) 。特に多剤併用(3剤以上)中の患者では、MIGS 後の薬剤減量による恩恵が大きい。標準化された患者報告アウトカム指標の開発と多様な人種集団を対象とした研究が今後の課題である6) 。
CyPass Micro-Stent(脈絡膜 上腔MIGS )は5年後の角膜内皮 細胞減少が判明し、2018年に市場から自主撤退した先例がある3) 。MIGS 全般にわたり、長期の安全性・費用対効果・薬剤非依存率に関するデータの蓄積が今後の課題である3) 7) 。
Freeman-Sheldon症候群に合併した若年性開放隅角緑内障 に対しKDBを施行し、眼圧 が40mmHgから10mmHgに低下、27ヶ月にわたり15mmHg未満で安定した報告がある。MIGS の従来適応を超えた特殊な病型への拡大が検討されている。
KDBによる線維柱帯 切除と深層強膜切除術 の併用では、術後眼圧 が上強膜 静脈圧以下に低下したことで大量の前房出血 とフィブリン塊を生じ、周辺虹彩前癒着 や集合管閉塞に至った症例が報告されている。眼圧 を大幅に下降させる手技同士の併用には注意が必要であり、KDB単独の眼圧 下降率約28.4%に対し、併用群では有意な上乗せ効果は得られなかったとされる。
ELIOS : 高精度の非熱的レーザーを用いて線維柱帯 に10個のマイクロチャネルを作成する新技術である。冷温レーザーにより組織の線維化を最小限に抑え、8年にわたる眼圧 下降維持が報告されている。術後1年時点で80%の患者が薬物治療を中止できたとされるMIMS (低侵襲ミニ強膜 切開術) : ステントを使用しないab externoの濾過手術 で、300μmの三角形刃を備えた600μm針で強膜 角膜 ドレナージ管を永久的に作成する。結果は有望であるが現在も研究段階にある
Q
MIGS後に再手術は必要ですか?
A
MIGS の効果はすべての緑内障 手術と同様に時間とともに減弱する可能性があります。単独MIGS では2年時に最大24%で再手術が必要となったとの報告があります6) 。白内障 手術との併用では再手術率が3%と大幅に低下します6) 。MIGS は結膜 を温存するため、将来的に線維柱帯切除術 やチューブシャント などの追加手術が必要になった場合にもその成功率を損なわないという利点があります。
日本緑内障 学会. 緑内障 診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
白内障 手術併用眼内ドレーン会議. 白内障 手術併用眼内ドレーン使用要件等基準(第3版). 日眼会誌. 2024;128:1013-1016.European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Gedde SJ, et al. Reporting Clinical Endpoints in Studies of Minimally Invasive Glaucoma Surgery. Ophthalmology. 2025;132(2):143-151.
Paik JM, et al. Outcomes and Complications of Minimally Invasive Glaucoma Surgery: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2025;19:487-503.
Singh A, et al. Minimally Invasive Glaucoma Surgery: A Review of Clinical and Patient-Reported Outcomes. Cureus. 2025;17(7):e87872.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern. 2020.
Samuelson TW, et al. Prospective, randomized, controlled pivotal trial of an ab interno implanted trabecular micro-bypass in primary open-angle glaucoma and cataract: two-year results. Ophthalmology. 2019;126:811-821.
Samuelson TW, et al. A Schlemm canal microstent for intraocular pressure reduction in primary open-angle glaucoma and cataract: the HORIZON Study. Ophthalmology. 2019;126:29-37.
Ahmed IIK , et al. A prospective randomized trial comparing hydrus and iStent microinvasive glaucoma surgery implants for standalone treatment of open-angle glaucoma: the COMPARE Study. Ophthalmology. 2020;127:52-61.
Falkenberry SM, et al. CE-IOL plus KDB vs CE-IOL plus iStent : 1-year multicenter RCT results. Ophthalmology. 2020.
Maheshwari D, et al. CE-IOL plus Tanito Microhook vs CE-IOL alone: a randomized single-center trial. 2023.
Sachdeva N, et al. Early to late explantation of Hydrus microstent MIGS device: A case series. Am J Ophthalmol Case Rep. 2024;36:102105.
Otsuka M, et al. Gas Tamponade Improved Cilio-Choroidal Effusion Induced by an Ab Interno Trabeculotomy with a Microhook: Two Cases. Int Med Case Rep J. 2024;17:479-486.