
発達緑内障(先天緑内障)(Developmental Glaucoma)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 発達緑内障とは
Section titled “1. 発達緑内障とは”発達緑内障(developmental glaucoma)は、房水流出路の発育異常に基づく緑内障である。発症時期により早発型発達緑内障と遅発型発達緑内障に分類される1)。
早発型は従来の原発先天緑内障(primary congenital glaucoma; PCG)に相当する。眼圧上昇の原因が線維柱帯の発達異常に限定され、3〜4歳以前に発症して角膜径の拡大(牛眼)を伴う。遅発型は隅角・線維柱帯の発達異常が軽度であるため発症が遅れ、原発開放隅角緑内障に類似した経過をたどる。10〜20歳代に発症する。
小児緑内障には複数の分類体系が存在する。緑内障診療ガイドラインでは早発型・遅発型・その他の先天異常を伴う発達緑内障の3型に分類する1)。国際的にはChildhood Glaucoma Research Network(CGRN)が策定した分類が世界緑内障学会(WGA)および米国眼科委員会(ABO)に採用されている2)。
| 分類 | 日本分類 | CGRN分類 |
|---|---|---|
| 原発・早期発症 | 早発型発達緑内障 | 原発先天緑内障(PCG) |
| 原発・遅発 | 遅発型発達緑内障 | 若年開放隅角緑内障(JOAG) |
| 先天異常合併 | その他の先天異常を伴う発達緑内障 | 続発:先天眼形成異常関連 |
| 全身疾患合併 | (上記に含む) | 続発:先天全身疾患関連 |
| 後天要因 | (上記に含む) | 続発:後天要因 |
| 術後 | (上記に含む) | 続発:白内障術後 |
PCGはさらに発症年齢により新生児期(0〜1か月)、乳児期(1〜24か月)、遅発性(2歳以上)に細分される2)。JOAGは4歳以降に発症し、眼球拡大を伴わず正常な隅角外観を呈する2)。
続発小児緑内障には、Axenfeld-Rieger異常・Peters異常・無虹彩症に伴う先天眼形成異常関連緑内障、Sturge-Weber症候群・Down症候群に伴う先天全身疾患関連緑内障、ぶどう膜炎・外傷・ステロイドに続発する後天要因緑内障、白内障術後緑内障が含まれる2)。
小児緑内障は小児期の失明原因の5%を占め、世界中で30万人以上が罹患している2)。
早発型の発症頻度は出生10万人あたり1.8〜2.4人(日本)であり、欧米では5〜10人と報告されている。血族結婚の多いスロバキアのロマ人では最も頻度が高く、出生10万人あたり80人である。75%が両眼性で、65%が男児に発症する。80%の症例が生後1年以内に発症する。大部分は孤発例であるが、約10〜40%に遺伝性を認め、常染色体劣性遺伝形式をとる。
大規模なオーストラレシアの疾患レジストリ(ANZRAG: 660名)では、小児緑内障のうちPCGが57.6%、JOAGが19.3%を占めた3)。PCGの診断年齢中央値は0.25歳、JOAGは14歳であった3)。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”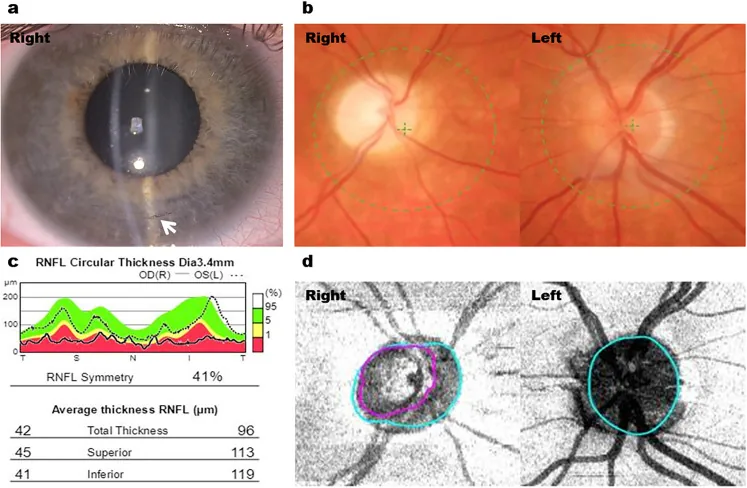
MIGS手技の小児応用
Section titled “MIGS手技の小児応用”低侵襲緑内障手術(MIGS)は結膜を温存する手技であり、将来の追加手術の選択肢を残す利点から小児への応用が進んでいる。ただしエビデンスは限定的である。
- KDB(Kahook Dual-Blade)ゴニオトミー:小児PCGへの応用が報告されている7)
- Trab360:小児緑内障に対する線維柱帯切開系手技として報告されている8)
- PreserFlo外路マイクロシャント:難治性小児緑内障への補助的選択肢として小規模報告がある9)
薬物の選択は成人開放隅角緑内障と同様であるが、小児特有の注意点がある。
- プロスタグランジン(PG)関連薬:小児ではノンレスポンダーが多いが、安全面と1日1回の点眼回数で有利
- β遮断薬:できるだけ低濃度のものを使用する。気管支喘息・徐脈の副作用に注意。新生児では無呼吸の報告がある
- 炭酸脱水酵素阻害薬(CAI):内服はアセタゾラミド5 mg/kg/日を3分服。眼圧下降効果が大きいが、長期使用で代謝性アシドーシスや発育不全を生じうる。点眼薬は副作用が少ないが効果も小さい
- 術後のピロカルピン:1〜2%を1日2〜3回、数週間使用する。周辺虹彩前癒着の予防が目的
遅発型発達緑内障の治療
Section titled “遅発型発達緑内障の治療”学童期以降であれば、まず薬物療法を試みる。早発型に比べ隅角異常が軽度であるため、薬物による治療効果は高い。
- 第一選択薬:PG関連薬(ラタノプロスト等)
- 第二選択薬:CAI点眼、またはβ遮断薬(副作用の自覚症状を的確に表現できる小児に限る)
- 眼圧が25 mmHgを超える場合:最初からPG関連薬を使用し、必要に応じてβ遮断薬やCAIを追加する
手術適応は慎重に判断する。眼圧の時期的変動が大きいため、30〜40 mmHg以上の高眼圧が数週間持続し薬物で降圧不良の場合、または眼圧が20 mmHg程度でも視野障害が末期の場合に手術を考慮する1)。
目標眼圧と長期管理
Section titled “目標眼圧と長期管理”目標眼圧は19〜20 mmHg以下が望ましいとされる。
眼圧コントロール後も長期的な管理が必要である。視機能の発達への配慮として、定期的な屈折検査・視力検査を行い、必要に応じて弱視治療や斜視治療を施行する。視力不良の最大原因は弱視であり、早期からの適切な屈折矯正や視能訓練が重要である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”隅角形成異常の組織学的所見
Section titled “隅角形成異常の組織学的所見”早発型発達緑内障の病理は以下のように要約される。
- 傍Schlemm管結合組織の異常肥厚:線維柱帯の発達が未熟であるため、傍Schlemm管結合組織が異常に厚い
- 細胞外マトリックスの蓄積:コラーゲン・エラスチン様線維と大量の無定形物質で構成される非層板状のコンパクトな組織がSchlemm管下に存在する。細胞突起の短い線維柱帯細胞、線維成分、基底板様物質からなる
- 毛様体の異常付着:毛様体が線維柱帯部位に付着し、筋収縮が強膜岬を前方に引いてSchlemm管および線維柱帯を圧迫する
- 虹彩根部の異所性:虹彩根部が線維柱帯の位置に存在する
- Schlemm管の発達不全:Schlemm管が存在しないか発達が不完全な症例がある
発生学的に線維柱帯細胞は神経堤由来であるのに対し、傍Schlemm管結合組織は血管内皮細胞由来である。起源の異なる組織の隣接点に最大の房水流出抵抗が存在する。
trabecular sheet(シート状物質)が圧縮されて線維柱帯の前に存在し房水流出を阻害するとともに、虹彩をつり上げて隅角拡大を防ぐことが発達緑内障特有の隅角所見の原因と推測されている。
眼球拡大の機序
Section titled “眼球拡大の機序”乳幼児の眼球被膜は弾性に富む。高眼圧が持続すると角結膜移行部を中心に眼球被膜が伸展され、角膜径が増大する(牛眼)。同時に、角膜実質に比し弾性の低いDescemet膜に破裂(Haab striae)が生じ、前房水が角膜実質や上皮に流入して角膜浮腫・混濁が急激に増悪する。
眼圧コントロール不良が持続すると、Zinn小帯の破裂による水晶体偏位、角膜びらん・潰瘍、眼球破裂のリスクも生じる。
小児で隅角手術が有効な理由
Section titled “小児で隅角手術が有効な理由”線維柱帯切開術は先天緑内障で有効性が高いとされる5)。この差異は小児の隅角に豊富に存在する弾性線維に起因すると考えられている。弾性線維が隅角構造の開口を促進し、術後の房水流出路の開存性を維持する5)。
外路線維柱帯切開術後には、Schlemm管の開存性が長期成績に関わるとされる5)。術後不成功の主な原因は、Schlemm管内壁の線維性増殖およびSchlemm管内皮の伸長である5)。
遺伝子異常と隅角発生
Section titled “遺伝子異常と隅角発生”CYP1B1はチトクロムP450ファミリーに属する酵素をコードする遺伝子であり、胎児期の眼球前眼部組織に高発現する。CYP1B1変異例ではチロシン代謝経路に異常が生じ、隅角組織の正常な分化・成熟が阻害されると推定されている。CYP1B1変異はPCGのみならず、JOAGや先天眼形成異常関連緑内障でも報告されている3)。
近年、TEK/ANGPT1変異が新たに同定された2)。TEKはSchlemm管内皮の発生・維持に関わる受容体型チロシンキナーゼをコードしており、PCGの新たな分子経路の関与が示唆されている。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”新しいMIGSデバイスの小児応用
Section titled “新しいMIGSデバイスの小児応用”PreserFlo外路マイクロシャントは前房から結膜下腔に房水をシャントするデバイスである。難治性小児緑内障への使用は小規模報告にとどまり、標準治療としての位置づけは今後の検証を要する9)。
OMNIサージカルシステムはTM切開と粘弾性物質のSchlemm管・コレクターチャネルへの注入(ビスコカナロストミー)を組み合わせた手技であり、Sturge-Weber症候群に伴う緑内障の生後4か月児への使用が報告されている。
外路から内路手技へのパラダイムシフトが進行している5)。内路手技は結膜弁・強膜弁の作製が不要で結膜を温存できるため、将来の追加手術の選択肢を残す戦略として有用である。
遺伝学的研究の進展
Section titled “遺伝学的研究の進展”TEK/ANGPT1変異がPCGの新規分子経路として同定され、Schlemm管の発生・維持に関わるメカニズムの解明が進んでいる2)。CYP1B1遺伝子に関する研究は小児緑内障領域で最も高い学術的関心を集めており、1955年から2022年までの文献計量分析では分子遺伝学が主要研究テーマ25編中13編を占めた6)。
現在の年齢別分類は予後の予測には有用であるが、遺伝的背景を考慮していない点が課題として指摘されている2)。遺伝子検査の普及により、表現型と遺伝型の対応に基づく新たな分類体系の構築が期待される。
QOL研究の動向
Section titled “QOL研究の動向”Stinglら(2024)のシステマティックレビューでは、小児緑内障コホートで使用された患者報告アウトカム尺度(PROM)10種を同定した。7種が最高品質評価5/7を達成したが、いずれも開発過程で小児緑内障患者の視点が含まれていなかった4)。小児緑内障に特異的なPROMの開発が求められている。
小児緑内障のQOLは視力障害のみならず、繰り返す手術、継続的な点眼治療、遺伝性への不安、将来の職業選択への影響など多面的な因子に影響される4)。
8. 参考文献
Section titled “8. 参考文献”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
