
Glaucoma dello sviluppo (glaucoma congenito) (Developmental Glaucoma)
Punti chiave in sintesi
Sezione intitolata “Punti chiave in sintesi”1. Cos’è il glaucoma dello sviluppo?
Sezione intitolata “1. Cos’è il glaucoma dello sviluppo?”Il glaucoma dello sviluppo (developmental glaucoma) è un glaucoma dovuto a un’anomalia dello sviluppo della via di deflusso dell’umore acqueo. In base all’età di insorgenza, si classifica in glaucoma dello sviluppo precoce e tardivo1).
Il tipo precoce corrisponde al classico glaucoma congenito primario (primary congenital glaucoma; PCG). La causa dell’aumento della pressione intraoculare è limitata a un’anomalia dello sviluppo del trabecolato, insorge prima dei 3-4 anni e si accompagna a un aumento del diametro corneale (buftalmo). Il tipo tardivo presenta un’anomalia dello sviluppo dell’angolo e del trabecolato meno grave, quindi l’insorgenza è ritardata e segue un decorso simile al glaucoma primario ad angolo aperto. Insorge tra i 10 e i 20 anni.
Sistema di classificazione
Sezione intitolata “Sistema di classificazione”Esistono diversi sistemi di classificazione per il glaucoma pediatrico. Le linee guida per il glaucoma classificano il glaucoma dello sviluppo in tre tipi: precoce, tardivo e con altre anomalie congenite associate1). A livello internazionale, la classificazione elaborata dal Childhood Glaucoma Research Network (CGRN) è adottata dalla World Glaucoma Association (WGA) e dall’American Board of Ophthalmology (ABO)2).
| Classificazione | Classificazione giapponese | Classificazione CGRN |
|---|---|---|
| Primario/insorgenza precoce | Glaucoma dello sviluppo precoce | Glaucoma congenito primario (PCG) |
| Primario/tardivo | Glaucoma dello sviluppo tardivo | Glaucoma giovanile ad angolo aperto (JOAG) |
| Con anomalie congenite | Glaucoma dello sviluppo con altre anomalie congenite | Secondario: correlato a malformazione oculare congenita |
| Con malattie sistemiche | (incluso sopra) | Secondario: correlato a malattia sistemica congenita |
| Fattori acquisiti | (incluso sopra) | Secondario: fattori acquisiti |
| Post-operatorio | (incluso sopra) | Secondario: dopo intervento di cataratta |
Il PCG è ulteriormente suddiviso in base all’età di insorgenza in neonatale (0-1 mese), infantile (1-24 mesi) e tardivo (≥2 anni)2). Il JOAG insorge dopo i 4 anni, senza ingrandimento del bulbo oculare e con aspetto angolare normale2).
Il glaucoma secondario infantile comprende il glaucoma correlato a malformazione oculare congenita associato ad anomalia di Axenfeld-Rieger, anomalia di Peters e aniridia; il glaucoma correlato a malattia sistemica congenita associato a sindrome di Sturge-Weber e sindrome di Down; il glaucoma da fattori acquisiti secondario a uveite, trauma o steroidi; e il glaucoma post-operatorio dopo intervento di cataratta2).
Epidemiologia
Sezione intitolata “Epidemiologia”Il glaucoma infantile rappresenta il 5% delle cause di cecità in età pediatrica e colpisce oltre 300.000 persone in tutto il mondo2).
L’incidenza del tipo precoce è di 1,8-2,4 per 100.000 nati (Giappone), mentre in Europa e negli Stati Uniti è riportata tra 5 e 10. La frequenza più alta si osserva nei Rom slovacchi, dove i matrimoni consanguinei sono frequenti, con 80 per 100.000 nati. Il 75% dei casi è bilaterale e il 65% si verifica nei maschi. L’80% dei casi si manifesta entro il primo anno di vita. La maggior parte sono sporadici, ma circa il 10-40% presenta ereditarietà con modalità autosomica recessiva.
In un ampio registro australasiatico di malattie (ANZRAG: 660 pazienti), il PCG rappresentava il 57,6% dei glaucomi infantili e il JOAG il 19,3%3). L’età mediana alla diagnosi era di 0,25 anni per il PCG e di 14 anni per il JOAG3).
Secondo le linee guida per il glaucoma, viene classificato in tre tipi: precoce, tardivo e glaucoma dello sviluppo associato ad altre anomalie congenite1). A livello internazionale, la classificazione CGRN è lo standard, che comprende il glaucoma congenito primario (PCG), il glaucoma giovanile ad angolo aperto (JOAG) e quattro tipi secondari (malformazioni oculari congenite, malattie sistemiche congenite, fattori acquisiti, post-cataratta)2). Il PCG è il tipo più comune di glaucoma infantile, rappresentando circa il 60%.
2. Principali sintomi e segni clinici
Sezione intitolata “2. Principali sintomi e segni clinici”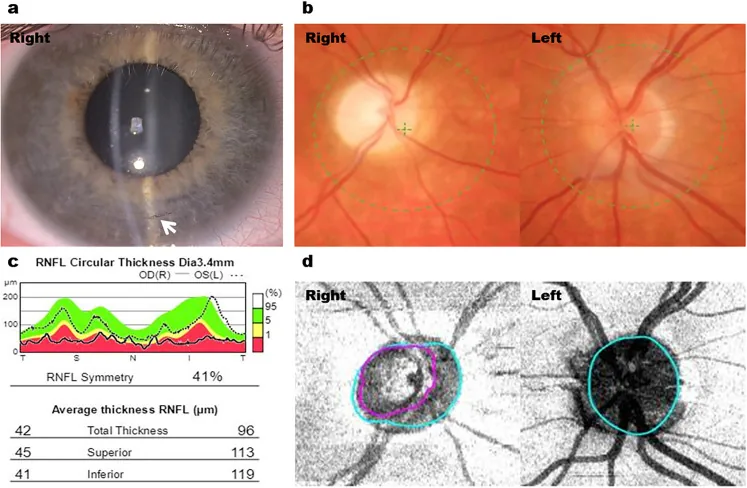
Applicazione pediatrica delle tecniche MIGS
Sezione intitolata “Applicazione pediatrica delle tecniche MIGS”La chirurgia mini-invasiva del glaucoma (MIGS) è una tecnica che preserva la congiuntiva, lasciando aperte le opzioni per futuri interventi aggiuntivi, favorendone l’applicazione nei bambini. Tuttavia, le evidenze sono limitate.
- Goniotomia KDB (Kahook Dual-Blade): è stata riportata l’applicazione nel PCG pediatrico7)
- Trab360: riportato come procedura di trabeculotomia per il glaucoma infantile8)
- Micro-shunt esterno PreserFlo: piccoli report come opzione aggiuntiva per il glaucoma infantile refrattario9)
Terapia farmacologica
Sezione intitolata “Terapia farmacologica”La scelta dei farmaci è simile a quella del glaucoma ad angolo aperto dell’adulto, ma ci sono considerazioni speciali nei bambini.
- Farmaci correlati alle prostaglandine (PG): nei bambini molti non-responder, ma vantaggiosi per sicurezza e frequenza di instillazione una volta al giorno
- Beta-bloccanti: utilizzare la concentrazione più bassa possibile. Attenzione agli effetti collaterali: asma bronchiale, bradicardia. Nei neonati sono stati riportati casi di apnea
- Inibitori dell’anidrasi carbonica (CAI): per via orale acetazolamide 5 mg/kg/die in 3 dosi. Effetto ipotensivo oculare marcato, ma l’uso prolungato può causare acidosi metabolica o ritardo della crescita. I colliri hanno meno effetti collaterali ma anche minore efficacia
- Pilocarpina post-operatoria: 1-2% 2-3 volte al giorno per alcune settimane. Scopo: prevenire le sinechie anteriori periferiche
Trattamento del glaucoma evolutivo tardivo
Sezione intitolata “Trattamento del glaucoma evolutivo tardivo”Dall’età scolare in poi, si può prima tentare una terapia farmacologica. Rispetto alla forma precoce, le anomalie dell’angolo sono più lievi, quindi il trattamento farmacologico è più efficace.
- Terapia di prima linea: farmaci correlati alle PG (es. latanoprost)
- Terapia di seconda linea: collirio CAI o beta-bloccante (solo in bambini in grado di descrivere accuratamente i sintomi soggettivi degli effetti collaterali)
- Se la pressione intraoculare supera i 25 mmHg: iniziare direttamente con un farmaco PG, quindi aggiungere un beta-bloccante o un CAI se necessario
L’indicazione chirurgica va valutata con cautela. A causa delle ampie fluttuazioni temporali della pressione intraoculare, si considera l’intervento in caso di ipertensione oculare di 30-40 mmHg o superiore persistente per diverse settimane e scarsamente controllata dai farmaci, o in caso di danno terminale del campo visivo anche con pressione intorno a 20 mmHg1).
Pressione intraoculare target e gestione a lungo termine
Sezione intitolata “Pressione intraoculare target e gestione a lungo termine”La pressione intraoculare target è considerata desiderabile al di sotto di 19-20 mmHg.
Dopo il controllo della pressione intraoculare, è necessaria una gestione a lungo termine. Per lo sviluppo della funzione visiva, eseguire regolari esami della refrazione e dell’acuità visiva e, se necessario, trattare l’ambliopia o lo strabismo. La causa principale della scarsa acuità visiva è l’ambliopia, quindi sono importanti una precoce correzione refrattiva adeguata e un training ortottico.
Nel glaucoma dello sviluppo precoce (glaucoma congenito primario), la chirurgia è la prima scelta, e si esegue una goniotomia o una trabeculotomia 1). Il tasso di successo è del 65-96%, migliore nei casi che si manifestano tra 1 e 24 mesi di vita. La terapia farmacologica viene utilizzata per ridurre l’edema corneale preoperatorio o come supporto postoperatorio. Nelle forme tardive, si prova prima la terapia farmacologica dopo l’età scolare. In tutti i tipi, l’intervento precoce e la gestione a lungo termine dell’ambliopia sono essenziali per preservare la funzione visiva.
6. Fisiopatologia e meccanismi patogenetici dettagliati
Sezione intitolata “6. Fisiopatologia e meccanismi patogenetici dettagliati”Reperti istologici dell’anomalia dell’angolo iridocorneale
Sezione intitolata “Reperti istologici dell’anomalia dell’angolo iridocorneale”La patologia del glaucoma dello sviluppo precoce può essere riassunta come segue:
- Ispessimento anomalo del tessuto connettivo iuxtacanalicolare: a causa dello sviluppo immaturo del trabecolato, il tessuto connettivo iuxtacanalicolare è anormalmente spesso.
- Accumulo di matrice extracellulare: un tessuto compatto non lamellare composto da collagene, fibre simil-elastina e una grande quantità di sostanza amorfa si trova sotto il canale di Schlemm. È costituito da cellule trabecolari con brevi prolungamenti, componenti fibrosi e sostanza simile alla membrana basale.
- Inserzione anomala del corpo ciliare: il corpo ciliare si attacca a livello del trabecolato e la contrazione muscolare tira lo sperone sclerale in avanti, comprimendo il canale di Schlemm e il trabecolato.
- Ectopia della radice dell’iride: la radice dell’iride si trova in corrispondenza del trabecolato.
- Sviluppo insufficiente del canale di Schlemm: in alcuni casi il canale di Schlemm è assente o sviluppato in modo incompleto.
Embriologicamente, le cellule trabecolari derivano dalla cresta neurale, mentre il tessuto connettivo iuxtacanalicolare deriva dalle cellule endoteliali vascolari. La massima resistenza al deflusso dell’umore acqueo si trova nel punto di contatto di questi tessuti di diversa origine.
Si ipotizza che il foglio trabecolare (sostanza lamellare) sia compresso e si trovi davanti al trabecolato, ostacolando il deflusso dell’umore acqueo e sollevando l’iride, impedendo l’ampliamento dell’angolo, causando così i reperti angolari caratteristici del glaucoma dello sviluppo.
Meccanismo dell’ingrandimento del bulbo oculare
Sezione intitolata “Meccanismo dell’ingrandimento del bulbo oculare”La capsula oculare dei neonati è molto elastica. Una pressione intraoculare elevata persistente stira la capsula oculare intorno alla giunzione corneo-congiuntivale, aumentando il diametro corneale (buftalmo). Contemporaneamente, la membrana di Descemet, meno elastica dello stroma corneale, si rompe (strie di Haab) e l’umore acqueo penetra nello stroma e nell’epitelio corneale, aggravando bruscamente l’edema e l’opacità corneale.
Se il controllo della pressione intraoculare rimane scarso, esiste anche il rischio di lussazione del cristallino per rottura della zonula di Zinn, erosione/ulcera corneale e rottura del bulbo oculare.
Perché la chirurgia dell’angolo è efficace nei bambini
Sezione intitolata “Perché la chirurgia dell’angolo è efficace nei bambini”La trabeculotomia è considerata altamente efficace nel glaucoma congenito 5). Questa differenza è attribuita alle abbondanti fibre elastiche presenti nell’angolo del bambino. Le fibre elastiche favoriscono l’apertura delle strutture angolari e mantengono la pervietà delle vie di deflusso dell’umore acqueo dopo l’intervento 5).
Dopo la trabeculotomia esterna, la pervietà del canale di Schlemm è correlata ai risultati a lungo termine 5). Le principali cause di insuccesso postoperatorio sono la proliferazione fibrosa della parete interna del canale di Schlemm e lo stiramento dell’endotelio del canale di Schlemm 5).
Anomalie genetiche e sviluppo dell’angolo
Sezione intitolata “Anomalie genetiche e sviluppo dell’angolo”CYP1B1 è un gene che codifica per un enzima della famiglia del citocromo P450, altamente espresso nei tessuti del segmento anteriore dell’occhio fetale. Nei casi di mutazione di CYP1B1, si verifica un’anomalia nella via metabolica della tirosina, che si presume inibisca la normale differenziazione e maturazione del tessuto angolare. Le mutazioni di CYP1B1 sono state riportate non solo nel PCG, ma anche nel JOAG e nel glaucoma associato a anomalie congenite dello sviluppo oculare 3).
Recentemente, sono state identificate nuove mutazioni TEK/ANGPT1 2). TEK codifica per un recettore tirosin-chinasi coinvolto nello sviluppo e nel mantenimento dell’endotelio del canale di Schlemm, suggerendo il coinvolgimento di una nuova via molecolare nel PCG.
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Nuovi dispositivi MIGS per bambini
Sezione intitolata “Nuovi dispositivi MIGS per bambini”Il micro-shunt esterno PreserFlo è un dispositivo che devia l’umore acqueo dalla camera anteriore allo spazio sottocongiuntivale. Il suo utilizzo nel glaucoma pediatrico refrattario è limitato a segnalazioni su piccola scala, e la sua posizione come trattamento standard richiede una futura validazione 9).
Il sistema chirurgico OMNI combina un’incisione del TM con l’iniezione di sostanza viscoelastica nel canale di Schlemm e nei canali collettori (viscocanalostomia), ed è stato riportato il suo utilizzo in un lattante di 4 mesi con glaucoma associato alla sindrome di Sturge-Weber.
È in corso un cambiamento di paradigma dalle procedure esterne a quelle interne 5). Le procedure interne non richiedono la creazione di lembi congiuntivali o sclerali e preservano la congiuntiva, il che è utile come strategia per lasciare opzioni per futuri interventi chirurgici aggiuntivi.
Progressi nella ricerca genetica
Sezione intitolata “Progressi nella ricerca genetica”Le mutazioni TEK/ANGPT1 sono state identificate come una nuova via molecolare del PCG, e la comprensione dei meccanismi coinvolti nello sviluppo e nel mantenimento del canale di Schlemm sta progredendo 2). La ricerca sul gene CYP1B1 attira il maggiore interesse accademico nel campo del glaucoma pediatrico, e in un’analisi bibliometrica dal 1955 al 2022, la genetica molecolare rappresentava 13 dei 25 principali temi di ricerca 6).
L’attuale classificazione per età è utile per la prognosi, ma è stato sottolineato che non considera il background genetico, il che rappresenta una sfida 2). Con la diffusione dei test genetici, si spera nella costruzione di un nuovo sistema di classificazione basato sulla corrispondenza tra fenotipo e genotipo.
Tendenze della ricerca sulla qualità della vita
Sezione intitolata “Tendenze della ricerca sulla qualità della vita”In una revisione sistematica di Stingl et al. (2024), sono state identificate 10 misure di esito riportate dal paziente (PROM) utilizzate in coorti di glaucoma pediatrico. Sette hanno raggiunto il punteggio di qualità massimo di 5/7, ma nessuna includeva il punto di vista dei pazienti con glaucoma pediatrico nel processo di sviluppo 4). È necessario lo sviluppo di PROM specifiche per il glaucoma pediatrico.
La qualità della vita nel glaucoma pediatrico è influenzata non solo dalla disabilità visiva, ma anche da fattori multidimensionali come interventi chirurgici ripetuti, trattamento continuo con colliri, preoccupazione per l’ereditarietà e impatto sulla futura scelta professionale 4).
8. Riferimenti
Sezione intitolata “8. Riferimenti”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
