
Glaucoma de Desenvolvimento (Glaucoma Congênito)
Pontos Principais em Resumo
Seção intitulada “Pontos Principais em Resumo”1. O que é glaucoma de desenvolvimento
Seção intitulada “1. O que é glaucoma de desenvolvimento”O glaucoma de desenvolvimento (developmental glaucoma) é um glaucoma causado por uma anormalidade no desenvolvimento da via de drenagem do humor aquoso. De acordo com a época de início, é classificado em glaucoma de desenvolvimento de início precoce e glaucoma de desenvolvimento de início tardio1).
O tipo de início precoce corresponde ao glaucoma congênito primário (PCG) clássico. A causa do aumento da pressão intraocular é limitada a uma anormalidade no desenvolvimento do trabeculado, ocorrendo antes dos 3-4 anos de idade com aumento do diâmetro da córnea (olho de boi). O tipo de início tardio apresenta anormalidade leve do ângulo e do trabeculado, portanto o início é retardado, e o curso é semelhante ao glaucoma primário de ângulo aberto. Ocorre na segunda e terceira décadas de vida.
Sistema de classificação
Seção intitulada “Sistema de classificação”Existem vários sistemas de classificação para glaucoma infantil. As diretrizes de prática clínica para glaucoma classificam em três tipos: início precoce, início tardio e glaucoma de desenvolvimento com outras anomalias congênitas1). Internacionalmente, a classificação estabelecida pela Childhood Glaucoma Research Network (CGRN) foi adotada pela World Glaucoma Association (WGA) e pelo American Board of Ophthalmology (ABO)2).
| Classificação | Classificação Japonesa | Classificação CGRN |
|---|---|---|
| Primário de início precoce | Glaucoma de desenvolvimento de início precoce | Glaucoma congênito primário (PCG) |
| Primário de início tardio | Glaucoma de desenvolvimento de início tardio | Glaucoma juvenil de ângulo aberto (JOAG) |
| Com anomalias congênitas | Glaucoma de desenvolvimento com outras anomalias congênitas | Secundário: relacionado a malformações oculares congênitas |
| Com doenças sistêmicas | (Incluído acima) | Secundário: relacionado a doenças sistêmicas congênitas |
| Fatores adquiridos | (Incluído acima) | Secundário: fatores adquiridos |
| Pós-operatório | (Incluído acima) | Secundário: pós-cirurgia de catarata |
O PCG é ainda subdividido por idade de início em neonatal (0–1 mês), infantil (1–24 meses) e tardio (≥2 anos)2). O JOAG inicia após os 4 anos de idade, sem aumento do globo ocular e com aspecto angular normal2).
O glaucoma secundário infantil inclui: glaucoma relacionado a malformações oculares congênitas como anomalia de Axenfeld-Rieger, anomalia de Peters e aniridia; glaucoma relacionado a doenças sistêmicas congênitas como síndrome de Sturge-Weber e síndrome de Down; glaucoma devido a fatores adquiridos como uveíte, trauma e esteroides; e glaucoma pós-cirurgia de catarata2).
Epidemiologia
Seção intitulada “Epidemiologia”O glaucoma pediátrico representa 5% das causas de cegueira na infância e afeta mais de 300.000 pessoas em todo o mundo2).
A incidência do tipo de início precoce é de 1,8 a 2,4 por 100.000 nascidos vivos (no Japão), enquanto na Europa e América é relatada como 5 a 10. A maior incidência é entre os ciganos eslovacos devido a casamentos consanguíneos, com 80 por 100.000 nascidos vivos. 75% dos casos são bilaterais e 65% ocorrem em meninos. 80% dos casos se manifestam no primeiro ano de vida. A maioria dos casos é esporádica, mas cerca de 10 a 40% são hereditários, com padrão autossômico recessivo.
Em um grande registro de doenças da Australásia (ANZRAG: 660 pacientes), o glaucoma congênito primário (PCG) representou 57,6% e o glaucoma juvenil de ângulo aberto (JOAG) 19,3% dos glaucomas pediátricos3). A mediana de idade ao diagnóstico para PCG foi de 0,25 anos e para JOAG foi de 14 anos3).
As diretrizes de prática clínica para glaucoma classificam o glaucoma de desenvolvimento em três tipos: início precoce, início tardio e glaucoma de desenvolvimento com outras anomalias congênitas1). Internacionalmente, a classificação CGRN é o padrão, dividindo o glaucoma em glaucoma congênito primário (PCG), glaucoma juvenil de ângulo aberto (JOAG) e quatro tipos secundários (malformações oculares congênitas, doenças sistêmicas congênitas, fatores adquiridos, pós-cirurgia de catarata)2). O PCG representa cerca de 60% dos glaucomas pediátricos, sendo o tipo mais comum.
2. Principais sintomas e achados clínicos
Seção intitulada “2. Principais sintomas e achados clínicos”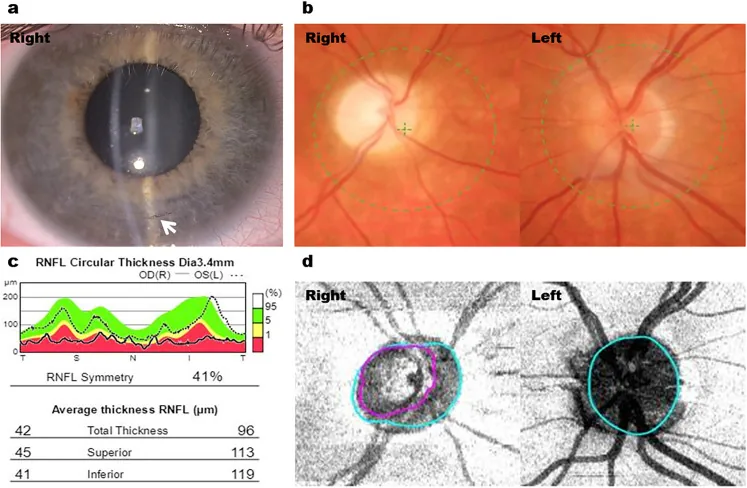
Aplicação pediátrica de técnicas MIGS
Seção intitulada “Aplicação pediátrica de técnicas MIGS”A cirurgia de glaucoma minimamente invasiva (MIGS) é um procedimento que preserva a conjuntiva, oferecendo a vantagem de manter opções para cirurgias adicionais no futuro, e sua aplicação em crianças está aumentando. No entanto, as evidências são limitadas.
- Goniotomia com KDB (Kahook Dual-Blade): Relatada aplicação em PCG pediátrico7)
- Trab360: Relatado como procedimento de trabeculotomia para glaucoma pediátrico8)
- Shunt microexterno PreserFlo: Pequenos relatos como opção adjuvante para glaucoma pediátrico refratário9)
Terapia medicamentosa
Seção intitulada “Terapia medicamentosa”A seleção de medicamentos é semelhante à do glaucoma de ângulo aberto em adultos, mas há considerações especiais em crianças.
- Medicamentos relacionados à prostaglandina (PG): Em crianças, muitos são não respondedores, mas são vantajosos em segurança e frequência de colírio uma vez ao dia.
- Betabloqueadores: Use a menor concentração possível. Cuidado com efeitos colaterais como asma brônquica e bradicardia. Em neonatos, há relatos de apneia.
- Inibidores da anidrase carbônica (IAC): Via oral: acetazolamida 5 mg/kg/dia dividido em 3 doses. Efeito hipotensor ocular grande, mas uso prolongado pode causar acidose metabólica e retardo do crescimento. Colírios têm menos efeitos colaterais, mas também menor efeito.
- Pilocarpina pós-operatória: 1-2% 2-3 vezes ao dia por algumas semanas. Objetivo: prevenir sinéquia anterior periférica.
Tratamento do glaucoma de desenvolvimento tardio
Seção intitulada “Tratamento do glaucoma de desenvolvimento tardio”Após a idade escolar, tente primeiro a terapia medicamentosa. Como a anormalidade angular é mais leve em comparação com o tipo precoce, o efeito do tratamento medicamentoso é maior.
- Primeira linha: Medicamentos PG (ex.: latanoprost)
- Segunda linha: Colírios IAC ou betabloqueadores (apenas em crianças que podem expressar com precisão os sintomas dos efeitos colaterais)
- Se PIO >25 mmHg: Use medicamentos PG desde o início, adicione betabloqueadores ou IAC conforme necessário.
A indicação cirúrgica é avaliada com cautela. Devido à grande variação temporal da PIO, a cirurgia é considerada se a PIO elevada (30-40 mmHg ou mais) persistir por várias semanas com má resposta medicamentosa, ou se a PIO estiver em torno de 20 mmHg com dano avançado ao campo visual1).
PIO alvo e manejo de longo prazo
Seção intitulada “PIO alvo e manejo de longo prazo”A PIO alvo desejada é 19-20 mmHg ou menos.
Após o controle da PIO, é necessário manejo de longo prazo. Para considerar o desenvolvimento da função visual, realize exames de refração e acuidade visual regulares, e trate ambliopia e estrabismo conforme necessário. A principal causa de baixa visão é a ambliopia, portanto, correção refrativa adequada e treinamento visual precoces são importantes.
No glaucoma de desenvolvimento precoce (glaucoma congênito primário), a cirurgia é a primeira escolha, sendo realizada goniotomia ou trabeculotomia 1). A taxa de sucesso é de 65 a 96%, sendo melhor nos casos que surgem entre 1 e 24 meses de idade. A terapia medicamentosa é usada para reduzir o edema corneano pré-operatório e como adjuvante pós-operatório. No tipo tardio, a terapia medicamentosa é tentada primeiro após a idade escolar. Em todos os tipos, a intervenção precoce e o manejo da ambliopia a longo prazo são essenciais para preservar a função visual.
6. Fisiopatologia e Mecanismo Detalhado
Seção intitulada “6. Fisiopatologia e Mecanismo Detalhado”Achados Histológicos da Anomalia do Ângulo
Seção intitulada “Achados Histológicos da Anomalia do Ângulo”A patologia do glaucoma de desenvolvimento precoce pode ser resumida da seguinte forma:
- Espessamento anormal do tecido conjuntivo paracanalicular de Schlemm: Devido ao desenvolvimento imaturo da malha trabecular, o tecido conjuntivo paracanalicular de Schlemm está anormalmente espesso
- Acúmulo de matriz extracelular: Abaixo do canal de Schlemm, existe um tecido compacto não lamelar composto por fibras colágenas e elásticas e grande quantidade de material amorfo. Consiste em células trabeculares com processos curtos, componentes fibrosos e material semelhante à lâmina basal
- Inserção anormal do corpo ciliar: O corpo ciliar se insere na área da malha trabecular, e a contração muscular puxa o esporão escleral para frente, comprimindo o canal de Schlemm e a malha trabecular
- Ectopia da raiz da íris: A raiz da íris está localizada na posição da malha trabecular
- Hipoplasia do canal de Schlemm: Em alguns casos, o canal de Schlemm está ausente ou subdesenvolvido
Embriologicamente, as células trabeculares são derivadas da crista neural, enquanto o tecido conjuntivo paracanalicular de Schlemm é derivado de células endoteliais vasculares. A maior resistência ao fluxo do humor aquoso está no ponto de encontro desses tecidos de origens diferentes.
Acredita-se que a lâmina trabecular (material em folha) esteja comprimida e presente anterior à malha trabecular, obstruindo o fluxo do humor aquoso, além de levantar a íris e impedir a abertura do ângulo, causando os achados angulares característicos do glaucoma de desenvolvimento.
Mecanismo de Aumento do Globo Ocular
Seção intitulada “Mecanismo de Aumento do Globo Ocular”A cápsula ocular do lactente é muito elástica. A hipertensão ocular persistente causa estiramento da cápsula ocular ao redor do limbo, aumentando o diâmetro da córnea (buftalmia). Simultaneamente, ocorre ruptura da membrana de Descemet (estrias de Haab), menos elástica que o estroma corneano, permitindo a entrada de humor aquoso no estroma e epitélio da córnea, agravando agudamente o edema e a opacidade corneana.
Se o controle da pressão intraocular permanecer inadequado, há risco de deslocamento do cristalino devido à ruptura das zônulas de Zinn, erosão e úlcera de córnea, e ruptura do globo ocular.
Por que a cirurgia do ângulo é eficaz em crianças
Seção intitulada “Por que a cirurgia do ângulo é eficaz em crianças”A trabeculotomia é considerada altamente eficaz no glaucoma congênito 5). Essa diferença é atribuída à abundância de fibras elásticas no ângulo da criança. Acredita-se que as fibras elásticas facilitem a abertura da estrutura angular e mantenham a patência da via de drenagem do humor aquoso após a cirurgia 5).
Após a trabeculotomia externa, a patência do canal de Schlemm é considerada importante para os resultados a longo prazo 5). A principal causa de insucesso cirúrgico é a proliferação fibrosa na parede interna do canal de Schlemm e o alongamento do endotélio do canal de Schlemm 5).
Anormalidades genéticas e desenvolvimento do ângulo
Seção intitulada “Anormalidades genéticas e desenvolvimento do ângulo”CYP1B1 é um gene que codifica uma enzima pertencente à família do citocromo P450, com alta expressão nos tecidos do segmento anterior do olho fetal. Mutações no CYP1B1 causam anormalidades na via metabólica da tirosina, prejudicando a diferenciação e maturação normais do tecido angular. Mutações no CYP1B1 foram relatadas não apenas no PCG, mas também no JOAG e no glaucoma associado a malformações oculares congênitas 3).
Recentemente, mutações no TEK/ANGPT1 foram identificadas como novos genes 2). TEK codifica um receptor tirosina quinase envolvido no desenvolvimento e manutenção do endotélio do canal de Schlemm, sugerindo o envolvimento de uma nova via molecular no PCG.
7. Pesquisas recentes e perspectivas futuras
Seção intitulada “7. Pesquisas recentes e perspectivas futuras”Novas aplicações de dispositivos MIGS em crianças
Seção intitulada “Novas aplicações de dispositivos MIGS em crianças”O PreserFlo é um shunt microexterno que desvia o humor aquoso da câmara anterior para o espaço subconjuntival. Seu uso no glaucoma infantil refratário ainda é limitado a pequenos relatos, e sua posição como tratamento padrão requer validação futura 9).
O sistema cirúrgico OMNI é um procedimento que combina incisão trabecular com injeção de material viscoelástico no canal de Schlemm e canais coletores (viscocanalostomia), e foi relatado seu uso em um lactente de 4 meses com glaucoma associado à síndrome de Sturge-Weber.
Está ocorrendo uma mudança de paradigma dos procedimentos externos para os internos 5). Os procedimentos internos não requerem a criação de retalho conjuntival ou escleral, preservando a conjuntiva e mantendo opções para cirurgias adicionais no futuro.
Avanços na pesquisa genética
Seção intitulada “Avanços na pesquisa genética”Mutações no TEK/ANGPT1 foram identificadas como uma nova via molecular no PCG, impulsionando a compreensão dos mecanismos de desenvolvimento e manutenção do canal de Schlemm 2). A pesquisa sobre o gene CYP1B1 atrai o maior interesse acadêmico na área de glaucoma infantil, com análise bibliométrica de 1955 a 2022 mostrando que a genética molecular foi o tópico principal em 13 dos 25 artigos de pesquisa principais 6).
Embora a classificação etária atual seja útil para prever o prognóstico, foi apontado que ela não considera o background genético, o que é um desafio 2). Com a disseminação dos testes genéticos, espera-se a construção de um novo sistema de classificação baseado na correspondência entre fenótipo e genótipo.
Tendências da Pesquisa em Qualidade de Vida
Seção intitulada “Tendências da Pesquisa em Qualidade de Vida”Na revisão sistemática de Stingl et al. (2024), foram identificadas 10 medidas de desfecho relatadas pelo paciente (PROM) usadas em coortes de glaucoma pediátrico. Sete atingiram a classificação de qualidade máxima de 5/7, mas nenhuma incluiu a perspectiva dos pacientes com glaucoma pediátrico durante o desenvolvimento 4). Há necessidade de desenvolver PROM específica para glaucoma pediátrico.
A qualidade de vida no glaucoma pediátrico é influenciada não apenas pela deficiência visual, mas também por múltiplos fatores, como cirurgias repetidas, tratamento contínuo com colírios, preocupação com a hereditariedade e impacto nas escolhas profissionais futuras 4).
Referências
Seção intitulada “Referências”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
