
Entwicklungsglaukom (angeborenes Glaukom) (Developmental Glaucoma)
Auf einen Blick
Abschnitt betitelt „Auf einen Blick“1. Was ist ein Entwicklungsglaukom?
Abschnitt betitelt „1. Was ist ein Entwicklungsglaukom?“Das Entwicklungsglaukom (developmental glaucoma) ist ein Glaukom, das auf einer Entwicklungsstörung des Kammerwasserabflusses beruht. Je nach Zeitpunkt des Auftretens wird es in ein frühmanifestes und ein spätmanifestes Entwicklungsglaukom unterteilt1).
Der frühmanifeste Typ entspricht dem klassischen primären kongenitalen Glaukom (primary congenital glaucoma; PCG). Die Ursache des erhöhten Augeninnendrucks ist auf eine Entwicklungsstörung des Trabekelwerks beschränkt, tritt vor dem 3. bis 4. Lebensjahr auf und geht mit einer Vergrößerung des Hornhautdurchmessers (Buphthalmus) einher. Der spätmanifeste Typ weist eine mildere Entwicklungsstörung des Kammerwinkels und Trabekelwerks auf, sodass das Auftreten verzögert ist und der Verlauf dem eines primären Offenwinkelglaukoms ähnelt. Er tritt im Alter von 10 bis 20 Jahren auf.
Klassifikationssystem
Abschnitt betitelt „Klassifikationssystem“Es gibt mehrere Klassifikationssysteme für das kindliche Glaukom. Die Glaukom-Leitlinien klassifizieren das Entwicklungsglaukom in drei Typen: frühmanifest, spätmanifest und mit anderen angeborenen Anomalien1). International wird die vom Childhood Glaucoma Research Network (CGRN) entwickelte Klassifikation von der World Glaucoma Association (WGA) und dem American Board of Ophthalmology (ABO) übernommen2).
| Klassifikation | Japanische Klassifikation | CGRN-Klassifikation |
|---|---|---|
| Primär/frühmanifest | Frühmanifestes Entwicklungsglaukom | Primäres kongenitales Glaukom (PCG) |
| Primär/spätmanifest | Spätmanifestes Entwicklungsglaukom | Juveniles Offenwinkelglaukom (JOAG) |
| Mit angeborenen Anomalien | Entwicklungsglaukom mit anderen angeborenen Anomalien | Sekundär: im Zusammenhang mit angeborener Augenfehlbildung |
| Mit systemischen Erkrankungen | (oben enthalten) | Sekundär: im Zusammenhang mit angeborener systemischer Erkrankung |
| Erworbene Faktoren | (oben enthalten) | Sekundär: erworbene Faktoren |
| Postoperativ | (oben enthalten) | Sekundär: nach Kataraktoperation |
PCG wird weiter nach dem Erkrankungsalter unterteilt in neonatal (0–1 Monat), infantil (1–24 Monate) und spät (≥2 Jahre)2). JOAG beginnt nach dem 4. Lebensjahr, ohne Vergrößerung des Augapfels und mit normalem Kammerwinkel2).
Sekundäre kindliche Glaukome umfassen Glaukom im Zusammenhang mit angeborener Augenfehlbildung bei Axenfeld-Rieger-Anomalie, Peters-Anomalie und Aniridie; Glaukom im Zusammenhang mit angeborener systemischer Erkrankung bei Sturge-Weber-Syndrom und Down-Syndrom; erworbenes Glaukom als Folge von Uveitis, Trauma oder Steroiden; sowie Glaukom nach Kataraktoperation2).
Epidemiologie
Abschnitt betitelt „Epidemiologie“Das kindliche Glaukom macht 5 % der Erblindungsursachen im Kindesalter aus und betrifft weltweit über 300.000 Menschen2).
Die Inzidenz des frühen Typs beträgt 1,8–2,4 pro 100.000 Geburten (Japan), in Europa und den USA werden 5–10 berichtet. Am häufigsten ist es bei den Roma in der Slowakei, wo Blutsverwandtenehen häufig sind, mit 80 pro 100.000 Geburten. 75 % sind bilateral, 65 % treten bei Jungen auf. 80 % der Fälle treten im ersten Lebensjahr auf. Die meisten sind sporadisch, aber etwa 10–40 % zeigen eine Vererbung mit autosomal-rezessivem Erbgang.
In einem großen australasischen Krankheitsregister (ANZRAG: 660 Patienten) machte PCG 57,6 % und JOAG 19,3 % der kindlichen Glaukome aus3). Das mediane Diagnosealter betrug 0,25 Jahre für PCG und 14 Jahre für JOAG3).
Gemäß den Glaukom-Leitlinien wird es in drei Typen eingeteilt: früher, später und entwicklungsbedingtes Glaukom mit anderen angeborenen Anomalien1). International ist die CGRN-Klassifikation der Standard, die das primäre kongenitale Glaukom (PCG), das juvenile Offenwinkelglaukom (JOAG) und vier sekundäre Typen (angeborene Augenfehlbildungen, angeborene systemische Erkrankungen, erworbene Faktoren, nach Kataraktoperation) umfasst2). PCG ist der häufigste Typ des kindlichen Glaukoms und macht etwa 60 % aus.
2. Hauptsymptome und klinische Befunde
Abschnitt betitelt „2. Hauptsymptome und klinische Befunde“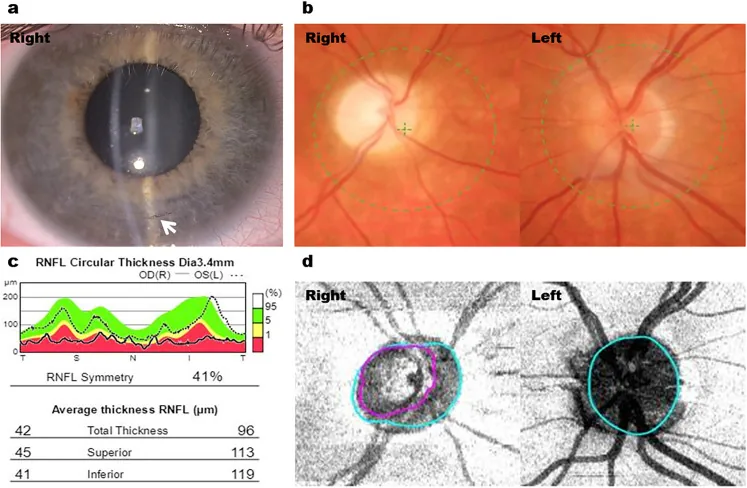
Pädiatrische Anwendung von MIGS-Verfahren
Abschnitt betitelt „Pädiatrische Anwendung von MIGS-Verfahren“Die minimalinvasive Glaukomchirurgie (MIGS) ist ein Verfahren, das die Bindehaut schont und somit die Option für zukünftige zusätzliche Eingriffe offen lässt, was ihre Anwendung bei Kindern fördert. Die Evidenz ist jedoch begrenzt.
- KDB (Kahook Dual-Blade) Goniotomie: Die Anwendung bei pädiatrischem PCG wurde berichtet7)
- Trab360: Als Trabekulotomie-ähnliches Verfahren für das kindliche Glaukom berichtet8)
- PreserFlo externer Mikro-Shunt: Kleine Berichte als adjuvante Option für refraktäres kindliches Glaukom9)
Medikamentöse Therapie
Abschnitt betitelt „Medikamentöse Therapie“Die Auswahl der Medikamente ist ähnlich wie beim adulten Offenwinkelglaukom, jedoch gibt es besondere Überlegungen bei Kindern.
- Prostaglandin (PG)-verwandte Medikamente: Bei Kindern viele Non-Responder, aber vorteilhaft hinsichtlich Sicherheit und einmal täglicher Applikation
- Betablocker: So niedrig wie möglich konzentriert verwenden. Achtung vor Nebenwirkungen wie Bronchialasthma, Bradykardie. Bei Neugeborenen wurden Apnoen berichtet
- Carboanhydrasehemmer (CAH): Oral Acetazolamid 5 mg/kg/Tag in 3 Dosen. Große drucksenkende Wirkung, aber Langzeitanwendung kann metabolische Azidose oder Wachstumsstörungen verursachen. Augentropfen haben weniger Nebenwirkungen, aber auch geringere Wirkung
- Postoperatives Pilocarpin: 1–2 % 2–3 mal täglich für einige Wochen. Ziel: Verhinderung von peripheren anterioren Synechien
Behandlung des spätmanifesten entwicklungsbedingten Glaukoms
Abschnitt betitelt „Behandlung des spätmanifesten entwicklungsbedingten Glaukoms“Ab dem Schulalter kann zunächst eine medikamentöse Therapie versucht werden. Da die Kammerwinkelanomalien im Vergleich zur Frühform milder sind, ist die medikamentöse Wirkung höher.
- Erstlinientherapie: PG-Verwandte (z. B. Latanoprost)
- Zweitlinientherapie: CAH-Augentropfen oder Betablocker (nur bei Kindern, die subjektive Nebenwirkungen genau beschreiben können)
- Bei Augeninnendruck über 25 mmHg: Von Anfang an PG-Verwandte verwenden, bei Bedarf Betablocker oder CAH hinzufügen
Die Operationsindikation ist sorgfältig zu stellen. Aufgrund der großen zeitlichen Schwankungen des Augeninnendrucks wird eine Operation in Betracht gezogen, wenn ein hoher Druck von 30–40 mmHg oder mehr über mehrere Wochen anhält und medikamentös nicht ausreichend gesenkt werden kann, oder wenn bei einem Druck um 20 mmHg bereits terminale Gesichtsfeldausfälle vorliegen1).
Zielaugeninnendruck und Langzeitmanagement
Abschnitt betitelt „Zielaugeninnendruck und Langzeitmanagement“Ein Zielaugeninnendruck unter 19–20 mmHg wird als wünschenswert angesehen.
Auch nach Kontrolle des Augeninnendrucks ist ein langfristiges Management erforderlich. Für die Entwicklung der Sehfunktion sollten regelmäßige Refraktions- und Sehschärfetests durchgeführt werden, und bei Bedarf eine Amblyopie- oder Schielbehandlung erfolgen. Die Hauptursache für schlechte Sehschärfe ist Amblyopie, daher sind frühzeitige adäquate Refraktionskorrektur und orthoptisches Training wichtig.
Bei der frühkindlichen Entwicklungsglaukom (primäres kongenitales Glaukom) ist die Operation die erste Wahl, es wird eine Goniotomie oder Trabekulotomie durchgeführt 1). Die Erfolgsrate liegt bei 65–96 % und ist bei Fällen, die zwischen dem 1. und 24. Lebensmonat auftreten, am besten. Medikamente werden zur Reduktion des präoperativen Hornhautödems oder als postoperative Unterstützung eingesetzt. Bei spätmanifesten Formen wird nach dem Schulalter zunächst eine medikamentöse Therapie versucht. Bei allen Formen sind eine frühzeitige Intervention und ein langfristiges Amblyopiemanagement für den Erhalt der Sehfunktion unerlässlich.
6. Pathophysiologie und detaillierte Pathogenese
Abschnitt betitelt „6. Pathophysiologie und detaillierte Pathogenese“Histologische Befunde der Kammerwinkelfehlbildung
Abschnitt betitelt „Histologische Befunde der Kammerwinkelfehlbildung“Die Pathologie des frühkindlichen Entwicklungsglaukoms lässt sich wie folgt zusammenfassen:
- Abnorme Verdickung des juxtakanalikulären Bindegewebes: Aufgrund der unreifen Entwicklung des Trabekelwerks ist das juxtakanalikuläre Bindegewebe abnormal dick.
- Akkumulation extrazellulärer Matrix: Ein nicht-lamelläres, kompaktes Gewebe aus Kollagen, elastinähnlichen Fasern und einer großen Menge amorpher Substanz befindet sich unter dem Schlemm-Kanal. Es besteht aus Trabekelzellen mit kurzen Zellfortsätzen, fibrösen Komponenten und basal membranähnlichem Material.
- Abnorme Ansatz des Ziliarkörpers: Der Ziliarkörper setzt an der Stelle des Trabekelwerks an, und die Muskelkontraktion zieht den Skleralsporn nach vorne, wodurch der Schlemm-Kanal und das Trabekelwerk komprimiert werden.
- Ektopie der Iriswurzel: Die Iriswurzel befindet sich an der Position des Trabekelwerks.
- Unzureichende Entwicklung des Schlemm-Kanals: In einigen Fällen fehlt der Schlemm-Kanal oder ist unvollständig entwickelt.
Embryologisch stammen die Trabekelzellen von der Neuralleiste ab, während das juxtakanalikuläre Bindegewebe von vaskulären Endothelzellen abstammt. Der maximale Widerstand gegen den Kammerwasserabfluss befindet sich an der Kontaktstelle dieser unterschiedlich abstammenden Gewebe.
Es wird vermutet, dass das Trabekelblatt (blattartige Substanz) komprimiert wird und vor dem Trabekelwerk liegt, wodurch es den Kammerwasserabfluss behindert und die Iris anhebt, was eine Erweiterung des Kammerwinkels verhindert – dies wird als Ursache für die charakteristischen Kammerwinkelbefunde des Entwicklungsglaukoms angesehen.
Mechanismus der Bulbusvergrößerung
Abschnitt betitelt „Mechanismus der Bulbusvergrößerung“Die Augenhülle von Säuglingen ist sehr elastisch. Anhaltend hoher Augeninnendruck dehnt die Augenhülle um den Hornhaut-Bindehaut-Übergang herum, was zu einer Vergrößerung des Hornhautdurchmessers führt (Buphthalmus). Gleichzeitig reißt die im Vergleich zum Hornhautstroma weniger elastische Descemet-Membran (Haab-Streifen), und Kammerwasser strömt in das Hornhautstroma und -epithel ein, was Hornhautödem und -trübung akut verschlimmert.
Bei anhaltend schlechter Augeninnendruckkontrolle besteht auch das Risiko einer Linsenluxation durch Ruptur der Zonula Zinnii, von Hornhauterosion/-ulkus und einer Bulbusruptur.
Warum die Kammerwinkelchirurgie bei Kindern wirksam ist
Abschnitt betitelt „Warum die Kammerwinkelchirurgie bei Kindern wirksam ist“Die Trabekulotomie gilt als hochwirksam bei angeborenem Glaukom 5). Dieser Unterschied wird auf die reichlich vorhandenen elastischen Fasern im Kammerwinkel von Kindern zurückgeführt. Elastische Fasern fördern die Öffnung der Kammerwinkelstrukturen und erhalten die Durchgängigkeit der Abflusswege nach der Operation 5).
Nach einer externen Trabekulotomie ist die Durchgängigkeit des Schlemm-Kanals für die Langzeitergebnisse von Bedeutung 5). Die Hauptursachen für postoperative Misserfolge sind die fibröse Proliferation der Innenwand des Schlemm-Kanals und die Dehnung des Endothels des Schlemm-Kanals 5).
Genetische Anomalien und Kammerwinkelentwicklung
Abschnitt betitelt „Genetische Anomalien und Kammerwinkelentwicklung“CYP1B1 ist ein Gen, das ein Enzym der Cytochrom-P450-Familie kodiert und in den Geweben des vorderen Augenabschnitts des Fötus stark exprimiert wird. Bei CYP1B1-Mutationen kommt es zu einer Anomalie im Tyrosinstoffwechsel, die vermutlich die normale Differenzierung und Reifung des Kammerwinkelgewebes hemmt. CYP1B1-Mutationen wurden nicht nur bei PCG, sondern auch bei JOAG und Glaukom im Zusammenhang mit angeborenen Augenfehlbildungen berichtet 3).
In den letzten Jahren wurden TEK/ANGPT1-Mutationen neu identifiziert 2). TEK kodiert für einen Rezeptor-Tyrosinkinase, der an der Entwicklung und Erhaltung des Endothels des Schlemm-Kanals beteiligt ist, was auf die Beteiligung eines neuen molekularen Signalwegs bei PCG hindeutet.
7. Aktuelle Forschung und zukünftige Perspektiven
Abschnitt betitelt „7. Aktuelle Forschung und zukünftige Perspektiven“Neue MIGS-Implantate für Kinder
Abschnitt betitelt „Neue MIGS-Implantate für Kinder“Der PreserFlo externe Mikro-Shunt ist ein Gerät, das Kammerwasser von der Vorderkammer in den subkonjunktivalen Raum ableitet. Seine Anwendung bei refraktärem pädiatrischem Glaukom ist auf kleine Fallberichte beschränkt, und seine Etablierung als Standardbehandlung bedarf zukünftiger Validierung 9).
Das OMNI-Chirurgiesystem kombiniert eine TM-Inzision mit der Injektion von Viskoelastikum in den Schlemm-Kanal und die Sammelkanäle (Viskokanalostomie) und wurde bei einem 4 Monate alten Säugling mit Glaukom im Zusammenhang mit dem Sturge-Weber-Syndrom eingesetzt.
Ein Paradigmenwechsel von externen zu internen Verfahren ist im Gange 5). Interne Verfahren erfordern keine Bildung von Bindehaut- oder Skleralappen und erhalten die Bindehaut, was als Strategie nützlich ist, um Optionen für zukünftige zusätzliche Operationen offen zu lassen.
Fortschritte in der genetischen Forschung
Abschnitt betitelt „Fortschritte in der genetischen Forschung“TEK/ANGPT1-Mutationen wurden als neuer molekularer Signalweg bei PCG identifiziert, und das Verständnis der Mechanismen, die an der Entwicklung und Erhaltung des Schlemm-Kanals beteiligt sind, schreitet voran 2). Die Forschung zum CYP1B1-Gen zieht das größte akademische Interesse im Bereich des pädiatrischen Glaukoms auf sich, und in einer bibliometrischen Analyse von 1955 bis 2022 machte die Molekulargenetik 13 von 25 Hauptforschungsthemen aus 6).
Die aktuelle Altersklassifikation ist nützlich für die Prognosevorhersage, aber es wurde darauf hingewiesen, dass sie den genetischen Hintergrund nicht berücksichtigt, was eine Herausforderung darstellt 2). Mit der Verbreitung von Gentests wird der Aufbau eines neuen Klassifikationssystems erwartet, das auf der Korrespondenz zwischen Phänotyp und Genotyp basiert.
Trends in der Lebensqualitätsforschung
Abschnitt betitelt „Trends in der Lebensqualitätsforschung“In einem systematischen Review von Stingl et al. (2024) wurden 10 patientenberichtete Ergebnismessungen (PROM) identifiziert, die in pädiatrischen Glaukom-Kohorten verwendet wurden. Sieben erreichten die höchste Qualitätsbewertung von 5/7, aber keine bezog die Perspektive pädiatrischer Glaukompatienten in den Entwicklungsprozess ein 4). Die Entwicklung von pädiatrischen Glaukom-spezifischen PROM ist erforderlich.
Die Lebensqualität bei pädiatrischem Glaukom wird nicht nur durch Sehbehinderung beeinflusst, sondern auch durch multifaktorielle Faktoren wie wiederholte Operationen, kontinuierliche Augentropfenbehandlung, Besorgnis über Vererbung und Auswirkungen auf die zukünftige Berufswahl 4).
8. Referenzen
Abschnitt betitelt „8. Referenzen“- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
