
发育性青光眼(先天性青光眼)
一目了然的要点
Section titled “一目了然的要点”1. 什么是发育性青光眼?
Section titled “1. 什么是发育性青光眼?”发育性青光眼(developmental glaucoma)是由于房水流出道发育异常导致的青光眼。根据发病时间分为早发型和晚发型发育性青光眼1)。
早发型相当于传统的原发性先天性青光眼(PCG)。眼压升高的原因仅限于小梁网发育异常,在3-4岁前发病,伴有角膜直径扩大(牛眼)。晚发型由于房角/小梁网发育异常较轻,发病较晚,病程类似于原发性开角型青光眼。通常在10-20岁发病。
儿童青光眼存在多种分类体系。日本青光眼指南将发育性青光眼分为早发型、晚发型和伴有其他先天异常的发育性青光眼三类1)。国际上,儿童青光眼研究网络(CGRN)制定的分类已被世界青光眼协会(WGA)和美国眼科委员会(ABO)采用2)。
| 分类 | 日本分类 | CGRN分类 |
|---|---|---|
| 原发性、早发型 | 早发型发育性青光眼 | 原发性先天性青光眼(PCG) |
| 原发性、晚发型 | 晚发型发育性青光眼 | 青少年开角型青光眼(JOAG) |
| 合并先天异常 | 伴有其他先天异常的发展性青光眼 | 继发性:与先天眼形成异常相关 |
| 合并全身疾病 | (包含在上述中) | 继发性:与先天全身疾病相关 |
| 后天因素 | (包含在上述中) | 继发性:后天因素 |
| 术后 | (包含在上述中) | 继发性:白内障术后 |
PCG根据发病年龄进一步细分为新生儿期(0~1个月)、婴儿期(1~24个月)和迟发性(2岁以上)2)。JOAG在4岁后发病,不伴有眼球扩大,房角外观正常2)。
继发性儿童青光眼包括:伴有Axenfeld-Rieger异常、Peters异常、无虹膜症等先天眼形成异常相关的青光眼;伴有Sturge-Weber综合征、Down综合征等先天全身疾病相关的青光眼;继发于葡萄膜炎、外伤、类固醇的后天因素青光眼;以及白内障术后青光眼2)。
儿童青光眼占儿童失明原因的5%,全球有超过30万人患病2)。
早发型青光眼的发病率在日本为每10万出生人口1.8~2.4人,而在欧美报告为5~10人。在近亲结婚较多的斯洛伐克罗姆人中发病率最高,为每10万出生人口80人。75%为双眼性,65%发生于男童。80%的病例在出生后1年内发病。大部分为散发病例,但约10%~40%有遗传性,呈常染色体隐性遗传。
在大型澳大拉西亚疾病登记处(ANZRAG:660名患者)中,儿童青光眼中PCG占57.6%,JOAG占19.3%3)。PCG的诊断年龄中位数为0.25岁,JOAG为14岁3)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”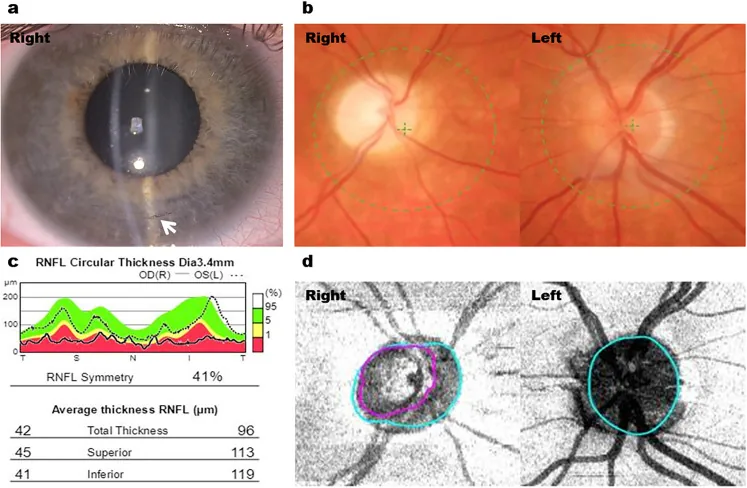
MIGS手术的儿童应用
Section titled “MIGS手术的儿童应用”微创青光眼手术(MIGS)是一种保留结膜的技术,由于保留了未来额外手术的选择,其在儿童中的应用正在推进。然而,证据有限。
- KDB(Kahook Dual-Blade)房角切开术:已有在儿童PCG中应用的报道7)
- Trab360:作为儿童青光眼的小梁切开类手术已有报道8)
- PreserFlo外路微型分流管:作为难治性儿童青光眼的辅助选择有小规模报道9)
药物的选择与成人开角型青光眼类似,但儿童有特殊的注意事项。
- 前列腺素(PG)相关药物:儿童中无应答者较多,但在安全性和每日一次滴眼方面具有优势。
- β受体阻滞剂:使用尽可能低的浓度。注意支气管哮喘和心动过缓的副作用。新生儿中有呼吸暂停的报道。
- 碳酸酐酶抑制剂(CAI):口服乙酰唑胺5 mg/kg/日,分三次服用。降眼压效果强,但长期使用可能导致代谢性酸中毒和发育不良。滴眼液副作用少但效果也较小。
- 术后毛果芸香碱:使用1-2%浓度,每日2-3次,持续数周。目的是预防周边虹膜前粘连。
迟发型发育性青光眼的治疗
Section titled “迟发型发育性青光眼的治疗”学龄期及以后,首先尝试药物治疗。与早发型相比,房角异常较轻,因此药物治疗效果较好。
- 一线药物:PG相关药物(如拉坦前列素)
- 二线药物:CAI滴眼液或β受体阻滞剂(仅限能准确描述主观副作用症状的儿童)
- 眼压超过25 mmHg时:从PG相关药物开始,必要时加用β受体阻滞剂或CAI。
手术适应症需谨慎判断。由于眼压随时间波动较大,当30-40 mmHg以上的高眼压持续数周且药物降压效果不佳,或眼压约20 mmHg但视野损害已至晚期时,考虑手术1)。
目标眼压与长期管理
Section titled “目标眼压与长期管理”目标眼压最好控制在19-20 mmHg以下。
眼压控制后仍需长期管理。为促进视功能发育,应定期进行屈光检查和视力检查,必要时进行弱视治疗或斜视治疗。视力不良的最大原因是弱视,早期进行适当的屈光矫正和视功能训练非常重要。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”房角发育异常的组织学表现
Section titled “房角发育异常的组织学表现”早发型发育性青光眼的病理总结如下:
- 近Schlemm管结缔组织异常增厚:由于小梁网发育不成熟,近Schlemm管结缔组织异常增厚。
- 细胞外基质积聚:由胶原、弹性蛋白样纤维和大量无定形物质组成的非层状致密组织存在于Schlemm管下方。由短细胞突的小梁细胞、纤维成分和基底膜样物质组成。
- 睫状体异常附着:睫状体附着于小梁网区域,肌肉收缩将巩膜突向前拉,压迫Schlemm管和小梁网。
- 虹膜根部异位:虹膜根部位于小梁网的位置。
- Schlemm管发育不全:部分病例Schlemm管缺失或发育不完全。
胚胎学上,小梁细胞来源于神经嵴,而近Schlemm管结缔组织来源于血管内皮细胞。不同起源组织的邻接点存在最大的房水流出阻力。
推测小梁片(片状物质)被压缩并存在于小梁网前方,阻碍房水流出,同时将虹膜向上拉,防止房角扩大,这是发育性青光眼特有房角表现的原因。
眼球扩大的机制
Section titled “眼球扩大的机制”婴幼儿的眼球被膜弹性丰富。持续高眼压时,角巩膜缘为中心的眼球被膜被拉伸,角膜直径增大(牛眼)。同时,弹性较低的Descemet膜发生破裂(Haab纹),房水流入角膜基质和上皮,导致角膜水肿和混浊急剧加重。
如果眼压控制不良持续存在,还会出现Zinn小带破裂导致的晶状体偏位、角膜糜烂/溃疡以及眼球破裂的风险。
儿童房角手术有效的原因
Section titled “儿童房角手术有效的原因”小梁切开术被认为对先天性青光眼非常有效5)。这种差异被认为源于儿童房角中丰富的弹性纤维。弹性纤维促进房角结构的开放,并维持术后房水流出通道的通畅5)。
外路小梁切开术后,Schlemm管的通畅性被认为与长期预后相关5)。术后失败的主要原因是Schlemm管内壁的纤维增生和Schlemm管内皮的伸长5)。
基因异常与房角发育
Section titled “基因异常与房角发育”CYP1B1是编码细胞色素P450家族酶的基因,在胎儿眼眼前段组织中高表达。在CYP1B1突变病例中,酪氨酸代谢途径出现异常,推测会阻碍房角组织的正常分化和成熟。CYP1B1突变不仅见于PCG,也见于JOAG和先天性眼发育异常相关的青光眼3)。
近年来,TEK/ANGPT1突变被新发现2)。TEK编码参与Schlemm管内皮发育和维持的受体酪氨酸激酶,提示PCG中涉及新的分子通路。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”新型MIGS装置在儿童中的应用
Section titled “新型MIGS装置在儿童中的应用”PreserFlo外路微型分流器是一种将房水从前房分流至结膜下腔的装置。其在难治性儿童青光眼中的使用仅限于小规模报告,作为标准治疗的地位有待未来验证9)。
OMNI手术系统结合了小梁网切开术和向Schlemm管及集合管注入粘弹性物质(粘弹剂管切开术),已有报道用于一名患有Sturge-Weber综合征相关青光眼的4个月大婴儿。
从外路到内路手术的范式转变正在进行中5)。内路手术无需制作结膜瓣和巩膜瓣,可保留结膜,因此作为保留未来额外手术选择策略是有用的。
遗传学研究的进展
Section titled “遗传学研究的进展”TEK/ANGPT1突变已被确定为PCG的新分子通路,推动了对Schlemm管发育和维持机制的理解2)。关于CYP1B1基因的研究在儿童青光眼领域引起了最高的学术关注,在1955年至2022年的文献计量分析中,分子遗传学在25个主要研究主题中占13个6)。
虽然目前的年龄分类对预测预后有用,但有人指出它没有考虑遗传背景2)。随着基因检测的普及,有望建立基于表型和基因型对应关系的新分类体系。
生活质量研究趋势
Section titled “生活质量研究趋势”Stingl等人(2024)的系统评价确定了在儿童青光眼队列中使用的10种患者报告结局指标(PROM)。其中7种达到了最高质量评分5/7,但所有指标在开发过程中均未纳入儿童青光眼患者的观点4)。需要开发针对儿童青光眼的特异性PROM。
儿童青光眼的生活质量不仅受视力障碍影响,还受反复手术、持续滴眼治疗、对遗传的担忧以及对未来职业选择的影响等多方面因素影响4)。
8. 参考文献
Section titled “8. 参考文献”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
