
Glaucome développemental (glaucome congénital) (Developmental Glaucoma)
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que le glaucome développemental ?
Section intitulée « 1. Qu’est-ce que le glaucome développemental ? »Le glaucome développemental (developmental glaucoma) est un glaucome dû à une anomalie du développement de la voie d’écoulement de l’humeur aqueuse. Selon l’âge d’apparition, on distingue le glaucome développemental précoce et le glaucome développemental tardif1).
Le type précoce correspond au glaucome congénital primitif (primary congenital glaucoma; PCG) classique. L’augmentation de la pression intraoculaire est limitée à une anomalie du développement du trabéculum, survient avant l’âge de 3 à 4 ans et s’accompagne d’une augmentation du diamètre cornéen (buphtalmie). Le type tardif a un développement anormal moins sévère de l’angle et du trabéculum, ce qui retarde l’apparition et suit une évolution similaire à celle du glaucome primitif à angle ouvert. Il survient entre 10 et 20 ans.
Système de classification
Section intitulée « Système de classification »Il existe plusieurs systèmes de classification pour le glaucome pédiatrique. Les directives cliniques pour le glaucome classent le glaucome développemental en trois types : précoce, tardif et avec anomalies congénitales associées1). Au niveau international, la classification établie par le Childhood Glaucoma Research Network (CGRN) est adoptée par la World Glaucoma Association (WGA) et l’American Board of Ophthalmology (ABO)2).
| Classification | Classification japonaise | Classification CGRN |
|---|---|---|
| Primitif/début précoce | Glaucome développemental précoce | Glaucome congénital primitif (PCG) |
| Primitif/tardif | Glaucome développemental tardif | Glaucome juvénile à angle ouvert (JOAG) |
| Anomalies congénitales associées | Glaucome développemental avec autres anomalies congénitales | Secondaire : lié à une malformation oculaire congénitale |
| Maladies systémiques associées | (Inclus ci-dessus) | Secondaire : lié à une maladie systémique congénitale |
| Facteurs acquis | (Inclus ci-dessus) | Secondaire : facteurs acquis |
| Postopératoire | (Inclus ci-dessus) | Secondaire : après chirurgie de la cataracte |
Le PCG est en outre subdivisé selon l’âge d’apparition en période néonatale (0-1 mois), infantile (1-24 mois) et tardive (≥2 ans)2). Le JOAG apparaît après l’âge de 4 ans, sans élargissement du globe oculaire et avec un aspect angulaire normal2).
Le glaucome secondaire de l’enfant comprend le glaucome lié à une malformation oculaire congénitale associée à l’anomalie d’Axenfeld-Rieger, à l’anomalie de Peters et à l’aniridie ; le glaucome lié à une maladie systémique congénitale associée au syndrome de Sturge-Weber et au syndrome de Down ; le glaucome acquis secondaire à une uvéite, un traumatisme ou des stéroïdes ; et le glaucome après chirurgie de la cataracte2).
Épidémiologie
Section intitulée « Épidémiologie »Le glaucome infantile représente 5 % des causes de cécité chez l’enfant et touche plus de 300 000 personnes dans le monde2).
L’incidence du type précoce est de 1,8 à 2,4 pour 100 000 naissances (Japon), et de 5 à 10 pour 100 000 naissances en Europe et aux États-Unis. La fréquence la plus élevée est observée chez les Roms de Slovaquie, où les mariages consanguins sont fréquents, avec 80 pour 100 000 naissances. 75 % des cas sont bilatéraux et 65 % surviennent chez les garçons. 80 % des cas se déclarent au cours de la première année de vie. La plupart sont sporadiques, mais environ 10 à 40 % présentent une hérédité, avec un mode de transmission autosomique récessif.
Dans un grand registre de maladies australasien (ANZRAG : 660 patients), le PCG représentait 57,6 % des glaucomes infantiles et le JOAG 19,3 %3). L’âge médian au diagnostic était de 0,25 an pour le PCG et de 14 ans pour le JOAG3).
Selon les directives cliniques pour le glaucome, il est classé en trois types : précoce, tardif et glaucome développemental associé à d’autres anomalies congénitales1). Au niveau international, la classification CGRN est la norme, comprenant le glaucome congénital primitif (PCG), le glaucome juvénile à angle ouvert (JOAG) et quatre types secondaires (anomalies oculaires congénitales, maladies systémiques congénitales, facteurs acquis, post-cataracte)2). Le PCG est le type le plus fréquent, représentant environ 60 % des glaucomes infantiles.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »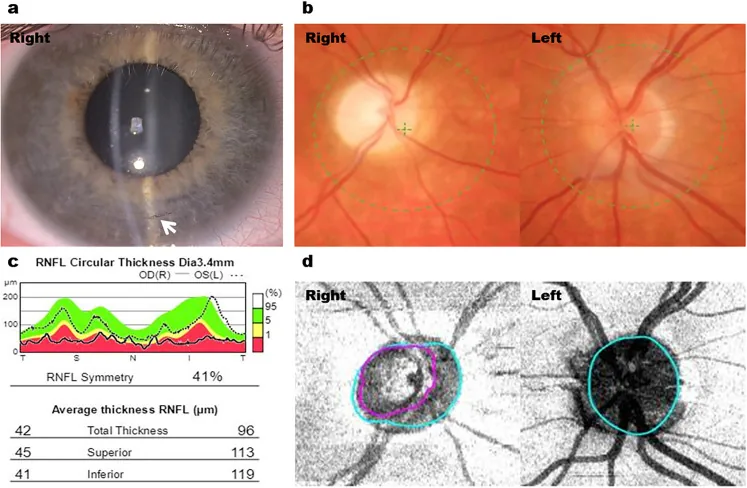
Application pédiatrique des techniques MIGS
Section intitulée « Application pédiatrique des techniques MIGS »La chirurgie mini-invasive du glaucome (MIGS) est une technique qui préserve la conjonctive, offrant l’avantage de laisser des options pour une chirurgie future, ce qui favorise son application chez l’enfant. Cependant, les preuves sont limitées.
- Goniotomie KDB (Kahook Dual-Blade) : son application dans le PCG pédiatrique a été rapportée7)
- Trab360 : rapporté comme technique de trabéculotomie pour le glaucome infantile8)
- Micro-shunt externe PreserFlo : de petits rapports existent comme option adjuvante pour le glaucome infantile réfractaire9)
Traitement médicamenteux
Section intitulée « Traitement médicamenteux »Le choix des médicaments est similaire à celui du glaucome à angle ouvert de l’adulte, mais il existe des considérations particulières chez l’enfant.
- Prostaglandines (PG) : chez l’enfant, beaucoup de non-répondeurs, mais avantage en termes de sécurité et de fréquence d’instillation une fois par jour
- Bêta-bloquants : utiliser la concentration la plus faible possible. Attention aux effets secondaires : asthme bronchique, bradycardie. Chez le nouveau-né, des cas d’apnée ont été rapportés
- Inhibiteurs de l’anhydrase carbonique (IAC) : par voie orale, acétazolamide 5 mg/kg/jour en 3 prises. Effet hypotenseur oculaire important, mais une utilisation prolongée peut entraîner une acidose métabolique ou un retard de croissance. Les collyres ont moins d’effets secondaires mais sont moins efficaces
- Pilocarpine postopératoire : 1 à 2 % 2 à 3 fois par jour pendant quelques semaines. Objectif : prévenir les synéchies antérieures périphériques
Traitement du glaucome développemental tardif
Section intitulée « Traitement du glaucome développemental tardif »À partir de l’âge scolaire, on peut d’abord essayer un traitement médicamenteux. Les anomalies de l’angle sont moins sévères que dans la forme précoce, donc le traitement médicamenteux est plus efficace.
- Traitement de première intention : prostaglandines (ex. latanoprost)
- Traitement de deuxième intention : collyre IAC ou bêta-bloquant (uniquement chez les enfants capables de décrire précisément les effets secondaires subjectifs)
- Si la pression intraoculaire dépasse 25 mmHg : commencer d’emblée par une prostaglandine, puis ajouter un bêta-bloquant ou un IAC si nécessaire
L’indication chirurgicale doit être évaluée avec prudence. En raison des fluctuations temporelles importantes de la pression intraoculaire, la chirurgie est envisagée en cas d’hypertension oculaire de 30 à 40 mmHg ou plus persistant plusieurs semaines et mal contrôlée par les médicaments, ou en cas de lésions du champ visuel terminales même avec une pression d’environ 20 mmHg1).
Pression intraoculaire cible et gestion à long terme
Section intitulée « Pression intraoculaire cible et gestion à long terme »La pression intraoculaire cible est généralement considérée comme souhaitable en dessous de 19 à 20 mmHg.
Après le contrôle de la pression intraoculaire, une gestion à long terme est nécessaire. Pour le développement de la fonction visuelle, des examens réguliers de la réfraction et de l’acuité visuelle doivent être effectués, et un traitement de l’amblyopie ou du strabisme doit être mis en place si nécessaire. La principale cause de mauvaise acuité visuelle est l’amblyopie, d’où l’importance d’une correction réfractive appropriée et d’une orthoptie précoces.
Dans le glaucome développemental précoce (glaucome congénital primitif), la chirurgie est le traitement de première intention, avec une goniotomie ou une trabéculotomie 1). Le taux de succès est de 65 à 96 %, meilleur pour les cas survenant entre 1 et 24 mois de vie. Les médicaments sont utilisés pour réduire l’œdème cornéen préopératoire ou en complément postopératoire. Dans les formes tardives, on essaie d’abord un traitement médicamenteux après l’âge scolaire. Dans tous les types, une intervention précoce et une gestion à long terme de l’amblyopie sont essentielles pour préserver la fonction visuelle.
6. Physiopathologie et mécanismes détaillés
Section intitulée « 6. Physiopathologie et mécanismes détaillés »Anomalies histologiques de l’angle iridocornéen
Section intitulée « Anomalies histologiques de l’angle iridocornéen »La pathologie du glaucome développemental précoce se résume comme suit :
- Épaississement anormal du tissu conjonctif juxtacanaliculaire : en raison du développement immature du trabéculum, le tissu conjonctif juxtacanaliculaire est anormalement épais.
- Accumulation de matrice extracellulaire : un tissu compact non lamellaire composé de fibres de collagène et d’élastine ainsi que d’une grande quantité de substance amorphe se trouve sous le canal de Schlemm. Il est constitué de cellules trabéculaires à prolongements courts, de composants fibreux et de substance ressemblant à une membrane basale.
- Insertion anormale du corps ciliaire : le corps ciliaire s’attache au niveau du trabéculum, et la contraction musculaire tire l’éperon scléral vers l’avant, comprimant le canal de Schlemm et le trabéculum.
- Position ectopique de la racine de l’iris : la racine de l’iris se trouve au niveau du trabéculum.
- Développement insuffisant du canal de Schlemm : dans certains cas, le canal de Schlemm est absent ou incomplètement développé.
Embryologiquement, les cellules trabéculaires dérivent de la crête neurale, tandis que le tissu conjonctif juxtacanaliculaire dérive des cellules endothéliales vasculaires. La résistance maximale à l’écoulement de l’humeur aqueuse se situe à la jonction de ces tissus d’origine différente.
On suppose que la compression de la lame trabéculaire (substance en feuillet) devant le trabéculum obstrue l’écoulement de l’humeur aqueuse et soulève l’iris, empêchant l’élargissement de l’angle, ce qui expliquerait les signes angulaires caractéristiques du glaucome développemental.
Mécanisme de l’élargissement du globe oculaire
Section intitulée « Mécanisme de l’élargissement du globe oculaire »La coque oculaire des nourrissons est très élastique. Une pression intraoculaire élevée persistante étire la coque autour de la jonction cornée-conjonctive, augmentant le diamètre cornéen (buphtalmie). Simultanément, la membrane de Descemet, moins élastique que le stroma cornéen, se rompt (stries de Haab), et l’humeur aqueuse s’infiltre dans le stroma et l’épithélium cornéens, aggravant brutalement l’œdème et l’opacité cornéens.
Si le contrôle de la pression intraoculaire reste insuffisant, il existe également un risque de luxation du cristallin par rupture de la zonule de Zinn, d’érosion ou d’ulcération cornéenne, et de rupture du globe oculaire.
Pourquoi la chirurgie de l’angle est efficace chez l’enfant
Section intitulée « Pourquoi la chirurgie de l’angle est efficace chez l’enfant »La trabéculotomie est considérée comme très efficace dans le glaucome congénital 5). Cette différence serait due aux fibres élastiques abondantes dans l’angle de l’enfant. Les fibres élastiques favorisent l’ouverture des structures de l’angle et maintiennent la perméabilité des voies d’écoulement de l’humeur aqueuse après l’opération 5).
Après une trabéculotomie externe, la perméabilité du canal de Schlemm est liée aux résultats à long terme 5). Les principales causes d’échec postopératoire sont la prolifération fibreuse de la paroi interne du canal de Schlemm et l’étirement de l’endothélium du canal de Schlemm 5).
Anomalies génétiques et développement de l’angle
Section intitulée « Anomalies génétiques et développement de l’angle »CYP1B1 est un gène codant pour une enzyme de la famille du cytochrome P450, fortement exprimé dans les tissus du segment antérieur de l’œil fœtal. Dans les cas de mutation de CYP1B1, une anomalie de la voie métabolique de la tyrosine se produit, ce qui inhiberait la différenciation et la maturation normales du tissu de l’angle. Les mutations de CYP1B1 ont été rapportées non seulement dans le PCG, mais aussi dans le JOAG et le glaucome associé à des anomalies congénitales du développement oculaire 3).
Récemment, des mutations TEK/ANGPT1 ont été nouvellement identifiées 2). TEK code pour un récepteur tyrosine kinase impliqué dans le développement et le maintien de l’endothélium du canal de Schlemm, suggérant l’implication d’une nouvelle voie moléculaire dans le PCG.
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Nouvelles applications pédiatriques des dispositifs MIGS
Section intitulée « Nouvelles applications pédiatriques des dispositifs MIGS »Le micro-shunt externe PreserFlo est un dispositif qui dérive l’humeur aqueuse de la chambre antérieure vers l’espace sous-conjonctival. Son utilisation dans le glaucome pédiatrique réfractaire ne fait l’objet que de rapports à petite échelle, et sa place en tant que traitement standard nécessite une validation future 9).
Le système chirurgical OMNI combine une incision du TM et l’injection de substance viscoélastique dans le canal de Schlemm et les canaux collecteurs (viscocanalostomie), et son utilisation a été rapportée chez un nourrisson de 4 mois atteint de glaucome associé au syndrome de Sturge-Weber.
Un changement de paradigme des procédures externes vers les procédures internes est en cours 5). Les procédures internes ne nécessitent pas la création de lambeaux conjonctivaux ou scléraux et préservent la conjonctive, ce qui est utile comme stratégie pour laisser des options pour des chirurgies supplémentaires futures.
Progrès de la recherche génétique
Section intitulée « Progrès de la recherche génétique »Les mutations TEK/ANGPT1 ont été identifiées comme une nouvelle voie moléculaire du PCG, et la compréhension des mécanismes impliqués dans le développement et le maintien du canal de Schlemm progresse 2). La recherche sur le gène CYP1B1 suscite le plus grand intérêt académique dans le domaine du glaucome pédiatrique, et dans une analyse bibliométrique de 1955 à 2022, la génétique moléculaire représentait 13 des 25 principaux thèmes de recherche 6).
La classification actuelle par âge est utile pour prédire le pronostic, mais il a été souligné qu’elle ne prend pas en compte le contexte génétique, ce qui constitue un problème 2). Avec la généralisation des tests génétiques, on espère la construction d’un nouveau système de classification basé sur la correspondance entre phénotype et génotype.
Tendances de la recherche sur la qualité de vie
Section intitulée « Tendances de la recherche sur la qualité de vie »Dans une revue systématique de Stingl et al. (2024), 10 mesures de résultats rapportés par les patients (PROM) utilisées dans des cohortes de glaucome pédiatrique ont été identifiées. Sept ont atteint la note maximale de qualité de 5/7, mais aucune n’incluait le point de vue des patients atteints de glaucome pédiatrique dans leur processus de développement 4). Le développement de PROM spécifiques au glaucome pédiatrique est nécessaire.
La qualité de vie dans le glaucome pédiatrique est influencée non seulement par la déficience visuelle, mais aussi par des facteurs multidimensionnels tels que les interventions chirurgicales répétées, le traitement continu par collyre, l’inquiétude concernant l’hérédité et l’impact sur le choix professionnel futur 4).
8. Références
Section intitulée « 8. Références »- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
