
Glôcôm Phát Triển (Glôcôm Bẩm Sinh)
Những Điểm Chính Yếu Lược
Phần tiêu đề “Những Điểm Chính Yếu Lược”1. Bệnh tăng nhãn áp phát triển là gì
Phần tiêu đề “1. Bệnh tăng nhãn áp phát triển là gì”Bệnh tăng nhãn áp phát triển (developmental glaucoma) là bệnh tăng nhãn áp do bất thường phát triển của đường dẫn lưu thủy dịch. Dựa vào thời điểm khởi phát, được phân loại thành tăng nhãn áp phát triển khởi phát sớm và tăng nhãn áp phát triển khởi phát muộn1).
Loại khởi phát sớm tương ứng với bệnh tăng nhãn áp bẩm sinh nguyên phát (PCG) cổ điển. Nguyên nhân tăng nhãn áp chỉ giới hạn ở bất thường phát triển của bè củng mạc, xảy ra trước 3-4 tuổi với sự mở rộng đường kính giác mạc (mắt bò). Loại khởi phát muộn có bất thường nhẹ ở góc và bè củng mạc nên khởi phát chậm, diễn tiến tương tự bệnh tăng nhãn áp góc mở nguyên phát. Xảy ra ở độ tuổi 10-20.
Hệ thống phân loại
Phần tiêu đề “Hệ thống phân loại”Có nhiều hệ thống phân loại cho bệnh tăng nhãn áp trẻ em. Hướng dẫn thực hành lâm sàng về bệnh tăng nhãn áp phân loại thành ba loại: khởi phát sớm, khởi phát muộn và tăng nhãn áp phát triển kèm các bất thường bẩm sinh khác1). Trên quốc tế, phân loại do Mạng lưới Nghiên cứu Bệnh tăng nhãn áp Trẻ em (CGRN) xây dựng đã được Hiệp hội Bệnh tăng nhãn áp Thế giới (WGA) và Hội đồng Nhãn khoa Hoa Kỳ (ABO) chấp nhận2).
| Phân loại | Phân loại Nhật Bản | Phân loại CGRN |
|---|---|---|
| Nguyên phát khởi phát sớm | Tăng nhãn áp phát triển khởi phát sớm | Tăng nhãn áp bẩm sinh nguyên phát (PCG) |
| Nguyên phát khởi phát muộn | Tăng nhãn áp phát triển khởi phát muộn | Tăng nhãn áp góc mở thiếu niên (JOAG) |
| Kèm dị tật bẩm sinh | Glôcôm phát triển kèm các dị tật bẩm sinh khác | Thứ phát: liên quan dị dạng mắt bẩm sinh |
| Kèm bệnh toàn thân | (Bao gồm ở trên) | Thứ phát: liên quan bệnh toàn thân bẩm sinh |
| Yếu tố mắc phải | (Bao gồm ở trên) | Thứ phát: yếu tố mắc phải |
| Sau phẫu thuật | (Bao gồm ở trên) | Thứ phát: sau phẫu thuật đục thủy tinh thể |
PCG được phân chia thêm theo tuổi khởi phát thành sơ sinh (0–1 tháng), trẻ nhũ nhi (1–24 tháng) và khởi phát muộn (≥2 tuổi)2). JOAG khởi phát sau 4 tuổi, không kèm phì đại nhãn cầu và góc tiền phòng bình thường2).
Glôcôm thứ phát ở trẻ em bao gồm: glôcôm liên quan dị dạng mắt bẩm sinh như bất thường Axenfeld-Rieger, bất thường Peters và vô mống mắt; glôcôm liên quan bệnh toàn thân bẩm sinh như hội chứng Sturge-Weber và hội chứng Down; glôcôm do yếu tố mắc phải như viêm màng bồ đào, chấn thương và steroid; và glôcôm sau phẫu thuật đục thủy tinh thể2).
Dịch tễ học
Phần tiêu đề “Dịch tễ học”Glôcôm trẻ em chiếm 5% nguyên nhân gây mù lòa ở trẻ nhỏ và ảnh hưởng đến hơn 300.000 người trên toàn thế giới2).
Tỷ lệ mắc thể khởi phát sớm là 1,8–2,4 trên 100.000 trẻ sinh sống (tại Nhật Bản), trong khi ở châu Âu và châu Mỹ là 5–10. Tỷ lệ cao nhất là ở người Di-gan Slovakia do kết hôn cận huyết, với 80 trên 100.000 trẻ sinh sống. 75% trường hợp là hai bên, và 65% xảy ra ở trẻ nam. 80% trường hợp xuất hiện trong năm đầu đời. Phần lớn là lẻ tẻ, nhưng khoảng 10–40% có tính di truyền theo kiểu lặn nhiễm sắc thể thường.
Trong một cơ sở dữ liệu bệnh lớn của châu Đại Dương (ANZRAG: 660 bệnh nhân), glôcôm bẩm sinh nguyên phát (PCG) chiếm 57,6% và glôcôm thiếu niên góc mở (JOAG) chiếm 19,3% các trường hợp glôcôm trẻ em3). Tuổi chẩn đoán trung vị của PCG là 0,25 tuổi, và của JOAG là 14 tuổi3).
Hướng dẫn thực hành lâm sàng về glôcôm phân loại glôcôm phát triển thành ba loại: khởi phát sớm, khởi phát muộn và glôcôm phát triển kèm các bất thường bẩm sinh khác1). Trên quốc tế, phân loại CGRN là tiêu chuẩn, chia glôcôm thành glôcôm bẩm sinh nguyên phát (PCG), glôcôm thiếu niên góc mở (JOAG) và bốn loại thứ phát (dị dạng mắt bẩm sinh, bệnh toàn thân bẩm sinh, yếu tố mắc phải, sau phẫu thuật đục thủy tinh thể)2). PCG chiếm khoảng 60% glôcôm trẻ em và là loại phổ biến nhất.
2. Triệu chứng chính và dấu hiệu lâm sàng
Phần tiêu đề “2. Triệu chứng chính và dấu hiệu lâm sàng”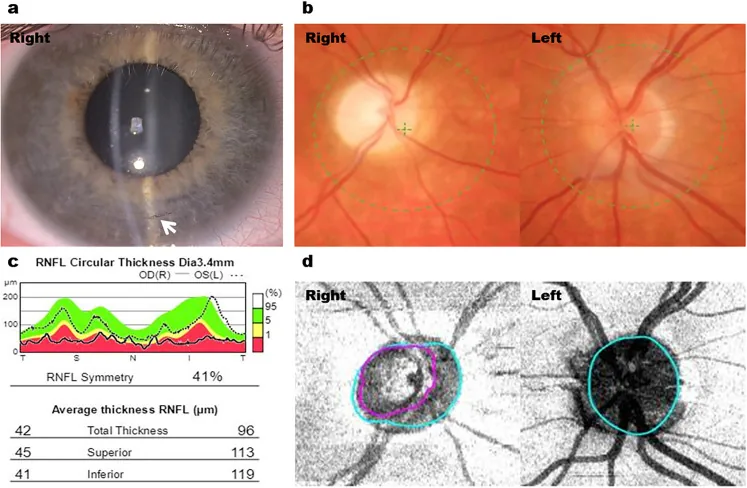
Ứng dụng kỹ thuật MIGS ở trẻ em
Phần tiêu đề “Ứng dụng kỹ thuật MIGS ở trẻ em”Phẫu thuật glôcôm xâm lấn tối thiểu (MIGS) là thủ thuật bảo tồn kết mạc, mang lại lợi thế giữ lại các lựa chọn cho phẫu thuật bổ sung trong tương lai, do đó ứng dụng ở trẻ em đang gia tăng. Tuy nhiên, bằng chứng còn hạn chế.
- Mở góc tiền phòng bằng KDB (Kahook Dual-Blade): Đã có báo cáo ứng dụng trong PCG ở trẻ em7)
- Trab360: Đã được báo cáo như một thủ thuật cắt bè cho glôcôm trẻ em8)
- Shunt vi mạch ngoài PreserFlo: Có báo cáo nhỏ như một lựa chọn bổ trợ cho glôcôm trẻ em kháng trị9)
Điều trị bằng thuốc
Phần tiêu đề “Điều trị bằng thuốc”Lựa chọn thuốc tương tự như glôcôm góc mở ở người lớn, nhưng có những cân nhắc đặc biệt ở trẻ em.
- Thuốc liên quan đến prostaglandin (PG): Ở trẻ em, nhiều trường hợp không đáp ứng, nhưng ưu điểm về an toàn và tần suất nhỏ mắt một lần mỗi ngày.
- Thuốc chẹn beta: Sử dụng nồng độ thấp nhất có thể. Chú ý tác dụng phụ như hen phế quản và nhịp tim chậm. Ở trẻ sơ sinh, đã có báo cáo về ngưng thở.
- Thuốc ức chế carbonic anhydrase (CAI): Đường uống: acetazolamide 5 mg/kg/ngày chia 3 lần. Hiệu quả hạ nhãn áp lớn, nhưng sử dụng lâu dài có thể gây nhiễm toan chuyển hóa và chậm phát triển. Thuốc nhỏ mắt có ít tác dụng phụ hơn nhưng hiệu quả cũng thấp hơn.
- Pilocarpine sau phẫu thuật: 1-2% 2-3 lần mỗi ngày trong vài tuần. Mục đích là ngăn ngừa dính mống mắt trước ngoại vi.
Điều trị glôcôm phát triển thể muộn
Phần tiêu đề “Điều trị glôcôm phát triển thể muộn”Sau tuổi đi học, hãy thử điều trị bằng thuốc trước. Vì bất thường góc nhẹ hơn so với thể sớm, hiệu quả điều trị bằng thuốc cao hơn.
- Lựa chọn đầu tay: Thuốc PG (ví dụ latanoprost)
- Lựa chọn thứ hai: Thuốc nhỏ mắt CAI hoặc thuốc chẹn beta (chỉ ở trẻ có thể diễn tả chính xác triệu chứng tác dụng phụ)
- Nếu nhãn áp >25 mmHg: Sử dụng thuốc PG ngay từ đầu, thêm thuốc chẹn beta hoặc CAI nếu cần.
Chỉ định phẫu thuật được cân nhắc thận trọng. Do nhãn áp dao động lớn theo thời gian, phẫu thuật được xem xét nếu nhãn áp cao (30-40 mmHg hoặc hơn) kéo dài vài tuần với đáp ứng thuốc kém, hoặc nếu nhãn áp khoảng 20 mmHg với tổn thương thị trường giai đoạn cuối1).
Nhãn áp mục tiêu và quản lý dài hạn
Phần tiêu đề “Nhãn áp mục tiêu và quản lý dài hạn”Nhãn áp mục tiêu mong muốn là 19-20 mmHg hoặc thấp hơn.
Sau khi kiểm soát nhãn áp, cần quản lý dài hạn. Để xem xét sự phát triển chức năng thị giác, thực hiện kiểm tra khúc xạ và thị lực định kỳ, điều trị nhược thị và lác nếu cần. Nguyên nhân chính gây thị lực kém là nhược thị, do đó, chỉnh khúc xạ phù hợp và tập luyện thị giác sớm rất quan trọng.
Trong bệnh tăng nhãn áp phát triển sớm (tăng nhãn áp bẩm sinh nguyên phát), phẫu thuật là lựa chọn đầu tiên, được thực hiện phẫu thuật mở góc tiền phòng hoặc cắt bè củng mạc 1). Tỷ lệ thành công là 65-96%, tốt nhất ở các trường hợp khởi phát từ 1-24 tháng tuổi. Điều trị bằng thuốc được sử dụng để giảm phù giác mạc trước phẫu thuật và hỗ trợ sau phẫu thuật. Ở thể muộn, điều trị bằng thuốc được thử trước tiên sau tuổi đi học. Ở tất cả các thể, can thiệp sớm và quản lý nhược thị lâu dài là cần thiết để duy trì chức năng thị giác.
6. Sinh lý bệnh và Cơ chế chi tiết
Phần tiêu đề “6. Sinh lý bệnh và Cơ chế chi tiết”Kết quả mô học của bất thường góc tiền phòng
Phần tiêu đề “Kết quả mô học của bất thường góc tiền phòng”Bệnh lý của tăng nhãn áp phát triển sớm có thể tóm tắt như sau:
- Dày bất thường mô liên kết cạnh ống Schlemm: Do sự phát triển chưa trưởng thành của bè củng mạc, mô liên kết cạnh ống Schlemm dày bất thường
- Tích tụ chất nền ngoại bào: Dưới ống Schlemm có mô đặc không phân lớp gồm sợi collagen và elastin cùng lượng lớn chất vô định hình. Bao gồm tế bào bè củng mạc có tua ngắn, thành phần sợi và chất giống màng đáy
- Bám dính bất thường của thể mi: Thể mi bám vào vùng bè củng mạc, và sự co cơ kéo cựa củng mạc ra trước, chèn ép ống Schlemm và bè củng mạc
- Lạc chỗ chân mống mắt: Chân mống mắt nằm ở vị trí bè củng mạc
- Kém phát triển ống Schlemm: Trong một số trường hợp, ống Schlemm không có hoặc phát triển không hoàn chỉnh
Về mặt phôi học, tế bào bè củng mạc có nguồn gốc từ mào thần kinh, trong khi mô liên kết cạnh ống Schlemm có nguồn gốc từ tế bào nội mô mạch máu. Sức cản dòng chảy thủy dịch lớn nhất nằm ở điểm tiếp giáp của các mô có nguồn gốc khác nhau này.
Người ta cho rằng tấm bè (chất dạng tấm) bị nén và nằm trước bè củng mạc, cản trở dòng chảy thủy dịch, đồng thời nâng mống mắt lên và ngăn góc mở rộng, gây ra các dấu hiệu góc đặc trưng của tăng nhãn áp phát triển.
Cơ chế phình to nhãn cầu
Phần tiêu đề “Cơ chế phình to nhãn cầu”Vỏ nhãn cầu của trẻ sơ sinh rất đàn hồi. Tăng nhãn áp kéo dài làm giãn vỏ nhãn cầu quanh vùng rìa, tăng đường kính giác mạc (mắt bò). Đồng thời, màng Descemet kém đàn hồi hơn nhu mô giác mạc bị rách (vân Haab), cho phép thủy dịch vào nhu mô và biểu mô giác mạc, làm trầm trọng thêm phù và đục giác mạc cấp tính.
Nếu kiểm soát nhãn áp kém kéo dài, có nguy cơ lệch thể thủy tinh do đứt dây chằng Zinn, trợt và loét giác mạc, và vỡ nhãn cầu.
Tại sao phẫu thuật góc lại hiệu quả ở trẻ em
Phần tiêu đề “Tại sao phẫu thuật góc lại hiệu quả ở trẻ em”Phẫu thuật cắt bè (trabeculotomy) được cho là rất hiệu quả trong bệnh glôcôm bẩm sinh 5). Sự khác biệt này được cho là do sự phong phú của các sợi đàn hồi ở góc mắt trẻ em. Các sợi đàn hồi được cho là tạo điều kiện cho cấu trúc góc mở ra và duy trì sự thông thoáng của đường dẫn lưu thủy dịch sau phẫu thuật 5).
Sau phẫu thuật cắt bè ngoài, sự thông thoáng của ống Schlemm được cho là ảnh hưởng đến kết quả lâu dài 5). Nguyên nhân chính của thất bại phẫu thuật là sự tăng sinh xơ ở thành trong của ống Schlemm và sự kéo dài của nội mô ống Schlemm 5).
Bất thường di truyền và sự phát triển góc
Phần tiêu đề “Bất thường di truyền và sự phát triển góc”CYP1B1 là gen mã hóa một enzyme thuộc họ cytochrom P450, được biểu hiện nhiều ở các mô của đoạn trước mắt thai nhi. Các đột biến CYP1B1 được cho là gây ra bất thường trong con đường chuyển hóa tyrosine, cản trở sự biệt hóa và trưởng thành bình thường của mô góc. Đột biến CYP1B1 đã được báo cáo không chỉ trong PCG mà còn trong JOAG và glôcôm liên quan đến dị tật mắt bẩm sinh 3).
Trong những năm gần đây, các đột biến TEK/ANGPT1 đã được xác định là gen mới 2). TEK mã hóa một thụ thể tyrosine kinase tham gia vào sự phát triển và duy trì nội mô ống Schlemm, cho thấy sự tham gia của một con đường phân tử mới trong PCG.
7. Nghiên cứu mới nhất và triển vọng tương lai
Phần tiêu đề “7. Nghiên cứu mới nhất và triển vọng tương lai”Ứng dụng mới của thiết bị MIGS ở trẻ em
Phần tiêu đề “Ứng dụng mới của thiết bị MIGS ở trẻ em”PreserFlo là một shunt vi mô đường ngoài dẫn lưu thủy dịch từ tiền phòng đến khoang dưới kết mạc. Việc sử dụng nó trong glôcôm trẻ em kháng trị vẫn chỉ giới hạn trong các báo cáo nhỏ, và vị trí của nó như một liệu pháp tiêu chuẩn cần được xác nhận thêm trong tương lai 9).
Hệ thống phẫu thuật OMNI là một thủ thuật kết hợp rạch bè với tiêm chất nhớt đàn hồi vào ống Schlemm và các kênh thu gom (visco canalostomy), và đã được báo cáo sử dụng ở một trẻ 4 tháng tuổi mắc glôcôm liên quan đến hội chứng Sturge-Weber.
Đang có sự chuyển đổi mô hình từ thủ thuật đường ngoài sang thủ thuật đường trong 5). Thủ thuật đường trong không yêu cầu tạo vạt kết mạc hay củng mạc, bảo tồn kết mạc và duy trì các lựa chọn cho phẫu thuật bổ sung trong tương lai.
Tiến bộ trong nghiên cứu di truyền
Phần tiêu đề “Tiến bộ trong nghiên cứu di truyền”Các đột biến TEK/ANGPT1 đã được xác định là con đường phân tử mới trong PCG, thúc đẩy sự hiểu biết về cơ chế phát triển và duy trì ống Schlemm 2). Nghiên cứu về gen CYP1B1 thu hút sự quan tâm học thuật cao nhất trong lĩnh vực glôcôm trẻ em, với phân tích thư mục từ năm 1955 đến 2022 cho thấy di truyền phân tử là chủ đề chính trong 13 trên 25 bài báo nghiên cứu chính 6).
Mặc dù phân loại theo độ tuổi hiện tại hữu ích trong việc tiên lượng, nhưng đã được chỉ ra rằng nó không xem xét đến nền tảng di truyền, đây là một thách thức 2). Với sự phổ biến của xét nghiệm di truyền, việc xây dựng một hệ thống phân loại mới dựa trên sự tương ứng giữa kiểu hình và kiểu gen được kỳ vọng.
Xu hướng Nghiên cứu Chất lượng Cuộc sống
Phần tiêu đề “Xu hướng Nghiên cứu Chất lượng Cuộc sống”Trong tổng quan hệ thống của Stingl và cộng sự (2024), đã xác định được 10 thước đo kết quả do bệnh nhân báo cáo (PROM) được sử dụng trong các đoàn hệ glôcôm nhi khoa. Bảy thước đo đạt được xếp hạng chất lượng cao nhất là 5/7, nhưng không có thước đo nào bao gồm quan điểm của bệnh nhân glôcôm nhi khoa trong quá trình phát triển 4). Cần phát triển PROM đặc hiệu cho glôcôm nhi khoa.
Chất lượng cuộc sống trong glôcôm nhi khoa bị ảnh hưởng không chỉ bởi suy giảm thị lực, mà còn bởi nhiều yếu tố như phẫu thuật lặp lại, điều trị nhỏ mắt liên tục, lo lắng về tính di truyền và tác động đến lựa chọn nghề nghiệp trong tương lai 4).
Tài liệu tham khảo
Phần tiêu đề “Tài liệu tham khảo”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
