Phân bố vết bớt màu rượu vang và nguy cơ
Chỉ vùng V1: Nguy cơ glôcôm 6,7%
Chỉ vùng V2: Nguy cơ glôcôm hầu như không có
Vùng V1+V2: Nguy cơ glôcôm tăng đáng kể lên 31,8%
Vùng V1+V2+V3: Nguy cơ triệu chứng thần kinh tăng gấp 4 lần

Hội chứng Sturge-Weber (SWS) là một hội chứng da-thần kinh bẩm sinh còn được gọi là u máu não-dây thần kinh sinh ba. Đặc trưng bởi ba triệu chứng chính: u máu dạng rượu vang ở mặt trong vùng dây thần kinh sinh ba, u máu màng não mềm cùng bên và u máu mắt. Năm 1879, Sturge báo cáo một trường hợp u máu mặt kèm mắt bò với liệt nửa người và động kinh, và năm 1929, Weber đã xác lập hội chứng này.
Nguyên nhân là do đột biến thể khảm soma ở gen GNAQ (đột biến sau hợp tử), không di truyền và hầu hết là các trường hợp lẻ tẻ 4)8). Được cho là do bất thường phát triển mạch máu do rối loạn thần kinh giao cảm trong thời kỳ phôi thai. Tần suất hiếm gặp, 1 trên 50.000 ca sinh, không có khác biệt về chủng tộc hay giới tính 5)7).
SWS được phân loại lâm sàng thành ba loại sau:
| Phân loại (Roach) | Đặc điểm |
|---|---|
| Loại I (cổ điển) | PWS + triệu chứng thần kinh + glôcôm |
| Loại II | PWS + glôcôm (không có tổn thương thần kinh) |
| Loại III (hiếm nhất) | Chỉ u máu màng não |
Glôcôm là biến chứng mắt quan trọng nhất trong SWS, với tỷ lệ mắc glôcôm cao nhất trong các hội chứng u mạch 2). Khi u máu lan đến mí mắt, glôcôm xảy ra với tần suất cao 30-70%. U máu màng mạch đi kèm ở khoảng 40% bệnh nhân.
Theo thời điểm khởi phát, glôcôm được chia thành loại khởi phát sớm và muộn. Khoảng 60% là loại khởi phát sớm xuất hiện từ khi sinh đến 4 tuổi, nguyên nhân chính là bất thường phát triển góc tiền phòng. 40% còn lại là loại khởi phát muộn xuất hiện sau giai đoạn trẻ nhỏ, với tăng áp lực tĩnh mạch thượng củng mạc và u máu màng mạch tham gia vào cơ chế bệnh sinh. Thường xuất hiện trước 10 tuổi.
Hội chứng Sturge-Weber là một hội chứng thần kinh da bẩm sinh với ba triệu chứng chính: u máu mặt ở vùng dây thần kinh sinh ba, u máu màng não mềm cùng bên, và u máu mắt. Nguyên nhân do đột biến thể khảm soma ở gen GNAQ, không di truyền và hầu hết là các ca lẻ tẻ 4)8). Các biến chứng chính bao gồm động kinh (75-90% khởi phát trước 3 tuổi), chậm phát triển trí tuệ, liệt nửa người, và glôcôm (30-70%). Cũng có type II (chỉ glôcôm) và type III (chỉ u máu màng não) mà không có đủ ba triệu chứng. Xem phần “Nguyên nhân và Yếu tố nguy cơ” để biết chi tiết.
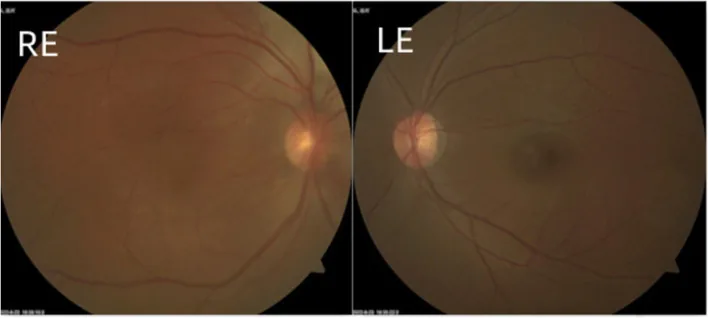
Ở type khởi phát sớm, triệu chứng ban đầu là chảy nước mắt, sợ ánh sáng, và co thắt mi mắt. Sau đó là suy giảm thị lực do tăng đường kính giác mạc và đục giác mạc (buphthalmos). Có thể thấy các vệt Haab, là các vết rách màng Descemet.
Type khởi phát muộn tương tự lâm sàng với glôcôm góc mở nguyên phát, ít triệu chứng chủ quan ở giai đoạn đầu. Khi tiến triển, xảy ra thu hẹp thị trường và giảm thị lực.
SWS gây ra bởi đột biến thể khảm soma ở gen GNAQ (nhiễm sắc thể 9q21.2) (c.548G→A, p.Arg183Gln)8). Đột biến này dẫn đến hoạt hóa liên tục con đường tín hiệu Gαq, gây tăng sinh không kiểm soát tế bào nội mô và dị dạng mạch máu4). Vì là đột biến thể khảm soma, không phải đột biến dòng mầm, nên không di truyền. Chẩn đoán phân tử cần sinh thiết mô bị ảnh hưởng (thường là da)4).
Việc phát hiện đột biến GNAQ bị ảnh hưởng bởi mẫu mô bệnh và phương pháp phân tích, do đó chẩn đoán phân tử cần được giải thích kết hợp với hình ảnh lâm sàng.
Phân bố vết bớt màu rượu vang và nguy cơ
Chỉ vùng V1: Nguy cơ glôcôm 6,7%
Chỉ vùng V2: Nguy cơ glôcôm hầu như không có
Vùng V1+V2: Nguy cơ glôcôm tăng đáng kể lên 31,8%
Vùng V1+V2+V3: Nguy cơ triệu chứng thần kinh tăng gấp 4 lần
Sự khác biệt về thời điểm khởi phát và nguyên nhân
Thể khởi phát sớm (khoảng 60%): Bất thường phát triển góc tiền phòng là nguyên nhân chính. Biểu hiện mắt bò và tăng đường kính giác mạc 1)
Thể khởi phát muộn (khoảng 40%): Tăng áp lực tĩnh mạch thượng củng mạc và sự tham gia của u mạch mạch máu hắc mạc là nguyên nhân chính 1)
Xâm lấn mi mắt: Nếu u mạch lan đến mi mắt, tỷ lệ mắc glôcôm tăng đáng kể
PWS hai bên: Khả năng là SWS cao hơn so với một bên 7)
Chẩn đoán glôcôm liên quan đến SWS đòi hỏi đo nhãn áp chính xác và khám phần trước, góc tiền phòng và đáy mắt. Ở trẻ em, thường cần khám dưới gây mê toàn thân.
Chụp mạch huỳnh quang đáy mắt rất hữu ích. Ở giai đoạn sớm, thấy hình ảnh mạch máu hắc mạc lớn, và ở giai đoạn muộn, toàn bộ phần khối u cho thấy tăng huỳnh quang. U máu hắc mạc lan tỏa có thể khó xác định khi khám đáy mắt thông thường.
Chụp CT đầu phát hiện vôi hóa trong vỏ não. Ngay cả ở giai đoạn sơ sinh khi vôi hóa chưa xuất hiện, MRI có tiêm gadolinium có thể phát hiện u mạch màng não mềm. Đánh giá lưu lượng máu não bằng SPECT cũng được sử dụng hỗ trợ.
SWS là một trong những bệnh u mạch, và là bệnh điển hình gây u máu hắc mạc. Cần phân biệt với các bệnh u mạch khác.
| Bệnh | Dấu hiệu mắt đặc trưng | Vị trí u máu/khối u |
|---|---|---|
| SWS | U máu hắc mạc, glôcôm | Mặt + màng não mềm |
| Bệnh von Hippel-Lindau | U máu võng mạc (vùng thái dương ngoại vi) | Võng mạc, tiểu não, thận |
| U xơ thần kinh loại 1 | Nốt Lisch ở mống mắt | U xơ thần kinh da |
| Xơ cứng củ | U mô thừa võng mạc | Não, da, thận, tim |
Hội chứng Klippel-Trenaunay-Weber cũng biểu hiện u máu da tương tự SWS, nhưng được phân biệt bởi có dị dạng tĩnh mạch chi và phì đại xương-mô mềm.
Ở bệnh nhân có vết bớt màu rượu vang trên mặt, khám mắt định kỳ bao gồm đo nhãn áp là cần thiết. Ở trẻ em, thực hiện đo nhãn áp bằng máy đo nhãn áp rebound, khám đoạn trước (đường kính giác mạc, đục giác mạc, có đường Haab), soi góc tiền phòng (đánh giá bất thường góc), và soi đáy mắt (đánh giá lõm đĩa thị, phát hiện u máu hắc mạc). Ở trẻ em thường cần khám dưới gây mê toàn thân. Ở thể khởi phát muộn, sự hiện diện của máu trong góc hoặc giãn mạch thượng củng mạc hữu ích cho chẩn đoán phân biệt. Chụp mạch huỳnh quang là cần thiết để đánh giá u máu hắc mạc, và đánh giá toàn thân bao gồm CT đầu và MRI có tiêm thuốc cản quang.
Điều trị tăng nhãn áp liên quan đến SWS đòi hỏi các chiến lược khác nhau tùy theo thời điểm khởi phát và cơ chế bệnh sinh.
Tăng nhãn áp bẩm sinh hoặc khởi phát ở trẻ nhũ nhi cần điều trị phẫu thuật 1). Phẫu thuật cắt bè (trabeculotomy) hoặc mở góc tiền phòng (goniotomy) là lựa chọn đầu tay 1). Tuy nhiên, tỷ lệ thành công thấp hơn so với tăng nhãn áp bẩm sinh nguyên phát, và thường cần phẫu thuật bổ sung.
Khi thực hiện phẫu thuật cắt bè củng mạc (trabeculectomy), có nguy cơ chảy máu từ u máu dẫn đến tụ máu hắc mạc trên diện rộng hoặc xuất huyết tống xuất. Nhìn chung, đáp ứng với phẫu thuật tăng nhãn áp không tốt, và thường cần phẫu thuật cắt bè củng mạc hoặc phẫu thuật đặt ống dẫn lưu.
Ở trẻ lớn hơn, áp lực tĩnh mạch thượng củng mạc tăng, do đó điều trị bằng thuốc là lựa chọn đầu tay 1). Thuốc ức chế sản xuất thủy dịch (thuốc chẹn beta, thuốc ức chế men carbonic anhydrase) được coi là hiệu quả nhất. Tác dụng hạ nhãn áp của thuốc tương tự prostaglandin được báo cáo là không nhất quán.
Nếu điều trị bằng thuốc hoặc tái tạo đường dẫn lưu không hiệu quả, hãy xem xét phẫu thuật cắt bè củng giác mạc hoặc phẫu thuật đặt ống dẫn lưu 1).
Phẫu thuật lọc và đặt ống dẫn lưu
Cắt bè củng giác mạc: Sử dụng thuốc kháng chuyển hóa (mitomycin C) có thể cải thiện kết quả. Tuy nhiên, ở mắt SWS, nguy cơ tràn dịch hắc mạc và xuất huyết tống xuất rất cao 1)
Thiết bị Ahmed: Báo cáo tỷ lệ thành công tích lũy 79% ở 24 tháng và 30% ở 60 tháng
Thiết bị Baerveldt hai giai đoạn: Báo cáo tất cả các trường hợp đạt áp lực <21 mmHg trong thời gian theo dõi trung bình 35 tháng
Phân tích tổng hợp GDD ở trẻ em: Phân tích 1221 mắt cho thấy tỷ lệ thành công 87% (KTC 95%: 83-91%) ở 12 tháng và 77% (KTC 95%: 71-83%) ở 24 tháng 9)
Xử trí biến chứng trong và sau phẫu thuật
Xuất huyết và tràn dịch hắc mạc: Khi có u máu hắc mạc, tụt áp lực nội nhãn đột ngột làm tăng nguy cơ bong hắc mạc và xuất huyết 1)
Các biện pháp phòng ngừa: Hạ áp lực nội nhãn trước phẫu thuật bằng thuốc thẩm thấu cao, mở củng mạc sau, đặt chỉ khâu củng mạc trước và khâu bổ sung chắc chắn
Lựa chọn thiết bị: Sử dụng GDD có van (Ahmed) hoặc hai giai đoạn (Baerveldt) làm giảm nguy cơ nhãn áp thấp
Quang đông thể mi: Trong các trường hợp kháng trị, hãy xem xét quang đông thể mi (CPC). Báo cáo 10/16 mắt (62,5%) duy trì áp lực nội nhãn 6-22 mmHg mà không có biến chứng (theo dõi trung bình 8,87 năm)
Trong phương pháp hai giai đoạn, một bao xơ hình thành xung quanh đĩa vài tuần trước khi đưa ống vào tiền phòng. Điều này ngăn ngừa tụt áp lực nội nhãn quá mức ngay sau phẫu thuật và giảm thiểu nguy cơ tràn dịch hắc mạc và xuất huyết. Phương pháp này đặc biệt hữu ích trong các trường hợp SWS có u máu hắc mạc.
Có báo cáo cho thấy netarsudil (thuốc ức chế Rho kinase) làm giảm hiệu quả nhãn áp trong glôcôm liên quan đến SWS ngay cả khi được thêm vào như lựa chọn thứ tư hoặc thứ năm. Thuốc này hoạt động bằng cách tăng cường dòng chảy thủy dịch qua bè củng mạc.
U mạch màng mạch lan tỏa liên quan đến SWS có thể cần được quản lý đồng thời với điều trị glôcôm.
Mặc dù khó điều trị hơn glôcôm bẩm sinh, nhưng thị lực có thể được bảo tồn nếu kiểm soát nhãn áp tốt từ sớm. Tuy nhiên, nếu u mạch màng mạch phát triển và gây bong võng mạc xuất tiết, đông lạnh có thể không đủ hiệu quả, dẫn đến suy giảm thị lực nghiêm trọng.
Vì tổn thương ảnh hưởng đến giác mạc, thể thủy tinh, võng mạc và thần kinh, nên thường khó đạt được thị lực tốt. Tuổi thọ trung bình của bệnh nhân SWS ngắn hơn so với dân số chung, và nếu có tổn thương màng não mềm hai bên, các triệu chứng thần kinh nặng hơn và tiên lượng xấu hơn.
Điểm quan trọng nhất là các biến chứng phẫu thuật liên quan đến u mạch màng mạch. Trong SWS, u mạch màng mạch xuất hiện ở khoảng 40% trường hợp, và sự tụt nhãn áp đột ngột trong phẫu thuật glôcôm có nguy cơ gây tràn dịch màng mạch, xuất huyết hoặc bong võng mạc 1). Các biện pháp phòng ngừa bao gồm dùng thuốc thẩm thấu trước phẫu thuật, thực hiện mở củng mạc sau, khâu chặt vạt củng mạc và sử dụng thiết bị dẫn lưu có van hoặc hai giai đoạn. Cũng cần lưu ý rằng thuốc chủ vận thụ thể alpha-2 (brimonidine) chống chỉ định ở trẻ dưới 2 tuổi 1). Xem phần «Điều trị Tiêu chuẩn» để biết chi tiết.
Nguyên nhân cơ bản của SWS là đột biến thể khảm soma ở gen GNAQ (c.548G→A, p.Arg183Gln)8). Đột biến này kích hoạt liên tục con đường tín hiệu Gαq, gây tăng sinh không kiểm soát tế bào nội mô và dị dạng mạch máu4). Đột biến xảy ra ở tế bào soma sớm sau thụ tinh, do đó sự phân bố của các tế bào đột biến quyết định sự đa dạng của kiểu hình lâm sàng (type I–III).
Trong Hướng dẫn điều trị Glôcôm (ấn bản thứ 5), các cơ chế tăng nhãn áp trong SWS được liệt kê như sau1).
Kiểm tra mô học của mắt đã bị khoét bỏ cho thấy các kết quả sau, tương tự như trong glôcôm bẩm sinh nguyên phát.
Trong các trường hợp khởi phát ở trẻ nhỏ, bất thường phát triển của góc tiền phòng được coi là yếu tố quan trọng nhất.
Trong các trường hợp khởi phát ở cuối tuổi thiếu niên đến sau 20 tuổi, nguyên nhân chính là tăng áp lực tĩnh mạch thượng củng mạc do u máu1). Soi góc tiền phòng cho thấy bất thường góc tối thiểu, nhưng thường thấy máu trong góc, tương quan với tăng áp lực tĩnh mạch thượng củng mạc. Trong tình trạng này, thuốc ức chế sản xuất thủy dịch được coi là hiệu quả nhất và điều trị bằng thuốc là lựa chọn đầu tiên.
Bởi vì cơ chế phát sinh glôcôm ở hai thể khác nhau về cơ bản. Ở thể khởi phát sớm, nguyên nhân chính là bất thường bẩm sinh của góc tiền phòng, trong đó có vấn đề ở bè củng mạc-giác mạc hoặc cấu trúc góc, do đó phẫu thuật góc (mở bè củng mạc-giác mạc hoặc mở góc) có hiệu quả để mở đường dẫn lưu về mặt vật lý1). Trong khi đó, ở thể khởi phát muộn, nguyên nhân chính là tăng áp lực tĩnh mạch thượng củng mạc, và cấu trúc góc tương đối bình thường. Trong tình trạng áp lực tĩnh mạch thượng củng mạc cao, thuốc ức chế sản xuất thủy dịch là hiệu quả nhất và điều trị bằng thuốc là lựa chọn đầu tiên1). Nếu điều trị bằng thuốc không hiệu quả, hãy xem xét phẫu thuật lọc hoặc phẫu thuật shunt ống có thể bắc cầu qua hệ thống tĩnh mạch thượng củng mạc. Xem phần “Phương pháp điều trị tiêu chuẩn” để biết chi tiết.
Trong quản lý glôcôm liên quan đến SWS, tiến bộ được kỳ vọng trong các lĩnh vực sau.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm, Savona. 2020.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Yeom S, Comi AM. Updates on Sturge-Weber Syndrome. Handb Clin Neurol. 2015;132:157-168. doi:10.1016/B978-0-444-62702-5.00011-1.
Yadav PS, Adhikari P, Mehta B, et al. Unmasking Sturge-Weber Syndrome in Adulthood: A Case with Extrafacial Port-Wine Stain and Delayed Neurological Symptoms. Ann Med Surg. 2024;86:3679-3682.
Ainuz BY, Wolfe EM, Wolfe SA. Surgical Management of Facial Port-Wine Stain in Sturge Weber Syndrome. Cureus. 2021;13(1):e12637.
Pathak BD, Sharma S, Adhikari A, et al. Sturge-Weber Syndrome with Bilateral Port-Wine Stain. Case Rep Pediatr. 2022;2022:2191465.
Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368:1971-1979.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(4):616-629.