กลุ่มอาการสเตอร์จ-เวเบอร์ (SWS) เป็นกลุ่มอาการทางผิวหนังและระบบประสาทแต่กำเนิดที่มีสามอาการหลัก: ปานแดงพอร์ตไวน์บนใบหน้า, hemangioma เยื่อหุ้มสมองชั้นเลปโตเมนิงซ์ด้านเดียวกัน, และ hemangioma ในตา เกิดจากการกลายพันธุ์แบบโมเสกโซมาติกของยีน GNAQ
ต้อหิน เป็นภาวะแทรกซ้อนทางตาที่สำคัญที่สุดใน SWS เกิดขึ้นใน 30-70% ของกรณีเมื่อ hemangioma ลามไปถึงเปลือกตาประมาณ 60% เป็นชนิดเริ่มมีอาการเร็ว (ตั้งแต่แรกเกิดถึง 4 ปี) จากความผิดปกติของมุมตา และประมาณ 40% เป็นชนิดเริ่มมีอาการช้า (หลังวัยทารก) จากความดันหลอดเลือดดำอีพิสเกลอรัลที่เพิ่มขึ้น โดยมีกลยุทธ์การรักษาที่แตกต่างกัน
ในชนิดเริ่มมีอาการเร็ว เลือกผ่าตัดเปิดทราบีคิวลาร์หรือโกนิโอโตมี ส่วนชนิดเริ่มมีอาการช้า การรักษาด้วยยายับยั้งการผลิตอารมณ์ขันน้ำเป็นทางเลือกแรก 1)
เนื่องจากอุบัติการณ์สูงของ hemangioma คอรอยด์ และความเสี่ยงที่เพิ่มขึ้นของการตกเลือดในคอรอยด์ และจอประสาทตาลอก ระหว่างการผ่าตัด การเลือกเทคนิคการผ่าตัดและการเตรียมตัวก่อนผ่าตัดจึงมีความสำคัญอย่างยิ่ง 1)
แม้ว่าจะดื้อต่อการรักษามากกว่าต้อหิน แต่กำเนิด แต่การควบคุมความดันลูกตา ตั้งแต่เนิ่นๆ สามารถรักษาการมองเห็น ได้
กลุ่มอาการสเตอร์จ-เวเบอร์ (SWS) เป็นกลุ่มอาการทางผิวหนังและระบบประสาทแต่กำเนิดที่เรียกอีกอย่างว่า encephalotrigeminal angiomatosis มีลักษณะสามอาการหลัก: ปานแดงพอร์ตไวน์บนใบหน้าในบริเวณเส้นประสาทไทรเจมินัล , hemangioma เยื่อหุ้มสมองชั้นเลปโตเมนิงซ์ด้านเดียวกัน, และ hemangioma ในตา ในปี 1879 สเตอร์จรายงานผู้ป่วยที่มีปานแดงบนใบหน้าร่วมกับตาบวม (buphthalmos) และมีอัมพาตครึ่งซีกและลมชัก และในปี 1929 เวเบอร์ได้กำหนดกลุ่มอาการนี้ขึ้น
สาเหตุเกิดจากการกลายพันธุ์แบบโมเสกในเซลล์ร่างกายของยีน GNAQ (การกลายพันธุ์หลังการปฏิสนธิ) ซึ่งไม่ใช่โรคทางพันธุกรรม และส่วนใหญ่เป็นผู้ป่วยประปราย 4) 8) เชื่อว่าเกิดจากความผิดปกติของการพัฒนาหลอดเลือดเนื่องจากความผิดปกติของระบบประสาทซิมพาเทติกในระยะตัวอ่อน ความถี่ของการเกิดพบน้อย คือ 1 ใน 50,000 คนเกิด ไม่มีความแตกต่างทางเชื้อชาติหรือเพศ 5) 7)
SWS ถูกจำแนกทางคลินิกเป็น 3 ชนิดดังนี้:
การจำแนก (Roach) ลักษณะ ชนิดที่ 1 (แบบคลาสสิก) PWS + อาการทางระบบประสาท + ต้อหิน ชนิดที่ 2 PWS + ต้อหิน (ไม่มีรอยโรคทางระบบประสาท) ชนิดที่ 3 (พบน้อยที่สุด) เฉพาะ hemangioma ของเยื่อหุ้มสมอง
ต้อหิน เป็นภาวะแทรกซ้อนทางตาที่สำคัญที่สุดใน SWS โดยมีอัตราการเกิดต้อหิน สูงที่สุดในกลุ่มโรคเนวัส 2) เมื่อ hemangioma ลามไปถึงเปลือกตา ต้อหิน จะเกิดขึ้นด้วยความถี่สูงถึง 30-70% Hemangioma ของคอรอยด์ พบร่วมในผู้ป่วยประมาณ 40%
ตามระยะเวลาที่เริ่มเกิด ต้อหิน แบ่งเป็นชนิดเริ่มต้นเร็วและเริ่มต้นช้า ประมาณ 60% เป็นชนิดเริ่มต้นเร็วที่เกิดขึ้นตั้งแต่แรกเกิดถึงอายุ 4 ปี สาเหตุหลักคือความผิดปกติของการพัฒนาของมุมช่องหน้าม่านตา ส่วนที่เหลือประมาณ 40% เป็นชนิดเริ่มต้นช้าที่เกิดขึ้นหลังวัยทารก โดยความดันหลอดเลือดดำเอพิสเกลอรัลที่เพิ่มขึ้นและ hemangioma คอรอยด์ มีส่วนเกี่ยวข้องในพยาธิกำเนิด มักเกิดขึ้นก่อนอายุ 10 ปี
Q
กลุ่มอาการสเตอร์จ-เวเบอร์คือโรคอะไร?
A
กลุ่มอาการสเตอร์จ-เวเบอร์ (Sturge-Weber syndrome) เป็นกลุ่มอาการทางระบบประสาทและผิวหนังแต่กำเนิดที่มีสามอาการหลัก ได้แก่ ปานแดงบนใบหน้าบริเวณเส้นประสาทไทรเจมินัล (trigeminal nerve), หลอดเลือดผิดปกติในเยื่อหุ้มสมองชั้นเลปโตเมนิงซ์ (leptomeningeal) ด้านเดียวกัน, และหลอดเลือดผิดปกติในตา เกิดจากการกลายพันธุ์แบบโมเสกในร่างกายของยีน GNAQ ไม่ได้ถ่ายทอดทางพันธุกรรม และส่วนใหญ่เป็นผู้ป่วยเดี่ยวๆ 4) 8) ภาวะแทรกซ้อนหลัก ได้แก่ อาการชัก (75-90% เริ่มก่อนอายุ 3 ปี), ปัญญาอ่อน, อัมพาตครึ่งซีก, และต้อหิน (30-70%) นอกจากนี้ยังมีชนิดที่ 2 (ต้อหิน อย่างเดียว) และชนิดที่ 3 (หลอดเลือดผิดปกติในเยื่อหุ้มสมองอย่างเดียว) โดยไม่มีสามอาการหลักครบ ดูรายละเอียดในหัวข้อ “สาเหตุและปัจจัยเสี่ยง”
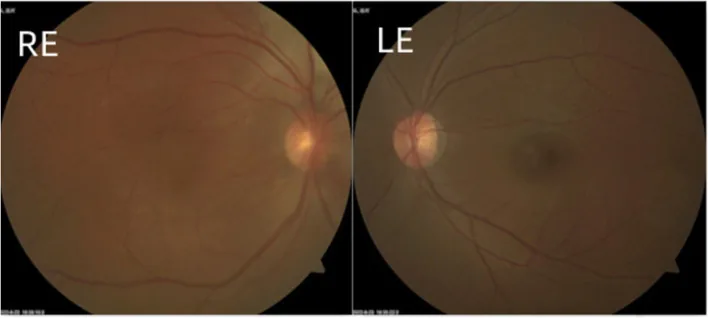
ภาพถ่ายจอตาในกลุ่มอาการสเตอร์จ-เวเบอร์ Zhang X, et al. Isolated diffuse choroidal
hemangioma without systemic symptoms: a case report. BMC Ophthalmol. 2023. Figure 2. PM
CI D: PMC10324158. License: CC BY.
ตาขวาแสดงสีแดงกระจายเข้มกว่าตาอีกข้าง โดยมีรอยโรคสีขาวเหลืองกระจายที่ขั้วหลังตา ซึ่งสอดคล้องกับ
hemangioma คอรอยด์ ที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
ในชนิดที่เริ่มต้นเร็ว อาการแรกเริ่มคือ น้ำตาไหล กลัวแสง และหนังตากระตุก ตามมาด้วยความบกพร่องทางการมองเห็น เนื่องจากเส้นผ่านศูนย์กลางกระจกตา เพิ่มขึ้นและกระจกตา ขุ่น (buphthalmos) อาจพบรอยแตกของเยื่อเดสเซเม็ท (Descemet’s membrane) ที่เรียกว่า Haab’s striae
ชนิดที่เริ่มต้นช้ามีลักษณะทางคลินิกคล้ายต้อหินมุมเปิด ปฐมภูมิ โดยมีอาการที่ผู้ป่วยรู้สึกน้อยในระยะแรก เมื่อดำเนินโรคจะเกิดการแคบลงของลานสายตาและการมองเห็น ลดลง
ต้อหิน 1) Hemangioma คอรอยด์ : เกิดขึ้นประมาณ 40% ของผู้ป่วย จอตามีสีแดงกระจาย (tomato ketchup fundus) อาจทำให้เกิดจอตาลอกแบบมีน้ำใต้จอตาผลการตรวจฟลูออเรสซีน แองจิโอกราฟี : ในระยะแรกพบรูปแบบหลอดเลือดคอรอยด์ ขนาดใหญ่ ระยะหลังพบการเรืองแสงมากเกินไปทั่วบริเวณก้อนการขยายและคดเคี้ยวของหลอดเลือดเอพิสเกลอราและเยื่อบุตา : พบเป็นสัญญาณของความดันหลอดเลือดดำเอพิสเกลอราเพิ่มขึ้นลักษณะมุมตา (ชนิดเริ่มต้นเร็ว) : มุมตาผิดปกติจากการสร้างไม่สมบูรณ์ โดยมีรากม่านตา เกาะสูงลักษณะมุมตา (ชนิดเริ่มต้นช้า) : ความผิดปกติของมุมตาน้อยมาก แต่มักพบเลือดในมุมตา ซึ่งบ่งชี้ถึงความดันหลอดเลือดดำเอพิสเกลอราเพิ่มขึ้น
ปานแดงสีไวน์พอร์ต (ปานไฟ) : ปรากฏตั้งแต่แรกเกิดบริเวณเส้นประสาทไทรเจมินัล แขนงที่ 1 (V1) และแขนงที่ 2 (V2) โดยปกติเป็นข้างเดียว แต่ก็อาจเป็นสองข้างได้7) สีจะเข้มขึ้นและหนาขึ้นตามอายุอาการชักจากโรคลมชัก : พบในผู้ป่วยประมาณ 80% โดย 75-90% เริ่มมีอาการก่อนอายุ 3 ปี พบอาการชักในผู้ป่วย 95% ที่มีรอยโรคที่เยื่อหุ้มสมองชั้นเลปโตเมนินซ์ทั้งสองข้างอาการทางระบบประสาท : อาจรวมถึงพัฒนาการทางจิตช้า (ประมาณ 50%) อัมพาตครึ่งซีกด้านตรงข้าม และตาบอดครึ่งซีกชนิดเดียวกัน หลอดเลือดผิดปกติที่เยื่อหุ้มสมองทำให้เกิดการฝ่อและหินปูนของเปลือกสมองกรณีที่เริ่มมีอาการในผู้ใหญ่ : มีรายงานผู้ป่วยที่มีอาการชักครั้งแรกเมื่ออายุ 55 ปี5) การวินิจฉัยอาจล่าช้าในกรณีที่ไม่ปกติซึ่งมีปานแดงสีไวน์พอร์ตนอกใบหน้า
SWS เกิดจากการกลายพันธุ์แบบโมเสกในเซลล์ร่างกายของยีน GNAQ (โครโมโซม 9q21.2) (c.548G→A, p.Arg183Gln)8) การกลายพันธุ์นี้ทำให้วิถีสัญญาณ Gαq ถูกกระตุ้นอย่างต่อเนื่อง ส่งผลให้เซลล์บุผนังหลอดเลือดเจริญเติบโตผิดปกติและเกิดความผิดปกติของหลอดเลือด4) เนื่องจากการกลายพันธุ์เป็นแบบโมเสกในเซลล์ร่างกาย ไม่ใช่การกลายพันธุ์ในเซลล์สืบพันธุ์ จึงไม่ถ่ายทอดทางพันธุกรรม การวินิจฉัยระดับโมเลกุลจำเป็นต้องตัดชิ้นเนื้อจากเนื้อเยื่อที่ได้รับผลกระทบ (โดยปกติคือผิวหนัง)4)
การตรวจหาการกลายพันธุ์ของ GNAQ ขึ้นอยู่กับตัวอย่างเนื้อเยื่อที่ได้รับผลกระทบและวิธีการวิเคราะห์ ดังนั้นการวินิจฉัยระดับโมเลกุลจึงต้องตีความร่วมกับลักษณะทางคลินิก
การกระจายของปานแดงสีไวน์พอร์ตและความเสี่ยง
เฉพาะบริเวณ V1 : ความเสี่ยงต่อโรคต้อหิน 6.7%
เฉพาะบริเวณ V2 : ความเสี่ยงต่อโรคต้อหิน แทบไม่มี
บริเวณ V1+V2 : ความเสี่ยงต่อโรคต้อหิน เพิ่มขึ้นอย่างมากเป็น 31.8%
บริเวณ V1+V2+V3 : ความเสี่ยงต่ออาการทางระบบประสาทเพิ่มขึ้น 4 เท่า
ความแตกต่างของระยะเวลาเกิดโรคและสาเหตุ
ชนิดที่เกิดเร็ว (ประมาณ 60%) : ความผิดปกติของพัฒนาการของมุมลูกตาส่วนหน้าเป็นสาเหตุหลัก แสดงอาการตาวัวและเส้นผ่านศูนย์กลางกระจกตา เพิ่มขึ้น 1)
ชนิดที่เกิดช้า (ประมาณ 40%) : ความดันหลอดเลือดดำอีพิสเกลอรัลสูงขึ้นและการมีส่วนร่วมของ hemangioma คอรอยด์ เป็นสาเหตุหลัก 1)
การลุกลามที่เปลือกตา : หาก hemangioma ลามไปถึงเปลือกตา อุบัติการณ์ของโรคต้อหิน จะเพิ่มขึ้นอย่างมีนัยสำคัญ
PWS ทั้งสองข้าง : มีโอกาสเป็น SWS สูงกว่าเมื่อเทียบกับข้างเดียว 7)
หากสงสัยกลุ่มอาการสเตอร์จ-เวเบอร์ ให้สังเกตตั้งแต่ระยะแรกเกิดถึงการเพิ่มขึ้นของเส้นผ่านศูนย์กลางกระจกตา ความขุ่นของกระจกตา และลักษณะของหัวประสาทตา หากมี hemangioma ที่เปลือกตา จำเป็นต้องตรวจคัดกรองโรคต้อหิน เป็นประจำ ทารกที่มีปานสีไวน์พอร์ตในบริเวณสาขาที่หนึ่งของเส้นประสาทไทรเจมินัล ควรได้รับการตรวจตาแต่เนิ่นๆ รวมถึงการวัดความดันลูกตา
การวินิจฉัยโรคต้อหิน ที่เกี่ยวข้องกับ SWS จำเป็นต้องมีการวัดความดันลูกตา อย่างแม่นยำและการตรวจส่วนหน้า มุมลูกตาส่วนหน้า และจอประสาทตา ในเด็ก มักจำเป็นต้องตรวจภายใต้การดมยาสลบ
การวัดความดันลูกตา ความดันลูกตา Goldmann ได้ยาก และเครื่องวัดแบบรีบาวด์ (เช่น iCare) มีประโยชน์ ต้องระมัดระวังในการตีความค่าที่วัดได้ในกรณีกระจกตา บวมหรือกระจกตา บางการตรวจส่วนหน้า : ตรวจสอบการเพิ่มขึ้นของเส้นผ่านศูนย์กลางกระจกตา (ปกติในทารกแรกเกิดประมาณ 10.5 มม.) ความขุ่นของกระจกตา และการมีเส้น Haab (รอยฉีกของเยื่อเดสเซเมท )การตรวจมุมลูกตาส่วนหน้า : จำเป็นสำหรับการระบุชนิดของโรคและการเลือกวิธีการรักษา ในชนิดที่เกิดเร็ว จะพบมุมลูกตาผิดปกติ (รากม่านตา เกาะสูงกว่าปกติ) ในชนิดที่เกิดช้า บางครั้งพบเลือดในมุมลูกตา ซึ่งบ่งชี้ถึงความดันหลอดเลือดดำอีพิสเกลอรัลสูงการตรวจจอประสาทตา : ประเมินการบุ๋มของหัวประสาทตา (การขยายของแอ่ง) หากมี hemangioma คอรอยด์ จอประสาทตา อาจมีสีแดงกระจาย
การตรวจฟลูออเรสซีน แองจิโอกราฟีของจอประสาทตา มีประโยชน์ ในระยะแรกจะเห็นรูปแบบหลอดเลือดคอรอยด์ ขนาดใหญ่ และในระยะหลังส่วนของเนื้องอกทั้งหมดจะแสดงการเรืองแสงมากเกินไป หลอดเลือดคอรอยด์ ชนิดกระจายอาจระบุได้ยากด้วยการตรวจตาปกติ
การตรวจซีทีสแกนศีรษะตรวจพบหินปูนในชั้นคอร์เทกซ์สมอง แม้ในระยะทารกแรกเกิดที่ยังไม่ปรากฏหินปูน การตรวจเอ็มอาร์ไอด้วยแกโดลิเนียมสามารถตรวจพบหลอดเลือดสมองชั้นเลปโตเมนิงซ์ได้ การประเมินการไหลเวียนเลือดสมองด้วยสเปกต์ก็ใช้เป็นส่วนเสริม
กลุ่มอาการสเตอร์จ-เวเบอร์ (SWS) เป็นหนึ่งในโรคปาน และเป็นโรคที่เป็นตัวแทนที่ทำให้เกิดหลอดเลือดคอรอยด์ การแยกโรคจากโรคปานอื่นๆ เป็นสิ่งสำคัญ
โรค ลักษณะทางตาที่เด่นชัด ตำแหน่งของหลอดเลือด/เนื้องอก SWS หลอดเลือดคอรอยด์ , ต้อหิน ใบหน้า + เลปโตเมนิงซ์ โรคฟอน ฮิปเพล-ลินเดา หลอดเลือดจอประสาทตา (บริเวณขมับส่วนปลาย) จอประสาทตา , สมองน้อย, ไตนิวโรไฟโบรมาโตซิสชนิดที่ 1 ก้อนลิชที่ม่านตา นิวโรไฟโบรมาที่ผิวหนัง โรคทูเบอรัส สเกลอโรซิส แฮมาร์โทมาจอประสาทตา สมอง ผิวหนัง ไต หัวใจ
นอกจากนี้ กลุ่มอาการคลิปเปล-เทรนอเนย์-เวเบอร์ยังแสดง hemangioma ผิวหนังคล้ายกับ SWS แต่แตกต่างกันตรงที่มีความผิดปกติของหลอดเลือดดำที่แขนขาและกระดูกและเนื้อเยื่ออ่อนโตเกิน
Q
วินิจฉัยโรคต้อหินใน SWS ได้อย่างไร?
A
ในผู้ป่วยที่มีปานสีแดงไวน์บนใบหน้า การตรวจตาเป็นประจำรวมถึงการวัดความดันลูกตา เป็นสิ่งจำเป็น ในเด็ก จะทำการวัดความดันลูกตา ด้วยเครื่อง rebound tonometer การตรวจส่วนหน้าของตา (เส้นผ่านศูนย์กลางกระจกตา ความขุ่นของกระจกตา การมีเส้น Haab) การตรวจมุมตา (ประเมินความผิดปกติของมุม) และการตรวจอวัยวะภายในตา (ประเมินการบุ๋มของจานประสาทตา ตรวจหา hemangioma คอรอยด์ ) ในเด็กมักต้องตรวจภายใต้การดมยาสลบ ในชนิดที่เริ่มมีอาการช้า การมีเลือดในมุมตาหรือการขยายของหลอดเลือดเหนือตาขาว มีประโยชน์ในการวินิจฉัยแยกโรค การตรวจหลอดเลือดด้วยฟลูออเรสซีน เป็นสิ่งจำเป็นในการประเมิน hemangioma คอรอยด์ และการประเมินทั่วร่างกายรวมถึง CT scan ศีรษะและ MRI ด้วยสารทึบแสง
การรักษาโรคต้อหิน ที่เกี่ยวข้องกับ SWS ต้องใช้กลยุทธ์ที่แตกต่างกันขึ้นอยู่กับระยะเวลาที่เริ่มมีอาการและกลไกการเกิดโรค
โรคต้อหินแต่กำเนิด หรือที่เริ่มในวัยทารกจำเป็นต้องได้รับการผ่าตัด 1) การผ่าตัด trabeculotomy หรือ goniotomy เป็นทางเลือกแรก 1) อย่างไรก็ตาม อัตราความสำเร็จต่ำกว่าเมื่อเทียบกับโรคต้อหินแต่กำเนิด ปฐมภูมิ และมักต้องผ่าตัดเพิ่มเติม
เมื่อทำการผ่าตัด trabeculectomy มีความเสี่ยงที่จะมีเลือดออกจาก hemangioma ทำให้เกิด hematoma ใต้คอรอยด์ ขนาดใหญ่หรือเลือดออกแบบ expulsive โดยทั่วไปการตอบสนองต่อการผ่าตัดต้อหิน ไม่ดี และมักต้องทำ trabeculectomy หรือการผ่าตัดใส่ท่อระบายน้ำ
ในทารกอายุต่ำกว่า 2 ปี ห้ามใช้ยาที่เป็น alpha-2 receptor agonist (brimonidine) เนื่องจากผลข้างเคียงกดระบบประสาทส่วนกลาง 1) หากต้องใช้ยา ควรเลือก beta-blocker และ carbonic anhydrase inhibitor ด้วยความระมัดระวัง
ในเด็กโต ความดันหลอดเลือดดำเหนือตาขาว สูงขึ้น ดังนั้นการรักษาด้วยยาจึงเป็นทางเลือกแรก 1) ยาที่ลดการผลิต aqueous humor (beta-blocker, carbonic anhydrase inhibitor) ถือว่ามีประสิทธิภาพมากที่สุด รายงานผลการลดความดันลูกตา ของยาที่คล้าย prostaglandin ไม่สม่ำเสมอ
หากการรักษาด้วยยาหรือการสร้างทางระบายน้ำใหม่ไม่ได้ผล ให้พิจารณาการตัดเนื้อเยื่อ trabecular หรือการผ่าตัดใส่ท่อระบายน้ำ 1)
การผ่าตัดกรองและการใส่ท่อระบายน้ำ
การตัดเนื้อเยื่อ trabecular : การใช้ยาต้านเมแทบอไลต์ (mitomycin C) อาจช่วยให้ผลลัพธ์ดีขึ้น อย่างไรก็ตาม ในตา SWS ความเสี่ยงของ choroidal effusion และ expulsive hemorrhage สูงมาก 1)
อุปกรณ์ Ahmed : มีรายงานอัตราความสำเร็จสะสม 79% ที่ 24 เดือน และ 30% ที่ 60 เดือน
อุปกรณ์ Baerveldt แบบสองขั้นตอน : มีรายงานว่าทุกกรณีมีความดัน <21 mmHg ในการติดตามผลเฉลี่ย 35 เดือน
การวิเคราะห์อภิมาน GDD ในเด็ก : การวิเคราะห์ 1221 ตา พบอัตราความสำเร็จ 87% (ช่วงความเชื่อมั่น 95%: 83-91%) ที่ 12 เดือน และ 77% (ช่วงความเชื่อมั่น 95%: 71-83%) ที่ 24 เดือน 9)
การจัดการภาวะแทรกซ้อนระหว่างและหลังผ่าตัด
เลือดออกและ choroidal effusion : ในกรณีที่มี choroidal hemangioma การลดความดันลูกตา อย่างรวดเร็วจะเพิ่มความเสี่ยงต่อการหลุดลอกของ choroid และเลือดออก 1)
มาตรการป้องกัน : การลดความดันลูกตา ก่อนผ่าตัดด้วยยาที่มีแรงดันออสโมซิสสูง การทำ posterior sclerotomy การวางไหมเย็บ scleral ล่วงหน้า และการเย็บเพิ่มเติมที่แข็งแรง
การเลือกอุปกรณ์ : การใช้ GDD แบบมีวาล์ว (Ahmed) หรือแบบสองขั้นตอน (Baerveldt) ช่วยลดความเสี่ยงของความดันต่ำ
การจี้แสงเลนส์ปรับเลนส์ตา : ในกรณีที่ดื้อต่อการรักษา ให้พิจารณาการจี้แสงเลนส์ปรับเลนส์ตา (CPC) มีรายงานว่า 10 ใน 16 ตา (62.5%) รักษาความดันลูกตา 6-22 mmHg โดยไม่มีภาวะแทรกซ้อน (ติดตามผลเฉลี่ย 8.87 ปี)
ในวิธีสองขั้นตอน จะเกิดแคปซูลรอบแผ่นรองรับหลายสัปดาห์ก่อนที่จะใส่ท่อเข้าไปในช่องหน้าม่านตา ซึ่งป้องกันการลดลงของความดันลูกตา ที่มากเกินไปทันทีหลังผ่าตัด และลดความเสี่ยงของ choroidal effusion และเลือดออกให้น้อยที่สุด วิธีนี้มีประโยชน์โดยเฉพาะในกรณี SWS ที่มี choroidal hemangioma
มีรายงานว่า netarsudil (ยายับยั้ง Rho kinase ) สามารถลดความดันลูกตา ในโรคต้อหิน ที่เกี่ยวข้องกับ SWS ได้อย่างมีประสิทธิภาพแม้จะใช้เป็นยาทางเลือกที่สี่หรือห้าก็ตาม ยานี้ออกฤทธิ์โดยเพิ่มการไหลออกของอารมณ์ขันน้ำผ่านทาง trabecular meshwork
Hemangioma คอรอยด์ ชนิดแพร่กระจายที่เกี่ยวข้องกับ SWS อาจต้องจัดการควบคู่ไปกับการรักษาโรคต้อหิน
ไม่มีอาการ : สังเกตอาการการทำงานของการมองเห็น ลดลงเนื่องจากจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา : สามารถเลือกใช้การจี้แข็งจอประสาทตา ด้วยแสง, การรักษาด้วยความร้อนผ่านรูม่านตา (TTT) หรือการรักษาด้วยแสงไดนามิก (PDT ) อย่างไรก็ตาม PDT ไม่ครอบคลุมโดยประกันHemangioma คอรอยด์ ชนิดแพร่กระจาย : พิจารณา PDT หรือการฉายรังสีขนาดต่ำ (ประมาณ 20 Gy)จอประสาทตาลอก ชนิดมีน้ำขังการจี้เย็น เป็นข้อบ่งชี้ หากผลไม่เพียงพอ ให้ทำการฉายรังสีการรับประทาน propranolol (ยาปิดกั้นเบตา) : มีรายงานถึงความเป็นไปได้ในการทำให้เนื้องอกเล็กลง แต่ไม่ครอบคลุมโดยประกัน
โปรดทราบว่าการผ่าตัด trabeculectomy ในตา SWS มีความเสี่ยงสูงมากต่อการเกิดน้ำรั่วใต้คอรอยด์ หรือเลือดออกในคอรอยด์ แบบเบียดดัน 1) หากมี hemangioma คอรอยด์ ควรพิจารณาการฉายรังสีก่อนผ่าตัด และแนะนำให้ใช้อุปกรณ์ระบายต้อหิน ชนิดมีวาล์วหรือแบบสองขั้นตอน สิ่งสำคัญคือต้องลดความดันลูกตา อย่างเพียงพอด้วยยาออสโมติกก่อนผ่าตัด และเตรียมพร้อมสำหรับการผ่าตัดเปิดตาขาว ส่วนหลัง
แม้ว่าจะรักษายากกว่าต้อหิน แต่กำเนิด แต่การมองเห็น สามารถรักษาไว้ได้หากควบคุมความดันลูกตา ได้ดีตั้งแต่เนิ่นๆ อย่างไรก็ตาม หาก hemangioma คอรอยด์ มีขนาดใหญ่ขึ้นและทำให้เกิดจอประสาทตาลอก ชนิดมีน้ำขัง การจี้เย็น อาจไม่ได้ผลเพียงพอ ทำให้เกิดความบกพร่องทางการมองเห็น อย่างรุนแรง
เนื่องจากรอยโรคส่งผลกระทบต่อกระจกตา เลนส์แก้วตา จอประสาทตา และเส้นประสาท จึงมักเป็นเรื่องยากที่จะได้การมองเห็น ที่ดี อายุขัยเฉลี่ยของผู้ป่วย SWS สั้นกว่าประชากรทั่วไป และหากมีรอยโรคที่เยื่อหุ้มสมองชั้นในทั้งสองข้าง อาการทางระบบประสาทจะรุนแรงขึ้นและการพยากรณ์โรคแย่ลง
Q
สิ่งที่ควรระวังเป็นพิเศษในการรักษาต้อหินใน SWS คืออะไร?
A
จุดสำคัญที่สุดคือภาวะแทรกซ้อนจากการผ่าตัดที่เกี่ยวข้องกับ hemangioma คอรอยด์ ใน SWS พบ hemangioma คอรอยด์ ในประมาณ 40% ของกรณี และการลดลงของความดันลูกตา อย่างรวดเร็วระหว่างการผ่าตัดต้อหิน มีความเสี่ยงที่จะทำให้น้ำรั่วใต้คอรอยด์ เลือดออก หรือจอประสาทตาลอก 1) มาตรการป้องกันรวมถึงการให้ยาออสโมติกก่อนผ่าตัด การทำผ่าตัดเปิดตาขาว ส่วนหลัง การเย็บแผ่นตาขาว ให้แน่น และการใช้อุปกรณ์ระบายชนิดมีวาล์วหรือแบบสองขั้นตอน นอกจากนี้ควรทราบด้วยว่ายากระตุ้นตัวรับอัลฟา-2 (brimonidine) ห้ามใช้ในเด็กอายุต่ำกว่า 2 ปี 1) ดูรายละเอียดในหัวข้อ «การรักษามาตรฐาน»
สาเหตุพื้นฐานของ SWS คือการกลายพันธุ์แบบโมเสกในเซลล์ร่างกายของยีน GNAQ (c.548G→A, p.Arg183Gln)8) การกลายพันธุ์นี้กระตุ้นวิถีสัญญาณ Gαq อย่างต่อเนื่อง ทำให้เกิดการเพิ่มจำนวนของเซลล์บุผนังหลอดเลือดที่ไม่สามารถควบคุมได้และความผิดปกติของหลอดเลือด4) การกลายพันธุ์เกิดขึ้นในเซลล์ร่างกายระยะแรกหลังการปฏิสนธิ ดังนั้นการกระจายของเซลล์ที่กลายพันธุ์จึงกำหนดความหลากหลายของฟีโนไทป์ทางคลินิก (ชนิด I–III)
ในแนวทางการรักษาโรคต้อหิน (ฉบับที่ 5) ได้ระบุกลไกการเพิ่มขึ้นของความดันลูกตา ใน SWS ดังต่อไปนี้1)
ความผิดปกติของมุมตาโดยปฐมภูมิ : ความผิดปกติแต่กำเนิดของทางระบายอารมณ์ขันน้ำ ซึ่งเป็นสาเหตุหลักของชนิดที่เริ่มมีอาการเร็วการฝ่อของคลองชเลมม์ : มีส่วนทำให้ความดันลูกตา เพิ่มขึ้นเนื่องจากความผิดปกติของโครงสร้างทางระบายอารมณ์ขันน้ำ1) ความดันหลอดเลือดดำอีพิสเกลอรัลสูง : เนื่องจาก hemangioma ที่ผิวตาและเบ้าตา ทำให้การระบายเลือดดำบกพร่อง เพิ่มความต้านทานต่อการไหลออกของอารมณ์ขันน้ำ เป็นสาเหตุหลักของชนิดที่เริ่มมีอาการช้า1) การเกิดพังผืดยึดม่านตา ส่วนปลาย (PAS ) : หลอดเลือดใหม่ในม่านตา และมุมตาอาจทำให้เกิดต้อหินมุมปิด ทุติยภูมิ2) 3) การเพิ่มการซึมผ่านของผนังหลอดเลือดบางที่เกี่ยวข้องกับ hemangioma คอรอยด์ : การรั่วซึมจากคอรอยด์ มีส่วนทำให้ความดันลูกตา เพิ่มขึ้น1)
การตรวจทางจุลกายวิภาคของลูกตาที่ถูกตัดออกพบผลดังต่อไปนี้ ซึ่งคล้ายคลึงกับที่พบในต้อหิน แต่กำเนิดปฐมภูมิ
trabecular meshwork ส่วน uveal กว้าง
กล้ามเนื้อซิลิอารีเกาะติดโดยตรงกับ trabecular meshwork
scleral spur ที่ยังไม่พัฒนาเต็มที่
โคนม่านตา เกาะติดด้านหน้า
ในกรณีที่เกิดโรคในวัยทารก ความผิดปกติของพัฒนาการของมุมช่องหน้าม่านตา ถือเป็นปัจจัยที่สำคัญที่สุด
ในกรณีที่เกิดโรคในช่วงวัยรุ่นตอนปลายถึงอายุ 20 ปีขึ้นไป สาเหตุหลักคือความดันหลอดเลือดดำอีพิสเกลอรัลที่สูงขึ้นจาก hemangioma 1) การตรวจ gonioscopy พบความผิดปกติของมุมน้อยมาก แต่มักพบเลือดในมุม ซึ่งสัมพันธ์กับความดันหลอดเลือดดำอีพิสเกลอรัลที่สูงขึ้น ในภาวะนี้ ยาที่กดการผลิต aqueous humor ถือว่ามีประสิทธิภาพมากที่สุด และการรักษาด้วยยาเป็นทางเลือกแรก
ความแก่ก่อนวัยของ trabecular meshwork : ถูกเสนอเป็นกลไกที่ทำให้เกิดโรคต้อหินมุมเปิด เรื้อรังในผู้ใหญ่ตอนต้นพยาธิสรีรวิทยาของ choroidal hemangioma : การเพิ่มจำนวนของหลอดเลือดผิดปกติในคอรอยด์ ทำให้เกิดรอยโรคยกตัวสีแดงถึงส้มแดงที่จอตา รอยโรคที่เกี่ยวข้องกับ SWS มักกระจาย ขอบเขตไม่ชัดเจน แสดงภาพทางคลินิกที่แตกต่างจาก choroidal hemangioma ชนิดเดี่ยวพยาธิสรีรวิทยาของสมอง : Leptomeningeal hemangioma ทำให้เกิดภาวะเลือดคั่งในหลอดเลือดดำ ในระยะแรกการไหลเวียนเลือดชดเชยเพิ่มขึ้น แต่ต่อมาปริมาณเลือดไปเลี้ยงสมองและการเผาผลาญกลูโคสลดลง ทำให้เกิดการเสื่อมและฝ่อของเซลล์ประสาท
Q
ทำไมวิธีการรักษาจึงแตกต่างกันระหว่างชนิดที่เกิดเร็วและชนิดที่เกิดช้า?
A
เนื่องจากกลไกการเกิดต้อหิน ของทั้งสองชนิดแตกต่างกันโดยพื้นฐาน ในชนิดที่เกิดเร็ว สาเหตุหลักคือความผิดปกติแต่กำเนิดของมุมช่องหน้าม่านตา ซึ่งมีปัญหาที่ trabecular meshwork หรือโครงสร้างของมุมเอง ดังนั้นการผ่าตัดมุม (trabeculotomy หรือ goniotomy) จึงมีประสิทธิภาพในการเปิดทางระบายออกทางกายภาพ1) ในขณะที่ชนิดที่เกิดช้า สาเหตุหลักคือความดันหลอดเลือดดำอีพิสเกลอรัลสูงขึ้น และโครงสร้างของมุมค่อนข้างปกติ ในภาวะความดันหลอดเลือดดำอีพิสเกลอรัลสูง ยาที่กดการผลิต aqueous humor มีประสิทธิภาพมากที่สุด และการรักษาด้วยยาเป็นทางเลือกแรก1) หากการรักษาด้วยยาไม่ได้ผล ให้พิจารณาการผ่าตัดกรอง หรือการผ่าตัด shunt tube ที่สามารถบายพาสระบบหลอดเลือดดำอีพิสเกลอรัล ดูรายละเอียดในหัวข้อ “วิธีการรักษามาตรฐาน”
ในการจัดการต้อหิน ที่เกี่ยวข้องกับ SWS คาดว่าจะมีความก้าวหน้าในด้านต่อไปนี้
การวินิจฉัยระดับโมเลกุลของการกลายพันธุ์แบบโมเสกโซมาติก GNAQ : การกลายพันธุ์ GNAQ ที่ระบุโดย Shirley และคณะในปี 2013 ได้อธิบายพื้นฐานโมเลกุลของ SWS และ port-wine hemangioma 8) ในอนาคต คาดว่าจะมีการวินิจฉัยตั้งแต่เนิ่นๆ และการรักษาเฉพาะบุคคลโดยอาศัยการตรวจทางพันธุกรรมอุปกรณ์ระบายน้ำต้อหิน แบบสองขั้นตอนคอรอยด์ ที่เกี่ยวข้องกับการผ่าตัดกรอง แบบดั้งเดิมเนทาร์ซูดิล (ยับยั้ง Rho kinase) : มีรายงานประสิทธิภาพในต้อหิน ที่เกี่ยวข้องกับ SWS ในฐานะยาที่ส่งเสริมการไหลของอารมณ์ขันจาก trabecular meshworkความสำคัญของการทำงานร่วมกันแบบสหสาขาวิชาชีพ : ความร่วมมือระหว่างกุมารเวชศาสตร์ ประสาทวิทยา จักษุวิทยา ผิวหนัง และจิตเวชศาสตร์เป็นสิ่งจำเป็นสำหรับการจัดการระยะยาวของ SWS6) มีรายงานว่าภาวะแทรกซ้อนทางจิตใจส่งผลต่อผลการผ่าตัด และความสำคัญของการดูแลแบบองค์รวมรวมถึงการสนับสนุนทางจิตใจเป็นที่ยอมรับการรักษาด้วยเลเซอร์ พัลส์ไดย์สำหรับปานแดงพอร์ตไวน์
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm, Savona. 2020.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Yeom S, Comi AM. Updates on Sturge-Weber Syndrome. Handb Clin Neurol. 2015;132:157-168. doi:10.1016/B978-0-444-62702-5.00011-1.
Yadav PS, Adhikari P, Mehta B, et al. Unmasking Sturge-Weber Syndrome in Adulthood: A Case with Extrafacial Port-Wine Stain and Delayed Neurological Symptoms. Ann Med Surg. 2024;86:3679-3682.
Ainuz BY, Wolfe EM, Wolfe SA. Surgical Management of Facial Port-Wine Stain in Sturge Weber Syndrome. Cureus. 2021;13(1):e12637.
Pathak BD, Sharma S, Adhikari A, et al. Sturge-Weber Syndrome with Bilateral Port-Wine Stain. Case Rep Pediatr. 2022;2022:2191465.
Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368:1971-1979.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(4):616-629.