توزیع همانژیوم پورت واین و خطر
فقط ناحیه V1: خطر گلوکوم ۶.۷٪
فقط ناحیه V2: خطر گلوکوم تقریباً صفر
نواحی V1 + V2: خطر گلوکوم به طور قابل توجهی به ۳۱.۸٪ افزایش مییابد
نواحی V1 + V2 + V3: خطر علائم عصبی ۴ برابر افزایش مییابد

سندرم استورج-وبر (Sturge-Weber Syndrome: SWS) که آنژیوماتوز انسفالوتریژمینال نیز نامیده میشود، یک سندرم نوروکوتانئوس مادرزادی (فاکوماتوز) است. سه علامت اصلی آن عبارتند از: لکه شرابی صورت (نِووس فلامئوس) در ناحیه عصب سهقلو، همانژیوم لپتومننژال همان طرف، و همانژیوم چشمی. در سال 1879، استورج موردی از همانژیوم صورت، بوفتالموس، همیپلژی و صرع را گزارش کرد و در سال 1929، وبر این سندرم را به عنوان یک موجودیت بالینی تثبیت کرد.
علت آن جهش سوماتیک موزاییک در ژن GNAQ (جهش پس از زیگوت) است و ارثی نیست و بیشتر موارد تک گیر هستند 4)8). تصور میشود که ناشی از ناهنجاری عروقی به دلیل اختلال سمپاتیک جنینی باشد. فراوانی بروز نادر است و یک مورد در ۵۰,۰۰۰ تولد رخ میدهد و تفاوت نژادی یا جنسیتی ندارد 5)7).
SWS بر اساس تصویر بالینی به سه نوع زیر طبقهبندی میشود:
| طبقهبندی (روچ) | ویژگی |
|---|---|
| نوع I (کلاسیک) | PWS + علائم عصبی + گلوکوم |
| نوع II | PWS + گلوکوم (بدون ضایعه عصبی) |
| نوع III (بسیار نادر) | فقط مننژیوما عروقی |
گلوکوم مهمترین عارضه چشمی در SWS است و بالاترین میزان بروز گلوکوم را در میان فاکوماتوزها دارد 2). اگر همانژیوم پلک را درگیر کند، گلوکوم با فراوانی ۳۰ تا ۷۰٪ ایجاد میشود. همانژیوم کوروئید در حدود ۴۰٪ از بیماران دیده میشود.
بر اساس زمان بروز، گلوکوم به دو نوع زودرس و دیررس تقسیم میشود. حدود ۶۰٪ موارد از نوع زودرس هستند که بلافاصله پس از تولد تا ۴ سالگی بروز میکنند و علت اصلی آن ناهنجاری رشدی زاویه است. حدود ۴۰٪ باقیمانده از نوع دیررس هستند که پس از دوران نوزادی بروز میکنند و افزایش فشار ورید اپیاسکلرا و همانژیوم کوروئید در علت آن نقش دارند. اغلب تا ۱۰ سالگی بروز میکند.
سندرم استورج-وبر یک اختلال عصبی-پوستی مادرزادی است که با سه علامت اصلی مشخص میشود: همانژیوم صورت (لکه شرابی) در ناحیه عصب سهقلو، همانژیوم لپتومننژال همان طرف، و همانژیوم چشمی. علت آن جهش موزاییک سوماتیک در ژن GNAQ است و ارثی نیست و بیشتر موارد پراکنده هستند 4)8). علائم عصبی مانند صرع (۷۵-۹۰٪ موارد تا سن ۳ سالگی)، ناتوانی ذهنی، و همیپارزی، و همچنین گلوکوم (۳۰-۷۰٪) از عوارض اصلی هستند. انواع II (فقط گلوکوم) و III (فقط همانژیوم مننژ) نیز وجود دارند که سه علامت اصلی را ندارند. برای جزئیات به بخش «علل و عوامل خطر» مراجعه کنید.
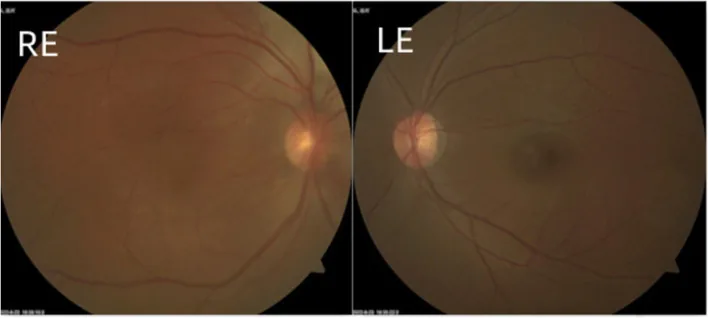
در نوع زودرس، اشکریزش، فتوفوبی و اسپاسم پلک علائم اولیه هستند. افزایش قطر قرنیه و کدورت قرنیه (بوفتالموس) منجر به اختلال بینایی میشود. ممکن است خطوط هاب (Haab) که نشانه پارگی غشای دسمه است، مشاهده شود.
نوع دیررس از نظر بالینی مشابه گلوکوم زاویه باز اولیه است و در مراحل اولیه علائم ذهنی کمی دارد. با پیشرفت، تنگی میدان بینایی و کاهش بینایی رخ میدهد.
SWS ناشی از جهش موزاییک سوماتیک در ژن GNAQ (کروموزوم ۹q21.2) (c.548G→A, p.Arg183Gln) است8). این جهش باعث فعال شدن دائمی مسیر سیگنالینگ Gαq و در نتیجه تکثیر کنترلنشده سلولهای اندوتلیال و ناهنجاری عروقی میشود4). از آنجا که این جهش سوماتیک موزاییک است و نه ژرمینال، ارثی نیست. برای تشخیص مولکولی، بیوپسی از بافت مبتلا (معمولاً پوست) لازم است4).
تشخیص جهش GNAQ تحت تأثیر نمونه بافت مبتلا و روش تحلیلی است، بنابراین تشخیص مولکولی باید در ترکیب با یافتههای بالینی تفسیر شود.
توزیع همانژیوم پورت واین و خطر
فقط ناحیه V1: خطر گلوکوم ۶.۷٪
فقط ناحیه V2: خطر گلوکوم تقریباً صفر
نواحی V1 + V2: خطر گلوکوم به طور قابل توجهی به ۳۱.۸٪ افزایش مییابد
نواحی V1 + V2 + V3: خطر علائم عصبی ۴ برابر افزایش مییابد
تفاوت در زمان بروز و علت بیماری
نوع زودرس (حدود 60%): ناهنجاری رشدی زاویه اتاق قدامی علت اصلی است. با چشم گاوی و افزایش قطر قرنیه تظاهر میکند1)
نوع دیررس (حدود 40%): افزایش فشار ورید اپیاسکلرا و درگیری همانژیوم کوروئید علت اصلی است1)
تهاجم پلکی: اگر همانژیوم به پلک گسترش یابد، بروز گلوکوم به طور قابل توجهی افزایش مییابد
PWS دوطرفه: در مقایسه با یکطرفه، احتمال SWS بیشتر است7)
برای تشخیص گلوکوم همراه با SWS، اندازهگیری دقیق فشار چشم و معاینه بخش قدامی، زاویه و فوندوس اهمیت دارد. در کودکان اغلب معاینه تحت بیهوشی عمومی ضروری است.
آنژیوگرافی فلورسئین مفید است. در مراحل اولیه، الگوی عروق کوروئید بزرگ دیده میشود و در مراحل پایانی، کل ناحیه تومور هیپرفلورسنس نشان میدهد. آنژیوم کوروئید منتشر ممکن است در معاینه معمول فوندوس به سختی قابل شناسایی باشد.
سیتی اسکن سر برای تشخیص کلسیفیکاسیون داخل قشر مغز استفاده میشود. حتی در دوره نوزادی که کلسیفیکاسیون ظاهر نشده است، امآرآی با گادولینیوم میتواند آنژیوم لپتومننژ را تشخیص دهد. ارزیابی جریان خون مغزی با اسپکت نیز به عنوان روش کمکی استفاده میشود.
سندرم استرج-ویبر یکی از فاکوماتوزها است و یک بیماری شایع ایجادکننده آنژیوم کوروئید میباشد. افتراق از سایر فاکوماتوزها مهم است.
| بیماری | یافتههای چشمی مشخص | محل آنژیوم/تومور |
|---|---|---|
| SWS | آنژیوم کوروئید، گلوکوم | صورت + لپتومننژ |
| بیماری فون هیپل-لینداو | آنژیوم رتین (محیطی تمپورال) | رتین، مخچه، کلیه |
| نوروفیبروماتوز نوع 1 | ندول Lisch عنبیه | نوروفیبروم پوستی |
| اسکلروز توبروز | همارتوم شبکیه | مغز، پوست، کلیه، قلب |
همچنین، سندرم کلیپل-ترنونه-وبر با همانژیوم پوستی مشابه SWS ظاهر میشود، اما با ناهنجاریهای وریدی اندامها و هیپرتروفی بافت نرم استخوانی افتراق داده میشود.
در بیمارانی که همانژیوم پورت واین در صورت دارند، معاینات منظم چشم پزشکی شامل اندازهگیری فشار داخل چشم ضروری است. در کودکان، اندازهگیری فشار با تونومتر برگشتی، معاینه بخش قدامی (قطر قرنیه، کدورت قرنیه، وجود خطوط هاب)، گونیوسکوپی (ارزیابی ناهنجاریهای زاویه)، و معاینه فوندوس (ارزیابی حفرات دیسک بینایی، تشخیص همانژیوم کوروئید) انجام میشود. در کودکان اغلب نیاز به معاینه تحت بیهوشی عمومی است. در نوع دیررس، وجود خون در زاویه و اتساع عروق اپی اسکلرال برای افتراق مفید است. آنژیوگرافی فلورسین برای ارزیابی همانژیوم کوروئید ضروری است و برای ارزیابی سیستمیک، سی تی اسکن سر و ام آر آی با کنتراست انجام میشود.
درمان گلوکوم همراه با SWS بسته به زمان شروع و مکانیسم پاتوژنز نیازمند استراتژیهای متفاوتی است.
گلوکوم مادرزادی یا شروع در شیرخوارگی نیاز به درمان جراحی دارد1). ترابکولوتومی یا گونیوتومی اولین انتخاب هستند1). با این حال، میزان موفقیت در مقایسه با گلوکوم مادرزادی اولیه کمتر است و اغلب نیاز به جراحی اضافی وجود دارد.
انجام ترابکولکتومی ممکن است منجر به خونریزی از همانژیوم و ایجاد هماتوم شدید فوق کوروئید یا خونریزی تخلیهای شود. به طور کلی، پاسخ به جراحی گلوکوم خوب نیست و اغلب نیاز به ترابکولکتومی یا جراحی شنت لولهای است.
در کودکان بزرگتر، به دلیل افزایش فشار ورید اپی اسکلرال، درمان دارویی اولین انتخاب است1). داروهای کاهشدهنده تولید زلالیه (بتا بلوکرها، مهارکنندههای کربنیک آنهیدراز) مؤثرترین هستند. اثر کاهش فشار داخل چشم داروهای پروستاگلاندین یکنواخت گزارش نشده است.
در صورت عدم موفقیت درمان دارویی یا جراحی بازسازی مسیر خروجی، ترابکولکتومی یا جراحی شانت لولهای در نظر گرفته میشود1).
جراحی فیلتراسیون / شانت لولهای
ترابکولکتومی: استفاده همزمان از داروی ضد متابولیت (میتومایسین C) ممکن است نتایج را بهبود بخشد. با این حال، در چشمهای مبتلا به SWS، خطر افیوژن کوروئید و خونریزی اکسپولسیو بسیار بالاست1).
دستگاه Ahmed: میزان موفقیت تجمعی 79% در 24 ماه و 30% در 60 ماه گزارش شده است.
دستگاه Baerveldt دو مرحلهای: در یک گزارش، تمام موارد در پیگیری متوسط 35 ماه به فشار داخل چشمی کمتر از 21 میلیمتر جیوه دست یافتند.
متاآنالیز GDD کودکان: تجزیه و تحلیل 1221 چشم نشان داد که میزان موفقیت 87% (95% CI: 83-91%) در 12 ماه و 77% (95% CI: 71-83%) در 24 ماه است9).
مدیریت عوارض حین و پس از جراحی
خونریزی و افیوژن کوروئید: در صورت وجود همانژیوم کوروئید، کاهش ناگهانی فشار داخل چشمی خطر جداشدگی و خونریزی کوروئید را افزایش میدهد1).
اقدامات پیشگیرانه: کاهش فشار داخل چشمی قبل از عمل با داروهای هیپراسمولار، انجام اسکلروتومی خلفی، قرار دادن بخیههای فلپ صلبیه از قبل و بخیههای اضافی محکم.
انتخاب دستگاه: استفاده از GDD دارای دریچه (Ahmed) یا دو مرحلهای (Baerveldt) خطر افت فشار خون را کاهش میدهد.
فتوکواگولاسیون سیکلی (CPC): در موارد مقاوم، فتوکواگولاسیون سیکلی در نظر گرفته میشود. در یک گزارش، 10 از 16 چشم (62.5%) بدون عارضه فشار داخل چشمی 6 تا 22 میلیمتر جیوه را حفظ کردند (میانگین پیگیری 8.87 سال).
در روش دو مرحلهای، چند هفته قبل از قرار دادن لوله در اتاق قدامی، یک کپسول در اطراف صفحه تشکیل میشود. این کار از کاهش بیش از حد فشار داخل چشمی بلافاصله پس از جراحی جلوگیری کرده و خطر افیوژن و خونریزی کوروئید را به حداقل میرساند. این روش به ویژه در موارد SWS که با همانژیوم کوروئید همراه است، مفید است.
گزارش شده است که نتارسودیل (مهارکننده Rho کیناز) حتی زمانی که به عنوان داروی خط چهارم تا پنجم اضافه میشود، فشار داخل چشم گلوکوم مرتبط با SWS را به طور مؤثر کاهش میدهد. این دارو با تسهیل خروج زلالیه از ترابکول عمل میکند.
همانژیوم منتشر کوروئید مرتبط با SWS ممکن است نیاز به مدیریت همزمان با درمان گلوکوم داشته باشد.
اگرچه این بیماری نسبت به گلوکوم تکاملی مقاومتر است، اما در صورت کنترل زودهنگام و خوب فشار داخل چشم، حفظ بینایی امکانپذیر است. با این حال، اگر همانژیوم کوروئید بزرگ شده و باعث جداشدگی اگزوداتیو شبکیه شود، حتی کرایوتراپی نیز ممکن است به اندازه کافی مؤثر نباشد و منجر به اختلال شدید بینایی شود.
از آنجایی که ضایعه قرنیه، عدسی، شبکیه و عصب را درگیر میکند، دستیابی به بینایی خوب اغلب دشوار است. امید به زندگی بیماران SWS در مقایسه با جمعیت عمومی کوتاهتر است و در صورت وجود ضایعه لپتومننژ دوطرفه، علائم عصبی شدیدتر و پیشآگهی بدتر است.
مهمترین نکته عوارض جراحی مرتبط با همانژیوم کوروئید است. در SWS، همانژیوم کوروئید در حدود 40% موارد دیده میشود و کاهش ناگهانی فشار داخل چشم در حین جراحی گلوکوم خطر افیوژن کوروئید، خونریزی و جداشدگی شبکیه را به همراه دارد 1). اقدامات پیشگیرانه شامل تجویز داروهای هیپراسمولار قبل از عمل، انجام اسکلروتومی خلفی، بخیه محکم فلپ صلبیه و استفاده از دستگاه تخلیه با دریچه یا دو مرحلهای توصیه میشود. همچنین باید توجه داشت که آگونیستهای گیرنده آلفا-۲ (بریمونیدین) در کودکان زیر ۲ سال منع مصرف دارند 1). برای جزئیات بیشتر به بخش «درمان استاندارد» مراجعه کنید.
علت اصلی SWS جهش موزاییک سوماتیک در ژن GNAQ (c.548G→A, p.Arg183Gln) است 8). این جهش به طور مداوم مسیر سیگنالدهی Gαq را فعال کرده و باعث تکثیر کنترلنشده سلولهای اندوتلیال و ناهنجاری عروقی میشود 4). از آنجایی که جهش در سلولهای سوماتیک اولیه پس از لقاح رخ میدهد، توزیع سلولهای جهشیافته تنوع فنوتیپ بالینی (انواع I تا III) را تعیین میکند.
در راهنمای بالینی گلوکوم (ویرایش پنجم)، پنج مکانیسم زیر برای افزایش فشار داخل چشم در SWS ذکر شده است 1):
بررسی بافتشناسی چشمهای خارج شده، یافتههای زیر را تأیید کرده است. این یافتهها مشابه موارد مشاهده شده در گلوکوم مادرزادی اولیه است.
در مواردی که در دوران نوزادی یا کودکی رخ میدهد، ناهنجاری رشدی زاویه (زاویه اتاق قدامی) مهمترین عامل در نظر گرفته میشود.
در مواردی که در اواخر نوجوانی تا دهه ۲۰ سالگی یا بعد از آن رخ میدهد، افزایش فشار ورید اپیاسکلرا ناشی از همانژیوم عامل اصلی است 1). در معاینه گونیوسکوپی، ناهنجاری زاویه حداقل است، اما خون اغلب در زاویه مشاهده میشود که با افزایش فشار ورید اپیاسکلرا همبستگی دارد. در این وضعیت، داروهای کاهشدهنده تولید زلالیه مؤثرترین هستند و درمان دارویی خط اول محسوب میشود.
زیرا مکانیسم ایجاد گلوکوم در این دو نوع اساساً متفاوت است. در نوع زودرس، ناهنجاری مادرزادی زاویه عامل اصلی است و از آنجایی که ترابکولوم و ساختار زاویه خود مشکل دارند، جراحی زاویه (ترابکولوتومی یا گونیوتومی) که مسیر خروجی را فیزیکی باز میکند، مؤثر است 1). در مقابل، در نوع دیررس، افزایش فشار ورید اپیاسکلرا عامل اصلی است و ساختار زاویه نسبتاً طبیعی است. در شرایط فشار بالای ورید اپیاسکلرا، داروهای کاهشدهنده تولید زلالیه مؤثرترین هستند و درمان دارویی خط اول محسوب میشود 1). در صورت عدم پاسخ به درمان دارویی، جراحی فیلتراسیون یا جراحی شنت لوله که میتواند سیستم وریدی اپیاسکلرا را دور بزند، در نظر گرفته میشود. برای جزئیات به بخش «روشهای درمان استاندارد» مراجعه کنید.
در مدیریت گلوکوم همراه با SWS، پیشرفتهای زیر در آینده مورد انتظار است.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm, Savona. 2020.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Yeom S, Comi AM. Updates on Sturge-Weber Syndrome. Handb Clin Neurol. 2015;132:157-168. doi:10.1016/B978-0-444-62702-5.00011-1.
Yadav PS, Adhikari P, Mehta B, et al. Unmasking Sturge-Weber Syndrome in Adulthood: A Case with Extrafacial Port-Wine Stain and Delayed Neurological Symptoms. Ann Med Surg. 2024;86:3679-3682.
Ainuz BY, Wolfe EM, Wolfe SA. Surgical Management of Facial Port-Wine Stain in Sturge Weber Syndrome. Cureus. 2021;13(1):e12637.
Pathak BD, Sharma S, Adhikari A, et al. Sturge-Weber Syndrome with Bilateral Port-Wine Stain. Case Rep Pediatr. 2022;2022:2191465.
Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368:1971-1979.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(4):616-629.