Porto şarabı lekesinin dağılımı ve risk
Sadece V1 bölgesi: Glokom riski %6.7
Sadece V2 bölgesi: Glokom riski neredeyse yok
V1 + V2 bölgeleri: Glokom riski %31.8’e önemli ölçüde artar
V1 + V2 + V3 bölgeleri: Nörolojik semptom riski 4 kat artar

Sturge-Weber sendromu (SWS), aynı zamanda ensefalotrigeminal anjiyomatozis olarak da adlandırılan konjenital bir nörokütanöz sendromdur (fakomatozis). Trigeminal sinir alanında yüzde porto şarabı lekesi (nevus flammeus), ipsilateral leptomeningeal hemanjiom ve oküler hemanjiom üçlüsü ile karakterizedir. 1879’da Sturge, yüz hemanjiomu, buftalmi, hemipleji ve epilepsi vakasını bildirmiş ve 1929’da Weber sendromu bir klinik antite olarak tanımlamıştır.
Nedeni GNAQ genindeki somatik mozaik mutasyondur (post-zigotik mutasyon) ve kalıtsal değildir, çoğu sporadiktir 4)8). Embriyonik dönemde sempatik sinir hasarına bağlı vasküler gelişim anomalisi olduğu düşünülmektedir. Görülme sıklığı 50.000 doğumda 1 gibi nadirdir ve ırk veya cinsiyet farkı yoktur 5)7).
SWS klinik görünüme göre aşağıdaki üç tipe ayrılır:
| Sınıflama (Roach) | Özellik |
|---|---|
| Tip I (Klasik) | PWS + nörolojik bulgular + glokom |
| Tip II | PWS + glokom (nörolojik lezyon yok) |
| Tip III (Çok nadir) | Sadece meningeal anjiyom |
Glokom, SWS’de en önemli oküler komplikasyondur ve fakomatozlar arasında en yüksek glokom insidansına sahiptir 2). Göz kapağında hemanjiyom varsa, %30-70 oranında glokom gelişir. Koroid hemanjiyomu hastaların yaklaşık %40’ında eşlik eder.
Glokom, başlangıç zamanına göre erken başlangıçlı ve geç başlangıçlı olarak ikiye ayrılır. Yaklaşık %60’ı doğumdan hemen sonra ile 4 yaş arasında ortaya çıkan erken başlangıçlı tiptir ve ana neden açı gelişim anomalisidir. Kalan yaklaşık %40’ı çocukluk döneminden sonra ortaya çıkan geç başlangıçlı tiptir ve episkleral venöz basınç artışı ile koroid hemanjiyomu etyolojide rol oynar. Çoğunlukla 10 yaşına kadar ortaya çıkar.
Sturge-Weber sendromu, trigeminal sinir alanında yüzde porto şarabı lekesi, aynı tarafta serebral leptomeningeal anjiyom ve oküler anjiyom ile karakterize konjenital bir nörokütanöz sendromdur. Nedeni GNAQ genindeki somatik mozaik mutasyondur, kalıtsal değildir ve çoğu sporadiktir 4)8). Nörolojik semptomlar (epilepsi %75-90, 3 yaşına kadar; zihinsel engel; hemiparezi) ve glokom (%30-70) ana komplikasyonlardır. Üç ana bulgunun tam olmadığı tip II (sadece glokom) ve tip III (sadece meningeal anjiyom) da mevcuttur. Ayrıntılar için “Nedenler ve Risk Faktörleri” bölümüne bakın.
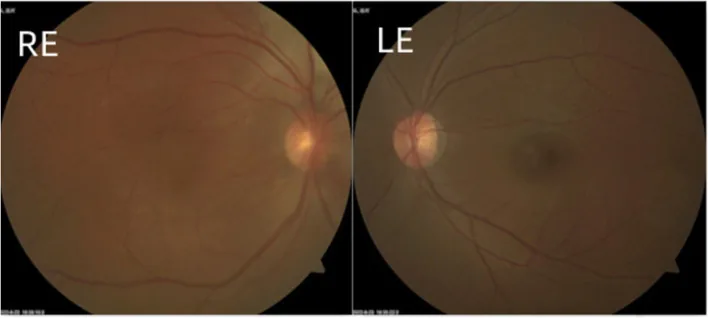
Erken başlangıçlı tipte ilk belirtiler sulanma, fotofobi ve blefarospazmdır. Kornea çapında artış ve kornea bulanıklığı (buftalmi) ile görme bozukluğu ortaya çıkar. Descemet membranında yırtık çizgileri olan Haab çizgileri görülebilir.
Geç başlangıçlı tip, primer açık açılı glokoma benzer ve erken evrelerde subjektif belirtiler azdır. İlerlemeyle birlikte görme alanı daralması ve görme azalması gelişir.
SWS, GNAQ genindeki (kromozom 9q21.2) somatik mozaik mutasyondan (c.548G→A, p.Arg183Gln) kaynaklanır8). Bu mutasyon, Gαq sinyal yolunun sürekli aktivasyonuna ve endotel hücrelerinin kontrolsüz çoğalmasına ve vasküler malformasyona yol açar4). Germ hattı mutasyonu değil, somatik mozaik mutasyon olduğu için kalıtsal değildir. Moleküler tanı için etkilenen dokudan (genellikle cilt) biyopsi gerekir4).
GNAQ mutasyonunun saptanması, etkilenen doku örneği ve analiz yönteminden etkilenir, bu nedenle moleküler tanı klinik bulgularla birlikte yorumlanmalıdır.
Porto şarabı lekesinin dağılımı ve risk
Sadece V1 bölgesi: Glokom riski %6.7
Sadece V2 bölgesi: Glokom riski neredeyse yok
V1 + V2 bölgeleri: Glokom riski %31.8’e önemli ölçüde artar
V1 + V2 + V3 bölgeleri: Nörolojik semptom riski 4 kat artar
Başlangıç zamanı ve etiyolojideki farklılıklar
Erken başlangıçlı tip (yaklaşık %60): Açı gelişim anomalisi ana nedendir. Büyük göz (buftalmi) ve kornea çapında artış ile kendini gösterir1)
Geç başlangıçlı tip (yaklaşık %40): Episkleral venöz basınç artışı ve koroid hemanjiyomu katılımı ana nedendir1)
Göz kapağı invazyonu: Hemanjiyom göz kapağına uzanırsa, glokom gelişme riski belirgin şekilde artar
Bilateral PWS: Tek taraflıya kıyasla SWS olma olasılığı daha yüksektir7)
SWS’ye eşlik eden glokom tanısı için hassas göz içi basıncı ölçümü ve ön segment, açı ve fundus muayenesi önemlidir. Çocuklarda sıklıkla genel anestezi altında muayene gerekir.
Floresein anjiyografi faydalıdır. Erken dönemde büyük koroid damar paterni görülür, geç dönemde tümör bölgesinin tamamı hiperfloresans gösterir. Diffüz koroid hemanjiyomu normal fundus muayenesinde tanımlanması zor olabilir.
Baş BT ile serebral korteks içinde kalsifikasyon tespit edilir. Kalsifikasyonun henüz ortaya çıkmadığı yenidoğan döneminde bile gadolinyumlu MRG ile leptomeningeal hemanjiyom tespit edilebilir. SPECT ile serebral kan akımı değerlendirmesi de yardımcı olarak kullanılır.
SWS bir fakomatozdur ve koroid hemanjiyomuna neden olan tipik bir hastalıktır. Diğer fakomatozlardan ayırt edilmesi önemlidir.
| Hastalık | Karakteristik göz bulguları | Hemanjiyom/tümör yeri |
|---|---|---|
| SWS | Koroid hemanjiyomu, glokom | Yüz + leptomeninks |
| von Hippel-Lindau hastalığı | Retina hemanjiyomu (temporal perifer) | Retina, serebellum, böbrek |
| Nörofibromatozis tip 1 | İris Lisch nodülü | Kutanöz nörofibrom |
| Tüberoskleroz | Retinal hamartom | Beyin, cilt, böbrek, kalp |
Ayrıca, Klippel-Trenaunay-Weber sendromu SWS’ye benzer kutanöz hemanjiyom gösterir, ancak ekstremitelerde venöz malformasyonlar ve kemik-yumuşak doku hipertrofisi ile ayırt edilir.
Yüzde porto şarabı lekesi olan hastalarda göz içi basıncı ölçümünü içeren düzenli oftalmolojik muayene zorunludur. Çocuklarda rebound tonometre ile göz içi basıncı ölçümü, ön segment muayenesi (kornea çapı, kornea bulanıklığı, Haab çizgileri varlığı), goniyoskopi (açı anomalilerinin değerlendirilmesi) ve fundus muayenesi (optik disk çukurluğu değerlendirmesi, koroidal hemanjiyom tespiti) yapılır. Çocuklarda sıklıkla genel anestezi altında muayene gerekir. Geç başlangıçlı tipte açıda kan varlığı ve episkleral damar genişlemesi ayırıcı tanıda faydalıdır. Koroidal hemanjiyom değerlendirmesi için floresein anjiyografi gereklidir ve sistemik değerlendirme için kraniyal BT ve kontrastlı MRG yapılır.
SWS’ye eşlik eden glokomun tedavisi, başlangıç zamanına ve patogenetik mekanizmaya göre farklı stratejiler gerektirir.
Konjenital veya bebeklik döneminde başlayan glokom cerrahi tedavi gerektirir1). Trabekülotomi veya gonyotomi ilk seçenektir1). Ancak başarı oranı primer konjenital glokoma göre daha düşüktür ve sıklıkla ek cerrahi gerekir.
Trabekülektomi yapılması, hemanjiyomdan kanamaya bağlı ciddi suprakoroidal hematom veya ekspulsif kanama riski taşır. Genel olarak glokom cerrahisine yanıt iyi değildir ve sıklıkla trabekülektomi veya tüp şant cerrahisi gerekir.
Daha büyük çocuklarda episkleral ven basıncı yüksek olduğundan ilaç tedavisi ilk seçenektir1). Aköz hümör üretimini baskılayan ilaçlar (beta blokerler, karbonik anhidraz inhibitörleri) en etkili olanlardır. Prostaglandin analoglarının göz içi basıncını düşürücü etkisinin tutarlı olmadığı bildirilmiştir.
İlaç tedavisi veya dış akım yolu rekonstrüksiyonu başarısız olduğunda trabekülektomi veya tüp şant cerrahisi düşünülür1).
Filtrasyon Cerrahisi / Tüp Şant
Trabekülektomi: Antimetabolit (mitomisin C) ile birlikte kullanım sonuçları iyileştirebilir. Ancak SWS’li gözlerde koroid efüzyonu ve ekspulsif kanama riski çok yüksektir1).
Ahmed cihazı: 24 ayda kümülatif başarı oranı %79, 60 ayda %30 olarak bildirilmiştir.
İki aşamalı Baerveldt cihazı: Ortalama 35 aylık takipte tüm vakaların 21 mmHg’nin altında göz içi basıncına ulaştığı bildirilmiştir.
Pediatrik GDD meta-analizi: 1221 gözün analizinde 12 ayda başarı oranı %87 (%95 GA: %83-91), 24 ayda %77 (%95 GA: %71-83) olarak bulunmuştur9).
Ameliyat Sırası ve Sonrası Komplikasyonların Yönetimi
Koroid kanaması ve efüzyonu: Koroid hemanjiyomu varlığında ani göz içi basıncı düşüşü koroid dekolmanı ve kanama riskini artırır1).
Önleyici tedbirler: Ameliyat öncesi hiperosmolar ilaçlarla göz içi basıncının düşürülmesi, arka sklerotomi yapılması, skleral flep sütürlerinin önceden yerleştirilmesi ve ek sıkı sütürler.
Cihaz seçimi: Valfii (Ahmed) veya iki aşamalı (Baerveldt) GDD kullanımı hipotoni riskini azaltır.
Siklofotokoagülasyon (CPC): Dirençli vakalarda siklofotokoagülasyon düşünülür. Bir raporda, 16 gözden 10’u (%62.5) komplikasyonsuz olarak 6-22 mmHg göz içi basıncını korumuştur (ortalama 8.87 yıl takip).
İki aşamalı yöntemde, tüp ön odaya yerleştirilmeden birkaç hafta önce plak etrafında bir kapsül oluşturulur. Bu, ameliyat sonrası aşırı göz içi basıncı düşüşünü önler ve koroid efüzyonu ve kanama riskini en aza indirir. Bu yöntem, özellikle koroid hemanjiyomu olan SWS vakalarında faydalıdır.
Netarsudil’in (Rho kinaz inhibitörü) dördüncü veya beşinci seçenek ilaç olarak eklendiğinde bile SWS’ye bağlı glokomda göz içi basıncını etkili bir şekilde düşürdüğü bildirilmiştir. Etki mekanizması trabeküler ağdan aköz hümör çıkışını kolaylaştırmaktır.
SWS’ye eşlik eden diffüz koroid hemanjiyomu, glokom tedavisine paralel olarak yönetim gerektirebilir.
Gelişimsel glokoma göre daha dirençli olmakla birlikte, erken dönemde iyi göz içi basıncı kontrolü sağlanırsa görme korunabilir. Ancak koroid hemanjiyomu büyüyüp eksüdatif retina dekolmanına yol açarsa, kriyoterapi bile yeterli yanıt vermeyebilir ve ciddi görme kaybı oluşabilir.
Lezyon kornea, lens, retina ve siniri etkilediğinden iyi görme elde etmek genellikle zordur. SWS hastalarının yaşam beklentisi genel popülasyona göre kısalmıştır ve bilateral leptomeningeal tutulum varsa nörolojik semptomlar daha şiddetli olup prognoz kötüdür.
En önemli nokta koroid hemanjiyomuna bağlı cerrahi komplikasyonlardır. SWS’de koroid hemanjiyomu yaklaşık %40 oranında görülür ve glokom cerrahisi sırasında ani göz içi basıncı düşüşü koroid efüzyonu, kanama ve retina dekolmanı riski taşır 1). Önleyici tedbirler olarak preoperatif hiperosmolar ajan uygulaması, arka sklerotomi yapılması, skleral flebin sıkı sütüre edilmesi ve valfli veya iki aşamalı drenaj cihazı kullanımı önerilir. Ayrıca 2 yaş altında alfa-2 reseptör agonistlerinin (brimonidin) kontrendike olduğu unutulmamalıdır 1). Detaylar için «Standart Tedavi» bölümüne bakın.
SWS’nin temel nedeni, GNAQ genindeki somatik mozaik mutasyondur (c.548G→A, p.Arg183Gln) 8). Bu mutasyon, Gαq sinyal yolunu sürekli olarak aktive eder ve endotel hücrelerinin kontrolsüz çoğalmasına ve vasküler malformasyona yol açar 4). Mutasyon, döllenmeden sonra erken somatik hücrelerde meydana geldiğinden, mutant hücrelerin dağılımı klinik fenotipin (tip I-III) çeşitliliğini belirler.
Glokom Tanı ve Tedavi Kılavuzu (5. Baskı)‘nda, SWS’de göz içi basınç artışının mekanizması olarak aşağıdaki beş madde sıralanmıştır 1):
Çıkarılan gözlerin histolojik incelemesinde aşağıdaki bulgular tespit edilmiştir. Bunlar primer konjenital glokomda görülenlere benzer.
Bebeklik veya çocukluk döneminde ortaya çıkan vakalarda, açı (ön kamara açısı) gelişim anomalisi en önemli faktör olarak kabul edilir.
Geç ergenlikten 20’li yaşlar ve sonrasında ortaya çıkan vakalarda, hemanjiyoma bağlı episkleral venöz basınç artışı ana nedendir 1). Gonyoskopide açı anomalisi minimaldir, ancak açıda sıklıkla kan gözlenir ve bu episkleral venöz basınç artışı ile korelasyon gösterir. Bu durumda, aköz hümör üretimini baskılayan ilaçlar en etkilidir ve ilaç tedavisi ilk seçenektir.
Çünkü her iki tipte glokomun oluşum mekanizması temelde farklıdır. Erken başlangıçlı tipte, açının konjenital gelişim anomalisi ana nedendir ve trabeküler ağ ve açı yapısının kendisinde sorun olduğu için, çıkış yolunu fiziksel olarak açan açı cerrahisi (trabekülotomi/gonyotomi) etkilidir 1). Öte yandan, geç başlangıçlı tipte episkleral venöz basınç artışı ana nedendir ve açı yapısı nispeten normale yakındır. Yüksek episkleral venöz basınç durumunda, aköz hümör üretimini baskılayan ilaçlar en etkilidir ve ilaç tedavisi ilk seçenektir 1). İlaç tedavisine yanıt alınamazsa, episkleral venöz sistemi baypas edebilen filtrasyon cerrahisi veya tüp şant cerrahisi düşünülür. Ayrıntılar için “Standart Tedavi Yöntemleri” bölümüne bakın.
SWS ile ilişkili glokom yönetiminde aşağıdaki alanlarda gelecekte ilerleme beklenmektedir.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm, Savona. 2020.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Yeom S, Comi AM. Updates on Sturge-Weber Syndrome. Handb Clin Neurol. 2015;132:157-168. doi:10.1016/B978-0-444-62702-5.00011-1.
Yadav PS, Adhikari P, Mehta B, et al. Unmasking Sturge-Weber Syndrome in Adulthood: A Case with Extrafacial Port-Wine Stain and Delayed Neurological Symptoms. Ann Med Surg. 2024;86:3679-3682.
Ainuz BY, Wolfe EM, Wolfe SA. Surgical Management of Facial Port-Wine Stain in Sturge Weber Syndrome. Cureus. 2021;13(1):e12637.
Pathak BD, Sharma S, Adhikari A, et al. Sturge-Weber Syndrome with Bilateral Port-Wine Stain. Case Rep Pediatr. 2022;2022:2191465.
Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368:1971-1979.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(4):616-629.