पोर्ट-वाइन धब्बे का वितरण और जोखिम
केवल V1 क्षेत्र : ग्लूकोमा जोखिम 6.7%
केवल V2 क्षेत्र : ग्लूकोमा का जोखिम लगभग नहीं
V1 + V2 क्षेत्र : ग्लूकोमा जोखिम 31.8% तक बढ़ जाता है
V1 + V2 + V3 क्षेत्र : तंत्रिका संबंधी लक्षणों का जोखिम 4 गुना बढ़ जाता है

स्टर्ज-वेबर सिंड्रोम (SWS) एक जन्मजात न्यूरोक्यूटेनियस सिंड्रोम (फैकोमैटोसिस) है, जिसे एन्सेफैलोट्राइजेमिनल एंजियोमैटोसिस भी कहा जाता है। इसकी तीन मुख्य विशेषताएं हैं: ट्राइजेमिनल तंत्रिका क्षेत्र में चेहरे का पोर्ट-वाइन दाग (फ्लेम नेवस), उसी तरफ का मस्तिष्क लेप्टोमेनिन्जियल हेमांगीओमा, और नेत्र हेमांगीओमा। 1879 में स्टर्ज ने चेहरे के हेमांगीओमा और बुफ्थाल्मोस के साथ हेमिप्लेजिया और मिर्गी के एक मामले की सूचना दी, और 1929 में वेबर ने सिंड्रोम को स्थापित किया।
इसका कारण GNAQ जीन का दैहिक मोज़ेक उत्परिवर्तन (पोस्ट-ज़ायगोटिक उत्परिवर्तन) है, जो वंशानुगत नहीं है और अधिकतर छिटपुट मामलों में होता है4)8)। इसे भ्रूण अवस्था में सहानुभूति तंत्रिका विकार के कारण संवहनी विकास असामान्यता माना जाता है। घटना दर दुर्लभ है, प्रति 50,000 जन्मों में 1, और जाति या लिंग का कोई पूर्वाग्रह नहीं है5)7)।
SWS को नैदानिक विशेषताओं के आधार पर निम्नलिखित तीन प्रकारों में वर्गीकृत किया गया है।
| वर्गीकरण (रोच) | विशेषताएँ |
|---|---|
| प्रकार I (शास्त्रीय) | PWS + तंत्रिका संबंधी लक्षण + ग्लूकोमा |
| प्रकार II | PWS + ग्लूकोमा (बिना तंत्रिका घाव के) |
| प्रकार III (अत्यंत दुर्लभ) | केवल मेनिन्जियल एंजियोमा |
ग्लूकोमा SWS में सबसे महत्वपूर्ण नेत्र संबंधी जटिलता है, जिसमें फेकोमेटोसिस में सबसे अधिक ग्लूकोमा घटना दर होती है2)। जब हेमांगीओमा पलक तक फैल जाता है, तो 30-70% की उच्च आवृत्ति पर ग्लूकोमा विकसित होता है। लगभग 40% रोगियों में कोरॉइडल हेमांगीओमा सहवर्ती होता है।
ग्लूकोमा की शुरुआत के समय के अनुसार, इसे प्रारंभिक प्रकार और देर से शुरू होने वाले प्रकार में विभाजित किया जाता है। लगभग 60% प्रारंभिक प्रकार के होते हैं, जो जन्म से 4 वर्ष की आयु तक होते हैं, जिसका मुख्य कारण कोण के विकास की असामान्यता है। शेष लगभग 40% देर से शुरू होने वाले प्रकार के होते हैं, जो शैशवावस्था के बाद होते हैं, जिसमें एपिस्क्लेरल शिरापरक दबाव में वृद्धि और कोरॉइडल हेमांगीओमा शामिल होते हैं। यह अक्सर 10 वर्ष की आयु से पहले होता है।
यह एक जन्मजात न्यूरोक्यूटेनियस सिंड्रोम है जिसकी त्रयी है: त्रिधारा तंत्रिका क्षेत्र में चेहरे का पोर्ट-वाइन धब्बा, उसी तरफ का मस्तिष्कावरणीय एंजियोमा, और नेत्र एंजियोमा। इसका कारण GNAQ जीन में दैहिक मोज़ेक उत्परिवर्तन है, जो वंशानुगत नहीं है और अधिकतर छिटपुट होता है4)8)। मुख्य जटिलताओं में न्यूरोलॉजिकल लक्षण (75-90% में 3 वर्ष की आयु से पहले मिर्गी, बौद्धिक अक्षमता, अर्धांगघात) और ग्लूकोमा (30-70%) शामिल हैं। पूर्ण त्रयी के बिना टाइप II (केवल ग्लूकोमा) और टाइप III (केवल मेनिन्जियल एंजियोमा) भी मौजूद हैं। विस्तृत जानकारी के लिए “कारण और जोखिम कारक” अनुभाग देखें।
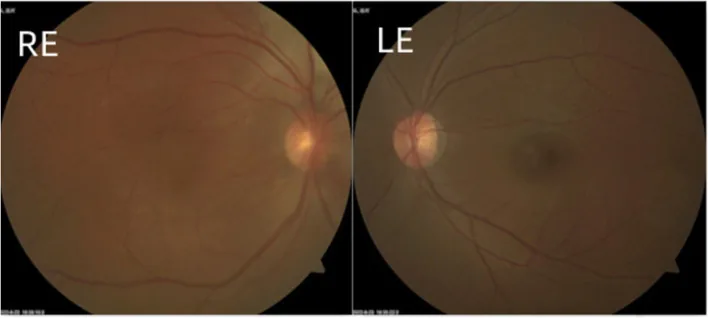
प्रारंभिक शुरुआत वाले प्रकार में, पहले लक्षण अश्रुपात, प्रकाश से घृणा और पलकों का फड़कना हैं। कॉर्नियल व्यास में वृद्धि और कॉर्नियल धुंधलापन (बुफथैल्मोस) के साथ दृष्टि दोष होता है। डेसीमेट झिल्ली में दरार की रेखाएं (हाब रेखाएं) देखी जा सकती हैं।
देर से शुरू होने वाला प्रकार प्राथमिक ओपन-एंगल ग्लूकोमा के समान होता है, जिसमें शुरुआत में कम व्यक्तिपरक लक्षण होते हैं। प्रगति के साथ, दृश्य क्षेत्र संकुचन और दृश्य तीक्ष्णता में कमी होती है।
SWS, GNAQ जीन (गुणसूत्र 9q21.2) में दैहिक मोज़ेक उत्परिवर्तन (c.548G→A, p.Arg183Gln) के कारण होता है8)। यह उत्परिवर्तन Gαq सिग्नलिंग मार्ग को स्थायी रूप से सक्रिय करता है, जिससे एंडोथेलियल कोशिकाओं का अनियंत्रित प्रसार और संवहनी विकृति उत्पन्न होती है4)। यह जनन कोशिका उत्परिवर्तन नहीं बल्कि दैहिक मोज़ेक उत्परिवर्तन है, इसलिए वंशानुगत नहीं है। आणविक निदान के लिए प्रभावित ऊतक (आमतौर पर त्वचा) की बायोप्सी आवश्यक है4)।
GNAQ उत्परिवर्तन का पता लगाना प्रभावित ऊतक के नमूने और विश्लेषण विधि पर निर्भर करता है, इसलिए आणविक निदान की व्याख्या नैदानिक चित्र के साथ मिलकर की जानी चाहिए।
पोर्ट-वाइन धब्बे का वितरण और जोखिम
केवल V1 क्षेत्र : ग्लूकोमा जोखिम 6.7%
केवल V2 क्षेत्र : ग्लूकोमा का जोखिम लगभग नहीं
V1 + V2 क्षेत्र : ग्लूकोमा जोखिम 31.8% तक बढ़ जाता है
V1 + V2 + V3 क्षेत्र : तंत्रिका संबंधी लक्षणों का जोखिम 4 गुना बढ़ जाता है
शुरुआत की उम्र और कारण में अंतर
प्रारंभिक प्रकार (लगभग 60%) : मुख्य कारण कोण का विकासात्मक असामान्यता। बैल की आँख (बुफ्थाल्मोस) और कॉर्निया के व्यास में वृद्धि दिखाई देती है1)
देर से शुरू होने वाला प्रकार (लगभग 40%) : मुख्य कारण एपिस्क्लेरल शिरापरक दबाव में वृद्धि और कोरॉइडल हेमैंजियोमा की भागीदारी1)
पलक पर आक्रमण : यदि हेमैंजियोमा पलक तक फैल जाता है, तो ग्लूकोमा विकसित होने की दर काफी बढ़ जाती है
द्विपक्षीय PWS : एकतरफा PWS की तुलना में SWS होने की संभावना अधिक होती है7)
SWS से जुड़े ग्लूकोमा के निदान के लिए सटीक आंखों के दबाव की जांच और पूर्व खंड, कोण और फंडस की जांच महत्वपूर्ण है। बच्चों में, सामान्य एनेस्थीसिया के तहत जांच अक्सर आवश्यक होती है।
फ्लोरेसेंट फंडस एंजियोग्राफी उपयोगी है। प्रारंभिक चरण में बड़े कोरॉइडल संवहनी पैटर्न दिखाई देते हैं, और देर से ट्यूमर का पूरा भाग अतिप्रतिदीप्ति दर्शाता है। फैलाना कोरॉइडल हेमांगीओमा को सामान्य फंडस परीक्षा में पहचानना कठिन हो सकता है।
सिर के सीटी स्कैन से मस्तिष्क प्रांतस्था में कैल्सीफिकेशन का पता लगाया जाता है। नवजात शिशुओं में भी जहां कैल्सीफिकेशन नहीं हुआ है, गैडोलीनियम-एन्हांस्ड एमआरआई द्वारा लेप्टोमेनिन्जियल एंजियोमा का पता लगाया जा सकता है। एसपीईसीटी द्वारा मस्तिष्क रक्त प्रवाह मूल्यांकन भी सहायक रूप से उपयोग किया जाता है।
एसडब्ल्यूएस एक फेकोमेटोसिस है और कोरॉइडल हेमांगीओमा उत्पन्न करने वाली एक प्रतिनिधि बीमारी है। अन्य फेकोमेटोसिस से विभेदक निदान महत्वपूर्ण है।
| रोग | विशिष्ट नेत्र संबंधी निष्कर्ष | हेमांगीओमा/ट्यूमर का स्थान |
|---|---|---|
| एसडब्ल्यूएस | कोरॉइडल हेमांगीओमा, ग्लूकोमा | चेहरा + लेप्टोमेनिन्जेस |
| वॉन हिप्पेल-लिंडौ रोग | रेटिनल हेमांगीओमा (टेम्पोरल परिधि) | रेटिना, सेरिबैलम, गुर्दा |
| न्यूरोफाइब्रोमैटोसिस टाइप 1 | आइरिस लिश नोड्यूल्स | त्वचीय न्यूरोफाइब्रोमास |
| ट्यूबरस स्क्लेरोसिस | रेटिनल हैमार्टोमा | मस्तिष्क, त्वचा, गुर्दे, हृदय |
इसके अलावा, क्लिपेल-ट्रेनाउने-वेबर सिंड्रोम में SWS के समान त्वचीय रक्तवाहिकार्बुद होते हैं, लेकिन यह अंगों की शिरापरक विकृति और हड्डी-कोमल ऊतक अतिवृद्धि की उपस्थिति से भिन्न होता है।
चेहरे पर पोर्ट-वाइन दाग वाले रोगियों में, अंतःनेत्र दबाव माप सहित नियमित नेत्र परीक्षण आवश्यक है। बच्चों में, रिबाउंड टोनोमीटर से अंतःनेत्र दबाव माप, पूर्व खंड परीक्षा (कॉर्नियल व्यास, कॉर्नियल अपारदर्शिता, हाब रेखाओं की उपस्थिति), गोनियोस्कोपी (कोण असामान्यताओं का मूल्यांकन), और फंडस परीक्षा (ऑप्टिक डिस्क कपिंग का मूल्यांकन, कोरॉइडल रक्तवाहिकार्बुद का पता लगाना) की जाती है। बच्चों में अक्सर सामान्य संज्ञाहरण के तहत परीक्षा की आवश्यकता होती है। देर से शुरू होने वाले प्रकारों में, कोण में रक्त की उपस्थिति या एपिस्क्लेरल शिराओं का फैलाव विभेदक निदान में उपयोगी होता है। कोरॉइडल रक्तवाहिकार्बुद के मूल्यांकन के लिए फ्लोरेसिन एंजियोग्राफी अपरिहार्य है, और प्रणालीगत मूल्यांकन के लिए सिर का सीटी स्कैन या कंट्रास्ट एमआरआई किया जाता है।
SWS से जुड़े ग्लूकोमा के उपचार के लिए शुरुआत की उम्र और रोगजनक तंत्र के अनुसार अलग-अलग रणनीतियों की आवश्यकता होती है।
जन्मजात या शैशवावस्था में शुरू होने वाले ग्लूकोमा के लिए सर्जिकल उपचार आवश्यक है 1)। ट्रैबेकुलोटॉमी या गोनियोटॉमी पहली पसंद हैं 1)। हालांकि, सफलता दर प्राथमिक जन्मजात ग्लूकोमा की तुलना में कम है, और अक्सर अतिरिक्त सर्जरी की आवश्यकता होती है।
ट्रैबेक्यूलेक्टॉमी करने पर रक्तवाहिकार्बुद से रक्तस्राव का जोखिम होता है, जिससे गंभीर सुप्राकोरॉइडल रक्तगुल्म या एक्सपल्सिव हेमरेज हो सकता है। सामान्यतः ग्लूकोमा सर्जरी की प्रतिक्रिया अच्छी नहीं होती है, और अक्सर ट्रैबेक्यूलेक्टॉमी या ट्यूब शंट सर्जरी की आवश्यकता होती है।
बड़े बच्चों में, एपिस्क्लेरल शिरापरक दबाव बढ़ा हुआ होता है, इसलिए दवा चिकित्सा पहली पसंद है 1)। जल उत्पादन को रोकने वाली दवाएं (बीटा-ब्लॉकर्स, कार्बोनिक एनहाइड्रेज़ अवरोधक) सबसे प्रभावी मानी जाती हैं। प्रोस्टाग्लैंडीन एनालॉग्स का अंतःनेत्र दबाव कम करने वाला प्रभाव असंगत बताया गया है।
जब दवा उपचार या बहिर्वाह पथ पुनर्निर्माण सफल नहीं होता है, तो ट्रैबेक्यूलेक्टोमी या ट्यूब शंट सर्जरी पर विचार किया जा सकता है 1)।
फिल्टरिंग सर्जरी और ट्यूब शंट
ट्रैबेक्यूलेक्टोमी : एंटीमेटाबोलाइट (माइटोमाइसिन C) के साथ संयोजन से परिणामों में सुधार हो सकता है। हालांकि, SWS आंखों में कोरॉइडल इफ्यूजन और एक्सपल्सिव हेमरेज का जोखिम बहुत अधिक होता है 1)।
अहमद डिवाइस : 24 महीने में संचयी सफलता दर 79% और 60 महीने में 30% होने की रिपोर्ट है।
दो-चरणीय बेरवेल्ड्ट डिवाइस : औसत 35 महीने के फॉलो-अप में सभी मामलों में 21 mmHg से कम इंट्राओकुलर दबाव प्राप्त करने की रिपोर्ट है।
बाल चिकित्सा GDD मेटा-विश्लेषण : 1,221 आंखों के विश्लेषण में 12 महीने में सफलता दर 87% (95% CI: 83-91%) और 24 महीने में 77% (95% CI: 71-83%) 9)।
ऑपरेशन के दौरान और बाद की जटिलताओं का प्रबंधन
कोरॉइडल हेमरेज और इफ्यूजन : कोरॉइडल हेमांगीओमा की उपस्थिति में, अचानक इंट्राओकुलर दबाव में कमी से कोरॉइडल डिटेचमेंट और हेमरेज का जोखिम बढ़ जाता है 1)।
निवारक उपाय : प्रीऑपरेटिव हाइपरऑस्मोटिक एजेंटों से इंट्राओकुलर दबाव कम करना, पोस्टीरियर स्क्लेरेक्टॉमी करना, स्क्लेरल फ्लैप टांके का पूर्व-स्थापन और मजबूत अतिरिक्त टांके लगाना।
डिवाइस चयन : वाल्वयुक्त (अहमद) या दो-चरणीय (बेरवेल्ड्ट) GDD का उपयोग हाइपोटोनी के जोखिम को कम करता है।
सिलिअरी बॉडी फोटोकोएग्यूलेशन : दुर्दम्य मामलों में सिलिअरी बॉडी फोटोकोएग्यूलेशन (CPC) पर विचार करें। एक रिपोर्ट में 16 में से 10 आंखों (62.5%) ने बिना जटिलताओं के 6-22 mmHg का इंट्राओकुलर दबाव बनाए रखा (औसत 8.87 वर्ष फॉलो-अप)।
दो-चरणीय विधि में, ट्यूब को पूर्वकाल कक्ष में डालने से कई सप्ताह पहले प्लेट के चारों ओर एक कैप्सूल बनने दिया जाता है। यह ऑपरेशन के तुरंत बाद अत्यधिक इंट्राओकुलर दबाव में कमी को रोकता है और कोरॉइडल इफ्यूजन और हेमरेज के जोखिम को कम करता है। यह कोरॉइडल हेमांगीओमा से जटिल SWS मामलों में विशेष रूप से उपयोगी है।
नेटार्सुडिल को चौथी या पाँचवीं पंक्ति की दवा के रूप में जोड़ने पर भी SWS से जुड़े ग्लूकोमा में अंतःनेत्र दबाव को प्रभावी ढंग से कम करने की सूचना मिली है। यह ट्रैबिकुलम से जलीय हास्य के बहिर्वाह को बढ़ावा देकर काम करता है।
SWS से जुड़े डिफ्यूज़ कोरॉइडल हेमांगीओमा को ग्लूकोमा उपचार के समानांतर प्रबंधित करने की आवश्यकता हो सकती है।
जन्मजात ग्लूकोमा की तुलना में दुर्दम्य होने के बावजूद, यदि प्रारंभिक अवस्था में अच्छा अंतःनेत्र दबाव नियंत्रण प्राप्त किया जाता है, तो दृष्टि को संरक्षित किया जा सकता है। हालांकि, यदि कोरॉइडल हेमांगीओमा बढ़ जाता है और एक्स्यूडेटिव रेटिनल डिटेचमेंट का कारण बनता है, तो क्रायोकोएग्यूलेशन भी पर्याप्त रूप से काम नहीं कर सकता है और गंभीर दृश्य हानि हो सकती है।
कॉर्निया, लेंस, रेटिना और तंत्रिका में शामिल होने के कारण, अच्छी दृश्य तीक्ष्णता प्राप्त करना अक्सर मुश्किल होता है। SWS रोगियों की जीवन प्रत्याशा सामान्य जनसंख्या की तुलना में कम होती है, और द्विपक्षीय लेप्टोमेनिन्जियल घावों के मामले में, न्यूरोलॉजिकल लक्षण अधिक गंभीर होते हैं और पूर्वानुमान खराब होता है।
सबसे महत्वपूर्ण बिंदु कोरॉइडल हेमांगीओमा से संबंधित सर्जिकल जटिलताएँ हैं। SWS में लगभग 40% मामलों में कोरॉइडल हेमांगीओमा सह-अस्तित्व में होता है, और ग्लूकोमा सर्जरी के दौरान अंतःनेत्र दबाव में तेजी से कमी से कोरॉइडल इफ्यूजन, रक्तस्राव और रेटिनल डिटेचमेंट का खतरा होता है1)। निवारक उपायों के रूप में प्रीऑपरेटिव हाइपरोस्मोटिक एजेंट प्रशासन, पोस्टीरियर स्क्लेरेक्टॉमी, स्क्लेरल फ्लैप की मजबूत सिलाई, और वाल्वयुक्त या दो-चरणीय ड्रेनेज डिवाइस के उपयोग की सिफारिश की जाती है। यह भी ध्यान दें कि 2 वर्ष से कम उम्र के बच्चों में अल्फा-2 रिसेप्टर एगोनिस्ट (ब्रिमोनिडाइन) वर्जित है1)। विवरण के लिए «मानक उपचार» अनुभाग देखें।
SWS का मूल कारण GNAQ जीन में दैहिक मोज़ेक उत्परिवर्तन (c.548G→A, p.Arg183Gln) है8)। यह उत्परिवर्तन Gαq सिग्नलिंग मार्ग को स्थायी रूप से सक्रिय करता है, जिससे एंडोथेलियल कोशिकाओं का अनियंत्रित प्रसार और संवहनी विकृतियाँ होती हैं4)। उत्परिवर्तन निषेचन के तुरंत बाद दैहिक कोशिकाओं में होता है, इसलिए उत्परिवर्तित कोशिकाओं का वितरण नैदानिक फेनोटाइप (प्रकार I–III) की विविधता को निर्धारित करता है।
ग्लूकोमा नैदानिक दिशानिर्देश (5वें संस्करण) के अनुसार, SWS में अंतर्नेत्र दबाव बढ़ने के निम्नलिखित पाँच तंत्र सूचीबद्ध हैं1)।
निकाले गए नेत्रों के ऊतकवैज्ञानिक अध्ययनों में निम्नलिखित निष्कर्ष पाए गए हैं, जो प्राथमिक जन्मजात ग्लूकोमा में देखे गए निष्कर्षों के समान हैं।
जब शैशवावस्था में रोग शुरू होता है, तो कोण की विकासात्मक असामान्यता को सबसे महत्वपूर्ण कारक माना जाता है।
जब किशोरावस्था के अंत या 20 वर्ष की आयु के बाद रोग शुरू होता है, तो एंजियोमा के कारण एपिस्क्लेरल शिरापरक दबाव में वृद्धि मुख्य कारण होती है 1)। गोनियोस्कोपी पर, कोण की असामान्यता न्यूनतम होती है, लेकिन कोण में अक्सर रक्त देखा जाता है, जो एपिस्क्लेरल शिरापरक दबाव में वृद्धि से संबंधित होता है। इस स्थिति में, जलीय हास्य उत्पादन को रोकने वाली दवाएं सबसे प्रभावी मानी जाती हैं, और दवा उपचार पहला विकल्प है।
ऐसा इसलिए है क्योंकि ग्लूकोमा के विकास के तंत्र मौलिक रूप से भिन्न हैं। प्रारंभिक शुरुआत वाले प्रकार में, कोण की जन्मजात विकासात्मक असामान्यता मुख्य कारण है; ट्रैबिकुलम या कोण संरचना में ही समस्या होती है, इसलिए कोण सर्जरी (ट्रैबिकुलोटॉमी, गोनियोटॉमी) जो बहिर्वाह पथ को शारीरिक रूप से खोलती है, प्रभावी है 1)। दूसरी ओर, देर से शुरू होने वाले प्रकार में, एपिस्क्लेरल शिरापरक दबाव में वृद्धि मुख्य कारण है, और कोण संरचना स्वयं अपेक्षाकृत सामान्य होती है। जब एपिस्क्लेरल शिरापरक दबाव अधिक होता है, तो जलीय हास्य उत्पादन को रोकने वाली दवाएं सबसे प्रभावी होती हैं, और दवा उपचार पहला विकल्प है 1)। यदि दवा उपचार अप्रभावी है, तो फ़िल्टरिंग सर्जरी या ट्यूब शंट सर्जरी पर विचार किया जाता है जो एपिस्क्लेरल शिरापरक प्रणाली को बायपास कर सकती है। विवरण के लिए «मानक उपचार» अनुभाग देखें।
SWS से जुड़े ग्लूकोमा के प्रबंधन में, निम्नलिखित क्षेत्रों में भविष्य में प्रगति की उम्मीद है।
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm, Savona. 2020.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Yeom S, Comi AM. Updates on Sturge-Weber Syndrome. Handb Clin Neurol. 2015;132:157-168. doi:10.1016/B978-0-444-62702-5.00011-1.
Yadav PS, Adhikari P, Mehta B, et al. Unmasking Sturge-Weber Syndrome in Adulthood: A Case with Extrafacial Port-Wine Stain and Delayed Neurological Symptoms. Ann Med Surg. 2024;86:3679-3682.
Ainuz BY, Wolfe EM, Wolfe SA. Surgical Management of Facial Port-Wine Stain in Sturge Weber Syndrome. Cureus. 2021;13(1):e12637.
Pathak BD, Sharma S, Adhikari A, et al. Sturge-Weber Syndrome with Bilateral Port-Wine Stain. Case Rep Pediatr. 2022;2022:2191465.
Shirley MD, Tang H, Gallione CJ, et al. Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ. N Engl J Med. 2013;368:1971-1979.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(4):616-629.