
發育性青光眼(先天性青光眼)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是發育性青光眼?
Section titled “1. 什麼是發育性青光眼?”發育性青光眼(developmental glaucoma)是由於房水流出道發育異常導致的青光眼。根據發病時間分為早發型和晚發型發育性青光眼1)。
早發型相當於傳統的原發性先天性青光眼(PCG)。眼壓升高的原因僅限於小樑網發育異常,在3-4歲前發病,伴有角膜直徑擴大(牛眼)。晚發型由於隅角/小樑網發育異常較輕,發病較晚,病程類似於原發性開放隅角青光眼。通常在10-20歲發病。
兒童青光眼存在多種分類體系。日本青光眼指南將發育性青光眼分為早發型、晚發型和伴有其他先天異常的發育性青光眼三類1)。國際上,兒童青光眼研究網絡(CGRN)制定的分類已被世界青光眼協會(WGA)和美國眼科委員會(ABO)採用2)。
| 分類 | 日本分類 | CGRN分類 |
|---|---|---|
| 原發性、早發型 | 早發型發育性青光眼 | 原發性先天性青光眼(PCG) |
| 原發性、晚發型 | 晚發型發育性青光眼 | 青少年開放隅角青光眼(JOAG) |
| 合併先天異常 | 伴有其他先天異常的發展性青光眼 | 續發性:與先天眼形成異常相關 |
| 合併全身疾病 | (包含於上述) | 續發性:與先天全身疾病相關 |
| 後天因素 | (包含於上述) | 續發性:後天因素 |
| 術後 | (包含於上述) | 續發性:白內障術後 |
PCG依發病年齡進一步細分為新生兒期(0~1個月)、嬰兒期(1~24個月)及遲發性(2歲以上)2)。JOAG在4歲後發病,不伴隨眼球擴大,且隅角外觀正常2)。
續發性兒童青光眼包括:伴隨Axenfeld-Rieger異常、Peters異常、無虹膜症等先天眼形成異常相關青光眼;伴隨Sturge-Weber症候群、唐氏症等先天全身疾病相關青光眼;續發於葡萄膜炎、外傷、類固醇的後天因素青光眼;以及白內障術後青光眼2)。
兒童青光眼占兒童失明原因的5%,全球有超過30萬人罹患2)。
早發型青光眼的發生率在日本為每10萬出生人口1.8~2.4人,而在歐美報告為5~10人。在近親結婚較多的斯洛伐克羅姆人中發生率最高,為每10萬出生人口80人。75%為雙眼性,65%發生於男童。80%的病例在出生後1年內發病。大部分為散發病例,但約10%~40%有遺傳性,呈體染色體隱性遺傳。
在大型澳大拉西亞疾病登記處(ANZRAG:660名患者)中,兒童青光眼中PCG占57.6%,JOAG占19.3%3)。PCG的診斷年齡中位數為0.25歲,JOAG為14歲3)。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”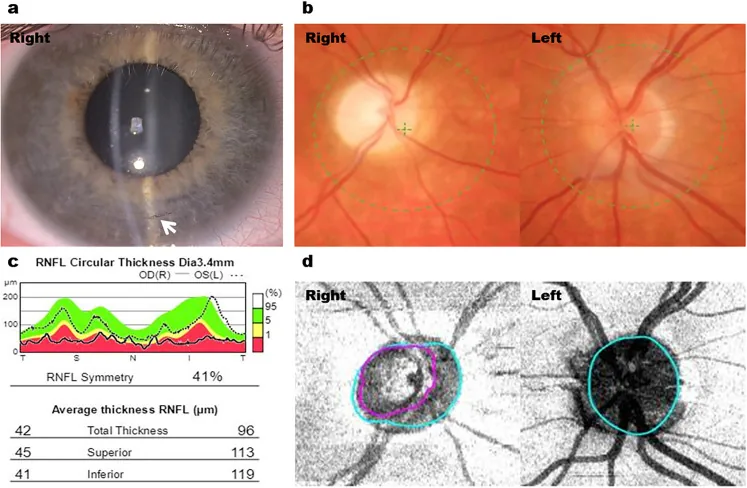
MIGS手術的兒童應用
Section titled “MIGS手術的兒童應用”微創青光眼手術(MIGS)是一種保留結膜的技術,由於保留了未來額外手術的選擇,其在兒童中的應用正在推進。然而,證據有限。
- KDB(Kahook Dual-Blade)隅角切開術:已有在兒童PCG中應用的報導7)
- Trab360:作為兒童青光眼的小樑切開類手術已有報導8)
- PreserFlo外路微型分流管:作為難治性兒童青光眼的輔助選擇有小規模報導9)
藥物的選擇與成人開放隅角青光眼類似,但兒童有特殊的注意事項。
- 前列腺素(PG)相關藥物:兒童中無反應者較多,但在安全性與每日一次點眼方面具有優勢。
- β阻斷劑:使用盡可能低的濃度。注意支氣管氣喘與心搏過緩的副作用。新生兒中有呼吸暫停的報告。
- 碳酸酐酶抑制劑(CAI):口服乙醯唑胺5 mg/kg/日,分三次服用。降眼壓效果強,但長期使用可能導致代謝性酸中毒與發育不良。點眼藥副作用少但效果也較小。
- 術後毛果芸香鹼:使用1-2%濃度,每日2-3次,持續數週。目的是預防周邊虹膜前粘連。
遲發型發育性青光眼的治療
Section titled “遲發型發育性青光眼的治療”學齡期及以後,首先嘗試藥物治療。與早發型相比,隅角異常較輕,因此藥物治療效果較好。
- 第一線藥物:PG相關藥物(如拉坦前列素)
- 第二線藥物:CAI點眼液或β阻斷劑(僅限能準確描述主觀副作用症狀的兒童)
- 眼壓超過25 mmHg時:從PG相關藥物開始,必要時加用β阻斷劑或CAI。
手術適應症需謹慎判斷。由於眼壓隨時間波動較大,當30-40 mmHg以上的高眼壓持續數週且藥物降壓效果不佳,或眼壓約20 mmHg但視野損害已至晚期時,考慮手術1)。
目標眼壓與長期管理
Section titled “目標眼壓與長期管理”目標眼壓最好控制在19-20 mmHg以下。
眼壓控制後仍需長期管理。為促進視功能發育,應定期進行屈光檢查與視力檢查,必要時進行弱視治療或斜視治療。視力不良的最大原因是弱視,早期進行適當的屈光矯正與視能訓練非常重要。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”隅角形成異常的組織學所見
Section titled “隅角形成異常的組織學所見”早發型發育性青光眼的病理總結如下:
- 近Schlemm管結締組織異常增厚:由於線維柱帶發育不成熟,近Schlemm管結締組織異常增厚。
- 細胞外基質積聚:由膠原蛋白、彈性蛋白樣纖維和大量無定形物質組成的非層狀緻密組織存在於Schlemm管下方。由短細胞突的線維柱帶細胞、纖維成分和基底板樣物質組成。
- 睫狀體異常附著:睫狀體附著於線維柱帶部位,肌肉收縮將鞏膜突向前拉,壓迫Schlemm管和線維柱帶。
- 虹膜根部異位:虹膜根部存在於線維柱帶的位置。
- Schlemm管發育不全:部分病例Schlemm管缺失或發育不完全。
胚胎學上,線維柱帶細胞來源於神經嵴,而近Schlemm管結締組織來源於血管內皮細胞。不同起源組織的鄰接點存在最大的房水流出阻力。
推測線維柱帶片(片狀物質)被壓縮並存在於線維柱帶前方,阻礙房水流出,同時將虹膜向上拉,防止隅角擴大,這是發育性青光眼特有隅角表現的原因。
眼球擴大的機轉
Section titled “眼球擴大的機轉”嬰幼兒的眼球被膜彈性豐富。持續高眼壓時,以角鞏膜緣為中心的眼球被膜被拉伸,角膜直徑增大(牛眼)。同時,彈性較低的Descemet膜發生破裂(Haab紋),房水流入角膜基質和上皮,導致角膜水腫和混濁急劇惡化。
如果眼壓控制不良持續存在,還會出現Zinn小帶破裂導致的晶狀體偏位、角膜糜爛/潰瘍以及眼球破裂的風險。
兒童隅角手術有效的原因
Section titled “兒童隅角手術有效的原因”小樑切開術被認為對先天性青光眼非常有效5)。這種差異被認為源於兒童隅角中豐富的彈性纖維。彈性纖維促進隅角結構的開放,並維持術後房水流出通道的通暢5)。
外路小樑切開術後,Schlemm管的通暢性被認為與長期預後相關5)。術後失敗的主要原因是Schlemm管內壁的纖維增生和Schlemm管內皮的伸長5)。
基因異常與隅角發育
Section titled “基因異常與隅角發育”CYP1B1是編碼細胞色素P450家族酶的基因,在胎兒眼前段組織中高度表現。在CYP1B1突變病例中,酪氨酸代謝途徑出現異常,推測會阻礙隅角組織的正常分化和成熟。CYP1B1突變不僅見於PCG,也見於JOAG和先天性眼發育異常相關的青光眼3)。
近年來,TEK/ANGPT1突變被新發現2)。TEK編碼參與Schlemm管內皮發育和維持的受體酪氨酸激酶,提示PCG中涉及新的分子路徑。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”新型MIGS裝置在兒童中的應用
Section titled “新型MIGS裝置在兒童中的應用”PreserFlo外路微型分流器是一種將房水從前房分流至結膜下腔的裝置。其在難治性兒童青光眼中的使用僅限於小規模報告,作為標準治療的地位有待未來驗證9)。
OMNI手術系統結合了小樑網切開術和向Schlemm管及集合管注入黏彈性物質(黏彈劑管切開術),已有報導用於一名患有Sturge-Weber症候群相關青光眼的4個月大嬰兒。
從外路到內路手術的範式轉變正在進行中5)。內路手術無需製作結膜瓣和鞏膜瓣,可保留結膜,因此作為保留未來額外手術選擇策略是有用的。
遺傳學研究的進展
Section titled “遺傳學研究的進展”TEK/ANGPT1突變已被確定為PCG的新分子路徑,推動了對Schlemm管發育和維持機制的理解2)。關於CYP1B1基因的研究在兒童青光眼領域引起了最高的學術關注,在1955年至2022年的文獻計量分析中,分子遺傳學在25個主要研究主題中佔13個6)。
雖然目前的年齡分類對預後預測有用,但有人指出它沒有考慮遺傳背景2)。隨著基因檢測的普及,有望建立基於表現型和基因型對應關係的新分類體系。
生活品質研究趨勢
Section titled “生活品質研究趨勢”Stingl等人(2024)的系統性回顧確定了在兒童青光眼隊列中使用的10種患者報告結果指標(PROM)。其中7種達到了最高品質評分5/7,但所有指標在開發過程中均未納入兒童青光眼患者的觀點4)。需要開發針對兒童青光眼的特異性PROM。
兒童青光眼的生活品質不僅受視力障礙影響,還受反覆手術、持續點眼治療、對遺傳的擔憂以及對未來職業選擇的影響等多方面因素影響4)。
8. 參考文獻
Section titled “8. 參考文獻”- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
- Knight LSW, et al. Childhood and Early Onset Glaucoma Classification and Genetic Profile in a Large Australasian Disease Registry. Ophthalmology. 2021;128:1549-1560.
- Stingl JV, et al. Systematic Review of Instruments for the Assessment of Patient-Reported Outcomes and Quality of Life in Patients with Childhood Glaucoma. Ophthalmol Glaucoma. 2024;7:391-400.
- Chihara E, Hamanaka T. Historical and Contemporary Debates in Schlemm’s Canal-Based MIGS. J Clin Med. 2024;13(16):4882.
- Jain D, Dhua S. Bibliometric analysis of pediatric glaucoma. Indian J Ophthalmol. 2023;71(5):2152-2157.
- Elhilali HM, et al. Kahook Dual Blade goniotomy vs conventional goniotomy in primary congenital glaucoma. Am J Ophthalmol. 2020;219:150-158.
- Areaux RG Jr, et al. Trab360 suture trabeculotomy in childhood glaucoma. J AAPOS. 2019;23(6):e52.
- Burgos-Blasco B, et al. PreserFlo microshunt in refractory pediatric glaucoma. J Glaucoma. 2022;31(12):983-988.
