視神經盤所見

原發性開放隅角青光眼
1. 什麼是原發性開放隅角青光眼?
Section titled “1. 什麼是原發性開放隅角青光眼?”原發性開放隅角青光眼(POAG)是一種慢性、進行性、不可逆的視神經疾病1)。它因視盤邊緣及視網膜神經纖維層(RNFL)喪失而導致視野缺損1)3)。前房角開放,外觀正常3)。通常為雙側性,但常不對稱3)。主要危險因子為眼壓升高及年齡增長1)。早期診斷與治療通常可預防視功能損害1)3)。
原發性開放隅角青光眼的分類
Section titled “原發性開放隅角青光眼的分類”在第5版青光眼診療指引中,原發性開放隅角青光眼(廣義)被定義為涵蓋傳統眼壓高於正常範圍的原發性開放隅角青光眼(狹義)及正常眼壓性青光眼(NTG)的疾病概念9)。臨床上為方便起見,將其分為高眼壓組(狹義POAG)及正常眼壓組(NTG)9)。
根據多治見研究的結果,當以平均值±2個標準差定義日本人的正常眼壓時,正常上限為19.9~20.0 mmHg,因此在日常診療中以20 mmHg為界區分兩者具有合理性9)11)。歐洲青光眼學會(EGS)指南將兩者分別記為POAG/HTG(高眼壓性青光眼)和POAG/NTG1)2)。兩者均為連續的疾病群,治療方針基本相同。
截至2020年,全球POAG患者估計約為5300萬人3)。40~80歲的患病率為3.0%。在歐洲,40歲以上人口中有2.99%(1230萬人)患有青光眼,其中超過半數(56.4%)估計未被診斷2)3)。不同種族和民族之間的患病率存在顯著差異。非裔美國人的患病率約為白人的3倍,是不可逆失明的主要原因3)。非裔加勒比人群的患病率更高3)。西班牙裔的患病率與非裔相當,有報告稱亞裔美國人的患病率也高於白人3)。
| 流行病學研究 | 對象 | POAG(廣義) | NTG | POAG(狹義) | PACG |
|---|---|---|---|---|---|
| 多治見研究11) | 岐阜縣40歲以上 | 3.9% | 3.6% | 0.3% | 0.6% |
| 久米島研究12) | 沖繩縣40歲以上 | 4.0% | — | 0.7% | 2.2% |
多治見研究顯示,40歲以上青光眼總盛行率為5.0%,其中絕大多數為開放隅角型11)。久米島研究顯示有地區差異,閉塞隅角青光眼的頻率高於多治見研究12)。廣義POAG中約90%相當於NTG,所有青光眼中約70%為正常眼壓型。Baltimore Eye Survey顯示,眼壓30 mmHg時患有POAG的比例在白人約7%,非裔美國人25%,這顯示使用特定眼壓切點進行篩檢有其限制3)。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”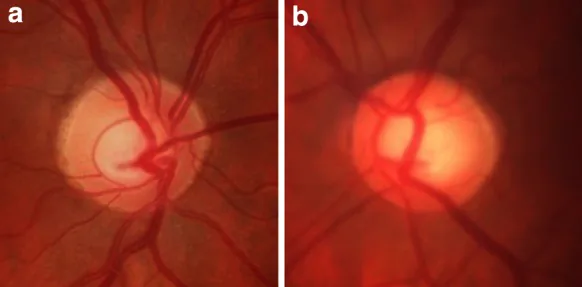
大多數原發性開放隅角青光眼患者在早期沒有症狀。視野缺損難以察覺,透過自覺症狀發現早期病例很困難。許多病例是在健康檢查或配鏡等其他原因就診眼科時,因發現高眼壓或視神經盤凹陷而被發現。
隨著疾病進展,會出現「部分模糊」或「有無法辨識物體的區域」等自覺症狀。更晚期的病例會出現視野發白、夜盲、眩光、跌倒或撞到物體等生活障礙。就診於低視力門診的青光眼患者的需求中,常包括閱讀、行走、書寫困難和畏光。
視野所見
臨床上最具特徵性的是視神經盤表現,需要透過立體觀察進行準確判斷。在與視神經損傷區域相對應的部位,視野檢查可檢測到缺損。視野表現包括弓狀暗點、鼻側階梯、旁中心暗點和普遍敏感度下降等特徵性模式3)。
關於視神經盤出血的病理機制,提出了血管學說和機械學說7)。血管學說認為一氧化氮訊號障礙導致自身調節能力下降,以及高剪切應力下視神經動脈破裂7)。出血的密度測定分析支持動脈來源7)。視神經盤出血引起的局部視網膜神經纖維壓迫可能導致結構和功能損害7)。
3. 病因與危險因子
Section titled “3. 病因與危險因子”原發性開放隅角青光眼的確定危險因子如下3)4)9)。
| 危險因子 | 概述 |
|---|---|
| 眼壓升高 | 唯一可修正因子3) |
| 年齡增長 | 最強的不可修正因子3) |
| 種族/民族 | 非洲裔、西班牙裔3) |
| 家族史 | OR 3~133) |
| 中央角膜厚度薄 | OHTS獨立因子3)4) |
| 低眼灌注壓 | 舒張期血壓降低3) |
| 第2型糖尿病 | 風險增加40~100%3)4) |
| 近視 | 存在爭議3)9) |
| 剝落症候群 | 進展風險高9) |
| 視盤出血 | 進展因子3)7) |
眼壓是POAG發病最重要的危險因子1)3)。流行病學調查顯示,隨著眼壓升高,POAG盛行率增加3)。臨床試驗證明,降低眼壓可減少POAG的發病風險及進展;早期青光眼試驗(EMGT)顯示,眼壓降低25%可使進展的相對風險降低50%2)3)。然而,視神經對眼壓的敏感性存在很大的個體差異,如正常眼壓性青光眼所示,即使在正常眼壓範圍內也可能發生視神經病變3)。
全身性危險因子
Section titled “全身性危險因子”據報導,第2型糖尿病使POAG的風險增加40~100%3)4)。視神經的微血管變化可能增加其敏感性3)。有全身性動脈高血壓的患者發生開放隅角青光眼的風險增加17%,合併糖尿病時風險增加48%3)。在接受降壓藥物治療的患者中,低舒張期灌注壓與青光眼風險增加相關3)。偏頭痛、睡眠呼吸中止、周邊血管痙攣(雷諾氏症候群)和心血管疾病也被報導為相關因子,但尚未獲得一致的結果2)3)。
家族史是強力的危險因子,已鑑定出許多基因位點,包括基因多型性。在孟德爾突變中,MYOC(肌纖蛋白)突變最常見,佔POAG的2-4%,其次是OPTN(視神經蛋白)2)。EGS第6版不建議對所有POAG患者進行基因分型,但建議對早發型家族考慮基因檢測2)。
OHTS顯示,薄中央角膜厚度(CCT)是POAG發病的獨立危險因子3)4)。薄角膜往往使眼壓測量值低於實際值,導致眼壓低估,從而增加風險。另一種理論認為,薄CCT反映了篩板、鞏膜等視神經周圍支持結構的剛性降低,提示對眼壓的脆弱性。CCT <555 μm且眼壓>25 mmHg的患眼,5年內轉化為青光眼的風險率據報導可達36%。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”原發性開放隅角青光眼的診斷需要評估眼壓、確認視神經盤損傷、確認隅角開放以及評估視野缺損3)9)。狹義POAG的確定診斷基於四個要素:①高眼壓,②視神經盤青光眼性變化,③與視神經盤變化一致的視野缺損,④排除其他眼壓升高原因。
Goldmann壓平眼壓計(GAT)是黃金標準,適用於需要精確眼壓測量的病例3)。它基於Imbert-Fick定律,壓平面積為15.09 mm²(直徑3.06 mm),在中央角膜厚度為520 μm時最為準確。應同時測量中央角膜厚度(CCT),注意薄角膜會導致低估,厚角膜會導致高估3)。
非接觸式眼壓計、回彈式眼壓計(iCare)和Tono-Pen作為輔助設備使用。iCare與Goldmann壓平眼壓計相關性良好,適用於眼瞼裂狹窄者和嬰幼兒。iCare HOME2允許患者在家中自行測量,有助於了解非門診時間的眼壓波動。有時會進行日間波動測量(phasing)以評估眼壓的日間和季節性變化。
對於確認隅角開放和排除續發性青光眼至關重要3)。檢查色素播散、剝落物質、新生血管和周邊虹膜前粘連的存在3)。初診時必須進行。
視神經盤評估與影像檢查
Section titled “視神經盤評估與影像檢查”視神經盤的立體臨床評估是黃金標準3)。使用光學同調斷層掃描(OCT)定量評估RNFL厚度和神經節細胞層被廣泛用作客觀輔助工具3)9)。隨著OCT的普及,許多POAG病例即使在早期階段也伴有黃斑部損傷,這重新認識到更早進行10度內視野檢查的必要性。對於進展監測,使用眼底照片和OCT評估隨時間的變化是有用的,但在晚期青光眼中,OCT檢測變薄存在限制(地板效應),因此視野檢查成為判斷進展的主要方法9)。OCT血管成像(OCTA)受地板效應影響較小,可能有利於晚期評估,但在臨床實踐中尚未建立標準化的使用方法9)。
使用Humphrey視野計的自動靜態閾值視野檢查是黃金標準3)。SITA(瑞典互動式閾值演算法)縮短了檢查時間。青光眼半視野測試(GHT)檢測上下半視野的不對稱性。頻率倍增技術(FDT)和SITA-SWAP(藍-黃視野檢查)也用於檢測早期視野缺損。對於進展評估,事件分析和趨勢分析結合使用;趨勢分析對進展速度的定量評估有用9)。
需要鑑別的疾病包括高眼壓症、NTG、原發性閉角型青光眼、色素性青光眼、剝落性青光眼、類固醇性青光眼、發育性青光眼、葡萄膜炎續發性青光眼、高坪虹膜症候群、燒毀型原發性開放隅角青光眼、自然緩解的類固醇性青光眼、Posner-Schlossman症候群緩解期3)。神經眼科疾病(顱內腫瘤引起的視神經病變、上方節段性視神經發育不全SSOH等)也是鑑別對象,可能需要影像檢查排除。YAG雷射玻璃體溶解術後的續發性開放隅角青光眼也列入鑑別診斷;已有因小梁網蛋白顆粒積聚導致慢性眼壓升高的病例報告,術後眼壓監測很重要8)。
青光眼疑似(glaucoma suspect)定義為具有持續性眼壓升高,或具有疑似青光眼之視神經盤、RNFL或視野所見之一的情況4)。在OHTS中,未經治療的OHT患者超過90%在5年內未進展為POAG4)。開始治療的判斷基於危險因子的數量與程度,或基於視神經/視野變化的進展所見4)。定期檢查(每6~12個月)監測結構與功能變化,當發現進展時開始治療。視神經存在青光眼性異常但常規靜態視野檢查無異常的狀態稱為前視野青光眼(preperimetric glaucoma),存在危險因子時可考慮治療9)。
5. 標準治療方法
Section titled “5. 標準治療方法”原發性開放隅角青光眼的治療目標為:①控制目標眼壓,②維持視神經與視網膜,③維持視野9)。降低眼壓是唯一有證據基礎的治療1)3)9)。
目標眼壓的設定
Section titled “目標眼壓的設定”目標眼壓根據青光眼分期、未治療時眼壓、預期壽命、年齡、視野缺損進展、家族史、對側眼狀況與危險因子個別設定9)。依分期的目標眼壓範例:早期≤19 mmHg,中期≤16 mmHg,晚期≤14 mmHg9)。此外,基於多項RCT(EMGT、OHTS、CIGTS、AGIS等)的證據,建議設定從未治療眼壓降低20~30% 為目標9)。
晚期病例進展對生活品質影響大,因此目標眼壓設定得更低;若預期壽命較長,則旨在更積極地減緩進展9)。目標眼壓並非絕對值,在追蹤中根據進展狀況適時修正9)。中期以後為獲得充分的進展減緩,通常以低teen至sub-teen為目標,達到此眼壓水準常需手術治療。
點眼藥治療
前列腺素FP受體促效劑:最廣泛使用的一線藥物。包括拉坦前列素、曲伏前列素、他氟前列素、比馬前列素。透過促進葡萄膜鞏膜流出,降低眼壓約25~35%,每日一次點眼9)。
EP2受體促效劑(奧米德內帕格異丙酯):具有新型作用機轉,2018年核准的一線候選藥物。非劣效於拉坦前列素。禁用於植入人工水晶體的眼,且不建議與FP受體促效劑併用9)。
β受體阻斷劑:抑制房水生成。包括噻嗎洛爾、卡替洛爾、倍他洛爾等。需注意全身性副作用(心搏過緩、支氣管痙攣)9)
碳酸酐酶抑制劑:抑制房水生成。包括多佐胺、布林佐胺眼藥水以及口服乙醯唑胺9)
α2促進劑(溴莫尼定):具有抑制房水生成和促進葡萄膜鞏膜流出雙重作用9)
Rho激酶抑制劑(利帕舒地爾):一種直接促進小梁網流出的新型藥物,在日本全球首次核准。主要副作用為結膜充血9)
雷射與手術治療
SLT(選擇性雷射小樑成形術):使用532 nm Q開關倍頻YAG雷射,光點大小400 μm,能量0.4~1.2 mJ,脈衝寬度3奈秒,照射小樑網1/2至全周9)。LiGHT試驗顯示其長期效果不亞於甚至優於眼藥水,EGS第6版、AAO PPP和英國NICE推薦作為一線治療1)2)10)
小樑切除術(合併MMC):最成熟的青光眼濾過手術。對於包括POAG在內的大多數類型青光眼是最常見的開放式手術。日本患者5年晚期感染發生率為2.2%9)
引流管植入手術:使用Baerveldt青光眼植入物(BG101-350、BG102-350、BG103-250)、Ahmed青光眼閥(FP7、FP8)和Ex-PRESS®微型引流管等6)9)
MIGS(微創青光眼手術):使用多種器械,包括iStent/iStent inject、Hydrus、Kahook Dual Blade、GATT、Trabectome、Xen、PreserFlo和OMNI,旨在重建小樑網流出通道6)13)14)
睫狀體光凝固術:包括連續波經鞏膜二極體雷射(2000 mW,2秒)和經鞏膜微脈衝雷射(2000 mW,80秒×2)。為難治病例的選擇9)
治療方針:基本原則是從單一藥物治療開始,並盡可能將合併用藥限制在兩種以內9)。藥物選擇需考量目標眼壓、副作用、點藥次數和使用感受。開始治療時,建議進行單眼試驗(單眼給藥以評估療效)9)。多藥合併使用時,複方眼藥水有助於維持遵醫囑性;日本已核准多種含有兩種成分的複方眼藥水9)。單一藥物療效不足時,可更換藥物或合併用藥(包括複方眼藥水),若仍無法達到目標眼壓或出現視野惡化,則考慮雷射治療或侵入性手術9)。
對於老年人等擔心全身副作用的病例,應避免使用β阻斷劑,在前列腺素相關藥物之後選擇碳酸酐酶抑制劑、α2促進劑和Rho激酶抑制劑。遵醫囑性不佳是病情進展的重要因素;在日本,約40%首次處方青光眼眼藥水的患者在治療開始約一年內中斷治療9)。建議提供書面說明、就診管理和提醒通知等持續性長期管理措施9)。
主要臨床試驗的證據
Section titled “主要臨床試驗的證據”| 臨床試驗 | 對象 | 結果 |
|---|---|---|
| OHTS | 高眼壓症患者 | 降低眼壓可抑制原發性開放角型青光眼的發生3)4) |
| EMGT | 新診斷的原發性開放角型青光眼 | 眼壓每降低1 mmHg,進展減少10%;降低25%可使進展風險降低50%2)3) |
| AGIS | 進展期原發性開放角型青光眼 | 維持低眼壓可保護視野3) |
| LiGHT試驗 | OAG/OHT 新發 | 一線SLT比眼藥水長期眼壓控制更佳10) |
| HORIZON | POAG + 白內障 | 合併Hydrus術後5年眼壓和眼藥水數量均降低13) |
| iStent關鍵試驗 | POAG + 白內障 | 術後2年眼壓和眼藥水數量低於單純白內障手術14) |
EMGT的長期追蹤數據顯示,未治療時的自然進展速度因疾病類型而異。高眼壓型(HTG)1.31 dB/年,正常眼壓型(NTG)0.36 dB/年,剝落性青光眼(PXFG)3.13 dB/年,其中剝落性青光眼進展最快3)。
LiGHT試驗6年結果顯示,SLT一線治療組69.8%的患者無需額外治療即可維持目標眼壓,進展率顯著低於眼藥水組(19.6% vs 26.8%,P=0.006)10)。SLT組的小樑切除術數量(13眼)顯著少於眼藥水組(32眼,P<0.001),白內障手術數量也顯著少於眼藥水組(57眼 vs 95眼,P=0.03)。未觀察到嚴重的雷射相關不良事件10)。基於這些結果,歐洲青光眼學會、美國眼科學會和英國NICE推薦SLT作為OAG/OHT的一線治療選擇1)2)3)10)。
蘇格蘭青光眼試驗中,小樑切除術實現了58%的眼壓下降,且視野進展少於藥物治療(42%)3)。Moorfields一線治療試驗顯示小樑切除術具有最大的降眼壓效果(60%)3)。
難治性POAG的手術策略
Section titled “難治性POAG的手術策略”MIGS術後眼壓控制不佳的處理是臨床挑戰6)。在多位專家的小組討論中,對於對側眼MIGS失敗的進展期POAG病例,討論了小樑切除術、引流管植入術和脈絡膜上腔引流術等選擇6)。Schlemm管手術失敗提示Schlemm管以外的流出通道受限,而小樑切除術效果有限提示傷口癒合反應旺盛6)。根據每個病例的特點制定個體化的手術策略至關重要6)。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”原發性開放隅角青光眼的最終共同路徑是視神經乳頭處視網膜神經節細胞(RGC)的喪失5)。RGC死亡是主要的病理過程,其喪失的模式和速度在結構和功能上均有定義5)。損傷機制大致分為眼壓依賴性因素和非眼壓依賴性因素。
眼壓依賴性機制
Section titled “眼壓依賴性機制”POAG中的眼壓升高被認為是由隅角和小樑網的功能性房水流出障礙引起的。病理上可見小樑網束和內皮網上的細胞外基質沉積、小樑間隙變窄以及Schlemm管閉塞。RGC軸突的初始損傷發生在視神經乳頭(ONH),導致順行和逆行軸突運輸受阻5)。ONH處篩板(LC)的物理重塑解釋了上極和下極RGC軸突的選擇性喪失5)。
POAG並非病理診斷的疾病,而是臨床症候群之一。常有家族史,遺傳是發病的重要因素。已鑑定出包括MYOC、OPTN在內的許多基因位點,但僅少數病例可由單基因突變解釋,提示多基因遺傳背景2)。
眼壓非依賴性機制
Section titled “眼壓非依賴性機制”血管調節障礙是重要的非眼壓依賴性因子7)。在原發性開放角型青光眼中,一氧化氮訊號受損導致自我調節能力下降,視神經動脈在高剪切應力下更容易破裂7)。視盤出血是血管調節障礙的生物標誌物,出血對RGC軸突的局部壓迫可能導致結構和功能損傷7)。
篩板前楔形缺損(PLWDs)在POAG中比健康眼更常見,且與視盤出血病史顯著相關7)。PLWDs被認為反映了非眼壓依賴性因素(如血管功能障礙)導致的視神經脆弱性7)。
其他非眼壓因素包括興奮毒性損傷(過量麩胺酸)、自體免疫介導的神經病變、神經營養因子喪失以及視網膜和脈絡膜血管的自我調節異常。腦脊髓液壓力降低可能增加視神經乳頭的經篩板壓力差,作為即使在正常眼壓下也能引起視神經病變的因素而受到關注。NTG中冷感症、偏頭痛等末梢循環障礙和心血管疾病的合併症較多,也提示循環障礙因素的參與。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”SLT一線治療的範式轉變
Section titled “SLT一線治療的範式轉變”LiGHT試驗的6年結果確立了SLT作為一線治療的地位10)。SLT一線治療組與眼藥水一線治療組相比,疾病進展率顯著降低,約70%的眼睛無需額外治療即可維持目標眼壓,所需的小樑切除術和白內障手術數量也顯著減少10)。EGS第6版、AAO PPP和英國NICE指南推薦SLT作為與眼藥水並列的一線治療選擇1)2)3)。
難治性POAG手術策略的演變
Section titled “難治性POAG手術策略的演變”MIGS失敗後進展期POAG的管理正在積極討論中6)。脈絡膜上腔分流器(如MINIject)可能繞過Schlemm管後的流出道障礙,並消除濾過泡相關併發症6)。Paul青光眼植入物(PGI)相比傳統引流管植入物,預期具有更可預測的術後早期眼壓和更小的管徑以保護角膜內皮6)。多種MIGS技術的聯合使用以及針對小樑網流出、葡萄膜鞏膜流出和脈絡膜上腔流出的不同機制組合也在探索中6)。HORIZON研究顯示,Hydrus Microstent聯合白內障手術在5年時顯著降低眼壓和眼藥水數量13)。
視盤出血的病理生理學
Section titled “視盤出血的病理生理學”已有報告指出視盤出血的發生部位(近端型 vs 遠端型)與進展風險相關7)。杯型(近端型)DH比視盤周圍型(遠端型)進展風險更高,提示在篩板層級對RGC軸突的壓迫性視神經病變可能參與其中7)。密度測定研究獲得了支持視盤出血源自動脈的證據7)。
- 各種MIGS術式的長期比較數據累積6)13)14)
- 透過大規模RCT驗證上脈絡膜分流術的有效性與安全性6)
- 開發最小化視盤出血復發的治療方法7)
- 開發針對非眼壓依賴性因子的神經保護治療
- 基於遺傳風險輪廓的個人化醫療實現
- 利用居家眼壓測量(如iCare HOME2)進行晝夜及長期波動監測
8. 參考文獻
Section titled “8. 參考文獻”- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2021.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
- American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern®. 2020.
- American Academy of Ophthalmology. Primary Open-Angle Glaucoma Suspect Preferred Practice Pattern®. 2020.
- Asrani SG, McGlumphy EJ, Al-Aswad LA, Chaya CJ, Lin S, Musch DC, Pitha I, Robin AL, Wirostko B, Johnson TV. The relationship between intraocular pressure and glaucoma: An evolving concept. Prog Retin Eye Res. 2024;103:101303. doi:10.1016/j.preteyeres.2024.101303.
- Huang MJ, Samuelson TW, De Francesco T, et al. Managing primary open-angle glaucoma in the setting of suboptimal surgical outcomes in the fellow eye. J Cataract Refract Surg. 2023;49(7):764. doi:10.1097/j.jcrs.0000000000001221.
- Verticchio Vercellin A, Pasquale LR, Harris A. Disc hemorrhages in open-angle glaucoma—between a rock and a hard place? JAMA Ophthalmol. 2024;142(10):950-951.
- de Vries E, Faraj C, Gerbrandy F, Hulsman C. Secondary open-angle glaucoma following YAG-laser vitreolysis. BMJ Case Rep. 2022;15(4):e248937. doi:10.1136/bcr-2022-248937.
- 日本緑内障学会緑内障診療ガイドライン作成委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Gazzard G, Konstantakopoulou E, Garway-Heath D, et al. Laser in Glaucoma and Ocular Hypertension (LiGHT) Trial: Six-Year Results of Primary Selective Laser Trabeculoplasty versus Eye Drops for the Treatment of Glaucoma and Ocular Hypertension. Ophthalmology. 2023;130(2):139-151.
- Iwase A, Suzuki Y, Araie M, et al. The prevalence of primary open-angle glaucoma in Japanese: the Tajimi Study. Ophthalmology. 2004;111(9):1641-1648.
- Sawaguchi S, Sakai H, Iwase A, et al. Prevalence of primary angle closure and primary angle-closure glaucoma in a southwestern rural population of Japan: the Kumejima Study. Ophthalmology. 2012;119(6):1134-1142.
- Ahmed IIK, De Francesco T, Rhee D, et al. Long-term Outcomes from the HORIZON Randomized Trial for a Schlemm’s Canal Microstent in Combination Cataract and Glaucoma Surgery. Ophthalmology. 2022;129(7):742-751.
- Samuelson TW, Sarkisian SR Jr, Lubeck DM, et al. Prospective, Randomized, Controlled Pivotal Trial of an Ab Interno Implanted Trabecular Micro-Bypass in Primary Open-Angle Glaucoma and Cataract: Two-Year Results. Ophthalmology. 2019;126(6):811-821.
