急性發作時的所見

原發性閉角型青光眼(PACG)和原發性閉角型青光眼疑似(PACS)
1. 什麼是原發性閉鎖隅角青光眼?
Section titled “1. 什麼是原發性閉鎖隅角青光眼?”原發性閉鎖隅角青光眼(PACG)是在無其他因素的情況下,因遺傳背景或年齡相關的前節形態變化導致原發性隅角閉鎖,引起眼壓上升,且已發生青光眼性視神經病變的疾病1)。原發性閉鎖隅角症(PAC)是指因原發性隅角閉鎖導致眼壓上升,或已形成周邊虹膜前粘連(PAS),但尚未發生青光眼性視神經病變的狀態1)。原發性閉鎖隅角症疑似(PACS)是指存在原發性隅角閉鎖,但無眼壓上升、無器質性PAS,也無青光眼性視神經病變的狀態1)。
原發性閉角病(primary angle closure disease:PACD)一詞被用作涵蓋這三個階段以及急性原發性閉角型青光眼(acute PACG)和急性原發性閉角(acute PAC)的總稱1)2)。使用PACD這個總稱的意義在於強調同一個人的病情可根據進展階段從PACS向PAC、再向PACG過渡的連續譜系,從而促進無縫追蹤和早期介入1)2)。
隅角鏡檢查的診斷標準如下2)12)。
| 分期 | ≥180度虹膜小樑網接觸(ITC) | 眼壓升高或PAS | 青光眼性視神經病變 |
|---|---|---|---|
| PACS | 有 | 無 | 無 |
| PAC | 有 | 有 | 無 |
| PACG | 有 | 有 | 有 |
2002年的Foster分類將ITC≥3個象限(270度)定義為PACS,但目前沿用2021年以後的美國Preferred Practice Pattern分類,以ITC≥180度為標準2)12)。
PACG和PAC有急性發作型和慢性型。急性原發性閉角型青光眼和急性原發性房角關閉時,眼壓常顯著升高至40–80 mmHg,出現視力下降、視物模糊、虹視、眼痛、頭痛、噁心、嘔吐、瞳孔對光反射減弱或消失等症狀1)2)。而慢性原發性閉角型青光眼(CACG)無急性眼壓升高史,中等程度眼壓升高(20–30 mmHg)緩慢進展1)。
多治見研究報告,40歲以上人群中PACS佔0.2%,PAC佔0.5%,PACG佔0.6%13)。另一項日本人群研究報告40歲以上PACG患病率為0.34–0.6%2)。全球40歲以上人群中約0.7%患有閉角型青光眼,2013年估計為2020萬人,其中1550萬人集中在亞洲2)11)。預計到2040年,患病人數將增加約50%,達到3200萬人,超過500萬人可能失明2)。
種族差異顯著:因紐特人2.5–3.8%,台灣3.0%,中國廣州1.5%,北京1.2%,新加坡1.1%,蒙古1.4%,泰國0.9%,南印度0.5–0.87%,孟加拉國0.4%2)。歐洲裔人群較低,為0–0.6%2)。在部分亞洲人群中,PACG的患病率與原發性開角型青光眼(POAG)相當2)11)。與POAG相比,PACG初診時單眼失明率更高,雙眼重度視力障礙風險約為3倍2)。
此外,PACG的發病年齡往往高於POAG,50歲以上女性的發病風險顯著增加2)。從PACG和POAG的性別比來看,POAG的性別差異很小,而PACG女性是男性的2至4倍2)。與男性相比,女性前房深度較淺,眼軸長度較短,這作為解剖學因素起到了作用2)。在日本,隨著人口老化,預計PACG患者的絕對數量將增加,因此需要完善診療體系並加強初級醫療中的窄角篩查2)11)。
並非所有PACS都需要統一進行雷射治療。在中國中山進行的Zhongshan Angle Closure Prevention試驗(ZAP試驗)中,未經治療的PACS眼在6年內進展為PAC或急性發作的比例約為4%,14年內約為12%,預防性雷射虹膜切開術的相對風險降低在6年為47%,14年為70%,但絕對獲益較小3)。新加坡的ANA-LIS試驗也顯示出類似趨勢,5年進展率為9.4%,LPI降低風險45%4)。基於這些結果,歐洲青光眼學會指南第6版不推薦對健康的PACS眼常規進行LPI,僅建議對高度遠視、需要頻繁散瞳、就醫困難等高危病例考慮LPI5)。日本青光眼診療指南第5版也將暗室試驗或俯臥試驗陽性、難以定期檢查、急性發作時無法及時就診、家族史陽性、因糖尿病視網膜病變等需要頻繁散瞳的病例列為手術適應症1)。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”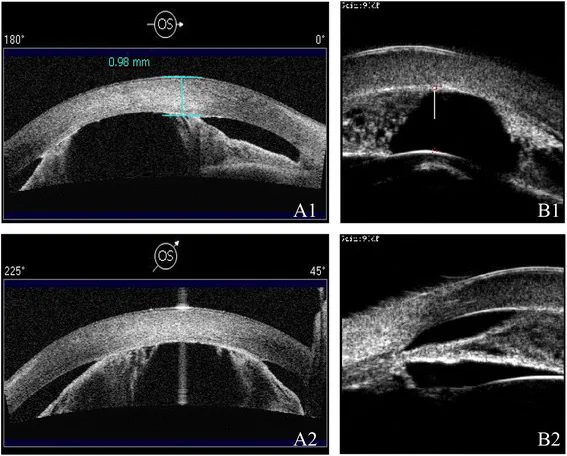
PACS和慢性PACG通常自覺症狀不明顯,患者常在晚期才察覺到視力下降或視野缺損1)2)。慢性期眼壓升高緩慢,因此視神經損傷可能在患者未察覺的情況下進展1)。此外,因輕度瞳孔阻滯導致的短暫眼壓升高(間歇性隅角閉鎖)可能反覆出現模糊的暗處視力模糊或輕度頭重感等症狀,透過問診發現這些症狀很重要2)。
相反地,急性發作時症狀劇烈。包括視力下降、視物模糊、虹視症(燈光周圍出現彩色光環)、劇烈眼痛伴同側頭痛、噁心嘔吐等迷走神經症狀1)2)。虹視症是因角膜水腫導致光線折射異常,在燈泡或路燈周圍看到彩色光環。頭痛和噁心可能成為主要表現,患者可能被誤導至神經內科或消化內科,因此對於原因不明的劇烈頭痛伴有眼部症狀的患者,必須進行眼科評估2)7)。此外,也存在症狀不明顯的亞急性發作,高眼壓持續而無明確疼痛,可導致視神經損傷進展,因此不應忽略眼底和隅角檢查1)2)。
慢性PACG的所見
眼壓:中度升高,20~30 mmHg
眼前節:淺前房、短眼軸、水晶體厚且位置偏前
隅角:PAS導致的器質性閉塞與功能性隅角關閉(appositional closure)並存
視神經:青光眼性凹陷、視盤邊緣變薄
視野:與原發性開放隅角青光眼相似的進行性視野缺損
症狀:通常無症狀,僅進展期患者自覺視力或視野異常
高褶虹膜的所見
前房:中央部深度大致正常
虹膜中央:平坦,無膨隆
虹膜根部:呈銳角向後彎曲,梯形,周邊隅角顯著狹窄
壓迫隅角鏡:雙峰徵(虹膜呈雙峰狀凹陷)
UBM:睫狀體前移,睫狀溝消失,虹膜根部增厚14)
確診:LPI術後散瞳仍可再現隅角關閉和眼壓升高
3. 原因與風險因素
Section titled “3. 原因與風險因素”解剖學易感因素與人口統計學風險
Section titled “解剖學易感因素與人口統計學風險”PACG是在遺傳和解剖學易感因素基礎上,加上年齡相關變化而發病的1)2)。主要風險因素如下。
| 類別 | 因素 | 概述 |
|---|---|---|
| 屈光 | 遠視 | 短眼軸導致的淺前房1)2) |
| 解剖 | 短眼軸長度 | 眼軸長度小於20 mm的小眼球風險極高2) |
| 解剖 | 淺前房 | 中央前房深度小於2.0–2.2 mm為高風險2) |
| 解剖 | 水晶體厚度及前位 | 隨年齡增長而增加,促進瞳孔阻滯1)2)10) |
| 解剖 | 小角膜直徑 | 水平直徑小於11 mm風險增加2) |
| 年齡 | 50歲及以上 | 患病率隨年齡增長而增加1)2) |
| 性別 | 女性 | 比男性更常見1)2) |
| 種族 | 亞洲人或因紐特人 | 因地區而異,是歐洲人的數倍至數十倍2)11) |
| 家族史 | 一等親有PACD家族史 | 遺傳易感性2) |
| 誘發藥物 | 抗膽鹼能藥、散瞳藥、擬交感神經藥 | 胃鏡檢查前用藥、安眠藥、抗精神病藥、感冒藥、三環類抗憂鬱藥、SSRI、鼻炎噴霧劑、部分吸入劑等2)7) |
發病機轉分類
Section titled “發病機轉分類”原發性閉鎖隅角青光眼及原發性閉鎖隅角疾病的成因通常非單一機轉,而是多種機轉複合參與1)2)10)。
- 相對性瞳孔阻滯:虹膜背面與水晶體前表面的接觸阻礙了房水從後房流向前房,導致後房壓力升高,虹膜向前膨隆覆蓋小樑網。這是PACD最常見的機轉1)2)。
- 高褶虹膜:睫狀體位置靠前,將虹膜根部向前推,散瞳時直接阻塞隅角的解剖形態異常1)14)。
- 水晶體因子:年齡相關的水晶體厚度增加及水晶體前移。在白內障進展期尤為明顯1)10)。
- 水晶體後方因子:由於睫狀體、脈絡膜或玻璃體的形態異常導致虹膜-水晶體膈前移1)。
已知誘發急性發作的生活因素包括:在暗處閱讀或看電影、長時間低頭姿勢(園藝、手術、長途駕駛)、夜間自然散瞳、具有抗膽鹼作用的藥物口服/吸入/滴鼻、散瞳檢查的影響、以及強烈的精神壓力等2)7)。特別是老年女性的胃鏡檢查前用藥、精神科藥物、帕金森氏症治療藥物、以及用於氣喘/慢性阻塞性肺疾病(COPD)的抗膽鹼吸入劑容易被忽略,與處方醫師的協作至關重要2)7)。對於有PAC傾向的患者,應指導其在使用非處方感冒藥、鼻炎藥、暈車藥或抗組織胺藥前諮詢眼科醫師2)。此外,50歲以上的遠視患者若推遲白內障手術,隨著水晶體增齡性增厚,發作風險會增加,因此白內障手術的適應症判斷本身即可成為預防性介入6)10)。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”隅角鏡檢查是診斷原發性閉鎖隅角疾病最重要的檢查,是黃金標準1)2)5)。點眼麻醉後,首先在第一眼位不加壓,使用短而窄的裂隙光進行靜態隅角鏡檢查。注意避免瞳孔因裂隙光而收縮,評估隅角隱窩的解剖結構(Schwalbe線、小樑網、鞏膜突、睫狀體帶)、微小PAS以及隅角色素沉著2)。然後通過動態/壓迫隅角鏡鑑別功能性關閉和器質性關閉(PAS)。根據Shaffer-Kanski分級,2級或以下(隅角≤20度)提示可能隅角關閉,1級或以下則關閉風險高。
van Herick法
Section titled “van Herick法”這是一種僅用裂隙燈顯微鏡即可完成的簡便篩查方法。將裂隙光從60度角照射到顳側角膜緣,通過周邊前房深度與角膜厚度的比值進行評估。當前房深度小於或等於角膜厚度的1/4(1~2級)時,隅角關閉的可能性很高,必須加做隅角鏡檢查2)。
| 檢查 | 特點 | 在PACD中的角色 |
|---|---|---|
| 眼前段OCT | 非接觸、快速、一次拍攝四個象限。定量評估AOD500、隅角隱窩面積、ITC指數等2) | 隅角關閉的客觀定量、病程比較、暗/明環境下的動態評估 |
| 超音波生物顯微鏡(UBM) | 接觸式,組織穿透深度高,可觀察到睫狀體2)14) | 診斷虹膜高褶(睫狀體前位、睫狀溝消失)、鑑別惡性青光眼 |
| 全周隅角相機 | 16面多鏡同時360度拍攝 | 隅角資訊的篩查和追蹤 |
| 眼軸長度測量 | 軸長<20 mm提示小眼球,水平角膜直徑<11 mm提示相對性眼前段小眼球2) | 識別高風險眼、手術計劃制定 |
| 角膜內皮細胞檢查 | 角膜內皮顯微鏡 | 評估發作眼內皮細胞減少,判斷LPI安全性 |
眼前段OCT可非接觸快速定量評估,也用於縱向進展預測。CASIA2的STAR Analysis可自動360度分析AOD500,對窄角篩查有用2)。但難以區分顏色信息或器質性關閉,因此不能替代隅角鏡檢查,而是補充工具2)5)。UBM為接觸式且耗時,但在分析睫狀體和虹膜後面方面優於眼前段OCT,對確診高褶虹膜不可或缺2)14)。
負荷試驗與鑑別診斷
Section titled “負荷試驗與鑑別診斷”暗室試驗、俯臥試驗、散瞳試驗等負荷試驗的診斷能力有限。據報導,ZAP試驗無法透過暗室俯臥試驗識別進展高風險族群3)。因此,診斷需綜合臨床所見、隅角所見和影像所見進行。
應始終考慮以下鑑別診斷1)2):
- 繼發性閉塞隅角:膨脹性白內障、水晶體半脫位、葡萄膜炎引起的虹膜後粘連、Vogt-小柳-原田病、眼內腫瘤、脈絡膜出血、托吡酯等磺胺類藥物誘發2)
- 惡性青光眼(房水引流異常)
- 新生血管性青光眼、剝落性青光眼1)
- 虹膜角膜內皮(ICE)症候群
- 中心性漿液性脈絡膜視網膜病變或後鞏膜炎引起的脈絡膜前膨隆
原發性閉角疾病原則上為雙眼性。若對側眼顯示深前房和寬隅角,應高度懷疑繼發性原因2)7)。特別是單眼急性發作伴有水晶體半脫位或外傷史時,考慮外傷性水晶體脫位;年輕患者雙眼急性發作時,考慮托吡酯等磺胺類藥物誘發2)。新生血管性青光眼需檢查虹膜紅變和後段疾病(糖尿病視網膜病變、視網膜中央靜脈阻塞等)病史1)。
視神經與視野評估
Section titled “視神經與視野評估”PACG的診斷必須證明青光眼性視神經病變1)2)。急性期由於角膜水腫,詳細的眼底觀察困難,但使用視網膜/視神經OCT而非間接檢眼鏡或前段OCT,可以在不散瞳的情況下評估視盤、視網膜神經纖維層(RNFL)和黃斑部神經節細胞複合體(GCC)2)。發作時RNFL因軸突腫脹而暫時增厚,1個月後恢復正常,3個月後變薄,因此需要縱向評估2)。視野檢查應在發作平息後進行,使用Humphrey 24-2 SITA或等效的自動靜態視野計,並按照與POAG相同的方法追蹤進展1)5)。
前段OCT非接觸、短時間內可定量評估360度隅角,適合門診篩查和縱向比較。CASIA2的STAR分析可從16個方向自動分析AOD500,並以彩色地圖顯示ITC區域2)。而UBM為接觸式且耗時,但由於使用超音波,可顯示睫狀體和虹膜後表面結構,對於診斷以睫狀體前位和睫狀溝消失為特徵的虹膜高褶症候群必不可少2)14)。當懷疑惡性青光眼、睫狀體腫瘤或水晶體後器質性病變時,UBM也是首選。臨床實踐中,前段OCT通常用於篩查和縱向評估,而UBM用於睫狀體評估、虹膜高褶確診和鑑別診斷2)5)。
5. 標準治療
Section titled “5. 標準治療”治療目標是解除隅角關閉、長期控制眼壓和預防視神經損傷1)2)5)。根據分期(PACS/PAC/PACG)和急性/慢性不同,治療策略有所不同。
PACS的管理
Section titled “PACS的管理”大多數PACS不會進展為PAC或PACG,但有一定比例會進展,因此建議根據風險進行管理1)2)3)。
| 風險 | 推薦管理 |
|---|---|
| 低風險(非老年女性、無家族史、醫療可及性好) | 觀察2)3)5) |
| 中高風險(高度遠視、PACG家族史、頻繁需要散瞳、醫療可及性差、常用抗膽鹼藥物) | 考慮LPI1)2)5) |
| 合併白內障病例 | 水晶體摘除也是一種選擇1)6) |
對於有風險的患者,具有抗膽鹼作用的非處方藥,如感冒藥、助眠藥和暈車藥,可能誘發急性發作。因此,患者教育和症狀出現時的緊急就診指導非常重要2)7)。
PAC / PACG(相對性瞳孔阻滯引起的病例)
Section titled “PAC / PACG(相對性瞳孔阻滯引起的病例)”青光眼診療指南第5版推薦將雷射虹膜切開術或水晶體摘除術解除瞳孔阻滯作為首選治療(推薦等級1A)1)。由於大多數病例為雙眼性,如果一隻眼出現PACG或PAC,應對另一隻眼的窄房角進行預防性LPI(1A)或水晶體摘除術(1A)1)。
- 雷射虹膜切開術(LPI):使用Nd:YAG單獨或聯合氬雷射進行。不推薦單獨使用氬雷射照射,因為內皮損傷風險大1)。併發症包括一過性眼壓升高、前房出血、侷限性白內障、角膜內皮損傷、繼發性水疱性角膜病變以及眩光、光暈等視覺症狀2)。
- 水晶體摘除術(超音波乳化吸除+人工水晶體植入):從根本上解除瞳孔阻滯,增加前房深度,加寬房角1)10)。EAGLE試驗比較了50歲以上症狀性PAC(眼壓≥30 mmHg)或PACG患者早期透明水晶體摘除與LPI的效果,3年後水晶體摘除組在生活品質(EQ-5D)和眼壓控制方面更優,不使用眼藥水維持眼壓控制的機率約高出10倍6)。英國的成本分析估計3年時具有良好成本效益,10年時節省成本2)6)。歐洲青光眼學會指南第6版強烈推薦50歲以上的PAC/PACG患者進行水晶體摘除或LPI5)。
- 周邊虹膜切除術:適用於因角膜混濁等原因難以進行LPI的病例1)。由於是侵入性內眼手術,存在併發症風險,但能可靠地恢復房水流通1)。
- LPI的部位選擇:雖然曾有報告推薦12點鐘方向,但由於視覺症狀(閃光感)的報告增多,近年來比較了顳上或水平(3點或9點)位置。隨機試驗結果不一致,但選擇上方象限被上眼瞼充分覆蓋的位置還是水平位置,由各機構自行決定2)。術後大多數閃光感(眩光、複視、線狀光視)在6個月內自然緩解2)。
EAGLE(Effectiveness in Angle-Closure Glaucoma of Lens Extraction)試驗是一項以英國為中心的多中心隨機對照試驗,將419例50歲以上的症狀性PAC(眼壓≥30 mmHg)或PACG患者隨機分配至早期透明晶狀體摘除(CLE)或LPI組6)。3年時,CLE組在QoL指標(EQ-5D)、眼壓控制和額外治療需求方面均優於LPI組;無需藥物即可維持目標眼壓的機率,CLE組約為LPI組的10倍6)。英國的成本分析顯示,3年時具有成本效益,10年時估計可節省成本2)6)。據此,美國眼科學會的原發性房角關閉疾病優選實踐模式也提出,即使在沒有影響視功能的白內障的病例中,對於高眼壓的PAC和PACG,早期晶狀體摘除可作為初始治療選擇2)。歐洲青光眼學會指南第6版也同等強烈推薦50歲以上PAC和PACG患者進行晶狀體摘除和LPI5)。日本青光眼診療指南第5版也將其列為與LPI並列的一線選擇,推薦等級為1A1)。
急性原發性隅角閉鎖青光眼(APAC)的治療
Section titled “急性原發性隅角閉鎖青光眼(APAC)的治療”急性發作是眼科急症,早期降低眼壓並解除瞳孔阻滯決定視功能預後1)2)7)。日本青光眼診療指南第5版推薦以下階梯式治療1)。
初始藥物治療:
- 高滲透壓藥:20% D-甘露醇1.0~2.0 g/kg,30~60分鐘內靜脈滴注。眼壓在開始滴注後60~90分鐘達到最低值,效果持續4~6小時。腎功能不全或心衰竭患者需謹慎使用1)。甘油300~500 mL,45~90分鐘內靜脈滴注,糖尿病患者需注意血糖1)。
- 縮瞳藥:1%或2%鹽酸毛果芸香鹼滴眼液,每小時滴眼2~3次1)。但若眼壓極高,瞳孔括約肌缺血導致對光反射消失,則縮瞳效果可能不佳,且頻繁滴眼可能因睫狀肌前移加重瞳孔阻滯,應避免1)。
- 抑制房水生成:聯合使用乙醯唑胺10 mg/kg靜脈注射或口服、β受體阻斷劑滴眼液、α2受體激動劑滴眼液、碳酸酐酶抑制劑滴眼液1)。
- 消炎:使用倍他米松等類固醇眼藥水鎮靜前眼部發炎1)。
手術治療:
青光眼診療指引第5版建議,對於急性原發性隅角閉鎖青光眼及急性原發性隅角閉鎖,首選水晶體重建術1)。若當天無法進行緊急手術,應先用上述藥物降低眼壓,待角膜透明後再進行LPI1)。LPI雷射設定範例:首先使用200–400 μm、200 mW、0.2秒的氬雷射拉伸虹膜;接著使用50 μm、800–1,000 mW、0.02秒將其削薄至即將穿孔;最後以Nd:YAG雷射2.0–4.0 mJ進行1–2次穿孔。為保護角膜內皮,總照射次數最好少於100次1)。角膜混濁時,考慮轉為手術周邊虹膜切除術。
亞太青光眼學會(APGS)與亞太眼科教授學會於2025年發布的關於急性原發性隅角閉鎖發作(APACA)共識提出,對於發病後眼壓超過50 mmHg的病例,僅靠傳統藥物治療起效慢且存在全身併發症風險,因此應積極考慮以下替代治療7)。
- 氬雷射周邊虹膜成形術(ALPI):使用低功率、長脈衝、大光斑雷射收縮周邊虹膜,機械性增寬隅角。一項隨機對照試驗顯示,ALPI後15分鐘平均眼壓降至30.8 mmHg,30分鐘降至24.1 mmHg,比傳統藥物治療更快達到目標眼壓7)。
- 雷射瞳孔成形術(LPP):使用532 nm雷射收縮並外翻瞳孔緣,解除瞳孔阻滯。即使角膜透明度稍差也可進行,常與ALPI合併使用7)。
- 前房穿刺(ACP):使用30 G針頭或15度刀片減壓前房,可立即降低眼壓。即使沒有氬雷射的設施也可進行7)。
這些替代治療建議避免對「熱而憤怒」的發作眼進行緊急小樑切除術或緊急超音波乳化術,這些手術以往是被迴避的7)。急性發作平息後的早期超音波乳化術可作為預防視網膜神經節細胞進一步損傷的選項加以考慮7)。
對側眼的管理:
APAC 後,對側眼若未進行預防性 LPI,約半數會在5年內發生急性發作 2)。原則上應盡快實施預防性 LPI,在等待期間開始使用縮瞳眼藥水(毛果芸香鹼)2)7)。長期使用毛果芸香鹼不適合做為慢性治療,因為它伴隨瞳孔散大不良、虹膜後粘連、白內障進展、視網膜剝離等風險,僅作為 LPI 實施前的過渡治療 2)。即使對側眼進行了預防性 LPI,仍有報告稱5-6年內可能發生 PACG,因此必須長期追蹤 2)。
慢性原發性閉角型青光眼的治療
Section titled “慢性原發性閉角型青光眼的治療”對於瞳孔阻滯解除後殘留的慢性眼壓升高(殘餘青光眼),採用類似於原發性開放角型青光眼的藥物治療、雷射治療和侵入性手術 1)。
- 藥物治療:首選前列腺素/前列腺素類似物 1)5)。根據需要加用β受體阻斷劑、α2受體激動劑、Rho激酶抑制劑和碳酸酐酶抑制劑。
- 水晶體摘除術:對解除瞳孔阻滯和開放隅角均有效,單獨使用也有降眼壓效果(建議等級1A)1)。但在廣泛 PAS(隅角≥50%)的病例中,降眼壓效果有限 1)10)。
- 隅角粘連分離術:適用於廣泛 PAS 的病例,與水晶體摘除聯合使用可同時預防再粘連和降低眼壓 1)。
- 小樑切開術:適用於小樑網開放的部分,也可用於 PAS 分離 1)。
- 小樑切除術:適用於藥物治療眼壓控制不佳、長期 PAS 或隅角觀察困難的病例。在窄隅角眼中,術後有前房消失、脈絡膜剝離、惡性青光眼等併發症的風險,因此需要嚴格管理 1)9)。歐洲青光眼學會指南第6版推薦將小樑切除術作為人工水晶體眼 PACG 的首選手術 5)。
- 微創青光眼手術(MIGS):閉角型眼睛曾為MIGS的禁忌症,但近年來由於與白內障超音波乳化術合併使用可確保進入隅角,其適應症已擴大。一項包含875例、23項研究的統合分析顯示,MIGS(合併或不合併超音波乳化術)術後1年眼壓平均降低7.71 mmHg(95%CI 5.16
10.26),青光眼用藥平均減少1.57種(95%CI 1.171.96)8)。內路小樑切開術(AIT)優於內視鏡睫狀體光凝術和iStent,超音波乳化合併MIGS比單純超音波乳化術的減藥效果更顯著8)。併發症發生率為16%,多為輕微的一過性前房積血8)。對於合併白內障的輕至中度原發性閉角型青光眼患者,超音波乳化合併MIGS可考慮作為轉向小樑切除術前的選擇8)。
高褶虹彩機制的治療
Section titled “高褶虹彩機制的治療”在高褶虹彩中,僅解除瞳孔阻滯可能無法控制眼壓1)14)。
- 毛果芸香鹼點眼液:可伸展周邊虹彩並開放隅角,但效果不確定,長期使用可能導致散瞳不良、虹彩後粘連及白內障進展1)。
- 雷射隅角成形術(LGP):使用Abraham透鏡,以氬雷射光斑大小500 μm、持續時間0.2~0.5秒、功率200 mW為標準,在周邊虹彩半周或全周每象限約15個光斑進行照射1)。合併瞳孔阻滯機制時,先進行雷射周邊虹彩切開術,再追加LGP1)。
- 水晶體摘除術:水晶體被置換為人工水晶體後,前房深度增加,且在閉角型眼中術後睫狀突進一步向後移動,使隅角進一步開放,因此被選為可靠的隅角開放手段1)6)14)。
- 追蹤觀察:長期有效性的數據有限,術後需繼續使用毛果芸香鹼點眼液,並透過超音波生物顯微鏡定期評估隅角1)14)。
- 水晶體摘除合併內視鏡睫狀體光凝術(ECP):小規模病例系列報告稱,該方法直接作用於睫狀突形態,可能改善眼壓控制2)。一項前瞻性比較試驗顯示,與單純超音波乳化術相比,術後眼壓無顯著差異,但前段光學同調斷層掃描測量顯示隅角開放更大2)。
- 患者教育:預先向患者說明雷射周邊虹膜切開術(LPI)並非高褶虹膜的根本解決方案,並告知即使術後仍有因散瞳刺激導致發作復發的風險1)14)。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”相對性瞳孔阻滯的惡性循環
Section titled “相對性瞳孔阻滯的惡性循環”大多數原發性隅角關閉疾病(PACD)以相對性瞳孔阻滯為基本機制1)2)。瞳孔區的虹膜-水晶體接觸導致房水從後房流向前房的阻力增加。當後房壓力相對升高時,虹膜向前膨隆,周邊部幾乎完全覆蓋小樑網,造成隅角功能性關閉。在急性發作時,水晶體前移和虹膜實質水腫進一步加重瞳孔阻滯,形成眼壓急劇升高的惡性循環1)2)。
瞳孔處於中度散大位置時,瞳孔阻滯最容易達到最大程度。這就是為什麼在暗處閱讀、夜間醒來、使用抗膽鹼能藥物以及低頭姿勢可能誘發發作的原因2)7)。
高褶虹膜與水晶體因素
Section titled “高褶虹膜與水晶體因素”在高褶虹膜中,睫狀體位置偏前,機械性地將虹膜根部向前推擠。中央前房深度相對保持,因此初看正常,但散瞳時周邊虹膜騎跨在睫狀突上直接關閉隅角1)14)。超音波生物顯微鏡(UBM)的特徵包括睫狀體前移、睫狀溝消失、虹膜根部厚且向前彎曲、隅角隱窩狹窄14)。
水晶體因素通過年齡相關的水晶體厚度增加和前移發揮作用。水晶體變厚時,虹膜-水晶體接觸面擴大,加強瞳孔阻滯1)10)。此外,水晶體越厚,前房越淺,進一步凸顯解剖學易感因素2)10)。這就是水晶體摘除術具有隅角開放效果的理論依據6)10)。
小樑網繼發性功能障礙與視神經病變
Section titled “小樑網繼發性功能障礙與視神經病變”長期或反覆的虹膜-小樑網接觸會導致小樑網本身發生不可逆的功能損害,進而形成周邊虹膜前粘連(PAS)1)2)。因此,即使解除了瞳孔阻滯,仍有相當比例的患者存在慢性眼壓升高,稱為殘餘性青光眼1)。根據亞太青光眼學會(APGS)共識,急性發作後即使LPI成功,仍有高達58%的病例可能進展為慢性原發性隅角關閉性青光眼(PACG)7)。目前提出了多種機制,包括小樑細胞的機械損傷、炎症介質的參與以及施萊姆管塌陷等,但完整的發病機制尚未完全闡明7)10)。
急性發作後的視網膜神經纖維層(RNFL)因發作後立即出現的軸突腫脹而暫時增厚,約1個月後恢復正常值,3個月後轉為變薄2)。這表明軸突腫脹和續發性變性在時間上是分離的,可透過OCT縱向評估進行追蹤。一項對未經治療的APAC病例進行4-10年長期追蹤的研究報告稱,18%的患者發展為法定失明,58%的患者視力低於20/402)。角膜內皮細胞密度也隨發作持續時間成比例下降,導致細胞形態的多形性(變異)和多極化(大小不一)2)。高眼壓和缺血的影響也波及睫狀體血流,房水生成本身可能暫時減少,有時會惡化藥物治療的反應性7)。
缺血-再灌流損傷與發作後神經節細胞損失
Section titled “缺血-再灌流損傷與發作後神經節細胞損失”急性發作時眼壓顯著升高會導致視神經盤和視網膜血流障礙,發作解除後的再灌流時產生氧化壓力和發炎性細胞激素7)。動物實驗和人體縱向研究表明,這種缺血-再灌流損傷導致眼壓降低後視網膜神經節細胞(RGC)的喪失仍會持續一段時間7)。這一發現強調了發作時「快速」降低眼壓的重要性,並為APGS推薦透過替代治療(ALPI、LPP、ACP)迅速降低眼壓提供了理論基礎7)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”ZAP試驗作為亞洲人群中的大規模隨機試驗,為PACS管理提供了基礎數據,並促使重新考慮預防性LPI的常規適應症3)。新加坡ANA-LIS試驗也支持這一點4)。同時,EAGLE試驗顯示了早期水晶體摘除術在PAC和PACG中的優越性,已被美國、歐洲和日本的主要指南採納1)2)5)6)。基於這些成果,2026年版的《原發性隅角閉鎖疾病優選實踐模式》明確將水晶體摘除術列為PAC和PACG的有力初始治療選擇2)。
急性發作治療的範式轉變
Section titled “急性發作治療的範式轉變”APGS/AAPPO 2025年共識提出,由於傳統藥物治療單獨使用起效慢,且在老年人和合併症患者中存在全身副作用風險,因此建議積極採用ALPI、LPP、ACP等替代技術快速降低眼壓,並在發作鎮靜後早期進行晶體乳化吸除術7)。這對於抑制發作後可能持續進展的RGC丟失(缺血-再灌注損傷)也具有重要意义7)。
圖像分析與AI篩查
Section titled “圖像分析與AI篩查”眼前段OCT的縱向分析報告顯示,晶體前拱高增加和房角寬度減少是3至6年後PACD進展的預測因素2)。未來,基於這些生物測量指標的個體風險評估有望指導LPI或晶體摘除術的適應症判斷。中國一項利用AI自動診斷和Markov模型的研究表明,對65歲以上人群進行群體篩查聯合AI可抑制PACG進展,但篩查費用的回收仍存在挑戰2)。
MIGS角色的擴展
Section titled “MIGS角色的擴展”MIGS最初在PACG中被視為禁忌,但隨著與白內障手術聯合使用以確保房角通路,它作為輕至中度PACG的微創選擇受到關注8)。薈萃分析顯示了AIT的優越性,但研究數量和追蹤期有限,需要進一步驗證長期療效和成本效益8)。與濾過手術相比,MIGS的濾過泡相關併發症和感染風險較低,可能對合併白內障的PACG手術選擇產生重大影響8)。
遺傳背景與未來預防
Section titled “遺傳背景與未來預防”近年來,全基因組關聯研究已鑑定出增加PACD風險的基因多態性(如PLEKHA7、COL11A1、PCMTD1-ST18等),促進了對解剖學易感性和個體化風險評估的理解2)。未來,可能針對家族史陽性或高風險種族人群建立結合遺傳信息和生物測量數據的篩查策略2)。
從患者指導的角度,對PACD風險人群進行急性發作症狀和及時就醫必要性的教育,提供避免使用具有瞳孔散大作用的非處方藥和處方藥的信息,並建議家屬(尤其是一等親)接受眼科檢查,對於長期視功能保護至關重要2)。
8. 參考文獻
Section titled “8. 參考文獻”-
日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
-
American Academy of Ophthalmology. Primary Angle-Closure Disease Preferred Practice Pattern®. San Francisco: American Academy of Ophthalmology; 2025.
-
He M, Jiang Y, Huang S, et al. Laser peripheral iridotomy for the prevention of angle closure: a single-centre, randomised controlled trial (Zhongshan Angle Closure Prevention Trial). Lancet. 2019;393(10181):1609-1618.
-
Baskaran M, Kumar RS, Friedman DS, et al. The Singapore Asymptomatic Narrow Angles Laser Iridotomy Study: Five-Year Results of a Randomized Controlled Trial. Ophthalmology. 2022;129(2):147-158.
-
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
-
Azuara-Blanco A, Burr J, Ramsay C, et al. Effectiveness of early lens extraction for the treatment of primary angle-closure glaucoma (EAGLE): a randomised controlled trial. Lancet. 2016;388(10052):1389-1397.
-
Chan PP, Zhang X, Aung T, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Asia Pac J Ophthalmol. 2025.
-
Paik B, Chua CH, Yip LW, Yip VCH. Outcomes and Complications of Minimally Invasive Glaucoma Surgeries (MIGS) in Primary Angle Closure and Primary Angle Closure Glaucoma: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2024;18:1573-1588.
-
Song BJ, Ramanathan M, Morales E, et al. Trabeculectomy and combined phacoemulsification-trabeculectomy: outcomes and risk factors for failure in primary angle closure glaucoma. J Glaucoma. 2016;25(9):763-769.
-
Tarongoy P, Ho CL, Walton DS. Angle-closure glaucoma: the role of the lens in the pathogenesis, prevention, and treatment. Surv Ophthalmol. 2009;54(2):211-225.
-
Quigley HA, Broman AT. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophthalmol. 2006;90(3):262-267.
-
Foster PJ, Buhrmann R, Quigley HA, Johnson GJ. The definition and classification of glaucoma in prevalence surveys. Br J Ophthalmol. 2002;86(2):238-242.
-
Yamamoto T, Iwase A, Araie M, et al. The Tajimi Study report 2: prevalence of primary angle closure and secondary glaucoma in a Japanese population. Ophthalmology. 2005;112(10):1661-1669.
-
Kumar RS, Baskaran M, Chew PT, et al. Prevalence of plateau iris in primary angle closure suspects: an ultrasound biomicroscopy study. Ophthalmology. 2008;115(3):430-434.
