非接觸型
特徵:目前臨床主流機型。無需表面麻醉,支援自動對位。
優點:患者負擔小,無感染風險,可短時間內重複測量。
限制:拍攝範圍較為有限。在角膜水腫或混濁嚴重時,難以進行準確拍攝。

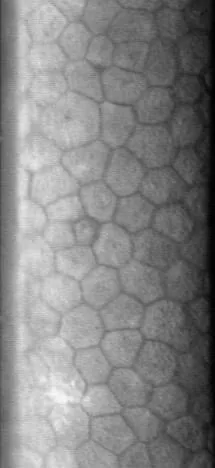
角膜內皮細胞檢查(鏡面顯微鏡)是利用鏡面反射原理拍攝和分析角膜內皮細胞的檢查。可以非侵入性地定量評估細胞密度、形態和大小不均。
角膜內皮細胞是角膜後表面的單層細胞,通過泵功能和屏障功能維持角膜透明性。然而,直接定量評估這些功能是困難的。因此,內皮功能的評估通常通過參數化形態異常的變化來進行。雖然裂隙燈顯微鏡的鏡面反射也可以定性評估內皮細胞,但使用鏡面顯微鏡可以實現形態參數的數值化。
主要適應症:
角膜內皮細胞通過泵功能和屏障功能維持角膜透明。角膜基質存在約50 mmHg的膨脹壓,但在正常眼中,內皮的泵功能克服這一壓力,從角膜中泵出多餘水分。內皮細胞幾乎沒有再生能力,因此受損後,剩餘細胞會擴大變扁以代償。但如果密度顯著下降,會發生代償不全,導致角膜水腫。
鏡面顯微鏡根據測量原理和接觸方式主要有三種類型。
非接觸型
特徵:目前臨床主流機型。無需表面麻醉,支援自動對位。
優點:患者負擔小,無感染風險,可短時間內重複測量。
限制:拍攝範圍較為有限。在角膜水腫或混濁嚴重時,難以進行準確拍攝。
接觸型
特點:將鏡頭直接接觸角膜進行拍攝的方式。需要點眼麻醉(0.4%奧布卡因)。
優點:比非接觸型能夠進行更廣範圍、更清晰的拍攝。即使在角膜水腫或混濁的情況下也能獲得可靠結果。據報導,在健康眼和移植後的角膜中,接觸型和非接觸型的細胞密度測量值大致相當[4]。
限制:需要點眼麻醉。需要熟練的操作技術。
共焦顯微鏡
特點:能夠對角膜各層進行斷層觀察的特殊設備。
優點:不僅可以評估內皮,還能立體評估上皮、基質及各層的細胞。也可用於觀察神經叢。
限制:與普通鏡面顯微鏡相比,操作更複雜,檢查時間更長。需要專用設備。
用於分析的細胞數過少會降低檢查的可靠性。Doughty等人報告,使用非接觸型鏡面顯微鏡測量時,分析25個細胞的變異係數約為±10%,而分析75個以上細胞時則收斂至約±2%[2]。Abib等人的分析也表明,雖然不同機型所需的樣本量不同,但均以數百個細胞為宜[3]。務必確認分析軟體自動識別的細胞數。
在角膜水腫或混濁的病例中,準確成像困難,分析結果的可靠性較低。此時應嘗試在透明度較高的部位重新拍攝。使用接觸型鏡面顯微鏡可以進行更廣範圍、更清晰的成像,因此很有用。
非接觸型無需點眼麻醉,雖然可能感到眩光,但基本無痛。接觸型則在使用0.4%奧布卡因點眼液進行表面麻醉後再接觸鏡頭,因此在麻醉有效期間不易感到疼痛。兩種檢查均在短時間內完成。
透過以下三個主要參數評估內皮細胞狀態。
| 參數 | 正常值 | 異常值參考 |
|---|---|---|
| 細胞密度(CD) | 70歲以上:平均2,200 cells/mm² | 400~500 cells/mm²以下 |
| CV值(變異係數) | 0.2~0.3 | 0.35以上 |
| 六角形細胞出現率(Hexagonality) | 60~70% | 50%以下 |
細胞密度是內皮評估的核心指標。多項研究顯示,隨著年齡增長,細胞密度會生理性下降[1][6],大致趨勢如下。
當細胞密度降至400~500 cells/mm²以下時,角膜無法維持透明性,導致水疱性角膜病變。
CV值是細胞面積的標準差除以平均細胞面積所得的值(變異係數),表示細胞大小不均。數值越高,表示細胞承受的壓力越大。正常值為0.2~0.3,0.35以上視為異常。
正常的角膜內皮細胞排列成規則的六角形。六角形細胞所佔比例越低,表示細胞型態越紊亂。正常值為60%~70%,50%以下視為異常。
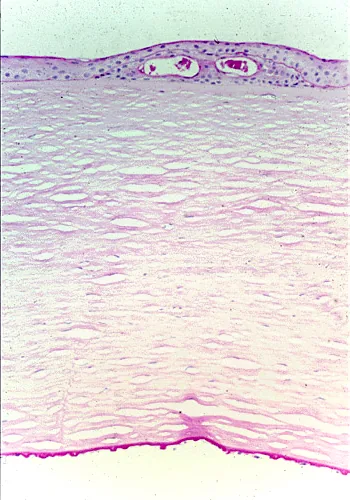
在Fuchs角膜內皮營養不良中,鏡面顯微鏡下可見以下特徵性表現:
根據檢查結果的異常情況,考慮以下處理措施。
CD < 1,000 cells/mm²(白內障手術前): 手術風險較高。應縮短超音波時間、選擇適當的黏彈性物質等調整術式,並向患者充分說明風險。由於各機構判斷標準不同,主治醫師的綜合判斷很重要。
CD < 400~500 cells/mm²: 水疱性角膜病變的風險迫在眉睫。應積極考慮角膜內皮移植術(DSAEK/DMEK)。與穿透性角膜移植術(PKP)相比,DSAEK/DMEK的內皮細胞存活率更高,視力恢復更快。
CV > 0.35 或六角形細胞比例 < 50%: 表示內皮壓力狀態。應查找原因,如Fuchs角膜內皮營養不良、ICE症候群、長期佩戴隱形眼鏡、眼內手術史等。
術後追蹤:
鏡面顯微鏡利用光的鏡面反射使內皮細胞可視化。當照明光照射到角膜基質與房水的界面(內皮細胞層)時,在折射率不同的介質邊界處部分光發生鏡面反射。通過接收該反射光獲得內皮細胞的影像。
細胞邊界(細胞間隙)處反射弱,呈暗線(dark line),而細胞體明亮。由此勾勒出細胞的輪廓。拍攝的細胞影像由影像分析軟體自動識別和量化,計算出CD、CV和六角形細胞比例。
角膜基質始終存在約50 mmHg的膨脹壓(swelling pressure: SP)。正常眼中,角膜內皮泵主動將Na⁺和HCO₃⁻輸送到房水側,克服該膨脹壓,使角膜保持生理厚度和透明性。
當內皮細胞密度降至500 cells/mm²以下時,剩餘內皮細胞的泵功能代償不足。超過角膜基質膨脹壓的水分流入,導致基質水腫並形成上皮下水疱(bulla)。這就是水疱性角膜病變(bullous keratopathy)。水疱破裂會引起劇烈疼痛,並喪失眼表屏障功能。
傳統的自動分析軟體在細胞密度低的區域或水腫病例中辨識精度存在挑戰。近年來,利用機器學習和深度學習的自動細胞邊界識別研究取得了進展。與手動分析的精度比較顯示出良好的相關性,未來有望在臨床中應用。
基礎研究表明,Rho相關激酶(ROCK)抑制劑可促進角膜內皮細胞的黏附和增殖。在日本,旨在促進角膜內皮細胞增殖的ROCK抑制劑眼藥水(Y-27632衍生物)的臨床開發正在進行中。在大皰性角膜病變和角膜內皮移植術後內皮密度恢復中的應用作為研究階段受到關注,但目前尚未在一般診療中廣泛應用。
長期佩戴隱形眼鏡(尤其是硬式鏡片)會導致慢性角膜缺氧,從而引起內皮細胞多形性增加(細胞大小不一)和多形核增加(非六邊形細胞形態增多)。表現為CV值升高和六角形細胞比例降低,但細胞密度本身通常保持在正常範圍內。
長期使用金剛烷胺(帕金森病藥物)和某些抗精神病藥物已被報導可引起角膜內皮損傷。通過鏡面顯微鏡可檢測到細胞密度降低和形態變化,因此正在研究對用藥患者進行定期監測的實用性。