非接触型
特征:目前临床主流机型。无需表面麻醉,支持自动对位。
优点:患者负担小,无感染风险,可短时间内重复测量。
局限性:拍摄范围较为有限。在角膜水肿或混浊严重时,难以进行准确拍摄。

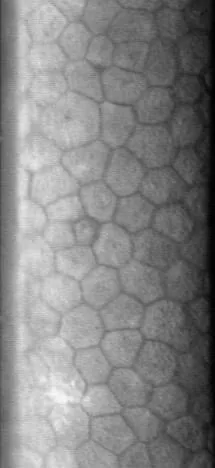
角膜内皮细胞检查(镜面显微镜)是利用镜面反射原理拍摄和分析角膜内皮细胞的检查。可以非侵入性地定量评估细胞密度、形态和大小不均。
角膜内皮细胞是角膜后表面的单层细胞,通过泵功能和屏障功能维持角膜透明性。然而,直接定量评估这些功能是困难的。因此,内皮功能的评估通常通过参数化形态异常的变化来进行。虽然裂隙灯显微镜的镜面反射也可以定性评估内皮细胞,但使用镜面显微镜可以实现形态参数的数值化。
主要适应症:
角膜内皮细胞通过泵功能和屏障功能维持角膜透明。角膜基质存在约50 mmHg的膨胀压,但在正常眼中,内皮的泵功能克服这一压力,从角膜中泵出多余水分。内皮细胞几乎没有再生能力,因此受损后,剩余细胞会扩大变扁以代偿。但如果密度显著下降,会发生代偿不全,导致角膜水肿。
镜面显微镜根据测量原理和接触方式主要有三种类型。
非接触型
特征:目前临床主流机型。无需表面麻醉,支持自动对位。
优点:患者负担小,无感染风险,可短时间内重复测量。
局限性:拍摄范围较为有限。在角膜水肿或混浊严重时,难以进行准确拍摄。
接触型
特点:将镜头直接接触角膜进行拍摄的方式。需要滴眼麻醉(0.4%奥布卡因)。
优点:比非接触型能够进行更广范围、更清晰的拍摄。即使在角膜水肿或混浊的情况下也能获得可靠结果。据报道,在健康眼和移植后的角膜中,接触型和非接触型的细胞密度测量值大致相当[4]。
局限性:需要滴眼麻醉。需要熟练的操作技术。
共聚焦显微镜
特点:能够对角膜各层进行断层观察的特殊设备。
优点:不仅可以评估内皮,还能立体评估上皮、基质及各层的细胞。也可用于观察神经丛。
局限性:与普通镜面显微镜相比,操作更复杂,检查时间更长。需要专用设备。
用于分析的细胞数过少会降低检查的可靠性。Doughty等人报告,使用非接触型镜面显微镜测量时,分析25个细胞的变异系数约为±10%,而分析75个以上细胞时则收敛至约±2%[2]。Abib等人的分析也表明,虽然不同机型所需的样本量不同,但均以数百个细胞为宜[3]。务必确认分析软件自动识别的细胞数。
在角膜水肿或混浊的病例中,准确成像困难,分析结果的可靠性较低。此时应尝试在透明度较高的部位重新拍摄。使用接触型镜面显微镜可以进行更广范围、更清晰的成像,因此很有用。
非接触型无需滴眼麻醉,虽然可能感到眩光,但基本无痛。接触型则在使用0.4%奥布卡因滴眼液进行表面麻醉后再接触镜头,因此在麻醉有效期间不易感到疼痛。两种检查均在短时间内完成。
通过以下三个主要参数评估内皮细胞状态。
| 参数 | 正常值 | 异常值参考 |
|---|---|---|
| 细胞密度(CD) | 70岁以上:平均2,200 cells/mm² | 400~500 cells/mm²以下 |
| CV值(变异系数) | 0.2~0.3 | 0.35以上 |
| 六角形细胞出现率(Hexagonality) | 60~70% | 50%以下 |
细胞密度是内皮评估的核心指标。多项研究表明,随着年龄增长,细胞密度会生理性下降[1][6],大致趋势如下。
当细胞密度降至400~500 cells/mm²以下时,角膜无法维持透明性,导致大疱性角膜病变。
CV值是细胞面积的标准差除以平均细胞面积得到的值(变异系数),表示细胞大小不均。数值越高,表明细胞承受的压力越大。正常值为0.2~0.3,0.35以上视为异常。
正常的角膜内皮细胞排列成规则的六角形。六角形细胞所占比例越低,表明细胞形态紊乱越严重。正常值为60%~70%,50%以下视为异常。
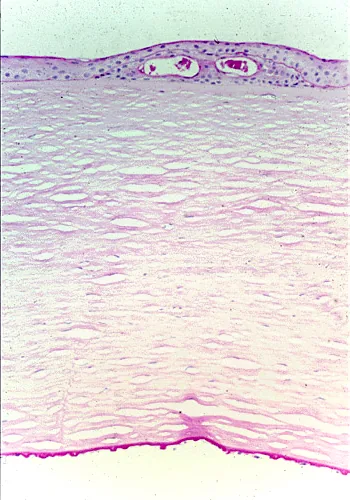
在Fuchs角膜内皮营养不良中,镜面显微镜下可见以下特征性表现:
根据检查结果的异常情况,考虑以下处理措施。
CD < 1,000 cells/mm²(白内障术前): 手术风险较高。应缩短超声时间、选择合适的粘弹剂等调整手术方式,并向患者充分说明风险。由于各机构的判断标准不同,主治医生的综合判断很重要。
CD < 400~500 cells/mm²: 大疱性角膜病变的风险迫在眉睫。应积极考虑角膜内皮移植术(DSAEK/DMEK)。与穿透性角膜移植术(PKP)相比,DSAEK/DMEK的内皮细胞存活率更高,视力恢复更快。
CV > 0.35 或六角形细胞比例 < 50%: 提示内皮应激状态。应查找原因,如Fuchs角膜内皮营养不良、ICE综合征、长期佩戴隐形眼镜、眼内手术史等。
术后随访:
镜面显微镜利用光的镜面反射使内皮细胞可视化。当照明光照射到角膜基质与房水的界面(内皮细胞层)时,在折射率不同的介质边界处部分光发生镜面反射。通过接收该反射光获得内皮细胞的图像。
细胞边界(细胞间隙)处反射弱,呈暗线(dark line),而细胞体明亮。由此勾勒出细胞的轮廓。拍摄的细胞图像由图像分析软件自动识别和量化,计算出CD、CV和六角形细胞比例。
角膜基质始终存在约50 mmHg的膨胀压(swelling pressure: SP)。正常眼中,角膜内皮泵主动将Na⁺和HCO₃⁻输送到房水侧,克服该膨胀压,使角膜保持生理厚度和透明性。
当内皮细胞密度降至500 cells/mm²以下时,剩余内皮细胞的泵功能代偿不足。超过角膜基质膨胀压的水分流入,导致基质水肿并形成上皮下水疱(bulla)。这就是大疱性角膜病变(bullous keratopathy)。水疱破裂会引起剧烈疼痛,并丧失眼表屏障功能。
传统的自动分析软件在细胞密度低的区域或水肿病例中识别精度存在挑战。近年来,利用机器学习和深度学习的自动细胞边界识别研究取得了进展。与手动分析的精度比较显示出良好的相关性,未来有望在临床中应用。
基础研究表明,Rho相关激酶(ROCK)抑制剂可促进角膜内皮细胞的黏附和增殖。在日本,旨在促进角膜内皮细胞增殖的ROCK抑制剂滴眼液(Y-27632衍生物)的临床开发正在进行中。在大疱性角膜病变和角膜内皮移植术后内皮密度恢复中的应用作为研究阶段受到关注,但目前尚未在一般诊疗中广泛应用。
长期佩戴隐形眼镜(尤其是硬性镜片)会导致慢性角膜缺氧,从而引起内皮细胞多形性增加(细胞大小不一)和多形核增加(非六边形细胞形态增多)。表现为CV值升高和六角形细胞比例降低,但细胞密度本身通常保持在正常范围内。
长期使用金刚烷胺(帕金森病药物)和某些抗精神病药物已被报道可引起角膜内皮损伤。通过镜面显微镜可检测到细胞密度降低和形态变化,因此正在研究对用药患者进行定期监测的实用性。