비접촉형

각막내피세포검사 (스페큘러 현미경)
1. 각막 내피 세포 검사란?
섹션 제목: “1. 각막 내피 세포 검사란?”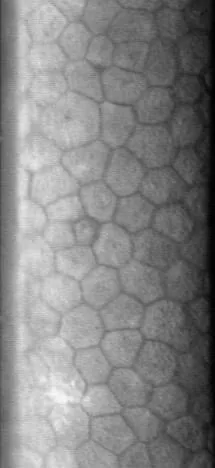
각막 내피 세포 검사(스페큘러 현미경)는 경면 반사법의 원리를 이용하여 각막 내피 세포를 촬영·분석하는 검사입니다. 세포 밀도, 형태, 크기 변이를 비침습적으로 정량 평가할 수 있습니다.
각막 내피 세포는 각막 후면의 단층 세포로, 펌프 기능과 장벽 기능을 통해 각막의 투명성을 유지합니다. 그러나 이러한 기능을 직접 정량 평가하는 것은 어렵습니다. 따라서 내피 기능 평가는 형태 이상의 변화를 파라미터화하여 수행하는 것이 일반적입니다. 세극등 현미경의 경면 반사로도 내피 세포의 정성적 평가는 가능하지만, 스페큘러 현미경을 사용하면 형태 파라미터의 수치화가 실현됩니다.
주요 적응증:
- 백내장 수술 전: 내피 세포 밀도 평가(보험 적용). 수술 방식 선택 및 환자 설명의 근거가 됩니다.
- 각막 내피 이식술(DSAEK/DMEK) 전후: 수술 전 평가와 수술 후 내피 밀도의 경시적 모니터링.
- Fuchs 각막 내피 이영양증 및 ICE 증후군: 구타타(guttata) 검출 및 밀도 감소의 정기 모니터링.
- 장기 콘택트렌즈 착용자: 만성적 산소 결핍에 의한 내피 변화 평가.
각막 내피 세포는 펌프 기능과 장벽 기능을 통해 각막을 투명하게 유지합니다. 각막 실질에는 약 50 mmHg의 팽윤압이 존재하지만, 정상안에서는 내피의 펌프 기능이 이를 극복하여 각막에서 과잉 수분을 제거합니다. 내피 세포는 재생 능력이 거의 없으므로 손상을 받으면 잔존 세포가 확대·편평화되어 보충하지만, 밀도가 현저히 감소하면 보상 부전이 되어 각막 부종이 발생합니다.
2. 장치의 종류와 특징
섹션 제목: “2. 장치의 종류와 특징”스페큘러 현미경에는 측정 원리·접촉 방식의 차이에 따라 주로 3종류가 있습니다.
접촉형
공초점 현미경
특징: 각막의 각 층을 단층적으로 관찰할 수 있는 특수 장비입니다.
장점: 내피뿐만 아니라 상피, 실질 및 각 층의 세포를 입체적으로 평가할 수 있습니다. 신경총 관찰에도 사용됩니다.
한계: 일반 스페큘러 현미경에 비해 조작이 복잡하고 검사 시간이 깁니다. 전용 장비가 필요합니다.
3. 검사 기술 및 주의사항
섹션 제목: “3. 검사 기술 및 주의사항”검사 절차
섹션 제목: “검사 절차”- 비접촉형의 경우: 점안 마취가 필요하지 않습니다. 턱받이와 이마받이에 머리를 고정하고, 주시등을 정면으로 주시하게 합니다. 자동 정렬로 자동 촬영합니다.
- 접촉형의 경우: 0.4% 옥시부프로카인 염산염 점안액으로 점안 마취를 시행합니다. 검사자가 렌즈를 각막에 접촉시켜 촬영합니다.
- 자동 분석: 촬영 후 장비가 자동으로 세포 밀도(CD), 변이 계수(CV), 육각형 세포 출현율(Hexagonality)을 출력합니다.
- 수동 수정: 자동 분석의 정확도가 낮은 경우, 수동 분석으로 경계를 수정하여 재계산합니다.
- CCT 동시 측정: 많은 기종에서 중심각막두께(CCT) 동시 측정을 지원합니다.
검사 신뢰성 확보
섹션 제목: “검사 신뢰성 확보”분석에 사용되는 세포 수가 너무 적으면 검사의 신뢰도가 떨어집니다. Doughty 등은 비접촉형 경면현미경 측정에서 분석 세포 수 25개일 때 변동계수가 약 ±10%인 반면, 75개 이상이면 약 ±2%로 수렴한다고 보고했습니다[2]. Abib 등의 분석에서도 기종별로 필요한 표본 크기는 다르지만, 모두 수백 개 수준의 세포 수가 바람직하다고 합니다[3]. 분석 소프트웨어가 자동 인식한 세포 수를 반드시 확인하십시오.
각막 부종이나 혼탁이 있는 경우 정확한 촬영이 어렵고 분석 결과의 신뢰성이 낮아집니다. 그런 경우 투명도가 높은 부위에서 다시 촬영을 시도하십시오. 접촉형을 사용하면 더 넓은 범위와 선명한 촬영이 가능하므로 유용합니다.
4. 결과 해석과 정상치
섹션 제목: “4. 결과 해석과 정상치”측정 파라미터와 정상·비정상치
섹션 제목: “측정 파라미터와 정상·비정상치”다음 세 가지 주요 파라미터로 내피 세포 상태를 평가합니다.
| 파라미터 | 정상치 | 비정상치 기준 |
|---|---|---|
| 세포 밀도 (CD) | 70세 이상: 평균 2,200 cells/mm² | 400~500 cells/mm² 이하 |
| CV값(변동계수) | 0.2~0.3 | 0.35 이상 |
| 육각형 세포 출현율(Hexagonality) | 60~70% | 50% 이하 |
세포 밀도(CD: Cell Density)
섹션 제목: “세포 밀도(CD: Cell Density)”세포 밀도는 내피 평가의 핵심 지표입니다. 여러 연구에서 연령에 따라 생리적으로 감소하는 것으로 나타났으며[1][6], 대략 다음과 같은 추이를 보입니다.
- 신생아: 3,500~4,000 cells/mm²
- 20대: 약 2,700 cells/mm²
- 70세 이상: 평균 2,200 cells/mm²
- 정상 연간 감소율: 0.5%/년
- 백내장 수술 후: 2%/년 (가속 감소)
- 녹내장 수술 후: 10%/년 (더욱 가속)
세포 밀도가 400~500 cells/mm² 이하로 감소하면 각막 투명성 유지가 불가능해져 수포성 각막병증이 발생합니다.
CV값 (변동계수)
섹션 제목: “CV값 (변동계수)”CV값은 세포 면적의 표준편차를 평균 세포 면적으로 나눈 값(변동계수)으로, 세포 크기의 부동(anisocytosis)을 나타냅니다. 증가할수록 세포 스트레스가 가해지고 있음을 의미합니다. 정상 범위는 0.2~0.3이며, 0.35 이상이면 이상으로 간주합니다.
육각형 세포 출현율 (Hexagonality)
섹션 제목: “육각형 세포 출현율 (Hexagonality)”정상 각막 내피 세포는 규칙적인 육각형으로 배열되어 있습니다. 이 육각형 세포가 차지하는 비율이 낮을수록 세포 형태의 혼란이 크다는 것을 나타냅니다. 정상 범위는 60~70%이며, 50% 이하가 이상 기준입니다.
Fuchs 각막 내피 이영양증의 스페큘러 소견
섹션 제목: “Fuchs 각막 내피 이영양증의 스페큘러 소견”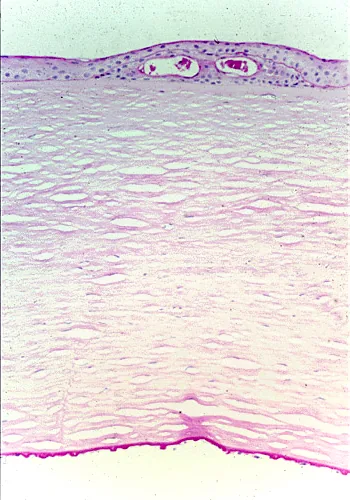
Fuchs 각막 내피 이영양증에서는 스페큘러 현미경으로 다음과 같은 특징적인 소견이 관찰됩니다.
- guttata (점적 각막) : 내피의 융기부(Descemet의 사마귀 모양 비후)가 검은색 원형 영역(dark area)으로 인식됩니다.
- 세포 밀도 감소 : guttata가 차지하는 면적만큼 내피 세포 밀도가 겉보기에 낮게 측정됩니다.
- CV값 증가 및 육각형 출현율 감소 : 내피 세포가 변형·확대되어 주변을 보충하므로 형태 지수도 악화됩니다.
5. 검사 소견에 대한 대응
섹션 제목: “5. 검사 소견에 대한 대응”검사치의 이상에 따라 다음과 같은 대응을 고려합니다.
CD < 1,000 cells/mm² (백내장 수술 전): 수술 위험이 높은 상태입니다. 초음파 시간 단축, 점탄성 물질 선택 등 수술 방식을 조정하고 환자에게 위험을 충분히 설명합니다. 기관마다 판단 기준이 다르므로 담당 의사의 종합적인 판단이 중요합니다.
CD < 400~500 cells/mm²: 수포성 각막병증의 위험이 임박했습니다. 각막내피이식술(DSAEK/DMEK)의 적응을 적극적으로 고려합니다. 전층각막이식(PKP)과 비교하여 DSAEK/DMEK는 내피세포 생착률이 높고 시력 회복이 빠릅니다.
CV > 0.35 또는 육각형 세포 비율 < 50%: 내피 스트레스 상태를 나타냅니다. Fuchs 각막내피이영양증, ICE 증후군, 장기간 콘택트렌즈 착용, 안내 수술 병력 등의 원인을 검색합니다.
수술 후 추적 관찰:
- 백내장 수술 후 1~3개월, 1년 후에 내피 밀도를 확인합니다. 내피세포 감소는 수술 후 1년까지 가장 크며, 이후 수년간 서서히 진행되는 것으로 보고되었습니다. 수술 전 내피 밀도, 연령, 초음파 사용 시간이 독립적 위험 인자로 확인되었습니다[5].
- 각막내피이식(DSAEK/DMEK) 후 6개월~1년마다 내피 밀도 모니터링을 지속합니다.
6. 측정 원리의 상세
섹션 제목: “6. 측정 원리의 상세”경면 반사법의 원리
섹션 제목: “경면 반사법의 원리”경면 현미경은 빛의 경면 반사를 이용하여 내피 세포를 가시화합니다. 각막 실질에서 방수로의 경계(내피 세포층)에 조명광을 비추면 굴절률이 다른 매질의 경계에서 일부 빛이 경면 반사합니다. 이 반사광을 수광하여 내피 세포의 상을 얻습니다.
세포 경계부(세포 간극)에서는 반사가 약해 어둡게 보이고(dark line), 세포체는 밝게 보입니다. 이로 인해 세포의 윤곽이 드러납니다. 촬영된 세포상을 이미지 분석 소프트웨어가 자동 인식 및 정량화하여 CD, CV, 육각형 세포 비율이 산출됩니다.
수포성 각막병증의 병태
섹션 제목: “수포성 각막병증의 병태”각막 실질에는 항상 약 50 mmHg의 팽윤압(swelling pressure: SP)이 존재합니다. 정상안에서는 각막 내피 펌프가 활발하게 Na⁺와 HCO₃⁻를 방수 쪽으로 수송하여 이 팽윤압을 이겨내 각막을 생리적 두께로 유지하고 투명성을 유지합니다.
내피 세포 밀도가 500 cells/mm² 이하로 감소하면 잔존 내피 세포에 의한 펌프 기능이 대체 부전이 됩니다. 각막 실질의 팽윤압을 초과하는 수분이 유입되어 실질 부종에서 상피하 수포(bulla) 형성에 이릅니다. 이것이 수포성 각막병증(bullous keratopathy)입니다. 수포가 파열되면 심한 통증을 일으키고 안구 표면의 장벽 기능도 상실됩니다.
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”AI 자동 세포 분석
섹션 제목: “AI 자동 세포 분석”기존의 자동 분석 소프트웨어는 특히 세포 밀도가 낮은 영역이나 부종 사례에서 인식 정확도에 문제가 있었습니다. 최근 기계 학습 및 딥러닝을 이용한 자동 세포 경계 인식 연구가 진행되고 있습니다. 수동 분석과의 정확도 비교에서도 좋은 상관관계가 보고되어 향후 임상 적용이 기대됩니다.
ROCK 억제제를 통한 내피 재생
섹션 제목: “ROCK 억제제를 통한 내피 재생”Rho 관련 키나제(ROCK) 억제제는 각막 내피 세포의 부착 및 증식을 촉진하는 것이 기초 연구에서 입증되었습니다. 일본에서는 각막 내피 세포 증식 촉진을 목적으로 한 ROCK 억제제 점안액(Y-27632 유도체)의 임상 개발이 진행 중입니다. 수포성 각막증 및 각막 내피 이식 후 내피 밀도 회복에의 응용이 연구 단계로서 주목받고 있지만, 현재 일반 진료에서 널리 적용되지는 않았습니다.
장기 콘택트렌즈 착용자의 내피 변화
섹션 제목: “장기 콘택트렌즈 착용자의 내피 변화”장기 콘택트렌즈 착용(특히 하드렌즈)에서는 만성적인 각막 산소 결핍으로 인해 내피의 다형성 증가(polymegethism: 세포 크기 다양성 증가) 및 다형핵 증가(pleomorphism: 육각형 이외의 세포 형태 증가)가 발생하는 것으로 보고되었습니다. CV 값 상승 및 육각형 비율 감소로 나타나지만, 세포 밀도 자체는 정상 범위에 머무는 경우가 많습니다.
약물 유발 각막 내피 손상
섹션 제목: “약물 유발 각막 내피 손상”아만타딘(파킨슨병 약물) 및 일부 항정신병 약물의 장기 사용으로 각막 내피 손상이 보고되었습니다. 경면현미경으로 세포 밀도 감소 및 형태 변화를 검출할 수 있는 경우가 있으며, 약물 투여 환자에 대한 정기적인 모니터링의 유용성이 검토되고 있습니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Sanchis-Gimeno JA, Lleó-Pérez A, Alonso L, Rahhal MS, Martínez Soriano F. Corneal endothelial cell density decreases with age in emmetropic eyes. Histol Histopathol. 2005;20(2):423-427. PMID: 15736046. https://pubmed.ncbi.nlm.nih.gov/15736046/
- Doughty MJ, Müller A, Zaman ML. Assessment of the reliability of human corneal endothelial cell-density estimates using a noncontact specular microscope. Cornea. 2000;19(2):148-158. PMID: 10746445. https://pubmed.ncbi.nlm.nih.gov/10746445/
- Abib FC, Holzchuh R, Schaefer A, Schaefer T, Godois R. The endothelial sample size analysis in corneal specular microscopy clinical examinations. Cornea. 2012;31(5):546-550. PMID: 22333658. https://pubmed.ncbi.nlm.nih.gov/22333658/
- Módis L Jr, Langenbucher A, Seitz B. Corneal endothelial cell density and pachymetry measured by contact and noncontact specular microscopy. J Cataract Refract Surg. 2002;28(10):1763-1769. PMID: 12388025. https://pubmed.ncbi.nlm.nih.gov/12388025/
- Lee NS, Ong K. Risk factors for corneal endothelial cell loss after phacoemulsification. Taiwan J Ophthalmol. 2024;14(1):83-87. PMID: 38654985; PMCID: PMC11034697. https://pmc.ncbi.nlm.nih.gov/articles/PMC11034697/
- Kaur K, Gurnani B. Specular Microscopy. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024. Bookshelf ID: NBK585127. https://www.ncbi.nlm.nih.gov/books/NBK585127/
