非接触型
特徴:現在の臨床で主流の機種。点眼麻酔不要でオートアライメントに対応する。
利点:患者負担が少なく、感染リスクがない。短時間で繰り返し測定できる。
限界:撮影範囲がやや限定的。角膜浮腫・混濁が高度な場合は正確な撮影が困難となる。

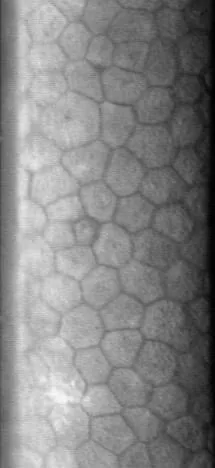
角膜内皮細胞検査(スペキュラーマイクロスコープ)は、鏡面反射法の原理を用いて角膜内皮細胞を撮影・解析する検査である。細胞密度・形態・大小不同を非侵襲的に定量評価できる。
角膜内皮細胞は角膜後面の単層細胞であり、ポンプ機能とバリア機能によって角膜の透明性を維持する。しかし、これらの機能を直接定量評価することは困難である。そのため内皮機能の評価には、形態異常の変化をパラメータ化して行うのが一般的である。細隙灯顕微鏡による鏡面反射でも内皮細胞の定性的評価は可能であるが、スペキュラーマイクロスコープを用いることで形態パラメータの数値化が実現する。
主な適応:
角膜内皮細胞はポンプ機能とバリア機能によって角膜を透明に保つ。角膜実質には約50 mmHgの膨潤圧が存在するが、正常眼では内皮のポンプ機能がこれに打ち勝って角膜から過剰な水分を汲み出す。内皮細胞は再生能がほぼないため、傷害を受けると残存細胞が拡大・扁平化して補填するが、密度が著しく低下すると代償不全となり角膜浮腫が生じる。
スペキュラーマイクロスコープには測定原理・接触様式の違いにより主に3種類がある。
非接触型
特徴:現在の臨床で主流の機種。点眼麻酔不要でオートアライメントに対応する。
利点:患者負担が少なく、感染リスクがない。短時間で繰り返し測定できる。
限界:撮影範囲がやや限定的。角膜浮腫・混濁が高度な場合は正確な撮影が困難となる。
接触型
特徴:レンズを直接角膜に接触させて撮影する方式。点眼麻酔(0.4%オキシブプロカイン)が必要。
利点:非接触型より広範囲かつ鮮明な撮影が可能。角膜浮腫・混濁例でも信頼性の高い結果が得られる。健常眼および移植後の角膜では接触型と非接触型の細胞密度測定値はおおむね同等と報告されている[4]。
限界:点眼麻酔が必要。熟練した手技が求められる。
共焦点顕微鏡
特徴:角膜の各層を断層的に観察できる特殊装置。
利点:内皮のみでなく上皮・実質・各層の細胞を立体的に評価できる。神経叢の観察にも対応する。
限界:通常のスペキュラーに比べ操作が複雑で検査時間が長い。専用機が必要。
解析に用いる細胞数が少なすぎると検査の信頼度は低下する。Doughtyらは非接触型スペキュラーマイクロスコープでの測定で、解析細胞数25個では変動係数が±10%程度であるのに対し、75個以上であれば±2%程度に収束すると報告している[2]。Abibらの解析でも、機種ごとに必要なサンプルサイズは異なるが、いずれも数百個オーダーの細胞数が望ましいとされる[3]。解析ソフトが自動認識した細胞数を必ず確認する。
角膜浮腫や混濁がある症例では正確な撮影が困難であり、解析結果の信頼性が低くなることに注意する。その場合は透明性の高い部位で撮影を再度試みる。接触型を用いると、より広範囲かつ鮮明な撮影が可能なため有用である。
非接触型では点眼麻酔が不要であり、まぶしさを感じることはあっても基本的に痛みはない。接触型では0.4%オキシブプロカイン点眼液による点眼麻酔を行ってからレンズを接触させるため、麻酔が効いている間は痛みを感じにくい。いずれも短時間で終了する検査である。
以下の3つの主要パラメータで内皮細胞の状態を評価する。
| パラメータ | 正常値 | 異常値の目安 |
|---|---|---|
| 細胞密度(CD) | 70歳以上 平均2,200 cells/mm² | 400〜500 cells/mm²以下 |
| CV値(変動係数) | 0.2〜0.3 | 0.35以上 |
| 六角形細胞出現率(Hexagonality) | 60〜70% | 50%以下 |
細胞密度は内皮評価の中心となる指標である。年齢とともに生理的に減少することが複数の研究で示されており[1][6]、おおよそ以下の推移をたどる。
400〜500 cells/mm²以下に減少すると角膜の透明性維持が不可能となり、水疱性角膜症を生じる。
CV値は細胞面積の標準偏差を平均細胞面積で除した値(変動係数)であり、細胞の大小不同を示す。増加するほど細胞ストレスがかかっていることを意味する。正常値は0.2〜0.3であり、0.35以上が異常の目安となる。
正常の角膜内皮細胞は規則正しい六角形に整列している。この六角形細胞の占める割合が低下するほど細胞形態の乱れが大きいことを示す。正常値は60〜70%であり、50%以下が異常値の目安である。
Fuchs角膜内皮ジストロフィでは、スペキュラーマイクロスコープで以下の特徴的な所見が観察される。
検査値の異常に応じて以下の対応を検討する。
CD < 1,000 cells/mm²(白内障手術前): 手術リスクが高い状態である。超音波時間の短縮・粘弾性物質の選択など術式を工夫し、患者へリスクを十分に説明する。施設によって判断基準は異なるため担当医の総合的な判断が重要である。
CD < 400〜500 cells/mm²: 水疱性角膜症のリスクが切迫している。角膜内皮移植術(DSAEK/DMEK)の適応を積極的に検討する。角膜全層移植(PKP)と比較してDSAEK/DMEKは内皮細胞の生着率が高く視力回復が早い。
CV値 > 0.35 または Hexagonality < 50%: 内皮ストレス状態を示す。Fuchs角膜内皮ジストロフィ・ICE症候群・コンタクトレンズ長期装用・眼内手術歴などの原因を検索する。
術後フォローアップ:
スペキュラーマイクロスコープは光の鏡面反射を利用して内皮細胞を可視化する。角膜実質から房水への界面(内皮細胞層)に照明光を当てると、屈折率の異なる媒体の境界で一部の光が鏡面反射する。この反射光を受光することで内皮細胞の像を得る。
細胞境界部(細胞間隙)では反射が弱く暗く見え(dark line)、細胞体は明るく見える。これにより細胞の輪郭が浮かび上がる。撮影した細胞像を画像解析ソフトウェアが自動認識・定量化することで、CD・CV・Hexagonalityが算出される。
角膜実質には常に約50 mmHgの膨潤圧(swelling pressure: SP)が存在する。正常眼では角膜内皮ポンプが活発にNa⁺とHCO₃⁻を房水側へ輸送し、この膨潤圧に打ち勝つことで角膜を生理的な厚さに保ち透明性を維持している。
内皮細胞密度が500 cells/mm²以下まで低下すると、残存内皮細胞によるポンプ機能が代償不全となる。角膜実質の膨潤圧を上回る水分が流入し、実質浮腫から上皮下水疱(bulla)の形成に至る。これが水疱性角膜症(bullous keratopathy)である。水疱が破裂すると激しい疼痛を生じ、眼表面のバリア機能も失われる。
従来の自動解析ソフトウェアは特に細胞密度が低い領域や浮腫例での認識精度に課題があった。近年、機械学習・深層学習を用いた自動細胞境界認識の研究が進んでいる。手動解析との精度比較においても良好な相関が報告されており、今後の臨床実装が期待される。
Rho関連キナーゼ(ROCK)阻害薬は角膜内皮細胞の接着・増殖を促進することが基礎研究で示されている。日本では角膜内皮細胞増殖促進を目的としたROCK阻害薬点眼液(Y-27632誘導体)の臨床開発が進んでいる。水疱性角膜症や角膜内皮移植後の内皮密度回復への応用が研究段階として注目されているが、現時点では一般診療での広い適用には至っていない。
長期コンタクトレンズ装用(特にハードレンズ)では、慢性的な角膜酸素欠乏によって内皮の多形性増加(polymegethism:細胞の大小不同増加)および多形核増加(pleomorphism:六角形以外の細胞形態増加)が生じることが報告されている。CV値の上昇・Hexagonality低下として現れるが、細胞密度自体は正常範囲に留まる場合が多い。
アマンタジン(パーキンソン病薬)や一部の抗精神病薬の長期使用で角膜内皮障害が報告されている。スペキュラーマイクロスコープで細胞密度低下・形態変化として検出できる場合があり、薬剤投与患者への定期的なモニタリングの有用性が検討されている。