進行性虹彩萎縮
瞳孔偏位:PASが多い方向に瞳孔が牽引される。
虹彩孔形成:瞳孔が牽引された逆方向に多発する。
ぶどう膜外反:虹彩色素上皮が表面に露出する。
PAS:Schwalbe線を越えて高く伸びる丈の高いPASが特徴的。
緑内障合併:3型のうち最も高頻度。

ICE症候群(虹彩角膜内皮症候群; iridocorneal endothelial syndrome)は、異常な角膜内皮細胞が膜様組織を伴って隅角および虹彩に伸展し、線維柱帯が閉塞されて眼圧上昇をきたす疾患である。角膜内皮の異常によって角膜浮腫をきたし、膜様組織の収縮により虹彩異常および周辺虹彩前癒着(PAS)を呈する。
30〜40歳代の女性に片眼性に好発する2)。遺伝性はなく、散発性である。家族歴を認めることはまれであり、他の眼疾患や全身疾患との一貫した関連はない。
ICE症候群は虹彩異常の状態によって以下の3つの臨床型に分類される。
ICE症候群は片眼性で散発的である点が、両眼性で常染色体優性遺伝の後部多形性角膜ジストロフィ(PPMD)やAxenfeld-Rieger症候群との最も簡便な鑑別点となる。
3型の区別は主に虹彩と角膜の臨床所見に基づく。進行性虹彩萎縮は多瞳孔症・瞳孔偏位・虹彩孔形成・ぶどう膜外反が顕著で、緑内障合併が最も多い。Chandler症候群は角膜浮腫が主体で虹彩変化は軽微であり、虹彩孔は認めずPASの丈も低い。Cogan-Reese症候群は虹彩前面の有茎性結節または平坦な色素病巣が特徴であり、虹彩萎縮は通常みられない。いずれの型も基本的な病態生理は共通であり、治療方針も同様である。
片眼性の視力低下(角膜浮腫による霧視)が最も多い初発症状である。羞明や疼痛を自覚することがある。瞳孔の偏位・虹彩異色など外見的な異常に気づいて受診する場合もある。角膜浮腫による疼痛と、隅角閉鎖による眼圧上昇に伴う痛みが混在する。
角膜所見:Chandler症候群では角膜内皮に金属様光沢を呈する「hammered silver appearance(打ち出しの銀様外観)」を認める。フックス角膜内皮ジストロフィの角膜滴状粉に類似するが、片眼性であることで鑑別可能である。角膜浮腫は眼圧が正常範囲であっても出現しうる。Descemet膜のひだ形成がみられることもある。
虹彩所見:型に応じて以下の所見が出現する2)。
進行性虹彩萎縮
瞳孔偏位:PASが多い方向に瞳孔が牽引される。
虹彩孔形成:瞳孔が牽引された逆方向に多発する。
ぶどう膜外反:虹彩色素上皮が表面に露出する。
PAS:Schwalbe線を越えて高く伸びる丈の高いPASが特徴的。
緑内障合併:3型のうち最も高頻度。
Chandler症候群
角膜浮腫:眼圧軽度上昇でも生じやすく、3型のうち最も顕著。
虹彩所見:瞳孔偏位・虹彩萎縮は軽度。虹彩孔は認めない。
PAS:丈が低い。
内皮所見:hammered silver appearance。スペキュラで大小不同・異型性が広範囲。
Cogan-Reese症候群
虹彩結節:有茎性の小結節と平坦な色素病巣の2種が認められる。
組織学的所見:メラニン含有紡錘形母斑細胞からなる良性病変4)。
ぶどう膜外反:合併することがある。
鑑別:虹彩悪性黒色腫との鑑別が必要な場合がある。
隅角所見:隅角鏡検査でSchwalbe線を越えて高く伸びるPASが認められ、ICE症候群に特徴的な所見である5)。PASは斑状で非常に前方に位置し、PAS間の線維柱帯は正常に見える5)。PASの形状はテント状、台形、広範な癒着などさまざまである。
| 臨床型 | 角膜浮腫 | 虹彩所見 | PAS丈 | 緑内障頻度 |
|---|---|---|---|---|
| 進行性虹彩萎縮 | 中等度 | 孔形成・偏位 | 高い | 最多 |
| Chandler | 顕著 | 軽度 | 低い | 中等度 |
| Cogan-Reese | 中等度 | 有色素性結節 | 中等度 | 中等度 |
ICE症候群の真の病因は未解明であるが、単純ヘルペスウイルス(HSV)の潜在感染が角膜内皮レベルで低グレードの炎症を惹起し、上皮様の活性化を引き起こすとの仮説がある。PCR検査ではICE患者の角膜・房水サンプルの60%以上からHSV DNAが検出されたと報告されている2)。エプスタイン・バーウイルス(EBV)の関与も指摘されている。
病理学的には、正常な内皮細胞が移動特性を持つ上皮様細胞に置換される。電子顕微鏡ではデスモソーム、トノフィラメント、微絨毛などの上皮的特徴が確認される。隣接する正常内皮細胞に対する毒性損傷(壊死性変化)も報告されている。
ICE症候群眼から切除されたDescemet膜の病理組織検査では、低立方体細胞の単層構造に部分的な二層・多層化を認め、免疫組織化学で上皮マーカー(AE1/AE3、CK8/18)と内皮マーカー(CD56、vimentin)の混合発現パターンが確認されている7)。この所見はICE症候群の本質である上皮様化生を病理学的に裏づけるものである。
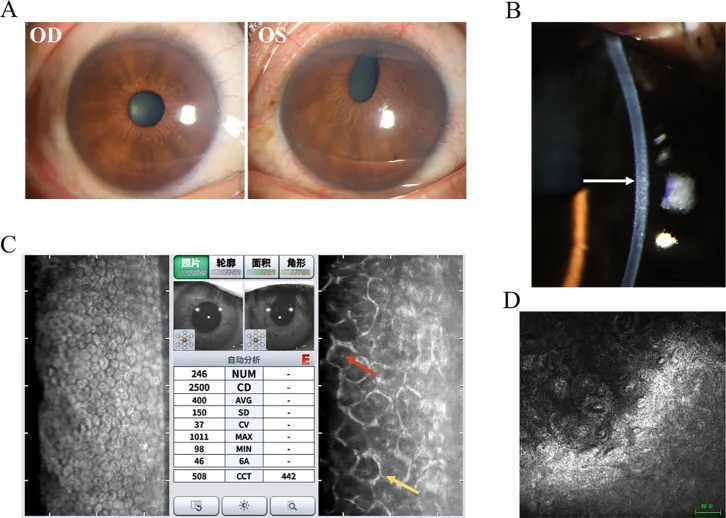
ICE症候群の確定診断に最も重要な検査である2)。スペキュラーマイクロスコープによって、細胞内にdark areaを持つ異常細胞(ICE細胞)を観察することで診断する。正常な六角形の内皮モザイクが消失し、多形性で「明暗反転(light-dark reversal)」を示す。中央に明るい点を持つ通常より大きく暗い内皮細胞が特徴的である。
角膜内皮細胞密度の著明な減少を認める。正常値は若年者で約3,500 cells/mm2、高齢者でも2,500〜3,000 cells/mm2であるが、500 cells/mm2以下に低下するとポンプ機能が破綻し水疱性角膜症を生じる。Cogan-Reese症候群の1例では763 cells/mm2まで低下した報告がある3)。
Chandler症候群ではスペキュラ検査で細胞の大小不同・異型性が広範囲に認められ、内皮細胞の境界が不明瞭であることが診断に役立つ。変動係数(CV値)は0.35以上で異常、六角形細胞出現率は50%以下で異常と判定される。
角膜内皮の丸石状腫脹細胞、六角形構造の消失、多形性の高輝度細胞、単核・二核の巨大内皮細胞を描出する2)。スペキュラーマイクロスコピーで角膜浮腫のため評価困難な場合にも有用である。
虹彩角膜角の癒着、角膜内皮層の高輝度肥厚、虹彩上の膜様組織を可視化する2)。PASの範囲・高さの定量的評価に優れる。
PASの評価に不可欠であり、続発閉塞隅角緑内障の診断と経過観察に用いる。ICE症候群ではSchwalbe線を越えるPASが特徴的であり、PAS間の線維柱帯は正常に見える点がPOAGとの鑑別に有用である5)。
眼圧測定、視神経乳頭写真、視野検査(ハンフリーまたはゴールドマン)、OCTによる網膜神経線維層(RNFL)厚評価を初期精密検査および経過観察に導入する2)。
ICE症候群の鑑別にあたっては、以下の疾患を除外する。
| 鑑別疾患 | 鑑別ポイント |
|---|---|
| Axenfeld-Rieger症候群 | 両眼性・先天性 |
| 後部多形性角膜ジストロフィ(PPMD) | 両眼性・家族性・性差なし |
| 虹彩分離症 | 高齢者に多い・性差なし |
| フックス角膜内皮ジストロフィ | 両眼性・角膜滴状粉 |
| 虹彩悪性黒色腫 | Cogan-Reeseとの鑑別が必要 |
前進する角膜内皮細胞膜が収縮を伴わずに線維柱帯を機能的に閉鎖する場合がある。この場合、隅角鏡検査で明らかなPASが視認されないため、「機能的な」隅角閉鎖が存在するにもかかわらず開放隅角緑内障と誤認される。片眼性の緑内障を見た場合はICE症候群を鑑別に含め、スペキュラーマイクロスコピーで角膜内皮を慎重に評価すべきである。
ICE症候群の治療は緑内障の眼圧コントロールと角膜代償不全への対応の二軸で構成される。薬物治療による長期の眼圧コントロールは困難になることが多く、最終的に手術的介入を要する症例が多い。
内科的治療
外科的治療
角膜内皮障害が進行し角膜混濁が高度となった場合、角膜内皮移植の適応となる。
Salekiら(2025)は、ICE症候群にDMEKを施行した最初の報告を発表した7)。60歳男性の左眼にDMEKを施行し、非矯正視力は術前1.1 LogMARから術後2ヶ月で0.54 LogMAR、10ヶ月で0.4 LogMARに改善した。眼圧は16mmHgで安定し、18ヶ月まで角膜透明性が維持された。
2段階手術アプローチとして、水晶体乳化吸引術+人工虹彩挿入を先行し、6ヶ月後にDSAEKを行う方法も報告されている1)。54歳女性の症例では、術後矯正視力が20/100から20/32に改善し、角膜内皮細胞密度1,640 cells/mm2が維持された1)。
Cogan-Reese症候群に嚢胞様黄斑浮腫(CME)がまれに合併することがある3)。局所NSAIDs(フルルビプロフェン1日3回)による治療で消退が得られたが、中止後に再発したとの報告がある3)。
同時施行は可能であるが、ICE症候群では眼圧コントロールと角膜移植を段階的に行うアプローチが報告されている。まず眼圧を安定させた上で角膜内皮移植を行うことで、移植片の生存率向上が期待される。緑内障手術と角膜移植の至適なタイミングは個々の症例に応じて判断する1)。
ICE症候群の根本的な異常は角膜内皮の上皮様化生(epithelialization)にある。正常な角膜内皮細胞は非増殖性の単層細胞であるが、ICE症候群ではこれが増殖・遊走能を持つ上皮様細胞に置換される。この過程はPPMDにも共通するが、ICEは片眼性で散発的であるのに対しPPMDは両眼性で常染色体優性遺伝である。
角膜内皮に異常が生じると、膜様組織が角膜裏面から隅角・虹彩前面にかけて増殖し、Schwalbe線を越えて線維柱帯上、さらに虹彩前面へと伸展する5)。この膜様組織が収縮することにより以下の病態が生じる。
丈の高いPAS形成による房水流出路の閉塞が主な機序である5)。加えて、膜様組織自体が線維柱帯を機能的に閉鎖することもあり、明らかなPASがなくても緑内障が発生しうる。薬物治療に抵抗性であるのは、膜様組織の進行が持続するためである。
変性した内皮細胞のポンプ機能不全と、緑内障による眼圧上昇の二重の機序が関与する。Chandler症候群では内皮細胞障害が顕著であり、眼圧が正常範囲であっても角膜浮腫を生じうる。角膜内皮細胞密度が500 cells/mm2以下に低下すると水疱性角膜症に至る。
膜様組織の収縮により虹彩が牽引され、瞳孔偏位・虹彩孔形成・ぶどう膜外反が生じる。進行性虹彩萎縮で最も顕著である。瞳孔の偏位はPASが多い方向に偏り、虹彩孔はその逆方向に多発する。
虹彩結節は組織学的にメラニン含有紡錘形母斑細胞からなり、Ki-67陽性率1%未満、melan-A陽性の良性病変である4)。まれに水晶体小帯脆弱性を伴い、白内障手術時にびまん性小帯離開を認めることがある4)。
ICE症候群眼から切除されたDescemet膜の免疫組織化学では、上皮マーカー(AE1/AE3、CK8/18)と内皮マーカー(CD56、vimentin)の混合発現パターンが確認されており、上皮様化生がICE症候群の本質的病態であることを裏づける7)。上皮性down-growth(上皮性内殖)との鑑別が重要であるが、臨床経過と組織学的所見の組み合わせで判断する。