限局型(nodular)
形態:境界明瞭、半球状に隆起した腫瘤
転移リスク:転移はまれ。最も予後良好な病型である1)
特徴:腫瘤が虹彩実質内に限局し、周辺虹彩への浸潤が少ない
治療適応:小型では虹彩切除術(iridectomy)が可能

ブドウ膜組織(虹彩・毛様体・脈絡膜)のメラノサイトに由来する悪性腫瘍のうち、虹彩を原発とするものが虹彩悪性黒色腫である。ぶどう膜メラノーマ全体の約2%を占めるに過ぎず、脈絡膜発生(90%超)・毛様体発生(約7%)と比較して最もまれな発生部位となる。
発生頻度は人口10万人あたり0.025人(欧米の約1/20)であり、さらに虹彩発生例はその一部に過ぎない。白人・淡色虹彩の人種に多く、東洋人での発生はまれである。脈絡膜や毛様体のメラノーマに比べ比較的悪性度が低く、進行が遅い傾向がある。
虹彩悪性黒色腫には毛様体からの浸潤によるものもある。大型・増大傾向・不整形・隅角浸潤の有無が悪性の判断指標となる。小型では局所切除(虹彩切除術)が選択可能な場合がある。
転移の様式はすべて血行性であり(ぶどう膜にリンパ管が存在しないため)、転移する場合は肝臓への向性が最も強い2)。脈絡膜メラノーマの12年死亡率が約40%であるのに対し、虹彩メラノーマでは転移頻度がはるかに低く予後は良好とされる。
虹彩悪性黒色腫は若年発症傾向があり、脈絡膜メラノーマの発症ピーク(約60歳)よりも早い年齢層でも発見される1)。
ぶどう膜メラノーマ全体でも白人で100万人あたり2〜8人と希少がんであり、さらに虹彩発生はその約2%を占めるに過ぎない。日本人での全ぶどう膜メラノーマ発生は人口10万人あたり0.025人(欧米の約1/20)であり、虹彩発生例はさらにまれである。虹彩に色素性病変を認めた場合は専門施設での精査が重要となる。
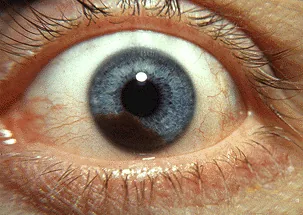
早期の小型病変では無症状のことが多く、健診や他疾患の検査中に偶然発見されることがある。病変の増大に伴い以下の症状が出現する。
虹彩面に充実性の有色素性〜無色素性腫瘤として認められる。悪性を示唆する臨床的指標は以下のとおりである。
限局型(nodular)
形態:境界明瞭、半球状に隆起した腫瘤
転移リスク:転移はまれ。最も予後良好な病型である1)
特徴:腫瘤が虹彩実質内に限局し、周辺虹彩への浸潤が少ない
治療適応:小型では虹彩切除術(iridectomy)が可能
びまん型(diffuse)
形態:虹彩全体に平坦に広がる浸潤性病変。境界不明瞭
転移リスク:限局型に比べ転移しやすい1)
特徴:眼圧上昇・隅角浸潤をきたしやすい。虹彩異色症(両眼の虹彩色の違い)として発見されることがある
治療適応:局所切除が困難で、放射線治療や眼球摘出術が必要となる場合が多い
発症は主に孤発性(sporadic)であり、明確な原因は不明である。主なリスク因子を以下に示す。
ぶどう膜メラノーマ(虹彩を含む)の遺伝子変異プロファイルは以下のとおりである。
| 変異遺伝子 | 変異頻度 | 転移リスク・特徴 |
|---|---|---|
| GNAQ/GNA11 | 83〜89% | 相互排他的な開始変異。転移リスクとの直接関連なし |
| BAP1 | 約45% | 最高転移リスク(大ピーク3.5年)、クラス2腫瘍 |
| SF3B1 | 約23% | 中程度リスク。遅発転移(大ピーク7年)が特徴 |
| EIF1AX | 約17% | 最低転移リスク |
GNAQ/GNA11変異はGTPase活性を障害し恒常的な活性化状態をもたらす開始変異であるが、腫瘍の大きさや転移リスクとの直接関連はない。二次ドライバー変異(BAP1・SF3B1・EIF1AX)は互いにほぼ完全に排他的に生じ、転移リスクの層別化に利用される。
BAP1変異は最高の転移リスクに関連し、EIF1AX変異は最低の転移リスクを示す。これらの変異情報は細針吸引生検で取得可能であり、転移サーベイランス計画の個別化に活用される1)。
GNAQ/GNA11変異が約85%に存在するが、転移リスクとの直接関連はない。転移リスクを規定するのは二次変異であり、BAP1変異(最高リスク、転移ピーク3.5年)、SF3B1変異(中等度リスク、遅発転移ピーク7年)、EIF1AX変異(最低リスク)の順に転移リスクが異なる。生検によりこれらの遺伝子プロファイルを取得することで、サーベイランス頻度の個別化が可能となる。
診断は主として画像検査と臨床所見の総合評価に基づく。虹彩メラノーマでは前眼部を中心とした検査が重要である。
原発腫瘍確定後、以下の転移スクリーニングを行う。
状況に応じて細針吸引生検を施行する。遺伝子プロファイル(GNAQ/GNA11・BAP1・SF3B1・EIF1AX)の取得が目的となる場合が増えている。腫瘍播種リスクを考慮し、適応は慎重に判断する。
治療方針は腫瘍のサイズ・形態・毛様体浸潤の有無・患者の全身状態を総合して決定する。
小型で虹彩母斑との鑑別が困難な病変では、まずUBMや前眼部OCTで腫瘍サイズを定期的にモニタリングする。増大・悪性化を示す指標(大型化・不整形・隅角浸潤・眼圧上昇)が出現した時点で治療に移行する。
小型虹彩メラノーマの第一選択。腫瘍を含む虹彩を切除する(iridectomy)。毛様体にも浸潤している場合は虹彩毛様体切除術(iridocyclectomy)を行う。眼球温存が可能で、切除検体から病理診断・遺伝子プロファイルの取得が行える利点がある。
中型(局所切除が困難な場合)に適応となる。
大型・眼球温存が困難な場合(びまん型・毛様体大規模浸潤例など)に適応となる。今日でも重要な選択肢の一つである。
転移性ぶどう膜メラノーマに対して、テベンタフスプ(tebentafusp)がHLA-A*02:01陽性患者に推奨される1,5)。
Nathan ら(2021)の第III相無作為化比較試験において、テベンタフスプは未治療の転移性ぶどう膜メラノーマ患者(HLA-A*02:01陽性)において、担当医選択(主にpembrolizumab)と比較して全生存期間の有意な改善を示した(mOS: 21.7ヶ月 vs 16.0ヶ月)4)。
テベンタフスプはT細胞受容体二重特異性融合蛋白(ImmTAC)であり、腫瘍関連抗原gp100をHLA-A*02:01複合体上で認識してT細胞を活性化する。投与はHLA-A*02:01陽性確認後に週1回静注で行う(20 mg→30 mg→68 mgの漸増)。
投与中は脈絡膜菲薄化・眼底脱色素・皮膚脱色素斑などの眼副作用が報告されており、定期的な眼科的モニタリングが必要である7)。gp100は正常脈絡膜メラノサイトにも発現しているため、これらの副作用は機序として説明される7)。
治療後の患眼監視は定期的な細隙灯顕微鏡・UBM・前眼部OCTで行う。局所再発の確認と転移サーベイランスを並行して実施する。治療後6ヶ月ごと5年間、以後は年1回10年間の肝臓転移サーベイランスが推奨される1)。
虹彩メラノサイトに腫瘍性増殖が生じることで発症する。ぶどう膜メラノーマの発症機序は皮膚メラノーマとは異なり、独自の分子経路による。
GNAQ/GNA11のQ209位変異が開始変異として最も多く、GTPase活性を障害することで恒常的なGTP結合活性化状態をもたらす。これによりMAPK経路(Ras/RAF/MEK/ERK)を含む複数のシグナル経路が持続的に活性化される5)。
二次ドライバー変異(BAP1・SF3B1・EIF1AX)は互いにほぼ完全に排他的に生じる。BAP1変異はクラス2(高転移リスク)に分類され、モノソミー3との関連が強い。SF3B1変異保持者の転移後全生存期間中央値は比較的良好で遅発転移が特徴である。
虹彩メラノーマは脈絡膜・毛様体メラノーマと比べ転移しにくい傾向がある。この特性に関連する要因として以下が挙げられる。
ぶどう膜にリンパ管が存在しないため、転移はすべて血行性に生じる2)。循環腫瘍細胞が血流に乗り、肝臓への強い向性(seed and soil理論)で肝転移をきたす。転移は原発腫瘍治療後25年以上後に出現することもあり2)、長期サーベイランスが必要な理由となっている。
腫瘍内不均一性が存在し、形態学的に異なる部位で遺伝子プロファイルが異なりうるため6)、生検サンプリングの場所が予後予測精度に影響する可能性がある。
テベンタフスプは第III相試験で全生存期間の有意な改善を示した初の転移性ぶどう膜メラノーマ治療薬である4)。2023年に報告された3年間追跡データ(Hassel et al.)では、3年全生存率が27%(対照群9%)と持続的な生存改善が確認されている9)。
gp100は虹彩メラノーマにも発現するため、虹彩メラノーマからの転移例においても同薬の適応が考慮される1)。投与中の眼副作用(脈絡膜菲薄化・眼底脱色素)は不可逆的な場合もあり、眼科専門家との連携が必要である7)。
Gαq阻害薬(YM-254890)とMEK阻害薬(trametinib/binimetinib)の併用が、in vitro・in vivoで相乗的抗腫瘍効果を示している5)。Gαq単独阻害ではMAPKシグナルが24時間で回復するが、MEK阻害薬との併用によりMAPKシグナルの回復が抑制される5)。臨床試験での評価が続けられている。
ぶどう膜メラノーマでは皮膚メラノーマに比べ免疫チェックポイント阻害薬の効果は著しく限定的であり7)、単剤での奏効率は約5%、併用療法でも12〜18%程度とされる1)。これはぶどう膜メラノーマの低い腫瘍変異量(TMB)や免疫微小環境の特性によると考えられる2)。
ただし、MBD4(methyl-CpG binding domain-4)遺伝子の生殖細胞系列または体細胞の機能喪失変異を持つ症例では、チェックポイント阻害薬への感受性が高まる可能性が報告されている2)。
Johansson ら(2020)は全ゲノム解析にて虹彩腫瘍にUVR誘発突然変異シグネチャーを同定した3)。これはぶどう膜メラノーマの中でも虹彩メラノーマが紫外線関連の遺伝子変化を有することを示す初の報告であり、発生機序の面で脈絡膜メラノーマとの差異を示す重要な知見である。この発見は紫外線防護の役割や、将来の予防・治療戦略に示唆を与えうる。
オートファジー関連9遺伝子シグネチャー(9-ARG)がぶどう膜メラノーマの予後予測に有用であることが示されている8)。高リスク群ではIL6-JAK-STAT3経路・血管新生関連経路が濃縮し、免疫細胞浸潤(CD8 T細胞・活性化記憶CD4 T細胞)が増加するものの免疫抑制的表現型を呈し、予後不良に関連するという逆説的知見が報告されている8)。これは眼が免疫特権臓器であることと関連すると考えられる。
Carter TJ, Broadfoot J, Coupland SE, et al. Uveal Melanoma UK national guidelines: 2023 update. Eur J Cancer. 2023;185:61-73.
Rantala ES, Hernberg MM, Piperno-Neumann S, et al. Metastatic uveal melanoma: The final frontier. Prog Retin Eye Res. 2022;90:101041.
Johansson PA, Brooks K, Newell F, et al. Whole genome landscapes of uveal melanoma show an ultraviolet radiation signature in iris tumours. Nat Commun. 2020;11:2408.
Nathan P, Hassel JC, Rutkowski P, et al. Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021;385(13):1196-1206.
Sriramareddy SN, Smalley KSM. MEK-ing the most of it: strategies to co-target Gαq and MAPK in uveal melanoma. Clin Cancer Res. 2021;27(5):1217-1219.
Fonseca C, Pinto-Proença R, Bergeron S, et al. Intratumoral heterogeneity in uveal melanoma. Ocul Oncol Pathol. 2021;7:17-25.
Krohn J, Vinnem LIH, Jansson RW, et al. Fundus hypopigmentation and choroidal thinning associated with tebentafusp therapy: report of a case and literature review. BMC Ophthalmol. 2025;25:464.
Chuah S, Chew V. Immune implication of an autophagy-related prognostic signature in uveal melanoma. Biosci Rep. 2021;41:BSR20211098.
Hassel JC, Piperno-Neumann S, Rutkowski P, et al. Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. NEJM Evid. 2023;2(8):EVIDoa2300071.