毛様体メラノーマ
発見時サイズ:解剖学的に隠れた位置のため、発見時に比較的大きいことが多い。
見張り血管(sentinel vessel):腫瘍直上の拡張・蛇行した強膜上血管を高頻度に伴う。診断の重要な手がかりとなる。
前眼部変化:水晶体・虹彩隔壁の前方移動、続発閉塞隅角緑内障を呈しやすい。
眼外進展:乳頭管(emissary canal)経由の眼外進展リスクがある。

毛様体悪性黒色腫は、毛様体のメラノサイトから発生する悪性腫瘍である。ぶどう膜(虹彩・毛様体・脈絡膜)のメラノサイトに由来するブドウ膜メラノーマのうち、毛様体由来が約7%を占める2)。
毛様体腫瘍を発見した場合は、まず悪性黒色腫の可能性を念頭に対応する必要がある。毛様体悪性黒色腫は経瞳孔で黒褐色の毛様体部隆起として観察されるが、腫瘍は毛様体実質から発生しているため、直視で観察しているのは色素上皮の色調である。したがって腫瘍が色素性か否かは、透光性検査によって判断する。
ブドウ膜メラノーマ全体の発生頻度は欧米の約1/20であり、本邦では人口10万人あたり0.025人とされる。脈絡膜からの発生が多く、毛様体はより少ない。中高年に発生し、やや男性優位である。
転移の様式はすべて血行性であり(ぶどう膜にリンパ管が存在しないため)、肝臓への強い向性を示す。転移後の全生存期間中央値は従来6ヶ月以下であったが、テベンタフスプ(tebentafusp)の登場により改善しつつある。
毛様体は眼底検査では見えにくい部位であり、散瞳後の前眼部観察(隅角鏡・スリットランプ)や、視力低下・見張り血管(sentinel vessel)・続発緑内障などの症状・所見を契機に発見されることが多い。健診では発見されにくいため、症状出現時の速やかな眼科受診が重要である。
毛様体メラノーマの自覚症状は、その解剖学的位置の特殊性から以下のような特徴を示す3)。
散瞳後の前眼部観察で、毛様体部に黒褐色の隆起性病変を確認する。以下の所見が診断の手がかりとなる。
毛様体メラノーマ
発見時サイズ:解剖学的に隠れた位置のため、発見時に比較的大きいことが多い。
見張り血管(sentinel vessel):腫瘍直上の拡張・蛇行した強膜上血管を高頻度に伴う。診断の重要な手がかりとなる。
前眼部変化:水晶体・虹彩隔壁の前方移動、続発閉塞隅角緑内障を呈しやすい。
眼外進展:乳頭管(emissary canal)経由の眼外進展リスクがある。
脈絡膜メラノーマとの比較
その他の重要な臨床所見として、虹彩根部異常(腫瘍による圧迫・変形)、水晶体圧排変形(前眼部の異常な形態)がある。腫瘍が大きくなると硝子体出血や白内障を合併することもある。
毛様体悪性黒色腫は毛様体のメラノサイトが腫瘍性に増殖することで発生する。ぶどう膜母斑からの悪性化も生じうる。
主なリスク因子を以下に示す。
遺伝子変異と転移リスクの対応を以下に示す1)。
| 変異遺伝子 | 変異頻度 | 転移リスク・特徴 |
|---|---|---|
| GNAQ/GNA11 | 83〜89% | 相互排他的な開始変異。転移リスクとの直接関連なし |
| BAP1 | 45% | 最も高い転移リスク(大ピーク3.5年)、クラス2 |
| SF3B1 | 23% | 中程度リスク。遅発転移(大ピーク7年)が特徴 |
| EIF1AX | 17% | 最も低い転移リスク |
GNAQ/GNA11変異は腫瘍形成初期の事象と考えられており、変異単独では腫瘍の大きさや転移リスクとの有意な関連はない。BAP1・SF3B1・EIF1AXの二次ドライバー変異は互いにほぼ完全に排他的に生じ、転移リスクの層別化に重要な意味を持つ7)。
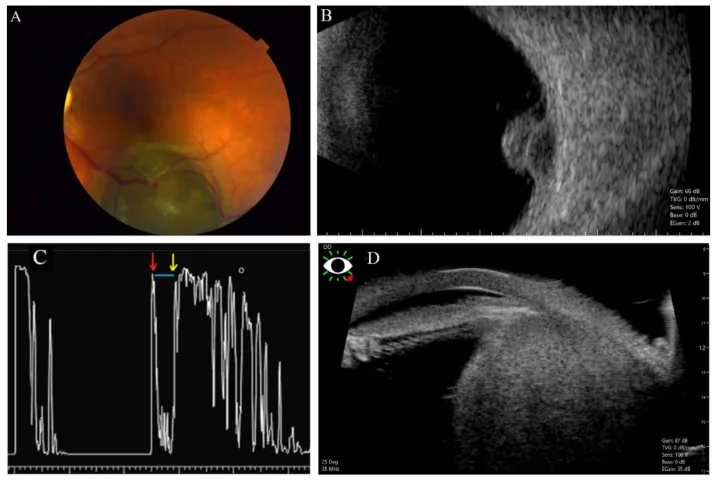
暗室で内視鏡光源を強膜外から当て、光が透過してくるか否かを経瞳孔で観察する。この透光性検査が毛様体腫瘍の性状判定に最も重要な基本検査である。
毛様体腫瘍の大きさ・形状・内部エコーを評価するうえで最重要の画像検査である。高周波超音波を用いて毛様体の詳細な形態を描出できる。腫瘍の境界・内部反射・隣接構造(虹彩・隅角・水晶体)への浸潤評価に優れる。
毛様体メラノーマではtall spikeとlow-medium内部反射が特徴的である3)。
T1強調画像で高信号、T2強調画像で低信号を示すが、毛様体の他の腫瘍でも同じ所見になることが多く、造影剤による増強もしばしば微弱である。MRI単独での確定診断は困難であり、他の所見と組み合わせて評価する。
毛様体腫瘍には良性から悪性まで複数の病態があり、正確な鑑別が治療方針を左右する。
毛様体平滑筋腫
透光性:あり(非色素性)。透光性検査で鑑別の最大の手がかりとなる。
形態:整った半球形。境界明瞭。
好発年齢:中若年。男女ともに発生。
治療:小型は経強膜全摘も可能。大型・合併症重篤例は眼球摘出。
毛様体黒色細胞腫
毛様体上皮囊胞
毛様体腺腫・腺癌
由来:毛様体の上皮(無色素上皮・色素上皮)からの発生。
頻度:まれな腫瘍であり、他の毛様体腫瘍との鑑別に病理組織検査が必要。
毛様体腫瘍には良性のものも含まれる。平滑筋腫・黒色細胞腫・上皮囊胞などの良性腫瘍も発生するため、必ずしも悪性黒色腫とは限らない。透光性検査・UBM・MRIなどで詳細評価を行い、増大傾向や症状に応じて経過観察または手術・放射線治療が選択される。
治療は腫瘍のサイズ・位置・症状・眼球温存の可能性を総合的に判断して選択する。
小型腫瘍:経強膜腫瘍全摘
腫瘍が比較的小さく前方に局在する場合、強膜の一部と腫瘍のみを切除する局所切除術(経強膜腫瘍全摘)が選択される。確定診断と治療を兼ねることができる。
中型腫瘍(疑診含む):放射線治療
放射線治療が眼球温存の主要な選択肢となる。
疑診例でも重粒子線などの放射線治療を考慮する場合がある。
大型腫瘍:眼球摘出術
眼球温存が困難な大型腫瘍では眼球摘出術が選択される。摘出検体により確定診断に至る。
状況に応じた生検
経強膜・経角膜経瞳孔の生検も検討される。腫瘍内不均一性を考慮し、形態学的に異なる領域からのサンプリングが推奨される7)。
転移性ぶどう膜メラノーマに対するテベンタフスプ(tebentafusp)は、HLA-A*02:01陽性患者に適応となる5)。第III相試験において、転移性ぶどう膜メラノーマの全生存期間を有意に改善した初の薬剤である。
英国ぶどう膜メラノーマガイドライン2023年更新版に基づき、以下のサーベイランスが推奨される1)。
予後は脈絡膜メラノーマと類似して不良な傾向がある。肝転移が予後を規定し、眼球摘出後数年〜10年以上経過してから転移が明らかになることがある。
小〜中型腫瘍では、経強膜腫瘍全摘、重粒子線治療、小線源療法(Ru-106)、陽子線治療などの眼球温存療法が選択できる。大型腫瘍では眼球摘出が必要な場合があるが、局所治療の選択は転移率・全生存率に影響しないことが示されており、生命予後を最優先としつつ温存の可否を専門施設で検討する。
ぶどう膜メラノーマの発症機序は皮膚メラノーマとは異なる独自の分子経路による。
GNAQ/GNA11のQ209位変異が最も多く検出される。これらの変異はGTPase活性を障害し、恒常的なGTP結合活性化状態をもたらす。GNAQ/GNA11変異によりMAPK経路(Ras/RAF/MEK/ERK)を含む複数のシグナル経路が持続的に活性化される6)。
二次ドライバー変異(BAP1・SF3B1・EIF1AX)は互いにほぼ完全に排他的に生じ、転移リスクの層別化に重要な意味を持つ7)。
毛様体は脈絡膜より前方に位置するため、虹彩・隅角への浸潤が生じやすい。これが続発閉塞隅角緑内障を引き起こす一因となる。また前方への腫瘍進展により水晶体偏位・白内障の原因ともなる。
眼外進展は乳頭管(emissary canal)経由で生じ、眼窩や全身への進展につながる。
ぶどう膜にリンパ管が存在しないため、転移はすべて血行性に生じる2)。肝臓への強い向性はseed and soil理論で説明される。転移巣においてもGNAQ(57%)とGNA11(36%)が相互排他的に検出される。
腫瘍内VEGF濃度は健常眼より有意に高い。硝子体内ベバシズマブ注射後に毛様体メラノーマが急速増大した症例が報告されており(基底径2.51→18.0 mm、高さ6.23→11.0 mm/7週間)4)、抗VEGF薬の硝子体内投与は禁忌となりうる。
腫瘍内不均一性が形態学的・遺伝的両面で存在し、生検の予後予測精度に影響する7)。モノソミー3は部位横断的に共通する一方、6q欠失は色素部位のみに限局する例もある。
テベンタフスプはHLA-A02:01陽性患者向けに設計されたT細胞受容体二重特異性融合蛋白である5)。腫瘍関連抗原gp100をHLA-A02:01複合体上で認識し、T細胞を活性化することで抗腫瘍効果を発揮する。第III相試験において転移性ぶどう膜メラノーマの全生存期間を有意に改善した初の薬剤であり、3年全生存率のデータが集積されつつある11)。
Krohnら(2025)の症例報告では、テベンタフスプ(週1回IV:20→30→68 mgの漸増)26ヶ月投与後に肝転移安定・新病変なしという良好な経過が記録された8)。右眼中心脈絡膜厚が241μmから123μmへ49%菲薄化し、眼底脱色素・眉毛睫毛のポリオーシス・皮膚脱色素斑が観察された。
gp100は正常脈絡膜メラノサイトにも発現しており、脈絡膜菲薄化の機序に関連すると考えられる8)。投与中は定期的な眼科的モニタリングが必要である。
Gαq阻害薬(YM-254890)とMEK阻害薬(trametinib/binimetinib)の併用が、in vitro・in vivoで相乗的抗腫瘍効果を示している6)。Gαq単独阻害ではMAPKシグナルが24時間で回復するが、MEK阻害薬との併用によりMAPKシグナルの回復が抑制される6)。
セルメチニブの第II相試験でPFS改善が示されたが、セルメチニブ+ダカルバジンの第III相試験(SUMIT試験)ではPFS改善は認められなかった6)。
ぶどう膜メラノーマでは皮膚メラノーマに比べ免疫チェックポイント阻害薬の効果は限定的である。眼が免疫特権臓器であることと免疫抑制的微小環境が関連すると考えられる。
転移性病変に対する局所アプローチとして、肝切除・ラジオ波焼灼術・肝動脈塞栓術・メルファランによる経皮的肝灌流化学療法(PHP)・イットリウム-90マイクロスフィア近接照射療法(SIRT)が研究されている。
オートファジー関連9遺伝子シグネチャー(9-ARG)がぶどう膜メラノーマの予後予測に有用であることが示されている(TCGA 80例+GEO 150例で検証)9)。高リスク群ではIL6-JAK-STAT3経路・血管新生・活性酸素種経路が濃縮し、免疫抑制的表現型であり予後不良に関連する9)。
Kujalaら(2013)はCIOM T分類を用いた毛様体・脈絡膜メラノーマの解剖学的進展に基づくステージングを報告しており、腫瘍の位置と予後の関係を層別化する根拠を提供している10)。