睫狀體黑色素瘤
發現時大小:由於解剖位置隱蔽,發現時通常較大。
哨兵血管:腫瘤正上方常伴有擴張、迂曲的鞏膜表面血管。這是重要的診斷線索。
前眼部變化:易出現水晶體-虹膜隔前移、續發性閉鎖性隅角青光眼。
眼外擴展:存在經導血管向眼外擴展的風險。

睫狀體惡性黑色素瘤是起源於睫狀體黑色素細胞的惡性腫瘤。在來源於葡萄膜(虹膜、睫狀體、脈絡膜)黑色素細胞的葡萄膜黑色素瘤中,睫狀體起源約占7% 2)。
發現睫狀體腫瘤時,應首先考慮惡性黑色素瘤的可能性。睫狀體惡性黑色素瘤經瞳孔觀察為黑褐色的睫狀體隆起,但由於腫瘤起源於睫狀體實質,直視下觀察到的是色素上皮的顏色。因此,腫瘤是否為色素性需通過透照檢查判斷。
日本葡萄膜黑色素瘤的總發生率約為歐美的1/20,為每10萬人0.025例。脈絡膜起源最多,睫狀體較少。好發於中老年人,男性略多。
轉移方式均為血行性(葡萄膜無淋巴管),對肝臟有強趨向性。轉移後中位總生存期以往不足6個月,但隨著tebentafusp的出現正在改善。
睫狀體在眼底檢查中難以看到,常在散瞳後前眼部觀察(房角鏡、裂隙燈)或因視力下降、哨兵血管、繼發性青光眼等症狀和體徵而被發現。健康檢查中難以發現,因此出現症狀時及時眼科就診很重要。
睫狀體黑色素瘤的主觀症狀因其解剖位置的特殊性而表現出以下特徵3)。
散瞳後前眼部檢查可見睫狀體區域有黑褐色隆起性病變。以下所見為診斷線索。
睫狀體黑色素瘤
發現時大小:由於解剖位置隱蔽,發現時通常較大。
哨兵血管:腫瘤正上方常伴有擴張、迂曲的鞏膜表面血管。這是重要的診斷線索。
前眼部變化:易出現水晶體-虹膜隔前移、續發性閉鎖性隅角青光眼。
眼外擴展:存在經導血管向眼外擴展的風險。
與脈絡膜黑色素瘤的比較
其他重要的臨床發現包括虹膜根部異常(腫瘤壓迫或變形)、水晶體受壓變形(前節異常形態)。腫瘤增大時可能併發玻璃體出血或白內障。
睫狀體惡性黑色素瘤由睫狀體黑色素細胞腫瘤性增殖引起。也可能由葡萄膜痣惡變而來。
主要風險因素如下所示。
基因突變與轉移風險的對應關係如下所示1)。
| 突變基因 | 突變頻率 | 轉移風險/特徵 |
|---|---|---|
| GNAQ/GNA11 | 83~89% | 互斥的起始突變。與轉移風險無直接關聯。 |
| BAP1 | 45% | 轉移風險最高(高峰3.5年),第2級 |
| SF3B1 | 23% | 中度風險。特點為晚期轉移(高峰7年) |
| EIF1AX | 17% | 轉移風險最低 |
GNAQ/GNA11突變被認為是腫瘤形成的早期事件,單獨突變與腫瘤大小或轉移風險無顯著關聯。BAP1、SF3B1和EIF1AX的二次驅動突變幾乎完全互斥發生,對轉移風險分層具有重要意義7)。
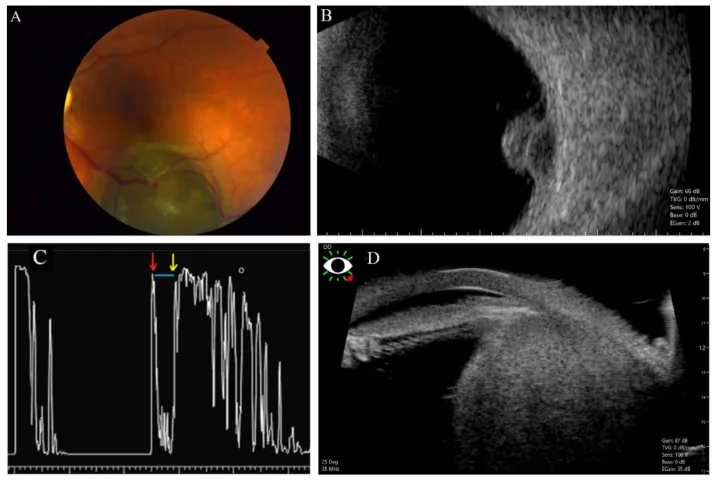
在暗室中,將內視鏡光源從鞏膜外照射,透過瞳孔觀察光線是否透射。此透照檢查是判斷睫狀體腫瘤性質最重要的基本檢查。
這是評估睫狀體腫瘤大小、形狀和內部回音最重要的影像檢查。高頻超音波可以顯示睫狀體的詳細形態。它在評估腫瘤邊界、內部反射以及向鄰近結構(虹膜、隅角、水晶體)的侵犯方面表現優異。
睫狀體黑色素瘤的特徵是高波峰和低-中內部反射 3)。
T1加權影像呈高信號,T2加權影像呈低信號,但其他睫狀體腫瘤也常出現相同表現,且顯影劑增強往往微弱。單獨依靠MRI難以確診,需結合其他發現進行評估。
睫狀體腫瘤包括從良性到惡性的多種病變,準確鑑別決定治療方針。
睫狀體平滑肌瘤
透光性:有(非色素性)。透光性檢查是鑑別診斷的最大線索。
形態:規則的半球形,邊界清晰。
好發年齡:中青年。男女均可發生。
治療:小型腫瘤可經鞏膜全切除。大型或併發症嚴重者需摘除眼球。
睫狀體黑色素細胞瘤
透光性:無(色素性)。與惡性黑色素瘤鑑別困難。
生長方式:特徵為緩慢增大。快速增大提示惡性黑色素瘤。
處理:定期進行UBM監測,如有增大趨勢,考慮切除和病理檢查。
睫狀體上皮囊腫
透光性:有(因囊液)。
特徵:有時可游離於玻璃體中。
鑑別:透過UBM確認囊壁和囊液的性質。
睫狀體腺瘤/腺癌
來源:起源於睫狀體上皮(無色素上皮或色素上皮)。
頻率:罕見腫瘤,需病理組織檢查以與其他睫狀體腫瘤鑑別。
睫狀體腫瘤也包括良性腫瘤。平滑肌瘤、黑色素細胞瘤、上皮囊腫等良性腫瘤也會發生,因此不一定是惡性黑色素瘤。透過透照檢查、UBM、MRI等進行詳細評估,根據生長趨勢和症狀選擇觀察、手術或放射治療。
治療根據腫瘤的大小、位置、症狀以及保留眼球的可能性的綜合判斷來選擇。
小型腫瘤:經鞏膜腫瘤全切除術
當腫瘤相對較小且位於前方時,可選擇局部切除(經鞏膜腫瘤全切除術),僅切除部分鞏膜和腫瘤。該方法可同時進行確診和治療。
中型腫瘤(包括疑似病例):放射治療
放射治療是保留眼球的主要選擇。
即使是疑似病例,也可能考慮重粒子線等放射治療。
大型腫瘤:眼球摘除術
對於難以保留眼球的大型腫瘤,選擇眼球摘除術。透過摘除檢體可得到確診。
依情況進行切片檢查
也可考慮經鞏膜、經角膜或經瞳孔的切片檢查。考量腫瘤內異質性,建議從形態不同的區域取樣7)。
替本塔司普(tebentafusp)用於轉移性葡萄膜黑色素瘤,適用於HLA-A*02:01陽性患者5)。在第三期試驗中,它是首個顯著改善轉移性葡萄膜黑色素瘤整體存活期的藥物。
根據2023年更新的英國葡萄膜黑色素瘤指引,建議進行以下監測1)。
預後與脈絡膜黑色素瘤相似,有不良傾向。肝轉移決定預後,眼球摘除術後數年至10年以上才可能發現轉移。
對於小到中型腫瘤,可以選擇經鞏膜腫瘤切除術、重粒子線治療、近距離放射治療(Ru-106)、質子線治療等保留眼球的療法。對於大型腫瘤,有時需要摘除眼球,但已有研究表明局部治療的選擇不影響轉移率和總存活率。在優先考慮生命預後的同時,應在專業機構討論保留的可能性。
葡萄膜黑色素瘤的發病機制與皮膚黑色素瘤不同,具有獨特的分子路徑。
GNAQ/GNA11的Q209位突變最為常見。這些突變損害GTP酶活性,導致持續的GTP結合活化狀態。GNAQ/GNA11突變導致包括MAPK路徑(Ras/RAF/MEK/ERK)在內的多個信號路徑持續活化6)。
二次驅動突變(BAP1、SF3B1、EIF1AX)幾乎完全互斥發生,對轉移風險分層具有重要意義7)。
由於睫狀體位於脈絡膜前方,容易向虹膜和前房角浸潤。這導致續發性閉角型青光眼。此外,腫瘤向前擴展可引起水晶體移位和白內障。
眼外擴展通過導血管發生,導致眼眶和全身擴散。
由於葡萄膜沒有淋巴管,所有轉移均為血行性2)。對肝臟的強烈趨向性可用種子和土壤理論解釋。在轉移灶中,GNAQ(57%)和GNA11(36%)互斥檢測到。
腫瘤內VEGF濃度顯著高於健康眼。有報導稱玻璃體內注射貝伐珠單抗後睫狀體黑色素瘤快速增大(基底直徑2.51→18.0 mm,高度6.23→11.0 mm,7週內)4),因此玻璃體內注射抗VEGF藥物可能是禁忌。
腫瘤內異質性在形態學和遺傳學兩方面都存在,影響活檢的預後預測準確性7)。3號染色體單體在腫瘤部位間普遍存在,而6q缺失在某些病例中可能僅限於色素區域。
替貝他司普是一種為HLA-A02:01陽性患者設計的T細胞受體雙特異性融合蛋白5)。它識別HLA-A02:01複合物上的腫瘤相關抗原gp100,激活T細胞發揮抗腫瘤作用。它是首個在III期試驗中顯著改善轉移性葡萄膜黑色素瘤總生存期的藥物,3年總生存率數據正在累積中11)。
在Krohn等人(2025)的病例報告中,替貝他司普(每週靜脈注射:20→30→68 mg遞增)治療26個月後,記錄到肝轉移穩定且無新病灶的良好病程8)。右眼中心脈絡膜厚度從241 μm減少49%至123 μm,並觀察到眼底脫色素、眉毛和睫毛的灰髮症以及皮膚脫色素斑。
gp100也在正常脈絡膜黑色素細胞上表現,被認為與脈絡膜變薄的機制有關8)。治療期間需要定期進行眼科監測。
Gαq抑制劑(YM-254890)與MEK抑制劑(曲美替尼/比美替尼)的聯合在體外和體內顯示出協同抗腫瘤作用6)。單獨抑制Gαq時,MAPK訊號在24小時內恢復,但與MEK抑制劑聯合可抑制MAPK訊號的恢復6)。
司美替尼的II期試驗顯示PFS改善,但司美替尼聯合達卡巴嗪的III期試驗(SUMIT試驗)未觀察到PFS改善6)。
在葡萄膜黑色素瘤中,免疫檢查點抑制劑的療效與皮膚黑色素瘤相比有限。這被認為與眼睛是免疫豁免器官以及免疫抑制微環境有關。
針對轉移性病變的局部方法正在研究中,包括肝切除術、射頻消融術、肝動脈栓塞術、美法侖經皮肝灌流化療(PHP)以及釔-90微球近接放療(SIRT)。
自噬相關9基因特徵(9-ARG)已被證明對預測葡萄膜黑色素瘤的預後有用(在80例TCGA和150例GEO中驗證)9)。在高風險組中,IL6-JAK-STAT3通路、血管新生和活性氧通路富集,免疫抑制表型與不良預後相關9)。
Kujala等人(2013)報告了使用CIOM T分類基於睫狀體和脈絡膜黑色素瘤解剖進展的分期,為分層腫瘤位置與預後的關係提供了依據10)。