瞳孔阻滯型閉角
虹膜向前膨隆:後房壓力升高,虹膜被推向前方的形態。
整體房角狹窄:虹膜從Schwalbe線區域向角膜側被擠壓。
暗處房角關閉加重:可觀察到散瞳使病情惡化的情況。

超音波生物顯微鏡(Ultrasound Biomicroscopy; UBM)是一種用於眼前段影像診斷的檢查設備。1990年代初,Foster和Pavlin首次將其引入,作為一種獲得顯微鏡級解析度眼部斷面圖像的方法。
通過使用30–50 MHz的高頻超音波,可以對裂隙燈顯微鏡無法觀察的眼前段結構(睫狀體、虹膜背面、隅角隱窩)進行高解析度成像。高頻化使組織解析度達到50–100 μm,優化用於評估眼前段5–10 mm的深度。
與常規B型超音波(5–10 MHz)相比,穿透深度有限(5–10 mm),但解析度顯著提高。由於高頻波的組織衰減較大,評估脈絡膜更深結構需要額外使用低頻B型超音波。
UBM特別有用的臨床情況如下所示。
常規B型超音波使用5–10 MHz觀察整個眼球(眼軸長度、視網膜、脈絡膜等)。超音波生物顯微鏡使用30–50 MHz的高頻,獲得組織解析度50–100 μm的高解析度圖像,專門用於眼前段。但由於高頻,穿透深度限於5–10 mm,觀察後部玻璃體和視網膜需要常規超音波。
UBM檢查的基本步驟如下。
也有安裝探頭帽並注入水進行檢查的方法(無需眼杯)。由於可以在任何體位下進行檢查,因此也適用於無法採取常規仰臥位的患者。
膜式超音波生物顯微鏡(例如UD-8060,托美公司)無需眼杯,在膜尖端塗抹Scopisol®後接觸檢查部位。這使得坐位檢查成為可能。
超音波生物顯微鏡能夠對前房隅角進行定量測量,通常使用以下參數。
| 參數 | 定義 |
|---|---|
| AOD500(隅角開放距離) | 鞏膜突前方500 μm處小樑網與虹膜間的垂直距離 |
| ARA(隅角隱窩面積) | AOD線與隅角隱窩圍成的三角形面積 |
| ACD(前房深度) | 中央角膜內皮到水晶體前表面的距離 |
| 水晶體拱高 | 左右鞏膜突連線前方水晶體的距離 |
AOD500的詳細定義是「鞏膜突前方500 μm處小樑網與虹膜間的垂直距離」,準確識別鞏膜突決定了測量精度。在原發性閉鎖隅角青光眼(PACG)中,AOD500和前房深度顯著減少,有助於診斷。
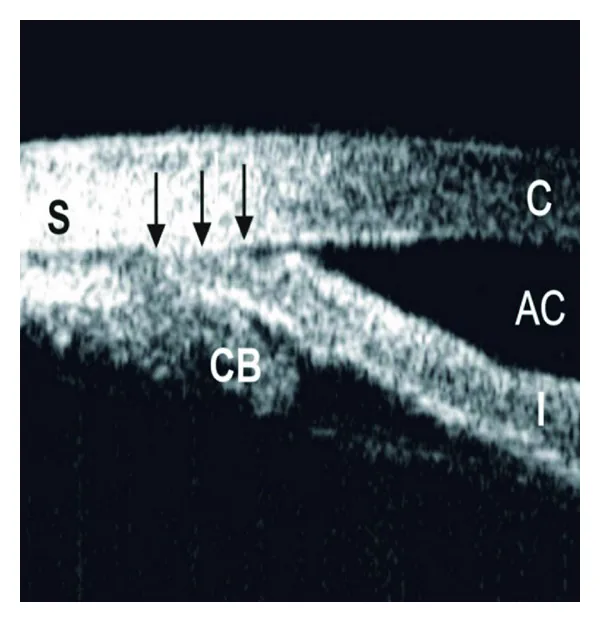
角膜前後面、鞏膜表面、虹膜前後面顯示為高亮度。角膜基質、虹膜基質、睫狀體為低亮度。正常眼中,虹膜輕度向前凸起或平坦,虹膜與睫狀突之間可見睫狀溝。
在前房角觀察中,鞏膜突和Schwalbe線的識別至關重要。鞏膜突是鞏膜向前房內突出的部分,前方附著有小樑網,是始終可確認的重要指標。
瞳孔阻滯型閉角
虹膜向前膨隆:後房壓力升高,虹膜被推向前方的形態。
整體房角狹窄:虹膜從Schwalbe線區域向角膜側被擠壓。
暗處房角關閉加重:可觀察到散瞳使病情惡化的情況。
高褶虹膜
無虹膜膨隆:中央虹膜平坦,不伴有瞳孔阻滯。
睫狀體前位及睫狀溝消失:特徵性表現。睫狀體向前移位,機械性推擠虹膜根部。
散瞳時虹膜根部阻塞房角:暗室散瞳下可確認關閉。
高褶虹膜中,中央前房相對較深,中央虹膜平坦,虹膜根部厚並向房角側彎曲,房角隱窩呈裂隙狀狹窄。睫狀體前位及睫狀溝消失是特徵性表現。
超音波生物顯微鏡觀察對於雷射虹膜切開術後仍未解除的高褶虹膜的確定診斷極為有用。如果雷射虹膜切開術後眼壓不下降,或散瞳後確認與術前相同的房角關閉,則可確診高褶虹膜。僅為了診斷而進行雷射虹膜切開術應避免,因其有大皰性角膜病變等風險,建議使用超音波生物顯微鏡觀察。
在接受雷射虹膜切開術治療原發性閉角型青光眼的患者中,約33%存在高褶虹膜,該組患者發生周邊虹膜前粘連及進一步房角關閉的風險較高。2)
惡性青光眼是由於睫狀體前旋或房水異常流入玻璃體腔等導致玻璃體前移而引起的閉角型青光眼。雖有特發性病例,但結合手術史確認UBM表現對診斷至關重要。
UBM可見以下表現:
ICL(植入式Collamer鏡片)植入後的拱高(ICL與水晶體前表面之間的間隙)通過UBM進行定量評估。合適的拱高範圍因型號和眼軸長度而異,拱高不足(<250 μm)會增加白內障進展風險,拱高過高(>1000 μm)會增加角膜內皮損傷和前房變淺的風險。長期追蹤中(每年1-2次)也使用UBM監測拱高變化。3)
外力導致眼壓急劇升高可引起隅角後退、虹膜斷裂、小樑網損傷和睫狀體分離。睫狀體分離時,超音波生物顯微鏡可清晰顯示房水在脈絡膜上腔積聚。
Yeilta等人報告了一例5×3×2 mm的虹膜睫狀體黑色素細胞瘤,通過超音波生物顯微鏡顯示(表現為邊界相對清晰的病變),並用於臨床診斷和管理。1) 即使對於高度色素沉著的腫瘤或伴有角膜混濁的眼內腫瘤,也能確定其後界,從而提高對鄰近結構浸潤的檢測準確性。
高褶虹膜難以與瞳孔阻滯型閉角青光眼鑑別,因為前房不淺(中央前房深度正常),裂隙燈檢查虹膜不向前膨隆。在暗室散瞳下通過超音波生物顯微鏡確認睫狀體前旋和睫狀溝消失是診斷的關鍵。
超音波生物顯微鏡本身是一種檢查設備,不進行治療。以下列出經超音波生物顯微鏡診斷的疾病的治療方法。
經超音波生物顯微鏡診斷的睫狀體分離,原則上選擇保守治療或外科再縫合/睫狀體固定術。
超音波生物顯微鏡使用高頻超音波(30–50 MHz)。物理原理如下。
超音波生物顯微鏡和前段光學同調斷層掃描(AS-OCT)作為前段成像設備互補使用。
| 項目 | UBM | AS-OCT |
|---|---|---|
| 原理 | 超音波(30–50 MHz) | 光(0.7–1.3 μm) |
| 接觸 | 接觸(有感染風險) | 非接觸 |
| 體位 | 仰臥位(基本) | 坐位(基本) |
| 睫狀體和虹膜背面 | 可觀察 | 不明確 |
| 眼底周邊部 | 可觀察到脈絡膜 | 困難 |
| 壓迫隅角檢查 | 可用眼杯進行 | 不可 |
| 角膜表層和淚液 | 不適合 | 有用 |
| 手術後立即 | 困難 | 可能 |
| 組織解析度(軸向) | 50~100 μm | 5~10 μm |
| 是否需要熟練操作者 | 高 | 低 |
超音波生物顯微鏡最大的優勢在於能夠可視化包括虹膜後方和睫狀體在內的結構。與AS-OCT相比,其缺點包括需要水浴浸沒法接觸眼球、影像獲取時間長、以及需要熟練的檢查者。
在腫瘤評估方面的差異:對於眼表鱗狀上皮腫瘤(OSSN),AS-OCT在顯示病變內部細節方面更具優勢。而對於無色素性虹膜腫瘤,超音波生物顯微鏡在確定病變後緣方面能力更強,且再現性更高。
閉角型青光眼的發生機制主要有兩種。
通過超音波生物顯微鏡術前鑑別這兩種機制,可以優化治療方案(單獨雷射虹膜切開術 vs. LI+LGP)。
超音波生物顯微鏡影像的自動定量分析軟體已經開發出來,能夠自動測量隅角開放距離、前房深度、水晶體拱高等參數。有望減少觀察者間和觀察者內的變異,提高診斷準確性。
在Yeilta等人的病例報告中,對於繼發於壞死性虹膜黑色素細胞瘤的色素播散性青光眼,使用超音波生物顯微鏡評估病變大小(5×3×2 mm),並採用虹膜睫狀體切除術合併青光眼分流術的外科管理被證明是有效的。1) 細針穿刺活檢(FNAB)的診斷率據報導為88-95%,超音波生物顯微鏡所見在鑑別黑色素細胞瘤和黑色素瘤中起輔助作用。
利用深度學習進行UBM影像隅角分類和自動診斷的研究正在進行中。有望應用於閉鎖性隅角青光眼的早期篩檢,但尚未實現臨床實施。4)
Yeilta YS, Oakey Z, Brainard J, Yeaney G, Singh AD. Necrotic iris melanocytoma with secondary glaucoma. Taiwan J Ophthalmol 2025;15:135–137.
Ritch R, Tham CC, Lam DS. Plateau iris syndrome. Ophthalmology 2004;111:1244–1246.
Gonzalez-Lopez F, Bilbao-Calabuig R, Mompean B, et al. Assessing vaulting changes after phakic collamer lens implantation by ultrasound biomicroscopy and optical coherence tomography. Eur J Ophthalmol 2016;26:36–41.
Jiang H, Wu Z, Lin Z, et al. Machine learning approaches to distinguish angle-closure from open-angle glaucoma using anterior segment features: a systematic review. Br J Ophthalmol 2022;106:1452–1458.