瞳孔ブロック型閉塞隅角
虹彩前方膨隆:後房圧が高まり虹彩が押し上げられる形態。
全体的な隅角狭小:Schwalbe線の部分から角膜側へ虹彩が押し付けられる。
暗所で隅角閉塞が増強:散瞳により悪化する様子を捉えられる。

超音波生体顕微鏡(Ultrasound Biomicroscopy; UBM)は、眼の前眼部(Anterior Segment)の画像診断に用いる検査装置である。1990年代初頭にFosterとPavlinによって、顕微鏡レベルの解像度で眼の断面図を得る手法として初めて導入された。
30〜50 MHzの高周波超音波を用いることで、細隙灯顕微鏡では観察できない前眼部構造(毛様体・虹彩裏面・隅角底)を高解像度で画像化する。高周波化により組織分解能は50〜100 μmに達し、前眼部の深さ5〜10 mmを評価するのに最適化されている。
一般的なBモード超音波(5〜10 MHz)と比較して、深達度は限られるが(5〜10 mm)、解像度が大幅に向上している。高周波は組織減衰が大きいため、脈絡膜より深い構造の評価には低周波Bモードが別途必要である。
UBMが特に有用な臨床場面を以下に示す。
通常のBモード超音波は5〜10 MHzで眼全体(前後径や網膜・脈絡膜など)を観察する。超音波生体顕微鏡は30〜50 MHzの高周波を用いることで、前眼部に特化した組織分解能50〜100 μmの高解像度画像を得る。ただし高周波ゆえ深達度は5〜10 mmに限られ、後部硝子体・網膜の観察には通常の超音波が必要となる。
UBM検査の基本手順を以下に示す。
プローブキャップを装着し水を注入して行う方法もある(アイカップ不要)。どのような体位でも検査が可能なため、通常の仰臥位が困難な患者にも対応できる。
メンブレン方式の超音波生体顕微鏡(例:UD-8060、トーメーコーポレーション)はアイカップを必要とせず、メンブレン先端にスコピゾール®を塗布して検査部位に当てる。坐位での検査が可能となった。
超音波生体顕微鏡は前房隅角の定量的測定が可能であり、以下のパラメータが標準的に用いられる。
| パラメータ | 定義 |
|---|---|
| AOD500(隅角開放距離) | 強膜突起から500 μm前方の線維柱帯と虹彩間の垂直距離 |
| ARA(隅角陥凹面積) | AODラインと隅角陥凹に囲まれた三角形の面積 |
| ACD(前房深度) | 中央角膜内皮から水晶体前面までの距離 |
| レンズボルト | 左右強膜突起を結ぶ垂直線より前方に位置する水晶体の距離 |
AOD500の詳細定義は「強膜突起から500 μm前方の線維柱帯と虹彩間の垂直距離」であり、強膜突起の正確な同定が測定精度を左右する。原発閉塞隅角緑内障(PACG)では、AOD500と前房深度が有意に減少しており、診断の助けとなる。
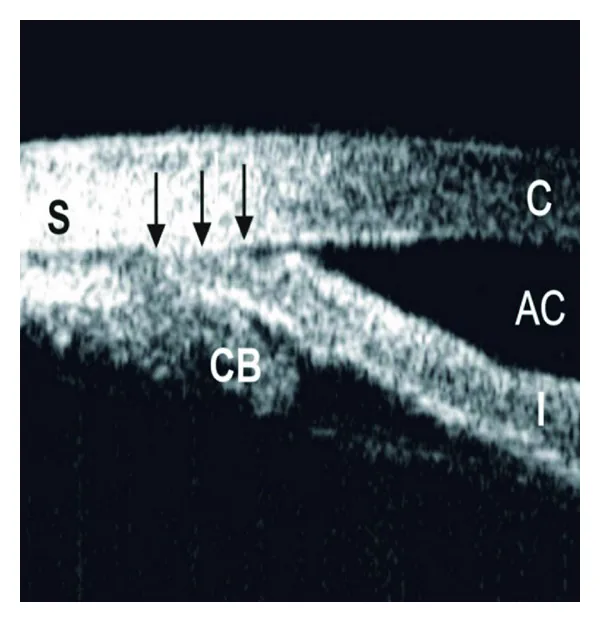
角膜前後面・強膜表面・虹彩前後面は高輝度として描出される。角膜実質・虹彩実質・毛様体は低輝度である。正常眼では虹彩は前方に軽度凸状もしくは平坦で、毛様体突起との間に毛様溝が確認できる。
前房隅角の観察では、強膜突起(scleral spur)とSchwalbe線の同定が不可欠である。強膜突起は前房内に突出した強膜の一部で、前方は線維柱帯に付着した構造であり、常に確認しうる重要な指標である。
瞳孔ブロック型閉塞隅角
虹彩前方膨隆:後房圧が高まり虹彩が押し上げられる形態。
全体的な隅角狭小:Schwalbe線の部分から角膜側へ虹彩が押し付けられる。
暗所で隅角閉塞が増強:散瞳により悪化する様子を捉えられる。
プラトー虹彩
虹彩彎曲なし:中央部虹彩は平坦で瞳孔ブロックは伴わない。
毛様体前方偏位・毛様溝消失:特徴的所見。毛様体が前方偏位し虹彩根部を機械的に押し上げる。
散瞳時に虹彩根部が隅角を閉塞:暗所散瞳下で閉塞が確認できる。
プラトー虹彩では前房の中央は比較的深く、虹彩中央部は平坦、虹彩根部は厚くて前房側に屈曲し、隅角底はスリット状に狭窄している。毛様体の前方偏位および毛様溝の消失が特徴的な所見である。
超音波生体顕微鏡による観察はレーザー虹彩切開術後でも解除されないプラトー虹彩の確定診断にきわめて有用である。レーザー虹彩切開術を施行しても眼圧が下降せず、あるいは散瞳で術前同様の隅角閉塞が確認されればプラトー虹彩の確定となる。診断のためだけにレーザー虹彩切開術を行うことは水疱性角膜症などのリスクから慎むべきで、超音波生体顕微鏡観察が推奨される。
原発閉塞隅角緑内障治療のためのレーザー虹彩切開術を受けた患者の約33%にプラトー虹彩が認められ、このグループは周辺虹彩前癒着形成や更なる隅角閉塞のリスクが高い。2)
悪性緑内障は毛様体前方回旋や硝子体腔内への房水異常流入などによって生じる硝子体の前方偏位に起因する閉塞隅角である。特発例もあるが、手術歴の有無とともにUBM所見を確認することが診断に不可欠である。
UBMでは以下の所見が認められる。
ICL(Implantable Collamer Lens)挿入後のVault(ICLと水晶体前面の間隙)はUBMで定量評価する。適正Vaultの範囲は機種・眼軸長によって異なるが、不足(<250 μm)では白内障進行リスクが、過剰(>1000 μm)では角膜内皮傷害・前房浅小化リスクが増加する。長期経過中のVault変化モニタリング(年1〜2回)にもUBMが用いられる。3)
外力による急激な前房内圧上昇により、隅角解離・虹彩離断・線維柱帯損傷・毛様体解離などが生じる。毛様体解離では上脈絡膜腔に房水が貯留していることが超音波生体顕微鏡で明瞭に描出される。
Yeiltaらは、超音波生体顕微鏡により5×3×2 mmの虹彩毛様体メラノサイトーマを描出し(境界が比較的明瞭な病変として確認)、臨床診断・管理に活用した症例を報告した。1) 高密度に色素沈着した腫瘍や前房内腫瘍で角膜混濁がある場合でも、後方境界を特定できるため隣接構造への浸潤検出精度が向上する。
プラトー虹彩は前房が浅くなく(中央前房深度は正常)、細隙灯顕微鏡でも虹彩が前膨隆せず平坦なため、瞳孔ブロック型閉塞隅角との鑑別が困難である。暗所散瞳下の超音波生体顕微鏡で毛様体前方偏位と毛様溝消失を確認することが診断の鍵となる。
超音波生体顕微鏡自体は検査装置であり、治療を行うものではない。超音波生体顕微鏡で診断された疾患の治療を以下に示す。
超音波生体顕微鏡で診断された毛様体解離は、原則として保存的治療または外科的再縫合・毛様体固定術が選択される。
超音波生体顕微鏡は高周波超音波(30〜50 MHz)を利用する。物理的原理を以下に示す。
超音波生体顕微鏡と前眼部光干渉断層計(AS-OCT)は、どちらも前眼部画像診断装置として相補的に用いられる。
| 項目 | UBM | AS-OCT |
|---|---|---|
| 原理 | 超音波(30〜50 MHz) | 光(0.7〜1.3 μm) |
| 接触 | 接触(感染リスクあり) | 非接触 |
| 体位 | 仰臥位(基本) | 坐位(基本) |
| 毛様体・虹彩裏面 | 観察可能 | 不明瞭 |
| 眼底周辺部 | 脈絡膜まで観察可能 | 困難 |
| 圧迫隅角検査 | アイカップで可能 | 不可 |
| 角膜表層・涙液 | 不向き | 有用 |
| 手術直後 | 困難 | 可能 |
| 組織分解能(軸方向) | 50〜100 μm | 5〜10 μm |
| 熟練者の必要性 | 高い | 低い |
超音波生体顕微鏡の最大の強みは虹彩後方・毛様体を含む構造の可視化である。AS-OCTと比較した欠点は、水浴浸漬法による眼への接触が必要なこと、画像取得に時間がかかること、熟練した検者が必要なことが挙げられる。
腫瘍評価においての違いとして、眼表面扁平上皮腫瘍(OSSN)ではAS-OCTが病変内部の詳細を示す点で優位性がある。一方、無色素性の虹彩腫瘍では超音波生体顕微鏡の方が病変の後方境界を特定する能力に優れ再現性も高い。
閉塞隅角緑内障の発生機序には主に2つがある。
超音波生体顕微鏡によりこれら2つの機序を術前に鑑別することで、治療方針(レーザー虹彩切開術単独 vs. LI+LGP)を最適化できる。
超音波生体顕微鏡画像の自動定量解析ソフトウェアが開発され、隅角開放距離・前房深度・レンズボルト等のパラメータを自動計測できるようになっている。検者間・検者内ばらつきの低減と診断精度の向上が期待される。
Yeiltaらの症例報告では、壊死性虹彩メラノサイトーマに続発した色素散布性緑内障に対し、超音波生体顕微鏡で病変サイズ(5×3×2 mm)を評価し、虹彩毛様体切除術と緑内障シャント術を組み合わせた外科的管理が有効であったことが示された。1) 細針吸引生検(FNAB)の診断率は88〜95%とされており、メラノサイトーマとメラノーマの鑑別に超音波生体顕微鏡所見が補助的役割を果たす。
ディープラーニングを用いたUBM画像の隅角分類・自動診断の研究が進行中である。閉塞隅角緑内障の早期スクリーニングへの応用が期待されているが、臨床実装には至っていない。4)
Yeilta YS, Oakey Z, Brainard J, Yeaney G, Singh AD. Necrotic iris melanocytoma with secondary glaucoma. Taiwan J Ophthalmol 2025;15:135–137.
Ritch R, Tham CC, Lam DS. Plateau iris syndrome. Ophthalmology 2004;111:1244–1246.
Gonzalez-Lopez F, Bilbao-Calabuig R, Mompean B, et al. Assessing vaulting changes after phakic collamer lens implantation by ultrasound biomicroscopy and optical coherence tomography. Eur J Ophthalmol 2016;26:36–41.
Jiang H, Wu Z, Lin Z, et al. Machine learning approaches to distinguish angle-closure from open-angle glaucoma using anterior segment features: a systematic review. Br J Ophthalmol 2022;106:1452–1458.