前房隅角支持型
代表例:AcrySof(Alcon)など
前房隅角に支持部を置く設計。角膜内皮細胞の慢性減少・瞳孔楕円化・核白内障が問題となり、現在は市場から撤退している。若年の屈折矯正には推奨されない。

有水晶体眼内レンズ(phakic intraocular lens; phakic IOL)は、水晶体を温存したまま眼内に挿入する屈折矯正用レンズである。角膜を削らないため角膜バイオメカニクスを保存でき、高度近視への矯正が可能である。取り出し可能な可逆性も特徴的な利点である。
phakic IOLは固定部位により3種類に分類される。
前房隅角支持型
代表例:AcrySof(Alcon)など
前房隅角に支持部を置く設計。角膜内皮細胞の慢性減少・瞳孔楕円化・核白内障が問題となり、現在は市場から撤退している。若年の屈折矯正には推奨されない。
虹彩固定型
後房型(ICL)
Visian ICL(STAAR Surgical):虹彩後面・水晶体前面の毛様溝に設置。
3.0mmの小切開で挿入可能。EVO/EVO+(中央孔付き)が現在の主流であり、安全性と有効性のエビデンスが最も豊富である。角膜内皮から離れており内皮細胞減少リスクが低い。
1986年にFyodorovが前房型を初報告した。後房型ICLはSTAAR Surgical社が1993年に開発を開始し、2005年に米国FDA承認を取得した。日本では2010年に承認され、2014年にEVO ICL(中央孔KS-AquaPORT付き)が承認された。2022年3月にはEVO/EVO+のFDA承認が得られ、世界で200万枚以上が使用されている1)。
後房型ICLはSTAAR Surgical社が開発した「コラマー(collamer)」素材で製造されている。
コラマーはガスと栄養素の透過性に優れ、炎症反応がきわめて少ない1)。
最新のEVO ICLは中央に直径0.36mmのポート(KS-Aquaport)を備えている。これにより以下の利点が生まれた。
適切な患者選択とインフォームドコンセントがphakic IOL手術の成功の鍵である。屈折矯正手術のガイドライン(第8版)では施術前のインフォームドコンセントの重要性を強調しており6)、以下の事項を説明する必要がある。
患者の職業・ライフスタイル・近視の程度・角膜形状・全身状態を包括的に評価した上で適応を判断する。
phakic IOLは成人の近視矯正を目的とした手術であり、近視進行を抑制するものではない。進行中の近視(成長期)には適応とならない。日本では近視管理用眼鏡(MiYOSMART®・Stellest®)や低濃度アトロピン点眼・オルソケラトロジーなどで小児期の近視進行を抑制した後、成人期に矯正が安定してからphakic IOLを検討することが理想的な流れである。
phakic IOL手術は一度行ったら終わりではなく、生涯にわたる継続的な経過観察が必要な手術である。屈折矯正手術のガイドライン(第8版)では術後の定期観察を推奨している6)。
モニタリング指標と間隔:
| 検査項目 | 術直後 | 術後1〜3か月 | 術後6か月 | 以後年1〜2回 |
|---|---|---|---|---|
| 裸眼・矯正視力 | 翌日 | 毎回 | 毎回 | 毎回 |
| 屈折検査 | 翌日 | 毎回 | 毎回 | 毎回 |
| vault測定(前眼部OCT) | 1週間後 | 毎回 | 毎回 | 毎回 |
| 角膜内皮細胞密度 | — | 1か月 | 6か月 | 年1回 |
| 眼圧 | 翌日(2時間後) | 毎回 | 毎回 | 毎回 |
| 隅角鏡検査 | — | vault過剰時 | — | 必要時 |
| 散瞳眼底検査 | — | 必要時 | 6か月 | 年1回 |
vaultは水晶体の加齢性膨隆により年単位で低下する傾向がある。特に40歳を超えると水晶体厚増加によりvaultが減少するため、フォローアップの強化が推奨される8)。角膜内皮細胞は後房型ICLでは比較的安定しているが、前房型の場合は慢性減少が起こりうるため継続した計測が必要である9)。
phakic IOL手術後の日常生活上の注意事項:
phakic IOL(有水晶体眼内レンズ)手術は日本では保険適用外(自由診療)である。費用は両眼で50〜70万円程度の施設が多い(施設・使用レンズにより異なる)。医療費控除の対象となる場合がある(屈折矯正のためのIC眼内レンズ手術が該当かは最新の国税庁の通達を確認)。視機能回復のための手術(円錐角膜等)では保険適用となる場合があるため、適応疾患については保険診療となりうることを確認する。
近視の世界的蔓延を背景に、phakic IOLを含む屈折矯正手術の需要は今後も増加すると予測される。小児期の近視管理(近視管理用眼鏡・オルソケラトロジー・アトロピン点眼等)で近視進行を抑制した後、成人になって度数が安定した段階でphakic IOLや角膜屈折矯正手術を選択するという「two-stage approach」が理想的とされる。高度近視眼では特に網膜合併症(裂孔・剝離・近視性黄斑症)のリスクがあるため、術前・術後の眼底管理も欠かせない。眼鏡・コンタクトレンズ・屈折矯正手術を患者のニーズ・眼の状態・ライフスタイルに応じて最適に組み合わせることが、現代の屈折矯正医療の目標である。
屈折矯正手術のガイドライン(第8版)に基づく適応基準を示す6)。
| 項目 | 基準 |
|---|---|
| 年齢 | 原則21-45歳(老視年齢では慎重に施術) |
| 矯正量 | 6D以上の近視を主な対象 |
| 中等度近視(3-6D未満) | 慎重適応 |
| 強度近視(15D超) | 慎重適応 |
| 前房深度(ICL) | ≥2.8mm(角膜内皮から3.0mm以上) |
| 乱視(Toric ICL) | 1.0D〜4.0D |
米国FDA承認に基づくVisian ICLの適応は21〜45歳・眼鏡面で-3.0D〜-20.0D・前房深度3.0mm以上である1)。
以下の場合はphakic IOLの適応外となる6)。
以下の場合は慎重に適応を検討する6)。
矯正量6D未満の中等度以下の近視では、角膜屈折矯正手術(LASIK/SMILE)が一般的な選択肢となる。6D以上の高度近視や角膜厚不足例ではphakic IOLが有利である。
| 比較項目 | phakic IOL | LASIK | SMILE |
|---|---|---|---|
| 適応近視範囲 | 〜20D | 〜10D | 〜10D |
| 角膜バイオメカニクス | 保存 | 変化あり | LASIK比で保存 |
| 可逆性 | あり(取り出し可能) | なし | なし |
| ドライアイリスク | 低い | 高い | 中程度 |
| 角膜拡張リスク | なし | あり | 低い |
| 将来の白内障手術 | IOL度数計算に影響なし | 計算誤差生じうる | 計算誤差生じうる |
角膜バイオメカニクスを保存できるため、LASIK・SMILEと比較してバイオメカニクス変化が少ないとされる7)。これはPost-refractive ectasia(角膜拡張症)のリスク回避につながる重要な優位点である。
ガイドライン(第8版)に基づく術前スクリーニング13項目を示す6)。
| No. | 検査項目 | 目的 |
|---|---|---|
| ① | 視力検査 | 裸眼・矯正視力の確認 |
| ② | 屈折値測定 | 球面・円柱度数・軸の確定 |
| ③ | 角膜曲率測定 | 角膜形状の把握 |
| ④ | 細隙灯顕微鏡検査 | 前眼部病変の除外 |
| ⑤ | 角膜形状解析 | 円錐角膜等の不正乱視評価 |
| ⑥ | 角膜厚測定 | 角膜内皮との距離算定に必要 |
| ⑦ | 涙液検査 | ドライアイの評価 |
| ⑧ | 眼底検査 | 網膜・硝子体・視神経の確認 |
| ⑨ | 眼圧測定 | 緑内障等の除外 |
| ⑩ | 瞳孔径測定(暗所) | ハロー・グレアリスクの評価 |
| ⑪ | 角膜径(WTW)測定 | ICLサイズ決定の基準 |
| ⑫ | 角膜内皮細胞検査 | 年齢別下限値との照合 |
| ⑬ | 前眼部画像解析 | 前房深度・毛様溝径の計測 |
水平角膜径(white-to-white; WTW)はICLサイズ決定に必須の指標である。前眼部OCTやUBMによる毛様溝径(sulcus-to-sulcus: STS)の直接計測はWTWノモグラム単独よりもvault予測精度が高く、推奨される11)。ICLのサイズは13.2mm・13.7mm・14.0mm・14.5mmの4種類があり、適切なサイズ選択がvault管理の鍵となる。
虹彩固定型(Artisan)の度数計算:Van der Hejdeノモグラムを使用し、屈折値・角膜屈折力・前房深度から度数を計算する9)。
EVO ICLは中央孔を有するため、周辺虹彩切開は不要である。従来モデル(中央孔なし)では手術2-3週間前に上方2箇所にNd:YAGレーザー虹彩切開術を行っていた1)。
理想的な中心vault(ICLと水晶体前面の間隙)は250-750μmである2)。
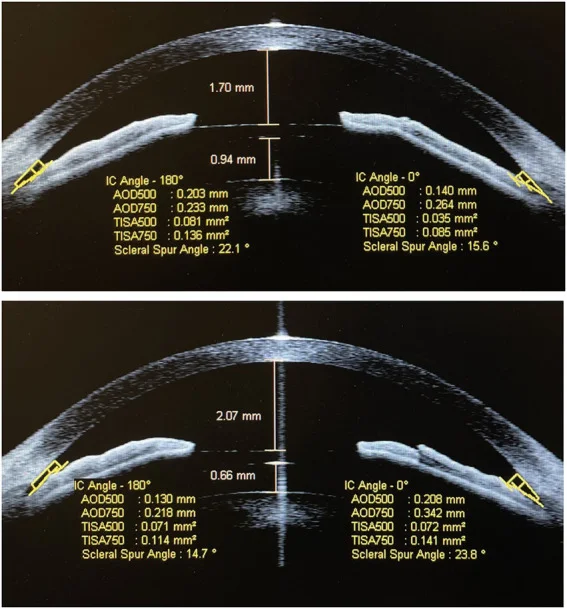
vault異常が検出された場合はICLのサイズ変更・交換が必要になる。
両眼同時手術は可能である。ただし、感染リスクが高いと判断された症例では、片眼ずつ施術することが望ましい6)。術後に一過性眼圧上昇が起こりうるため、手術当日は2時間以上の経過観察を行う。
術後合併症の全体像を以下に示す6)。EVO ICLの6か月時の角膜内皮細胞減少率は平均2.2%1)、8年後の追跡では3.6±7.9%と安定化が確認されている8)。
長期成績の概要:
| 合併症 | 特徴・機序 | 対応 |
|---|---|---|
| 感染性眼内炎 | 最重篤。高度バリアプレコーションズで予防 | 緊急硝子体手術・抗菌薬 |
| ハロー・グレア | 光学帯より瞳孔径が大きい場合に出現 | 術前暗所瞳孔径測定で評価 |
| 角膜内皮障害 | 前房型で特にリスク高い | 定期内皮細胞計測・前房型では経過観察 |
| 一過性眼圧上昇 | OVD残留・ステロイドレスポンス | OVD除去・ステロイド減量・IOP降下薬 |
| 白内障 | vault低下による水晶体接触 | ICLサイズ変更・白内障手術 |
| 閉塞隅角緑内障 | vault過大→虹彩前方偏位 | ICL交換・レーザー虹彩切開 |
| 網膜剝離 | 高度近視眼素因+手術侵襲 | 術前網膜精査・必要時予防的光凝固 |
| 光視症 | 虹彩切開/切除部由来 | EVO ICLで軽減 |
EVO ICLの6ヶ月時の角膜内皮細胞減少率は平均2.2%であった1)。8年後の追跡では減少率3.6±7.9%と安定化が報告されている1)。
ガイドライン(第8版)に基づき、視力・屈折・vault・角膜内皮細胞密度・眼圧・眼底を術後1日・1週間・1か月・3か月・6か月に確認し、以後6〜12か月ごとに生涯継続する6)。vault値は加齢とともに水晶体の膨隆(thickening)により経時的に低下する傾向があるため、40歳以降は特に注意が必要である。
術後早期の眼圧上昇には複数の原因がある2)。
| 合併症 | 発生率 | 対応 |
|---|---|---|
| 一過性眼圧上昇(OVD残留) | 約18%(術後1〜6時間)1) | 自然改善、必要時降圧薬 |
| TASS | 0.24%(827眼中2眼)3) | ステロイド全身・局所投与 |
| 感染性眼内炎 | 0.017〜0.036%4) | 緊急抗菌薬硝子体注射 |
| 前房出血 | 稀(虹彩毛様体嚢胞破裂) | 保存的治療5) |
| 前嚢下白内障 | EVO ICLで0%1) | ICLサイズ変更・白内障手術 |
| ハロー・グレア | 約5〜15% | 術前評価・光学帯サイズ選択 |
| 網膜剝離 | 高近視眼に増加 | 術前網膜精査・必要時予防的光凝固 |
Liら(2023)はphakic IOL手術後1週間で発症した遅発性TASS 2例を報告した3)。角膜後面のKPと前房内フィブリン形成を認めたが、ステロイド全身・局所投与(プレドニゾロン0.5 mg/kg内服+1%点眼1時間毎)を4-5週間行い改善した。発生率は0.24%(827眼中2眼)であった。
Zhengら(2023)はphakic IOL術後20日目に発症したStaphylococcus epidermidis眼内炎の1例を報告した4)。硝子体注射(バンコマイシン1 mg+セフタジジム2 mg)を2回施行し、ICL摘出や硝子体手術なしで視力22/20まで回復した。発生率は約0.017-0.036%と推定されている。
コラマーはきわめて高い生体適合性を持つ。スペキュラーマイクロスコピーとレーザーフレアセルメーターによる検査で炎症反応がないことが確認されている1)。コラーゲン含有により生体組織との親和性が高く、ガスと代謝産物の透過性に優れている。
コラマーの物性:
ICLの光学部は水晶体の上方にアーチ状に架かる形で配置される。水晶体との間のvaultが適切に維持されることで、房水が水晶体表面を流れ白内障形成を防ぐ。
EVO ICLの中央ポート(KS-Aquaport)は後房から前房への生理的な房水の流れを可能にする。これにより瞳孔ブロックの予防・水晶体への栄養供給維持・前嚢下白内障リスク低減が得られる。
FDA試験では99.7%の眼で満足なvaultが得られ、閉塞隅角・色素散布・前嚢下白内障の発生は0件であった1)。
phakic IOLは角膜を切削しないため、角膜バイオメカニクスを保存できる。LASIKやSMILEと比較してバイオメカニクス変化が少ないとされる7)。これはPost-refractive ectasia(角膜拡張症)のリスク回避につながる重要な優位点である。
角膜バイオメカニクス指標の術後変化:
| 指標 | phakic IOL | LASIK | SMILE |
|---|---|---|---|
| 角膜ヒステリシス(CH) | 変化なし | 有意低下 | LASIK比で保存 |
| 角膜抵抗係数(CRF) | 変化なし | 有意低下 | LASIK比で保存 |
| 後面角膜エレベーション | 変化なし | 上昇あり | 軽度の変化 |
角膜バイオメカニクスの保存は、将来の角膜拡張症リスク(Post-refractive ectasia)の予防にとって重要な優位点である7)。phakic IOLは将来的に白内障手術が必要になった場合でも、角膜形状が変化していないためIOL度数計算が通常通り行える。
Toric ICL(乱視矯正用ICL)は近視と乱視を同時に矯正できる。術後の軸回旋(rotation)が矯正効果に影響するため、正確な軸合わせが重要である5)。アルフォンソらの5年追跡では、Toric ICLの長期的な軸安定性と良好な屈折予測性が確認されている10)。乱視1.0〜4.0Dが主な適応範囲であり(日本眼科学会ガイドライン)6)、これを超える高度乱視では術後残余乱視が生じやすい。
後房型phakic IOLの8年間追跡研究では、等価球面度数の安定した長期予測性が確認されている8)。角膜内皮細胞密度は年間0.5〜1.0%の自然減少に加え、phakic IOL関連の追加減少が生じる(前房型で顕著、後房型では軽微)9)。vaultは加齢に伴う水晶体膨隆で経時的に低下傾向にあるため、定期的なvaultモニタリングが必要である。
白内障発生率はEVO ICL以前のモデルで5年間約2〜5%であったが、EVO ICLではvault改善により低下傾向にある1)。5年間追跡研究でも長期的な有効性と安全性が報告されている10)。
phakic IOL挿入後に白内障手術が必要となった場合の処理として、ESCRSガイドラインでは虹彩固定型の場合に虹彩損傷の有無・周辺虹彩切開の開通性・角膜内皮細胞密度と形態の確認を推奨している12)。後房型ICLは摘出してから通常の白内障手術を行い、IOL度数計算は屈折矯正手術前のデータを用いる。
前眼部OCT・UBMのデータをAIで解析し、最適なvaultを予測するシステムの研究が進められている。従来のノモグラム(WTW+ACD)を超える精度が期待されている。Sunら(2023年)は高vault症例に対してICLを90°回転させることで平均vault 1,249μmから459μmへの改善を報告した13)。
近視の世界的拡大により、phakic IOLの需要は今後も増加すると予測される。2050年には世界人口の49億人が近視、9.4億人が強度近視になると報告されており14)、高度近視の屈折矯正手術としてphakic IOLの役割は増大している。Packerのメタアナリシス(2016年)では中央孔設計(EVO)ICLが非中央孔比較で前嚢下白内障・閉塞隅角・瞳孔ブロックのリスクを有意に低減することが確認された15)。
Toric ICLは近視と乱視を一度の手術で矯正する。術後軸回旋(回旋偏位)の管理が臨床上の課題であるが、安定した長期成績が報告されている10)。
2020年7月にCEマーク承認を取得した革新的なphakic IOLである。非球面の焦点深度拡張型(EDOF)光学系を備え、近方および中間視力の矯正を提供する。21-60歳が対象年齢で、米国ではFDA承認待ちの段階である1)。
ICL挿入後に残余屈折誤差を角膜屈折矯正手術(LASIK/PRK)でタッチアップする「bioptics」と呼ばれる方法が一部施設で実施されている。強度近視への対応幅を広げる可能性が検討されている。phakic IOLは角膜バイオメカニクスを保存するため、角膜屈折矯正術の前段階としても好適とされる。
拡張焦点深度(EDOF)型・多焦点型の光学設計を持つ次世代phakic IOLの開発が進行中である。
前眼部OCT・UBMのデータをAIで解析し、最適なvaultを予測するシステムの研究が進められている。従来のWTW+ACDノモグラムを超える予測精度が期待される。術前の前眼部解析データを機械学習モデルに入力することで個別化されたレンズサイズ選択が可能になると考えられている。