กล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ (UBM ) คือการตรวจภาพตัดขวางส่วนหน้าของลูกตาโดยใช้อัลตราซาวนด์ความถี่สูง (30-50 MHz) พัฒนาโดย Foster และ Pavlin ในช่วงต้นทศวรรษ 1990
ความละเอียดเนื้อเยื่อ 50-100 μm เพื่อมองเห็นส่วนหน้า (ความลึก 5-10 มม.)
สามารถมองเห็นโครงสร้างที่ไม่สามารถสังเกตได้ด้วยระบบแสง (รวมถึง AS-OCT ) เช่น ด้านหลังม่านตา ซิลิอารีบอดี และช่องหลัง
มีประโยชน์โดยเฉพาะในการวินิจฉัยต้อหินมุมปิด (แยกความแตกต่างระหว่าง pupillary block กับ plateau iris) ต้อหินชนิดร้าย การบาดเจ็บส่วนหน้า เนื้องอกส่วนหน้า และการประเมิน vault หลัง ICL
เป็นการตรวจแบบสัมผัส (ต้องนอนหงาย หยอดยาชา และใช้ถ้วยครอบตา) และต้องใช้ความชำนาญ ซึ่งเป็นข้อเสียเมื่อเทียบกับ AS-OCT
สามารถประเมินการปิดมุมเชิงหน้าที่แบบไดนามิกโดยการถ่ายภาพเปรียบเทียบในสภาพสว่างและมืด
การใช้เสริมกับ AS-OCT ช่วยเพิ่มความแม่นยำในการวินิจฉัยส่วนหน้า
การตรวจด้วยคลื่นเสียงความถี่สูงแบบจุลทรรศน์ (Ultrasound Biomicroscopy; UBM ) เป็นเครื่องมือวินิจฉัยที่ใช้ในการถ่ายภาพส่วนหน้าของดวงตา (Anterior Segment) ถูกนำมาใช้ครั้งแรกในช่วงต้นทศวรรษ 1990 โดย Foster และ Pavlin เพื่อให้ได้ภาพตัดขวางของดวงตาที่มีความละเอียดระดับจุลทรรศน์
โดยใช้คลื่นเสียงความถี่สูง 30-50 MHz ทำให้สามารถถ่ายภาพโครงสร้างส่วนหน้า (ซิลิอารีบอดี , ผิวด้านหลังของม่านตา , และก้นมุม) ซึ่งไม่สามารถสังเกตได้ด้วยกล้องจุลทรรศน์ชนิดกรีด (slit lamp) ได้ด้วยความละเอียดสูง ความถี่สูงให้ความละเอียดเนื้อเยื่อ 50-100 ไมโครเมตร ซึ่งเหมาะสมที่สุดสำหรับการประเมินความลึก 5-10 มม. ของส่วนหน้า
เมื่อเปรียบเทียบกับอัลตราซาวนด์ B-mode ทั่วไป (5-10 MHz) ความลึกในการทะลุทะลวงมีจำกัด (5-10 มม.) แต่ความละเอียดดีขึ้นอย่างมาก เนื่องจากความถี่สูงมีการลดทอนของเนื้อเยื่อมาก การประเมินโครงสร้างที่ลึกกว่าคอรอยด์ จึงจำเป็นต้องใช้ B-mode ความถี่ต่ำแยกต่างหาก
ต่อไปนี้เป็นสถานการณ์ทางคลินิกที่ UBM มีประโยชน์เป็นพิเศษ:
การประเมินสัณฐานวิทยาของมุมในโรคต้อหินมุมปิด (PACG ) : การแยกความแตกต่างระหว่างชนิดบล็อกรูม่านตา , ม่านตา แบบที่ราบสูง (plateau iris), และการอุดตันจากเลนส์ตาการวินิจฉัยโรคต้อหินชนิดร้าย (malignant glaucoma) : การยืนยันการหมุนไปข้างหน้าของซิลิอารีบอดี และการเคลื่อนไปข้างหน้าของวุ้นตา การประเมินเนื้องอกของซิลิอารีบอดี และม่านตา : การกำหนดขอบเขต, ความลึกของการแทรกซึม, และขอบเขตด้านหลังการประเมินก่อนและหลังการใส่ ICL (เลนส์แก้วตาเทียม ชนิดเฟคิก) : การวัด vault (ช่องว่างระหว่างเลนส์ตาและ ICL )การบาดเจ็บที่ส่วนหน้า : การประเมินมุมฉีกขาด (angle recession ), ม่านตาฉีกขาด (iridodialysis ), และซิลิอารีบอดี ฉีกขาด (cyclodialysis)ม่านตาอักเสบ (uveitis)ซิลิอารีบอดี หลังการผ่าตัดต้อหิน : การประเมินโครงสร้างภายในของตุ่มกรอง (filtering bleb)
Q
การตรวจด้วยคลื่นเสียงความถี่สูงแบบจุลทรรศน์แตกต่างจากการตรวจอัลตราซาวนด์ทั่วไปอย่างไร?
A
อัลตราซาวนด์ B-mode ทั่วไปใช้ความถี่ 5-10 MHz เพื่อสังเกตดวงตาทั้งหมด (เส้นผ่านศูนย์กลางหน้า-หลัง, จอประสาทตา , คอรอยด์ ฯลฯ) การตรวจด้วยคลื่นเสียงความถี่สูงแบบจุลทรรศน์ใช้ความถี่สูง 30-50 MHz เพื่อให้ได้ภาพความละเอียดสูงที่มีความละเอียดเนื้อเยื่อ 50-100 ไมโครเมตร ซึ่งเฉพาะทางสำหรับส่วนหน้า อย่างไรก็ตาม เนื่องจากความถี่สูง ความลึกในการทะลุทะลวงจึงจำกัดอยู่ที่ 5-10 มม. และการสังเกตวุ้นตา ส่วนหลังและจอประสาทตา จำเป็นต้องใช้อัลตราซาวนด์ทั่วไป
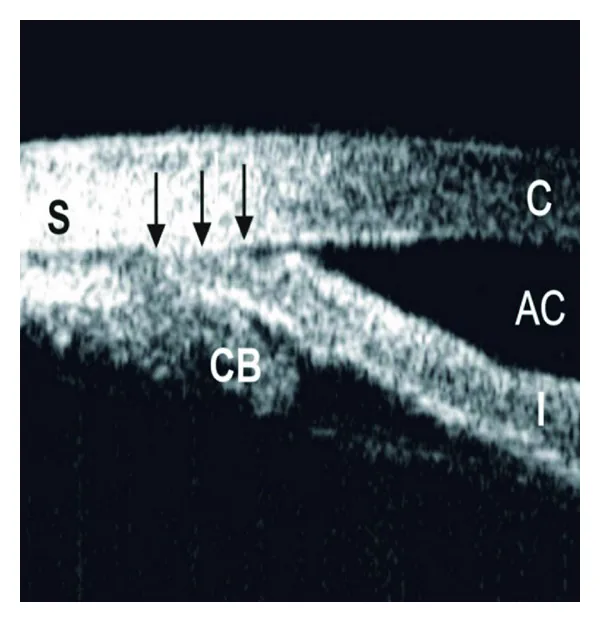
ภาพอัลตราซาวนด์ชีวกล้อง (UBM) แสดงการยึดติดของม่านตาส่วนหน้า (PAS) Dorairaj S, et al. Changing trends of imaging in angle closure evaluation. ISRN Ophthalmol. 2012. Figure 4. PM
CI D: PMC3914273. License: CC BY.
ภาพอัลตราซาวนด์ชีวกล้อง (UBM ) แสดงการยึดติดของม่านตา ส่วนหน้า (PAS ) S: ตาขาว , CB: ซิลิอารีบอดี , AC: ช่องหน้าม่านตา , I: ม่านตา , C: กระจกตา , และลูกศรสีดำแสดงขอบเขตของ PAS สอดคล้องกับการยึดติดของม่านตา ส่วนหน้าที่กล่าวถึงในหัวข้อ “2. เทคนิคและขั้นตอนการตรวจ”
ขั้นตอนพื้นฐานของการตรวจ UBM มีดังนี้:
หยอดยาชาเฉพาะที่ (oxybuprocaine 0.4%)
เติมน้ำหรือ Scopisol (methylcellulose ฯลฯ) ลงในถ้วยครอบตา
ให้ผู้ป่วยนอนหงายและติดถ้วยครอบตาเข้ากับดวงตา
จุ่มปลายหัววัดลงในของเหลวแล้วสแกน (ระวังอย่าสัมผัสลูกตาโดยตรง)
หันหัววัดไปในทิศทางต่างๆ เพื่อถ่ายภาพมุมช่องหน้าม่านตา และซิลิอารีบอดี โดยรอบ
ถ่ายภาพในสภาวะ สว่างและมืด เพื่อประเมินการเปลี่ยนแปลงรูปร่างของม่านตา (การอุดตันเชิงหน้าที่) จากการขยายรูม่านตา
นอกจากนี้ยังมีวิธีใส่ปลอกครอบหัววัดและฉีดน้ำ (ไม่ต้องใช้ถ้วยครอบตา) สามารถตรวจในท่าใดก็ได้ จึงเหมาะสำหรับผู้ป่วยที่ไม่สามารถนอนหงายได้
เครื่องอัลตราซาวนด์ชีวกล้องแบบเมมเบรน (เช่น UD-8060, Tomey Corporation) ไม่ต้องใช้ถ้วยครอบตา ทา Scopisol® ที่ปลายเมมเบรนแล้ววางลงบนบริเวณที่ตรวจ ทำให้สามารถตรวจในท่านั่งได้
คุณลักษณะที่ใหญ่ที่สุดของกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์คือความสามารถในการถ่ายภาพตัดขวางของมุมในที่มืด การถ่ายภาพทั้งในที่สว่างและมืดช่วยให้สามารถประเมินการเปลี่ยนแปลงรูปร่างของม่านตา จากการขยายม่านตา (การกระตุ้นให้เกิดมุมปิด) ได้แบบไดนามิก การเปรียบเทียบสว่าง-มืดนี้เป็นขั้นตอนที่จำเป็นในการประเมินการปิดแบบหน้าที่
กล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์สามารถวัดเชิงปริมาณของมุมช่องหน้าม่านตา ได้ และใช้พารามิเตอร์ต่อไปนี้เป็นมาตรฐาน
พารามิเตอร์ คำจำกัดความ AO D500 (ระยะเปิดมุม)ระยะตั้งฉากระหว่าง trabecular meshwork และม่านตา ที่ 500 ไมโครเมตรด้านหน้าของ scleral spur ARA (พื้นที่ร่องมุม) พื้นที่สามเหลี่ยมที่ล้อมรอบด้วยเส้น AO D และร่องมุม ACD (ความลึกช่องหน้าม่านตา ) ระยะจาก endothelium กระจกตา ส่วนกลางถึงผิวหน้าของเลนส์ Lens vault ระยะของเลนส์ที่อยู่ด้านหน้าเส้นแนวตั้งที่เชื่อม scleral spur ซ้ายและขวา
คำจำกัดความโดยละเอียดของ AO D500 คือ “ระยะตั้งฉากระหว่าง trabecular meshwork และม่านตา ที่ 500 ไมโครเมตรด้านหน้าของ scleral spur” และการระบุ scleral spur ที่แม่นยำมีผลต่อความแม่นยำในการวัด ในโรคต้อหินมุมปิดปฐมภูมิ (PACG ) ค่า AO D500 และความลึกช่องหน้าม่านตา ลดลงอย่างมีนัยสำคัญ ซึ่งช่วยในการวินิจฉัย
พื้นผิวด้านหน้าและด้านหลังของกระจกตา พื้นผิวตาขาว และพื้นผิวด้านหน้าและด้านหลังของม่านตา จะถูกแสดงเป็น ความสว่างสูง ส่วนเนื้อกระจกตา เนื้อม่านตา และซิลิอารีบอดี ้เป็น ความสว่างต่ำ ในตาปกติ ม่านตา จะนูนไปข้างหน้าเล็กน้อยหรือแบน และสามารถมองเห็นร่องซิลิอารีระหว่างม่านตา กับซิลิอารีโพรเซส
ในการสังเกตมุมห้องหน้าตา การระบุ สเคลอรัล สเปอร์ (scleral spur) และ เส้นชวาลเบ (Schwalbe line) เป็นสิ่งจำเป็น สเคลอรัล สเปอร์เป็นส่วนหนึ่งของตาขาว ที่ยื่นเข้าไปในห้องหน้าตา ยึดติดกับทราบีคิวลาด้านหน้า และเป็นตัวบ่งชี้สำคัญที่สามารถยืนยันได้เสมอ
มุมปิดชนิดบล็อกรูม่านตา
การโป่งของม่านตา ไปข้างหน้า : รูปแบบที่ม่านตา ถูกดันไปข้างหน้าเนื่องจากความดันในห้องหลังตาเพิ่มขึ้น
การตีบแคบของมุมโดยรวม : ม่านตา ถูกกดไปทางกระจกตา จากบริเวณเส้นชวาลเบ
การปิดมุมที่เพิ่มขึ้นในที่มืด : สามารถสังเกตการแย่ลงได้เมื่อรูม่านตา ขยาย
ม่านตาแบบที่ราบสูง (Plateau Iris)
ไม่มีความโค้งของม่านตา : ม่านตา ส่วนกลางแบนและไม่มีบล็อกรูม่านตา
การเคลื่อนของซิลิอารีบอดี ้ไปข้างหน้าและการหายไปของร่องซิลิอารี : ผลการตรวจที่จำเพาะ ซิลิอารีบอดี ้เคลื่อนไปข้างหน้าและดันรากม่านตา โดยกลไก
การปิดมุมโดยรากม่านตา เมื่อรูม่านตา ขยาย : สามารถยืนยันการปิดได้ภายใต้การขยายรูม่านตา ในที่มืด
ในม่านตา แบบที่ราบสูง ห้องหน้าตาส่วนกลางค่อนข้างลึก ม่านตา ส่วนกลางแบน รากม่านตา หนาและโค้งไปทางห้องหน้าตา และก้นมุมแคบเป็นร่อง การเคลื่อนของซิลิอารีบอดี ้ไปข้างหน้าและการหายไปของร่องซิลิอารีเป็นผลการตรวจที่จำเพาะ
การสังเกตด้วยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพมีประโยชน์อย่างมากในการวินิจฉัยที่แน่นอนของม่านตา แบบที่ราบสูงที่ไม่หายไปแม้หลังการตัดม่านตาด้วยเลเซอร์ หากความดันลูกตา ไม่ลดลงหลังการตัดม่านตาด้วยเลเซอร์ หรือหากยืนยันการปิดมุมที่คล้ายกับก่อนผ่าตัดเมื่อรูม่านตา ขยาย ก็จะยืนยันม่านตา แบบที่ราบสูง ควรหลีกเลี่ยงการตัดม่านตาด้วยเลเซอร์ เพียงเพื่อการวินิจฉัยเนื่องจากความเสี่ยงของโรคกระจกตาพุพอง และแนะนำให้สังเกตด้วยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ
พบม่านตา แบบที่ราบสูงในประมาณ 33% ของผู้ป่วยที่ได้รับการตัดม่านตาด้วยเลเซอร์ เพื่อรักษาต้อหินมุมปิดปฐมภูมิ และกลุ่มนี้มีความเสี่ยงสูงต่อการเกิดพังผืดยึดม่านตา ส่วนปลายด้านหน้าและการปิดมุมเพิ่มเติม 2)
โรคต้อหินชนิดร้าย เป็นมุมปิดที่เกิดจากการเคลื่อนของวุ้นตา ไปข้างหน้าอันเนื่องมาจากการหมุนของซิลิอารีบอดี ไปข้างหน้าหรือการไหลของอารมณ์ขันที่เป็นน้ำผิดปกติเข้าไปในโพรงวุ้นตา แม้จะมีกรณีที่ไม่ทราบสาเหตุ การตรวจผล UBM ร่วมกับประวัติการผ่าตัดเป็นสิ่งจำเป็นสำหรับการวินิจฉัย
ในการตรวจ UBM จะพบผลดังต่อไปนี้:
การหมุนของซิลิอารีบอดี ไปข้างหน้า : ซิลิอารีบอดี เคลื่อนไปข้างหน้า ดันม่านตา และซิลิอารีบอดี ไปยังเลนส์หรือวุ้นตา การเคลื่อนของวุ้นตา ไปข้างหน้า : อารมณ์ขันที่เป็นน้ำสะสมในโพรงวุ้นตา และวุ้นตา ทั้งหมดเคลื่อนไปข้างหน้าการปิดมุมโดยรอบ : มุมปิดโดยรอบโดยไม่แสดงลักษณะของบล็อกรูม่านตา
Vault (ช่องว่างระหว่าง ICL และผิวหน้าของเลนส์) หลังการใส่ ICL (เลนส์คอลลาเมอร์ที่ปลูกฝังได้) จะถูกประเมินเชิงปริมาณด้วย UBM ช่วง vault ที่เหมาะสมจะแตกต่างกันไปตามรุ่นและความยาวแกนตา แต่การขาด (<250 μm) เพิ่มความเสี่ยงต่อการลุกลามของต้อกระจก ในขณะที่มากเกินไป (>1000 μm) เพิ่มความเสี่ยงต่อความเสียหายของเอ็นโดทีเลียมกระจกตา และความตื้นของช่องหน้าม่านตา UBM ยังใช้ในการติดตามการเปลี่ยนแปลงของ vault ในระยะยาว (ปีละ 1-2 ครั้ง) 3)
ความดันในช่องหน้าม่านตา ที่เพิ่มขึ้นอย่างกะทันหันจากแรงภายนอกทำให้เกิดการฉีกขาดของมุมตา ม่านตาฉีกขาด ความเสียหายของ trabecular meshwork และการแยกตัวของซิลิอารีบอดี ในการแยกตัวของซิลิอารีบอดี การสะสมของอารมณ์ขันที่เป็นน้ำในช่องเหนือคอรอยด์ จะเห็นได้ชัดเจนด้วยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ
Yeilta และคณะรายงานกรณีที่ melanocytoma ของม่านตา และซิลิอารีบอดี ขนาด 5×3×2 มม. ถูกแสดงภาพด้วยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (เป็นรอยโรคที่มีขอบเขตค่อนข้างชัดเจน) และใช้ในการวินิจฉัยและการจัดการทางคลินิก 1) แม้ในเนื้องอกที่มีเม็ดสีหนาแน่นหรือเนื้องอกในช่องหน้าม่านตา ที่มีกระจกตา ขุ่น สามารถระบุขอบเขตด้านหลังได้ ซึ่งช่วยเพิ่มความแม่นยำในการตรวจหาการลุกลามไปยังโครงสร้างข้างเคียง
Q
ทำไมม่านตาแบบที่ราบสูงจึงวินิจฉัยได้ยาก?
A
ในม่านตา แบบที่ราบสูง ช่องหน้าม่านตา ไม่ตื้น (ความลึกช่องหน้าม่านตา ส่วนกลางปกติ) และม่านตา ไม่โป่งไปข้างหน้าแม้ภายใต้กล้องจุลทรรศน์ชนิดกรีด ทำให้แยกจากมุมปิดชนิดบล็อกรูม่านตา ได้ยาก การยืนยันการหมุนของซิลิอารีบอดี ไปข้างหน้าและการหายไปของซิลิอารีซัลคัสด้วยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพภายใต้การขยายม่านตา ในที่มืดเป็นกุญแจสำคัญในการวินิจฉัย
กล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์เป็นเครื่องมือตรวจวินิจฉัย ไม่ใช่การรักษา การรักษาโรคที่วินิจฉัยด้วยกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์แสดงไว้ด้านล่าง
การตัดม่านตาด้วยเลเซอร์ (LPI /LI)การผ่าตัดต้อกระจก : การเปลี่ยนเลนส์แก้วตาเทียม จะเพิ่มความลึกของช่องหน้า ซึ่งคาดว่าจะทำให้มุมเปิดกว้างขึ้น
การสร้างมุมด้วยเลเซอร์ (LGP ) : ทางเลือกแรก การหดตัวด้วยความร้อนรอบม่านตา จะทำให้มุมเปิดกว้างขึ้นการตัดม่านตาด้วยเลเซอร์ (LI)รูม่านตา จากนั้นเพิ่ม LGP การผ่าตัดต้อกระจก : บ่งชี้เมื่อมีต้อกระจก ร่วมด้วยยาหยอดพิโลคาร์พีน : การรักษาแบบประคับประคอง ผลไม่แน่นอน ต้องระวังผลข้างเคียงจากการใช้ระยะยาว (การขยายตัวไม่ดี การยึดติดของม่านตา ด้านหลัง การลุกลามของต้อกระจก )
การจี้ทำลายซิลิอารีบอดี ้ (การทำลายซิลิอารีบอดี้ ) : หากยืนยันการหมุนไปข้างหน้าของซิลิอารีบอดี ้การผ่าตัดวุ้นตา : เมื่อวุ้นตา เคลื่อนไปข้างหน้าเป็นหลัก การตัดวุ้นตา ออกเพื่อสร้างทางเดินการไหลของอารมณ์ขันน้ำปกติขึ้นใหม่
สำหรับซิลิอารีบอดี ้ฉีกขาดที่วินิจฉัยด้วยกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ โดยหลักการแล้วจะเลือกการรักษาแบบประคับประคองหรือการเย็บซ้ำด้วยการผ่าตัด/การตรึงซิลิอารีบอดี ้
Vault ไม่เพียงพอ : เปลี่ยน ICL (ขนาดใหญ่ขึ้น) หรือผ่าตัดต้อกระจก เร็วVault มากเกินไป : เปลี่ยน ICL (ขนาดเล็กลง) หรือนำ ICL ออก
กล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพเป็นการตรวจแบบสัมผัส (ใช้ถ้วยครอบตาหรือเมมเบรน) และต้องใช้ยาชาหยอดตาเฉพาะที่
ในกรณีลูกตาทะลุ หรือบาดเจ็บรุนแรงของส่วนหน้าดวงตา การตรวจแบบสัมผัสเป็นข้อห้ามโดยหลักการ และควรเลือกการตรวจแบบไม่สัมผัส เช่น CT
การตรวจ Gonioscopy ยังคงเป็นมาตรฐานทองคำ การตรวจ Gonioscopy จำเป็นสำหรับการประเมินการมีอยู่และขอบเขตของพังผืดม่านตา ส่วนปลายด้านหน้า (PAS ) และเส้นเลือดใหม่
Q
ความผิดปกติที่พบในการตรวจ UBM ได้รับการรักษาอย่างไร?
A
สำหรับต้อหินมุมปิด (ชนิดปิดกั้นรูม่านตา ) จะทำการผ่าม่านตา ด้วยเลเซอร์หรือผ่าตัดต้อกระจก สำหรับม่านตา แบบที่ราบสูง จะทำการปรับมุมด้วยเลเซอร์ (LGP ) ต้อหินชนิดร้าย (การหมุนของซิลิอารีบอดี ้ไปข้างหน้า) รักษาด้วยการจี้แสงซิลิอารีบอดี ้หรือการตัดน้ำวุ้นตา ในความผิดปกติของ Vault หลังใส่ ICL จะพิจารณาเปลี่ยนหรือนำ ICL ออก แผนการรักษาจะพิจารณาจากกลไกการอุดตันที่ยืนยันโดยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ
กล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพใช้คลื่นอัลตราซาวนด์ความถี่สูง (30-50 MHz) หลักการทางฟิสิกส์แสดงไว้ด้านล่าง
ความยาวคลื่น : 50-30 μm (สอดคล้องกับ 30-50 MHz)ความละเอียดเนื้อเยื่อ : 50-100 μm (แนวแกน)หลักการสร้างสัญญาณ : ความเข้มของการสะท้อนเปลี่ยนแปลงตามความแตกต่างของอิมพีแดนซ์เสียงของเนื้อเยื่อ ทำให้เกิดภาพตัดขวางปรับให้เหมาะสมสำหรับส่วนหน้า : ช่วงความถี่ที่เหมาะสมสำหรับการประเมินความลึก 5-10 มม.ข้อจำกัดด้านความลึก : เนื่องจากคลื่นความถี่สูงมีการลดทอนในเนื้อเยื่อมาก จึงใช้โหมด B ความถี่ต่ำ (5-10 MHz) เพื่อประเมินโครงสร้างที่ลึกกว่าคอรอยด์
กล้องจุลทรรศน์ชีวภาพด้วยคลื่นเสียงความถี่สูง (UBM ) และเครื่องตรวจวัดชั้นตาส่วนหน้าด้วยแสง (AS-OCT ) ถูกใช้เสริมกันเป็นอุปกรณ์ถ่ายภาพวินิจฉัยส่วนหน้าของดวงตา
รายการ UBM AS-OCT หลักการ คลื่นเสียงความถี่สูง (30-50 MHz) แสง (0.7-1.3 μm) การสัมผัส สัมผัส (มีความเสี่ยงติดเชื้อ) ไม่สัมผัส ท่าทาง นอนหงาย (พื้นฐาน) นั่ง (พื้นฐาน) ซิลิอารีบอดี และพื้นผิวด้านหลังของม่านตา สามารถสังเกตได้ ไม่ชัดเจน บริเวณรอบนอกของจอตา สามารถสังเกตได้ถึงคอรอยด์ ยาก การตรวจมุมด้วยการกด เป็นไปได้ด้วยถ้วยตา ไม่สามารถทำได้ ผิวกระจกตา และน้ำตา ไม่เหมาะสม มีประโยชน์ ทันทีหลังการผ่าตัด ยาก เป็นไปได้ ความละเอียดของเนื้อเยื่อ (แนวแกน) 50–100 ไมโครเมตร 5–10 ไมโครเมตร ความจำเป็นของผู้เชี่ยวชาญที่มีทักษะ สูง ต่ำ
จุดแข็งที่สุดของกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์คือ การมองเห็น โครงสร้างรวมถึงด้านหลังม่านตา และซิลิอารีบอดี AS-OCT คือต้องสัมผัสดวงตาด้วยวิธีการแช่น้ำ ใช้เวลาในการเก็บภาพนาน และต้องมีผู้ตรวจที่มีทักษะ
ความแตกต่างในการประเมินเนื้องอก : ในเนื้องอกเยื่อบุผิวสความัสที่ผิวตา (OSSN ) AS-OCT เหนือกว่าในการแสดงรายละเอียดภายในรอยโรค ในทางกลับกัน ในเนื้องอกม่านตา ที่ไม่มีเม็ดสี กล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ดีกว่าในการระบุขอบด้านหลังของรอยโรคและมีความสามารถในการทำซ้ำสูงกว่า
มีกลไกหลักสองประการที่ทำให้เกิดต้อหินมุมปิด
การอุดตันรูม่านตา แบบสัมพัทธ์ : ความดันในช่องหลังตาเพิ่มขึ้นทำให้ม่านตา โค้งไปข้างหน้าและปิดมุม UBM ยืนยันการโป่งของม่านตา ไปข้างหน้าและการตีบแคบของมุมโดยรวมกลไกม่านตา แบบที่ราบสูง : การเคลื่อนไปข้างหน้าของซิลิอารีบอดี แต่กำเนิดดันโคนม่านตา ขึ้นด้านบนโดยกลไก UBM ยืนยันการเคลื่อนไปข้างหน้าของซิลิอารีบอดี และการหายไปของร่องซิลิอารี
โดยการแยกแยะกลไกทั้งสองนี้ก่อนการผ่าตัดด้วยกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ สามารถปรับแผนการรักษาให้เหมาะสม (การตัดม่านตาด้วยเลเซอร์ เพียงอย่างเดียวเทียบกับ LI + LGP )
เนื้อหาต่อไปนี้ยังอยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
ซอฟต์แวร์วิเคราะห์เชิงปริมาณอัตโนมัติสำหรับภาพกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ได้รับการพัฒนา ทำให้สามารถวัดค่าพารามิเตอร์ต่างๆ เช่น มุมเปิดของช่องว่าง ความลึกของช่องหน้าม่านตา และเลนส์โวลต์ได้โดยอัตโนมัติ คาดว่าจะช่วยลดความแปรปรวนระหว่างผู้ตรวจและภายในผู้ตรวจ และเพิ่มความแม่นยำในการวินิจฉัย
ในรายงานผู้ป่วยของ Yeilta และคณะ ขนาดของรอยโรค (5×3×2 มม.) ได้รับการประเมินด้วยกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์ในโรคต้อหินชนิดเม็ดสี ทุติยภูมิจากเมลาโนไซโตมาเนื้อตายของม่านตา และการจัดการโดยการผ่าตัดร่วมกับการตัดม่านตา และซิลิอารีบอดี และการผ่าตัดชันต์ต้อหิน ได้ผลดี 1) อัตราการวินิจฉัยของการเจาะดูดเซลล์ด้วยเข็มเล็ก (FNAB) รายงานว่าอยู่ที่ 88-95% และผลการตรวจด้วยกล้องจุลทรรศน์ชีวภาพอัลตราซาวนด์มีบทบาทเสริมในการแยกแยะเมลาโนไซโตมาจากเมลาโนมา
การวิจัยเกี่ยวกับการจำแนกมุมและการวินิจฉัยอัตโนมัติของภาพ UBM โดยใช้การเรียนรู้เชิงลึกกำลังดำเนินอยู่ คาดว่าจะนำไปประยุกต์ใช้ในการคัดกรองโรคต้อหินมุมปิด ในระยะเริ่มต้น แต่ยังไม่ถึงขั้นนำไปใช้ทางคลินิก 4)
Yeilta YS, Oakey Z, Brainard J, Yeaney G, Singh AD. Necrotic iris melanocytoma with secondary glaucoma. Taiwan J Ophthalmol 2025;15:135–137.
Ritch R, Tham CC, Lam DS. Plateau iris syndrome. Ophthalmology 2004;111:1244–1246.
Gonzalez-Lopez F, Bilbao-Calabuig R, Mompean B, et al. Assessing vaulting changes after phakic collamer lens implantation by ultrasound biomicroscopy and optical coherence tomography. Eur J Ophthalmol 2016;26:36–41.
Jiang H, Wu Z, Lin Z, et al. Machine learning approaches to distinguish angle-closure from open-angle glaucoma using anterior segment features: a systematic review. Br J Ophthalmol 2022;106:1452–1458.